优化卵巢癌Ⅰ期临床研究管理中国专家经验
2019-06-26吴小华尹如铁高雨农
吴小华,张 剑,尹如铁,娄 阁,高雨农
1.复旦大学附属肿瘤医院妇瘤科,复旦大学上海医学院肿瘤学系,上海 200032;
2.复旦大学附属肿瘤医院肿瘤内科,复旦大学上海医学院肿瘤学系,上海 200032;
3.四川大学华西第二医院妇产科,四川 成都 610041;
4.哈尔滨医科大学附属肿瘤医院妇科,黑龙江 哈尔滨 150081;
5.北京肿瘤医院妇瘤科,北京 100142
卵巢癌是女性生殖器官常见的恶性肿瘤之一,也是中国妇科恶性肿瘤主要死亡原因之一。国际上抗肿瘤治疗迅速发展,而国内的各类抗肿瘤新药也不断涌现,陆续进入临床试验阶段。然而,国内针对卵巢癌的Ⅰ期临床研究数量明显少于其他瘤种。近年来随着新药的研发,尤其是多聚腺苷二磷酸核糖聚合酶[poly(ADP-ribose)polymerase,PARP]抑制剂在卵巢癌中的突破性疗效,国内逐步开展了一系列卵巢癌Ⅰ期临床研究。Ⅰ期临床研究需要妇科肿瘤医师、Ⅰ期临床试验病房、肿瘤内科医师与护士的共同参与和紧密协作。如何在保证受试者自愿参与试验、保护受试者权益的基础上,确保新药临床试验顺利进行,获取高质量的临床数据,成为各临床研究中心工作的重中之重。基于一项研究编号为ZL-2306-002的Ⅰ期临床研究,中国专家进行了深入的总结与讨论,旨在优化Ⅰ期临床试验的流程,为国内抗肿瘤新药临床研究的开展提供参考与经验。
1 卵巢癌治疗现状与进展
卵巢癌是世界范围内常见的妇科癌症死亡原因之一。在美国,每年约有22 000名妇女被诊断患有此病,每年死亡例数达14 000例[1]。而在中国,2011年新发卵巢癌达45 224例,死亡病例为18 430例,呈逐年升高的趋势[2]。卵巢癌在早期阶段存在治愈的可能,但约70%的患者在诊断时已处于晚期[3]。目前主要治疗手段包括手术切除(肿瘤细胞减灭术),以及紫杉醇和铂类药物的联合化疗。虽然60%~80%的卵巢癌患者在积极的一线治疗后可获得完全的临床缓解,但80%的晚期患者在接受铂类药物化疗后复发[4]。卵巢癌一旦复发后,将难以治愈,同时患者对含铂类药物的化疗逐渐产生耐药,对化疗所致不良反应的耐受性越来越低,后续有效的治疗手段越来越少,有远处转移的卵巢癌患者5年的生存率仅为29%[5]。
靶向治疗药物的出现为复发性卵巢癌的治疗带来了新的曙光,如血管生成抑制剂和PARP抑制剂等。贝伐珠单抗为人源化靶向血管内皮细胞生长因子的单克隆抗体,于2014年经美国食品药品管理局(Food and Drug Administration,FDA)批准上市,联合化疗用于治疗对含铂类药物化疗耐药的复发性卵巢癌患者,经之后的相关研究表明,贝伐珠单抗的应用同样可使铂类敏感的卵巢癌患者总生存获益,因此在2016年该药的适应证拓展至维持治疗铂类敏感患者,这也是第1个在美国批准的用于卵巢癌患者维持治疗的药物[6]。
近年来免疫疗法成为备受关注的一种新的肿瘤治疗措施,其中程序性死亡[蛋白]-1(programmed death-1,PD-1)抗体、 程序性死亡[蛋白]配体-1(programmed death ligand-1,PD-L1)抗体尤其引人瞩目。多个抗PD-L1及抗PD-1抗体的临床试验结果表明它们对包括恶性黑色素瘤在内的一些恶性肿瘤具有明显的抗肿瘤效应。同样,抗PD-L1和抗PD-1抗体(如纳武单抗、帕博丽珠单抗等)被认为可在卵巢癌的辅助治疗中起到显著效果[7-8]。
PARP抑制剂是迅速崛起的复发性卵巢癌患者治疗的新选择,它们通过抑制DNA的损伤修复而抑制癌细胞的增殖。现有的PARP抑制剂有奥拉帕尼、尼拉帕尼、芦卡帕尼和他拉唑帕尼,为对铂类药物化疗敏感的复发性卵巢癌患者提供了更好的治疗选择。
以PARP为靶点的靶向治疗在卵巢癌患者中具有坚实的科学基础。PARP-1和PARP-2是DNA结合酶,其功能为检测DNA单链损伤并促进修复。PARP发现DNA损伤后,可将损伤转换成细胞内信号,然后再激活碱基切除修复通路。这条通路对于存在同源重组缺陷(homologous recombination deficiency,HRD)的细胞尤为重要[9]。在DNA双链修复出现缺陷的背景下,细胞DNA损伤修复会更多地依赖于单链损伤修复通路;因此,当PARP抑制剂用于BRCA基因异常等原因导致HRD广泛存在的卵巢癌患者时,它可引起的DNA单链损伤修复被阻断、结合HRD等引起的DNA双链修复缺陷双重打击能够产生彼此协同效应和增强诱导细胞凋亡的效应,同时PARP抑制剂本身具有的诱导细胞凋亡的作用机制也提示其应用于非BRCA基因异常的卵巢癌患者时亦会产生抗肿瘤效应。临床前体外及体内研究均证实了该靶点的有效性[10-11]。
尼拉帕利是一种强效且具有高度选择性的PARP-1和PARP-2抑制剂。一项Ⅲ期、随机、安慰剂对照的全球多中心临床试验结果显示,尼拉帕利在铂类药物化疗敏感的复发性卵巢癌受试者中作为维持治疗药物显著地延长了受试者的无进展生存期,证实了PARP抑制剂在复发性卵巢癌受试者中的临床有效性[12]。更为重要的是,尼拉帕利在携带gBRCA突变的卵巢癌受试者及未携带gBRCA突变的卵巢癌受试者中都表现出显著的有效性。基于在该临床Ⅲ期研究中获得的强大的临床支持性数据,2017年3月,尼拉帕利获得美国FDA快速批准上市,用于铂类药物化疗敏感的复发性卵巢癌的维持治疗[13]。再鼎医药(上海)有限公司于2016年9月获得了尼拉帕利在中国(包括中国香港和中国澳门)的独家研发、生产和销售的权利,将其编号为ZL-2306,并于2017年申办了ZL-2306-002研究:一项评价尼拉帕利在卵巢癌、输卵管癌、原发性腹膜癌(统称卵巢癌)患者中的药代动力学、安全性、耐受性的开放、单臂、Ⅰ期临床试验。
自2017年12月,由复旦大学附属肿瘤医院、四川大学华西第二医院、哈尔滨医科大学附属肿瘤医院与北京肿瘤医院开展了尼拉帕利的Ⅰ期临床试验(ZL-2306-002)。该试验共入组36例卵巢癌患者,并随机分配至不同剂量组(100、200和300 mg),目的在于评估尼拉帕利不同剂量组患者的药物动力学参数和安全性数据,进而摸索该新型抗肿瘤药物最适合中国患者的剂量。该研究于2018年7月顺利完成入组患者的随访,初步研究结果于2018年在中国临床肿瘤学会年会上发布。ZL-2306-002研究获取的数据质量高,患者跟踪情况良好,为尼拉帕利在中国人群中的应用(剂量、安全性)提供了更有价值的参考。
2 优化Ⅰ期临床试验流程
ZL-2306临床I期流程图见图1。
2.1 患者来源和知情同意,提高入组效率
Ⅰ期临床试验虽入组患者例数不多,但由于其评估指标的特殊性,入组标准更为严苛,对入组患者的一致性也具有更高的要求,因此高效的患者入组是临床试验成功开展的重要一环。对外宣传临床试验是加快患者入组的方法之一,有研究中心将临床试验患者招募信息推广至省、市、县所有医院,确保所有相关的患者群体可获得招募信息;全科临床医师对临床试验入组和排除标准的熟知可使医师快速识别出目标患者,从而保证符合标准的门诊患者或住院患者不被遗漏,因此各个研究中心均在临床试验启动会召开时要求每个相关科室的医师参与学习,掌握临床试验的入组和排除标准;合理利用医院现有的患者数据库也是筛选患者的有效方法,除了筛查就诊患者的数据资料,有研究中心设有以病种为分类单位的出院患者登记簿,记有患者出入院日期、主治医师、手术类型、术后病理学检查结果、住院号、详细家庭住址、身份证号及联系方式。若经筛选出现符合标准的患者,项目负责人可通过电话联系该患者,并通知其主治医师,进行进一步的沟通。值得一提的是,有研究中心因加入临床试验时间较晚,从试验启动到试验入组通道关闭,院方仅给予10 h,因此该中心在确定研究后即开始进行准备工作,熟悉入组和排除标准,收集相关的患者信息。试验启动后,项目组迅速从门诊、住院部和医院的体检中心筛查出目标患者,非项目医师也可根据先前了解到的试验入组和排除标准,将接收的患者推荐至项目医师,之后专人接待、沟通,主要研究者根据临床经验初步判断目标患者入选的可能性,在这10 h内入组了足够数量的患者。
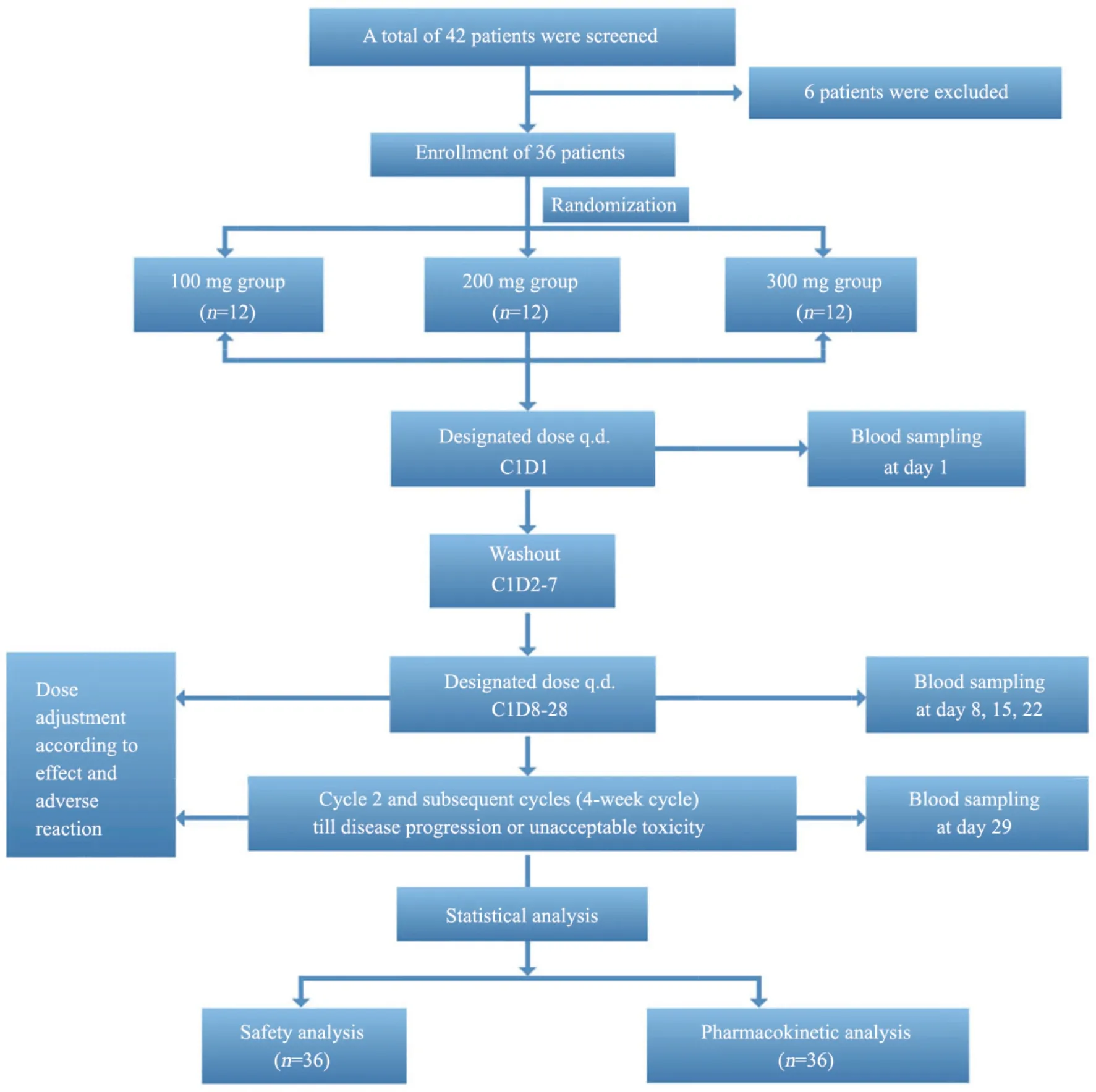
图1 ZL-2306临床Ⅰ期研究流程图Fig.1 Flowchart of stage Ⅰ study of ZL-2306
2.2 入组和排除审核,减少方案异质性
多中心的Ⅰ期临床研究需要确保入组患者的统一性,特别是肿瘤患者,因患者的病情复杂,先前的干预治疗手段多种多样,在患者入组时,需严格把控入组标准,以确保试验结果的准确性。在该Ⅰ期临床试验过程中,各个中心在患者入组阶段保持与申办方、招募公司的密切联系,患者既往治疗史的判定或出现任何有争议的病例,均进行三方探讨,继而确定该患者是否入组,中心还设有临床研究管理专员,掌握所有申办方和临床研究协调员(clinical research coordinator,CRC)的联系方式,在入组过程中出现任何问题,均可与其他机构进行及时沟通。除此之外,保证科室之间的密切合作,这对筛选出适合临床研究的患者非常有利。例如,肿瘤科保持与外科的紧密联系,可更清楚患者的系统性治疗方案(减瘤术),对患者的实验室检查、影像学检查等方面也会有更进一步的认知,从而保证患者诊疗流程的规范化,减少方案的异质性。
2.3 临床用药和随访,提高患者依从性
一个成功的临床试验离不开患者的高度依从,而这一点则需要从患者对临床试验的认知与信任做起。关于患者对临床试验的认知,除了在入组初期对患者进行充分的宣教与获得知情同意之外,有的中心于医院走廊张贴临床试验介绍海报,患者与患者家属等候时,不经意间就获知了临床试验基本信息,加深了对临床试验的理解,于是当医师对患者进行临床试验项目的介绍时,患者就不会觉得陌生,更易接受入组,这也让部分患者在了解临床试验后,主动联系医师,询问是否有可参与的临床研究项目,为后续工作带来了极大的便利;患者对临床试验的信任,需要临床试验相关工作人员自始至终的努力,明确以患者为中心的工作原则,坚守赫尔辛基宣言——公正、尊重人格、力求使受试者最大程度地获益和尽可能避免伤害。为此,有中心负责人建立了微信群,将所有的临床试验工作人员纳入群中,可及时了解到患者的病情变化和随访情况,也可在问题出现的第一时间给予工作人员反馈。在临床试验进行过程中,保持患者的依从也需要医师较强的医患沟通能力。患者可能因为各种各样的问题(不良事件、费用等)产生负面情绪。此时,良好的沟通技巧可安抚患者,化解此类矛盾,有研究中心保证了所有参与项目的护士与医师持有临床试验规范标准(good clinical practice,GCP)证书,同时经过系统的临床试验患者沟通培训,有效地提高了医师对于项目整体的医患沟通能力。
2.4 完善数据管理
临床试验的最终结果需要完整而系统的患者数据。在肿瘤领域药物相关的Ⅰ期临床试验过程中,因涉及药物动力学分析,需要密集地对患者进行采血,以得到完整的药物动力学参数,同时还需要获得准确的安全性数据,对患者的不良事件进行评估和归纳,完善的患者数据管理显得尤为重要。系统地分配各个临床试验相关工作,专人、专职、专区,形成独立的工作小组,是各个临床中心高效管理患者、准确记录患者数据的基础,例如,有研究中心以科主任负责制统筹管理临床试验的进行。一线医师分管临床试验的申报、伦理答辩、申办方沟通、患者筛选、入组期间的管理、不良事件的上报处理和试验结束后的总结等,而临床试验管理专员则负责制定临床试验汇总表,每月科会向临床医师汇报近1个月签署知情同意书、随机入组人数、已完成入组人数、合同签署入组人数等情况;有研究中心每月组织全科回顾入组情况,形成一个分析、总结、改进、分析的闭环,提高试验后续工作效率,弥补不足之处,并为CRC专门设立研究接待工作场所,进行患者管理工作,系统地分配临床试验的工作任务,如医疗组中的影像学医师进行疗效评估,下级医师收治患者、完善记录、管理随访,护理团队领取发放药物、采集样本、观察记录不良事件,项目管理团队(CRC与研究护士)则协助其他研究者的工作,并监督、稽查申办者,药事管理协助进行临床研究用药的接收、储存、发放和回收等。在系统合理的工作分配制度、高效的运营流程、明确的责任制度之上再搭建完善的患者数据管理与保存系统,每日项目医师集体查房、开展病例讨论与该领域最新进展讨论,更进一步地保证患者数据的完整和科学合理性。
2.5 有效的不良反应处理
肿瘤药物引起的不良反应往往较大,同时肿瘤患者身体虚弱,不良事件的发生较为频繁,及时对出现不良事件的患者进行相应的治疗与心理疏导,也是临床试验开展过程中的重要一环。患者需要严密的跟踪随访,对出现严重不良事件的患者,更需要保持监测,直至症状完全缓解。例如,在该尼拉帕利的Ⅰ期临床试验过程中,患者常见的不良事件集中在消化系统和血液系统,患者需不良事件管理建议,必要时考虑减量治疗,无法耐受时考虑中断用药,例如,3~4级的血小板减少,需要患者中断用药,对症支持治疗,后续持续观察患者血小板计数情况,直至血小板计数回升至可接受范围内,再考虑患者是否继续接受该方案治疗或更换新方案治疗。在整个过程中,医师与护理团队需保持高度的警觉,预防任何严重不良事件的再次进展,同时加强对患者的心理辅导,使其正确认识用药过程中产生的不良事件,避免患者因轻微的不良事件而退出研究。
2.6 细致的患者关爱
患者关爱始终是临床研究工作中值得探讨的内容。重症患者在生理和心理上备受折磨,让他们感受到医务工作者的体贴与关爱,树立疾病缓解和治愈的信心,给予他们生活下去的希望,是临床试验工作者应尽的责任。在开展尼拉帕利Ⅰ期临床试验的过程中,有研究中心专门为进行采血的患者开设等候室,保证患者与其家属在等待采血的过程中拥有足够的休息空间,还设有专员对这些患者进行耐心细致的沟通,及时帮助患者和家属;也有中心组建患者家属沟通微信群,随时随地掌握患者情况,只要患者或其家属反馈治疗过程中产生的问题,不论何时何地,医师均会及时解答,给予相应的支持。
3 卵巢癌Ⅰ期临床研究现状分析
国内卵巢癌Ⅰ期临床研究现状见表1。
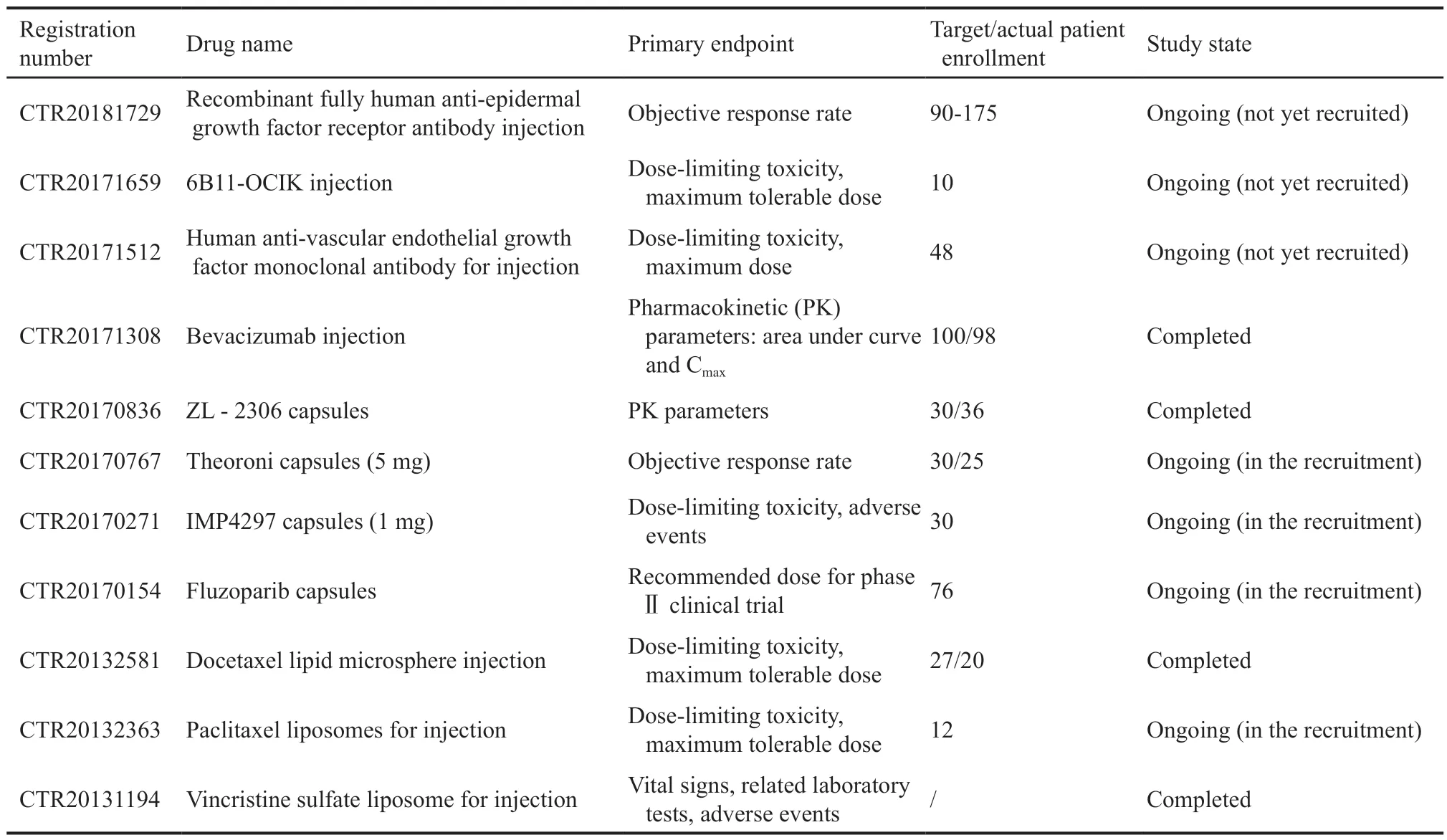
表1 国内卵巢癌Ⅰ期研究Tab.1 Stage Ⅰ studies of ovarian cancer in China
目前国内PARP抑制剂的相关Ⅰ期临床试验共有11项,其中3项已完成,剩余8项仍在进行中。设定的主要临床终点有客观缓解率(objective response rate,ORR)、剂量限制性毒性(dose-limiting toxicity,DLT)、最大耐受剂量(maximum tolerated dose,MTD)、PK参数和不良事件等,主要评估药品的药物代谢动力学参数与最合适的用药剂量。对应的适应证主要为晚期卵巢癌等恶性实体瘤。值得一提的是,仅一项Ⅰ期临床试验为国外制药公司申办,由此可见国内研发PARP抑制剂的制药公司和学术机构众多,不少药物已进入临床试验阶段。虽然各类PARP抑制剂在作用机制上有一定区别,疗效可能也会有所不同,但无论如何,国内PARP抑制剂的研发热潮必将使卵巢癌等实体瘤患者获益。
近年的国内卵巢癌Ⅰ期临床研究更是覆盖了各种作用机制的新型药物,既有生物制剂类靶向药物,也有小分子靶向类药物。这些药物具有不同的机制,针对不同亚型与突变体的卵巢癌患者,为卵巢癌患者带来了更多的选择。
4 结论
总体而言,卵巢癌Ⅰ期临床试验的顺利开展离不开医务工作者丰富的临床经验、强大的科研能力和细致入微的患者管理,临床试验中心也需配备相应的工作小组与数据管理系统,保证临床试验合理高效的运行与临床数据的完整和科学性。当然,我们依然需要探索更为全面的不良事件处理方案、多中心合作与资源共享模式,加强患者关爱,使更多的重症患者从临床试验中获益。
