纳米γ-氧化铁的制备及其吸附性能研究
2019-06-15韩宇霞赵斯琴
张 斌 ,韩宇霞 ,赵斯琴 ,2,长 山 ,2
(1.内蒙古师范大学,化学与环境科学学院,内蒙古呼和浩特010022;2.内蒙古师范大学,内蒙古自治区功能材料物理与化学重点实验室)
随着中国工业的不断发展,每年有大量的染料废水排放到环境中,使得水资源受到越来越严重的污染。这些染料废水成分复杂,含有大量的有毒有机污染物,有机污染物以烷烃类、取代苯类、多环芳烃类为主[1],而且这些污染物具有致癌性[2],会给人类带来严重的危害。
目前已知的水处理方法有氧化法[3]、膜分离法[4]、电解法[5]和吸附法。其中吸附法具有对污染物的吸附范围广、选择性高、吸附率高以及吸附剂容易回收且可循环利用等优点[6],已逐渐成为比较理想的废水处理方法。近年来氧化铁在污水处理方面得到广泛的应用,其对水中的有毒金属、有机污染物、无机离子有很好的去除能力。介孔γ-Fe2O3具有比表面积大、种类繁多、可重复利用、制备方法多且简单等优点[7],其孔道结构有助于提高其对有机染料的吸附性能,其磁响应性能能够将其从废水中分离出来[8],因此其在废水处理方面具有很大的应用价值。笔者以固相法制备了介孔γ-Fe2O3纳米粒子,并将其作为吸附剂吸附水中的染料直接耐酸大红4BS,探讨了其在不同吸附条件下的吸附性能。
1 实验部分
1.1 试剂及仪器
试剂:九水硝酸铁(分析纯),十二烷基三甲基溴化铵(DTAB),直接耐酸大红4BS(分析纯)。
仪器:UltimaⅣ型X射线衍射仪(XRD),Autosorb-IQ-C型比表面及孔隙率分析仪,Lake Shore 7407型振动样品磁强计,R50/500/12型管式电炉,722N型分光光度计,SHA-BA型恒温振荡器。
1.2 纳米γ-Fe2O3的制备
称取4.5 g硝酸铁和0.5 g DTAB于研钵中,混合研磨1.5 h,得到橘黄色粉末,室温下自然晾干。称取一定量粉末放入管式电炉中,在200℃加热2 h,得到 γ-Fe2O3。
1.3 纳米γ-Fe2O3对4BS的吸附性能研究
1.3.1 纳米γ-Fe2O3对4BS的吸附实验
移取20 mL 4BS质量浓度为100 mg/L的染料溶液,置于150 mL锥形瓶中,调节pH为2,加入100 mg γ-Fe2O3,室温下振荡 1 h,磁性分离,取上清液,测试其吸光度,根据公式(1)(2)计算染料的吸附率(η,%)和吸附量(Q,mg/g)。

式中:ρ0为吸附前 4BS 的质量浓度,mg/L;ρe为吸附后4BS的质量浓度,mg/L;V为溶液的体积,L;m为γ-Fe2O3的质量,g。
1.3.2 纳米γ-Fe2O3的重复利用实验
将吸附4BS的γ-Fe2O3用NaOH溶液脱附,超声20 min。然后用乙醇清洗3次,用蒸馏水洗至中性。然后在100℃烘干,用于下一次吸附。反复5次,计算吸附率。实验条件与1.3.1节一致。
2 结果与讨论
2.1 γ-Fe2O3样品表征
2.1.1 XRD分析
图1为固相法制备γ-Fe2O3样品的XRD谱图。由图 1看出,γ-Fe2O3样品 XRD谱图中出现了6个明显的衍射峰,衍射峰的位置和强度均与γ-Fe2O3(JCPDS:No.39-1346)的特征衍射峰相符,即2θ=30.3、35.6、43.3、53.7、57.3、62.9°处的衍射峰分别对应于(220)(311)(400)(422)(511)(440)晶面[9],说明制备的样品为γ-Fe2O3粒子。由Scherrer公式计算γ-Fe2O3样品的平均晶粒尺寸为18.5 nm。
由于γ-Fe2O3和Fe3O4都属于尖晶石型晶体,因此很难用XRD峰的位置来辨别它们,但可以用衍射峰的d值进行辨别。根据Bragg公式计算出γ-Fe2O3样品各晶面的晶面间距值(d值),并与γ-Fe2O3(JCPDS:No.39-1346)和 Fe3O4(JCPDS:No.19-629)卡片d值数据进行对比,结果见表1。由表1看出,γ-Fe2O3样品XRD峰位置所对应的d值都与γ-Fe2O3的JCPDS卡片中的d值基本一致,进一步证实了制备的γ-Fe2O3样品为γ-Fe2O3。
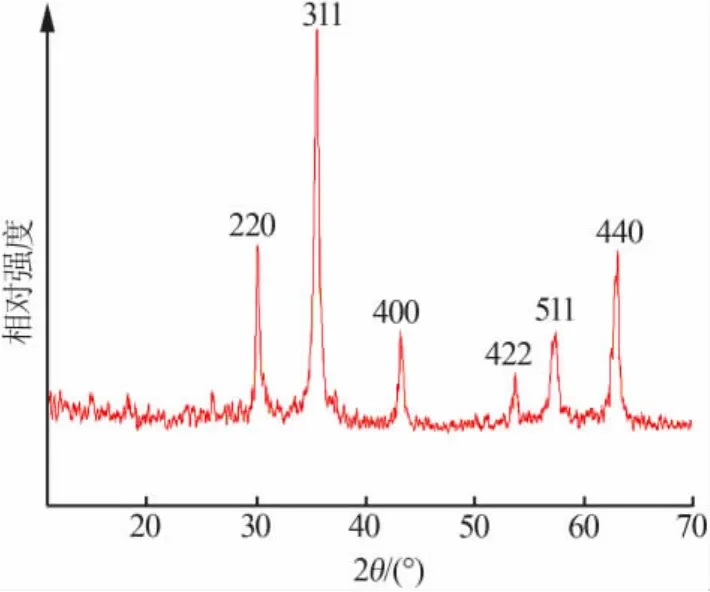
图1 固相法制备γ-Fe2O3的XRD谱图

表 1 γ-Fe2O3样品 d值及与 γ-Fe2O3和Fe3O4的JCPDS卡片标准d值对比
2.1.2 N2吸附-脱附曲线及孔径分布分析
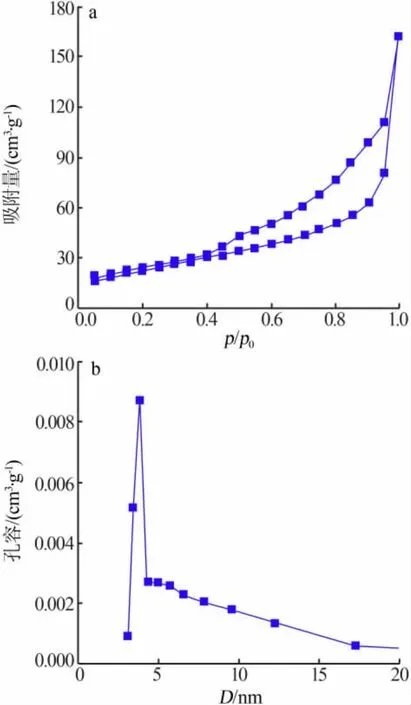
图2 γ-Fe2O3样品N2吸附-脱附曲线(a)和孔径分布图(b)
图2为γ-Fe2O3样品N2吸附-脱附曲线及孔径分布图。由图2a可知,γ-Fe2O3样品N2吸附-脱附等温线为 LangmuirⅣ型[10],相对压力为 0.4~1.0 时出现了H3型滞后环,说明γ-Fe2O3样品具有介孔结构。由测试结果可知,样品的比表面积为83.2 m2/g,孔容为0.25 cm3/g。由图2b可知,γ-Fe2O3样品最可几孔径为3.8 nm,属于介孔范围。
2.1.3 磁性分析
图3为γ-Fe2O3样品的磁滞回线。由图3看出,γ-Fe2O3具有一定的剩磁和顽磁,表明制备的介孔γ-Fe2O3纳米粒子具有铁磁性[11]。 γ-Fe2O3样品的最大饱和磁化强度(Ms)为 63.7 A·m2/kg,比体相 γ-Fe2O3的 74 A·m2/kg 小,主要是因为表面效应[12-13]。
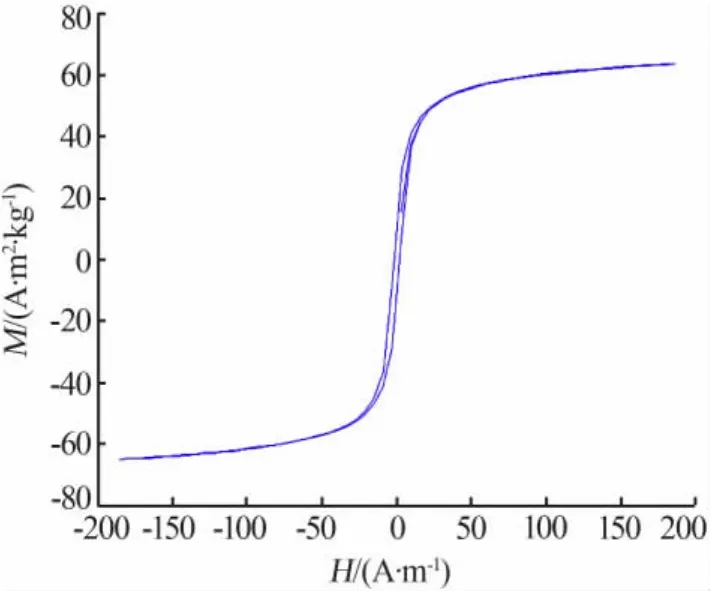
图3 γ-Fe2O3样品的磁滞回线
2.2 吸附条件对吸附性能的影响
2.2.1 吸附时间的影响
图4为吸附时间对γ-Fe2O3吸附4BS的影响。实验条件同1.3.1节。由图4可知,当吸附时间为5 min时吸附率达到95%,吸附时间为10~30 min时吸附率有较弱的增强,之后趋于稳定。这是由于,随着吸附时间的增加,吸附剂表面吸附位点基本被占据,导致吸附速率变慢[14]。
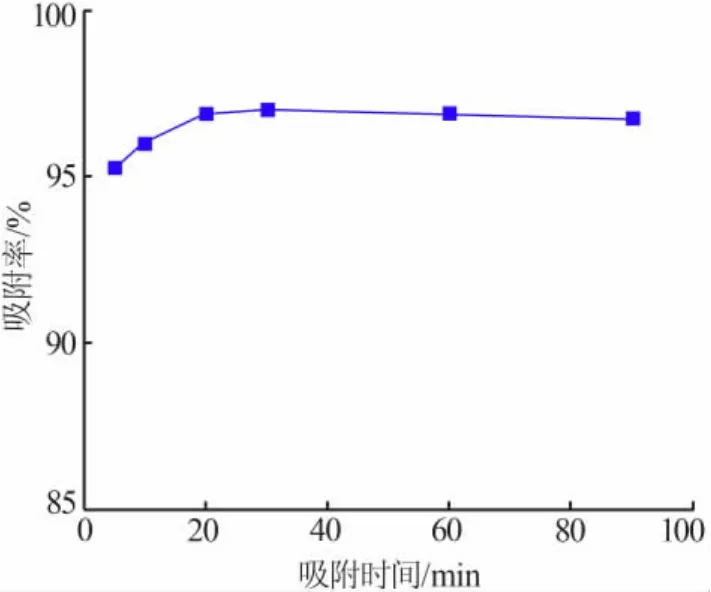
图4 吸附时间对γ-Fe2O3吸附4BS的影响
利用准一级和准二级吸附动力学模型进行拟合,结果见表2。
准一级动力学模型:
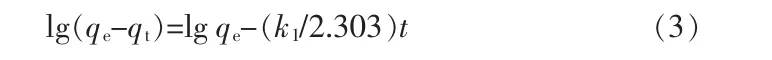
式中:qe、qt分别为平衡时、t时刻的吸附量;k1为准一级吸附速率常数。
准二级动力学模型:

式中:k2为准二级吸附速率常数。
由γ-Fe2O3吸附4BS的两个动力学方程得到表2数据。由表2可知,准一级动力学方程线性相关系数R2=0.100 9;而准二级动力学方程线性相关系数R2=1,表明准二级动力学模型能够更好地描述介孔γ-Fe2O3对4BS的吸附。
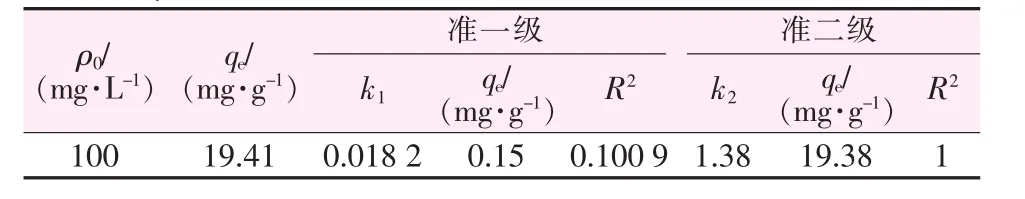
表2 γ-Fe2O3吸附4BS的两种动力学模型拟合相关数据
2.2.2 溶液质量浓度的影响
图5为溶液初始质量浓度对γ-Fe2O3吸附4BS的影响。实验条件同1.3.1节。由图5看出,随着溶液初始质量浓度的增大4BS吸附率逐渐下降;4BS吸附量在溶液初始质量浓度小于600 mg/L时逐渐升高,大于600 mg/L后趋于平稳。这是因为,吸附剂表面的吸附位点有限,当其达到吸附饱和后吸附量将不再增加,因此吸附量趋于平衡。

图5 溶液初始质量浓度对γ-Fe2O3吸附4BS的影响
采用Langmuir和Freundlich吸附理论对吸附数据进行拟合,结果见表3。
Langmuir吸附等温式:

式中:q∞为极限吸附量;KL为吸附平衡常数。
Freundlich吸附等温式:
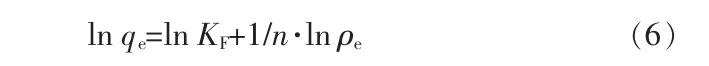
式中:KF为Freundlich平衡常数;n为与温度有关的常数。
由γ-Fe2O3吸附4BS的两个吸附等温方程计算得到表3数据。由表3看出,γ-Fe2O3吸附4BS数据拟合得到的Langmuir吸附等温式的线性相关系数R2=0.994 4,Freundlich吸附等温式的线性相关系数R2=0.890 9。由此可知,介孔γ-Fe2O3对4BS的吸附符合Langmuir吸附等温模型,属于单分子层吸附。
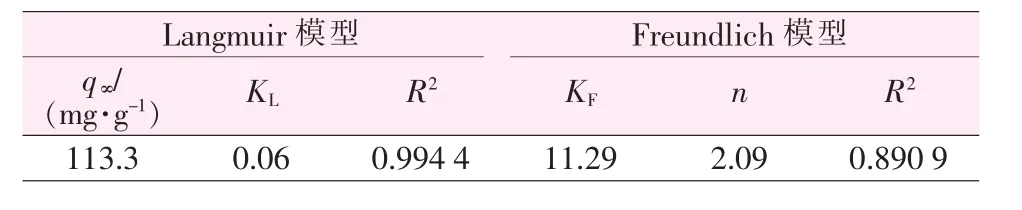
表 3 γ-Fe2O3吸附 4BS的Langmuir和Freundlich吸附等温方程参数
2.2.3 吸附剂的再生实验
图6为γ-Fe2O3再生次数与吸附4BS的关系。由图6可知,γ-Fe2O3纳米粒子对4BS进行5次吸附再生实验后,吸附率仍能达到88%以上,说明γ-Fe2O3再生效果较好,可重复使用。
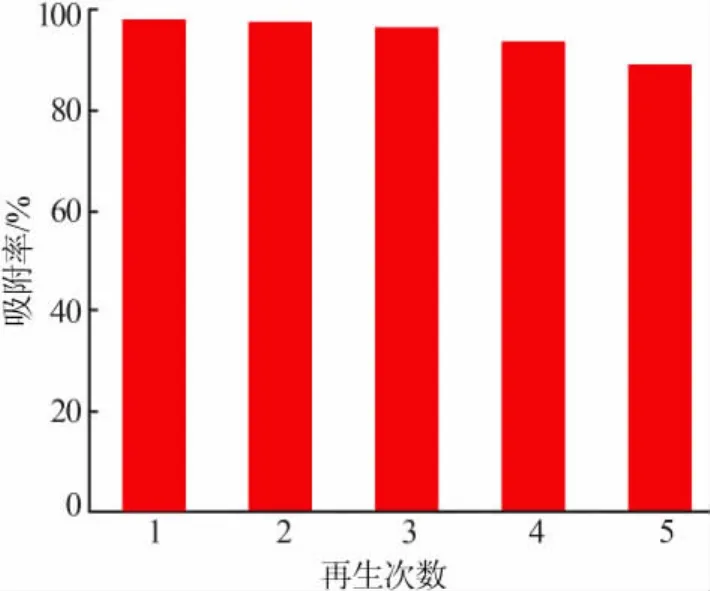
图6 γ-Fe2O3再生次数与吸附率的关系
3 结论
1)用固相法制备了介孔γ-Fe2O3纳米粒子,其晶粒尺寸为18.5 nm,具有铁磁性,最大饱和磁化强度为63.7 A·m2/kg,比表面积为 83.2 m2/g,最可几孔径为3.8 nm。2)介孔γ-Fe2O3对4BS的吸附速率较快,当吸附时间为5 min时吸附率达到95%,吸附过程符合准二级吸附动力学模型;介孔γ-Fe2O3对4BS的吸附符合Langmuir吸附等温模型,属于单分子层吸附。3)将吸附剂进行脱附处理后可有效地重复利用,具有一定的使用价值。
