贝伐珠单抗联合FOLFIRI方案治疗转移性结直肠癌的临床疗效评估
2019-06-08李卫星
李卫星

【摘要】目的 评估贝伐珠单抗联合FOLFIRI方案治疗转移性结直肠癌的临床疗效。方法 回顾性分析2016年10月~2018年12月我院收治的62例转移性结直肠癌患者临床资料,根据治疗方式不同分为对照组(n=25)与研究组(n=37)。治疗后6~8周,评估近期疗效;随访1年,评估患者中位无疾病进展时间(PFS);并记录不良反应。结果 治疗后6~8周,研究组有效率、疾病控制率高于对照组,差异有统计学意义(P<0.05);对照组中位PFS为7.89[95%CI(6.726,9.055)],研究组中位PFS为10.49[95%CI(9.892,11.093)]个月,差异有统计学意义(P<0.05);两组不良反应主要以Ⅰ~Ⅱ级为主,Ⅲ~Ⅳ级不良反应相对较少,两组不良反应率对比,差异无统计学意义(P>0.05)。结论 贝伐珠单抗联合FOLFIRI方案治疗转移性结直肠癌可提高临床疗效及疾病控制率,延长患者的中位无疾病进展时间,且联合方案不会增加患者的不良反应发生情况。
【关键词】转移性结直肠癌;贝伐珠单抗;FOLFIRI方案
【中图分类号】R735.34 【文献标识码】A 【文章编号】ISSN.2095.6681.2019.36..03
直肠癌在恶性肿瘤中发病率较高,约50~60%患者会发生同时性或异时性远处转移,其中约80-90%为不可切除的肝转移,且25%的大肠癌患者初诊断时就为晚期,失去手术治疗的机会,预后较差。晚期转移性结直肠癌患者主要采用化疗手段进行治疗,主要达到延长生存期、降低药物毒性,从而提高患者的生存质量[1-2]。但大部分肿瘤细胞的耐药性导致化疗效果较差,疾病缓解情况不理想[3]。而贝伐珠单抗可抑制血管内皮生长因子,用于治疗各类转移性癌症,因此,本研究旨在评估贝伐珠单抗联合FOLFIRI方案治疗转移性结直肠癌的临床疗效。现报告如下。
1 资料与方法
1.1 一般资料
回顾性分析2016年10月~2018年12月我院收治的62例转移性结直肠癌患者临床资料。经病理组织学或细胞学检查已证实;均伴有远处器官转移;均具有可测量的肿瘤病灶;均无法采用手术治疗;且患者的预计生存期>3个月;排除存在其他恶性肿瘤者、本研究药物过敏者、肝肾、凝血功能异常者。根据治疗方式不同分为对照组(n=25)与研究组(n=37)。对照组中男14例,女11例;年龄33~72岁,平均(54.69±3.12)岁;KPS评分为43~84分,平均(76.25±1.25)分;左半肠癌18例,右半肠癌7例;转移部位肝、肺、骨、淋巴结、其他分别为11例、4例、2例、4例、4例。研究组中男21例,女16例;年龄35~73岁,平均(54.71±3.11)岁;KPS评分为42~85分,平均(76.27±1.23)分;左半肠癌26例,右半肠癌11例;转移部位肝、肺、骨、淋巴结、其他分别为16例、6例、3例、6例、6例。统计学比较两组一般资料,差异无统计学意义(P>0.05),具有可对比性。
1.2 方法
1.2.1 对照组:采用FOLFIRI方案进行化疗,入院后常规检测患者血常规、肝肾功能等,治疗第1 d,采用伊立替康(江苏恒瑞医药公司,国药准字H3272050)静脉滴注,180 mg/m2;第1~2 d,采用400 mg/m2四氢叶酸钙(江苏恒瑞医药公司,国药准字H1618323)400 mg/m2 5-氟尿嘧啶(山西普德药业有限公司,国药准字H3278766)静脉滴注,1次/2周。
1.2.2 研究组:在对照组基础上,加用贝伐珠单抗(Roche Pharma (Switzerland) Ltd,进口药品注册证号S20170035)治療,于化疗前的第1 d,采用贝伐珠单抗5 mg/kg进行静脉滴注,滴注时间需>90 min。如患者耐受性良好,可将时间缩短,1次/2周。两组均持续治疗到病情进展或药物毒性不可耐受。
1.3 评价指标
(1)近期疗效:治疗后6~8周,根据《实体瘤治疗疗效评价标准-RECIST》进行疗效评断:①完全缓解(CR):所有病灶消失;②部分缓解(PR):从最开始的病灶直径之和减少≤30%;③:疾病进展(PD):病灶直径之和相对增加≥20%或出现新病灶;④疾病稳定(SD):病灶减少程度未达到PR,增加程度也未达到PD水平。有效率=CR+PR/总例数×100%;疾病控制率=CR+PR+SD/总例数×100%。(2)生存分析:随访1年,记录所有患者疾病无进展生存期(PFS)情况。(3)不良反应:参照世界卫生组织(WHO)抗癌药物急性与亚急性表现和分度标准评估不良反应情况,包括0级为无症状、Ⅰ期为轻度副反应、Ⅱ期为中度副反应、Ⅲ期为重度副反应、Ⅳ期表示威胁生命,毒副作用,包括肠道反应、高血压、骨髓抑制等情况。
1.4 统计学方法
采用SPSS 20.0软件进行数据处理,以x±s表示计量资料,组间用独立样本t检验,组内用配对样本t检验,计数资料用百分比表示,采用x2检验,存分析采用Kapalan-Meier法,行Log-rank检验,P<0.05为差异具有统计学意义。
2 结 果
2.1 近期疗效
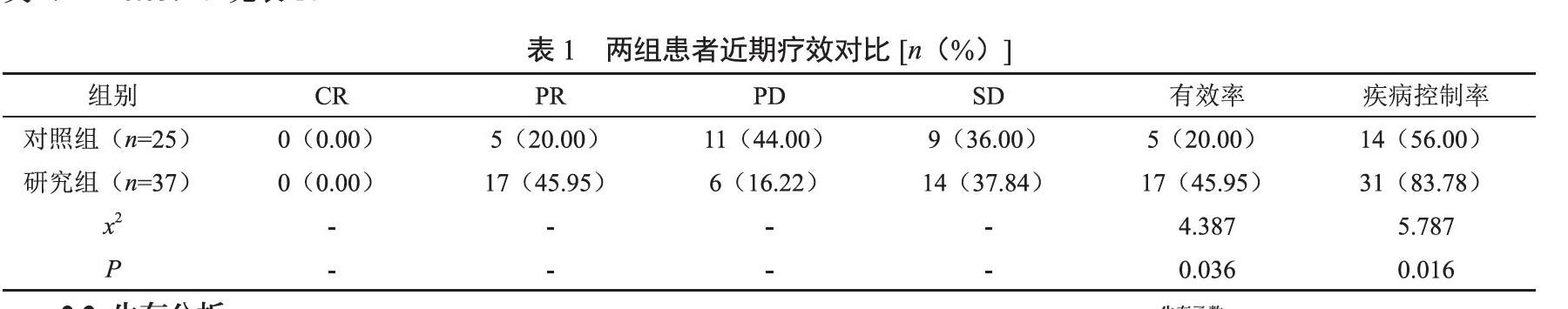
治疗后6~8周,研究组有效率为45.95%高于对照组20.00%,差异有统计学意义(P<0.05);治疗后,研究组疾病控制率为83.78%高于对照组56.00%,差异有统计学意义(P<0.05)。见表1。
2.2 生存分析
所有患者中位随访时间为1年,无失访,患者出现疾病进展后采用局部治疗或进行二线治疗。死亡28例,病死率45.16%,包括对照组15例(60.00%),观察组13例(35.14%),组间比较差异无统计学意义(x2=3.725,P=0.054)。其中对照组中位PFS为7.89[95%CI(6.726,9.055)]个月,研究组中位PFS为10.49[95%CI(9.892,11.093)]个月,差异有统计学意义(x2=14.101,P=0.000)。见图1。
2.3 不良反应
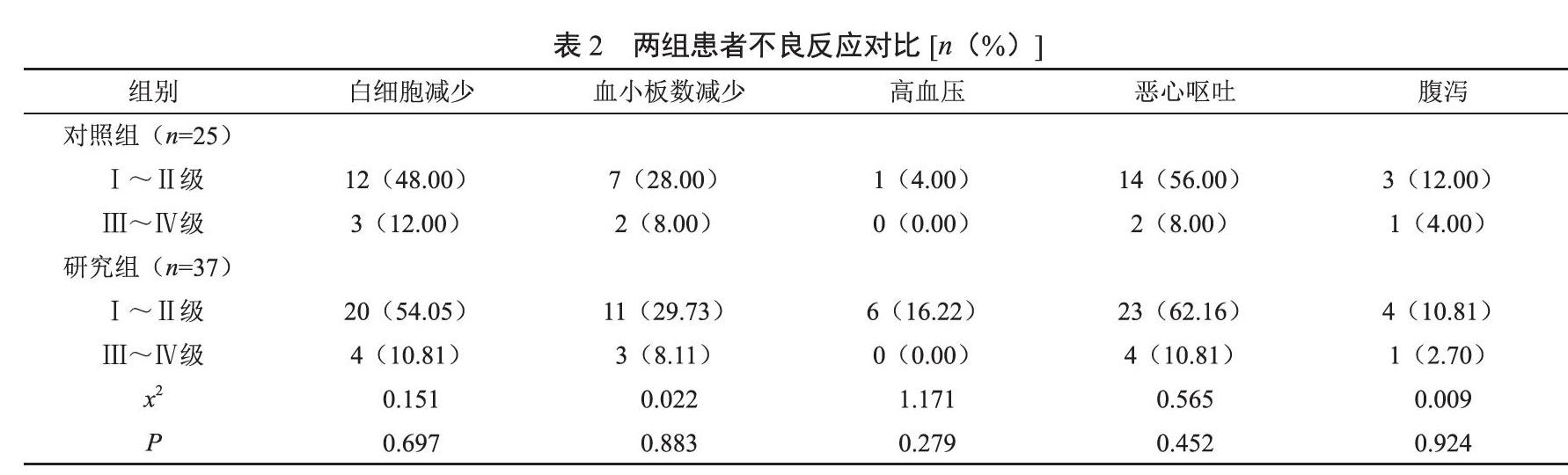
本研究中,两组不良反应主要以Ⅰ~Ⅱ级为主,Ⅲ~Ⅳ级不良反应相对较少。两组不良反应情况对比,差异无统计学意义(P>0.05)。见表2。
图1 化疗方案与联合方案无进展生存曲线
3 讨 论
FOLFIRI化疗方案是一线治疗转移性结直肠癌较为常用的治疗手段,其中伊立替康、四氢叶酸钙、5-氟尿嘧啶是药物常用的药物,其中伊立替康是细胞毒类药物,属于拓扑异构酶Ⅰ抑制剂,伊立替康及其活性代谢物(SN-38)可与拓扑异构酶I-DNA复合物向结合,从而阻止拓扑异构酶I修复DNA缺口,最终导致细胞死亡,且与其他类型抗肿瘤药物无交叉耐药性,具有相加或协同细胞毒作用;5-氟尿嘧啶经过酶转化为5-氟尿嘧啶核苷酸而具有抗肿瘤活性,可抑制DNA合成,最终导致肿瘤细胞死亡;四氢叶酸钙主要用于高剂量甲氨喋呤等叶酸拮抗剂的解救,可抑制DNA合成[4-7]。
在多个肿瘤类型中,血管生成是肿瘤发展的关键性驱动因素,当肿瘤直径≥2 mm时,其存活与生长需要独立的血液供应,当肿瘤血管生成可为肿瘤细胞提供血氧,从而导致肿瘤不断发展、转移[8-9]。由于肿瘤血管系统结构异常,有效的药物无法到达肿瘤组织,因此无法抑制肿瘤的发展与转移。而血管的生成关键调节因素是血管内皮生长因子(VEGF)和其受体的相互作用,高水平VEGF预后不佳[10]。贝伐珠单抗是充足人源化血管内皮生长因子受体(VEGFR)的单克隆抗体,通过与VEGFR相结合,使VEGF失去生物活性,从而减少肿瘤血管形成,有效抑制肿瘤的生长,减少肿瘤血供、氧供和其他营养物质的供应,降低现存血管通透性,从而达到抑制肿瘤生长的目的[11-12]。贝伐珠单抗是首个被批准用于肿瘤治疗的抗VEGF药物,目前主要用于治疗实体肿瘤,如转移性结直肠癌、非小细胞肺癌、乳腺癌、肾癌等[13]。贝伐珠单抗与大部分化疗药物不同,作用于肿瘤微环境,通过与VEGF特异性结合,发挥其作用,很少出现获得性耐药,在化疗的同时可延长患者生存,具有靶向性强、特异性高、毒副作用低的特点[14-15]。本研究结果显示,治疗后6~8周,研究组有效率、疾病控制率均高于对照组;所有患者中位随访时间为1年,无失访,患者出现疾病进展后采用局部治疗或进行二线治疗,其中对照组中位PFS为7.89[95%CI(6.726,9.055)]个月,研究组中位PFS为10.49[95%CI(9.892,11.093)]个月,研究组中位PFS较长,且两组不良反应主要以Ⅰ~Ⅱ级为主,Ⅲ~Ⅳ级不良反应相对较少,两组不良反应无明显差异,表明转移性结直肠癌患者采用贝伐珠单抗联合FOLFIRI方案治疗可提高近期疗效,延长中位PFS,且不会增加不良反应情况。
综上所述,贝伐珠单抗联合FOLFIRI方案治疗转移性结直肠癌可提高临床疗效及疾病控制率,延长患者的中位无疾病进展时间,且联合方案不会增加患者的不良反应发生情况。
参考文献
[1] 杨牡丹,刘晓玲,高 峻.贝伐珠单抗联合化疗治疗转移性结直肠癌疗效和安全性评价[J].中国药物与临床,2016,16(02):255-257.
[2] 冯 芬,胡 斌,招丽蓉,等.血清VEGF水平与贝伐珠单抗联合化疗治疗转移性结直肠癌患者疗效的关系研究[J].现代生物医学进展,2017,17(31):6136-6139.
[3] Stein A,Petersen V,Schulze M,et al.Bevacizumab plus chemo-therapy as first-line treatment for patients with metastatic colorectal cancer:results from a large German community-based observational cohort study[J].Acta Oncol,2015,54(02):171-178.
[4] 陈 燕,陈国明,詹 莹,等.3种化疗方案治疗转移性结直肠癌的成本-效果分析[J].中国药房,2015,25(32):4465-4467.
[5] 房文通,吴 迪,李 茜,等.转移性结直肠癌3种一线化疗方案的药物经济学评价[J].中国医院药学杂志,2017,37(22):2271-2276.
[6] 王正洪,方 亮,蒋明东,等.FOLFOX6方案与FOLFIRI方案治疗晚期结直肠癌的疗效和安全性比较及肿瘤转移的临床特点分析[J].实用医院临床杂志,2018,15(01):91-100.
[7] 招丽蓉,王 巍,伍 婧,等.VEGF的SNP状态预测贝伐株单抗治疗转移性结直肠癌的长期疗效[J].实用癌症杂志,2017,32(04):531-535.
[8] Price TJ,Beeke C,Ullah S,et al.Does the primary site of color-ectal cancer impact outcomes for patients with metastatic disease?[J].Cancer,2015,121(06)830-835.
[9] 代懷杰,许春蕾,汤旭山,等.贝伐珠单抗联合化疗治疗转移性结直肠癌的疗效观察[J].肿瘤预防与治疗,2018,31(03):166-172.
[10] 赵源浩.靶向抗肿瘤单克隆抗体类药物联合常规化疗方案治疗转移性结直肠癌的临床进展[J].中国药房,2018,29(14):2012-2016.
[11] 李晓旭,荣 斌,张金迪,等.贝伐珠单抗联合化疗在结直肠癌中的研究概况[J].中西医结合心血管病电子杂志,2018,06(34):31-32,35.
[12] 李金娜,张 颖,王 颖.不可切除转移性结直肠癌维持治疗的研究进展[J].医学综述,2019,25(07):1322-1326.
[13] 周 明,宋媛媛,陈晓媛,等.贝伐珠单抗注射液生物类似药临床研究设计及审评的考虑[J].中国临床药理学杂志,2019,35(18):2188-2192.
[14] 焦 婉,肖菊香,锁爱莉,等.贝伐珠单抗联合化疗治疗晚期结直肠癌的疗效观察[J].西安交通大学学报(医学版),2016,37(01):108-112.
[15] 韩建雄,骆成俊,杨 波,等.贝伐珠单抗联合不同化疗方案治疗转移性结直肠癌的疗效及安全性分析[J].解放军医药杂志,2019,31(10):27-30.
本文编辑:董 京
