氯化琥珀胆碱注射液不同溶剂中降解杂质的检测
2019-06-06卢伍党
马 延,陈 涛,卢伍党,赵 妮,李 斐
(西安力邦医药科技有限责任公司,陕西 西安 710065)
氯化琥珀胆碱是一种用于静脉给药的超短效去极化骨骼肌肉松弛剂,通用名为琥珀胆碱、司可林,化学名为二氯化2′,2-〔(1,4-二氧代-1,4-亚丁基)双(氧)〕双〔N,N,N-三甲基乙胺〕二水合物。氯化琥珀胆碱可替代乙酰胆碱,与胆碱能受体的运动终板结合产生去极化,肌松(弛缓性麻痹)作用起效很快(静脉注射后1 min内起效),单剂量给药大约可持续4~6 min。氯化琥珀胆碱起效快,肌松完全,代谢迅速,临床得以广泛应用,目前尚无一种非去极化肌松药能完全具备其优点。氯化琥珀胆碱能提供较满意的气管内插管条件,已成为使用时间最长的肌松药,是目前困难插管和紧急插管时唯一被选用的肌松药[1-7]。但由于本品结构中含有酯键,不稳定,易发生水解反应。氯化琥珀胆碱在水溶液中主要水解产生琥珀酸、氯化胆碱和氯化琥珀单胆碱,在丙二醇溶液中主要水解杂质与丙二醇发生反应,产生新的降解杂质。氯化琥珀胆碱中降解杂质文献[8-9]有报道,但杂质检测不全。美国药典委员会(USP)收载的标准中未检测注射液中的杂质,原料药标准中对主要降解杂质琥珀酸、氯化琥珀单胆碱和氯化胆碱进行检测。氯化琥珀胆碱注射液的国内报道文献和标准中,仅对降解杂质氯化胆碱进行了检测。本研究中参照USP标准[9],采用高效液相色谱(HPLC)法检测氯化琥珀胆碱在不同溶剂注射液中的主要降解杂质。现报道如下。
1 仪器与试药
仪器:Thermo Ultimate 3000型高效液相色谱仪,Chromeleon色谱工作站(Thermo Fisher Scientific),Sartorious BS210S型电子天平(德国赛多利斯)。
试药:乙腈(色谱纯,Merck公司,批号为20160824);戊烷磺酸钠(批号为20161028)、氯化钠(批号为20160824)、硫酸(批号为20160504)均为分析纯,购自国药集团化学试剂有限责任公司;氯化琥珀单胆碱对照品(USPReference standard,批号为H01364);琥珀酸对照品(Dr.Ehrenstorfer GmbH,批号为91511);氯化琥珀胆碱对照品(USP Reference standard,批号为R071NO)氯化琥珀胆碱注射液(西安汉丰药业有限责任公司,水溶剂,批号为1701101;丙二醇溶剂,批号为1701161,规格为每支2 mL∶100 mg)。
2 方法与结果
2.1 色谱条件
色谱柱:Shimadzu GL柱(250 mm×4.6 mm,5μm);流动相:缓冲盐(取戊烷磺酸钠3.85 g,氯化钠2.9 g,2 mol/L的硫酸溶液10 mL,置1 000 mL水中,溶解,摇匀)-乙腈(95∶5);检测波长:214 nm;流速:1.0 mL/min;进样量:50μL;柱温:30°C。
2.2 溶液制备
称取琥珀酸对照品约12.5 mg,精密称定,置25 mL容量瓶中,加流动相溶解并稀释至刻度,摇匀,作为贮备液;再各称取氯化琥珀单胆碱对照品和氯化琥珀胆碱对照品约20 mg,精密称定,置10 mL容量瓶中,加流动相溶解并稀释至刻度,摇匀,作为贮备液;分别精密量取贮备液各1 mL,置同一10 mL容量瓶中,加流动相稀释至刻度,摇匀,作为对照品溶液。精密吸取氯化琥珀胆碱注射液2 mL,置10 mL容量瓶中,加流动相溶解并稀释至刻度,摇匀,作为供试品溶液。
2.3 样品杂质测定
取样品,按2.2项下方法配制对照品溶液和供试品溶液,分别进样,并进样空白溶剂。结果,空白溶剂不干扰杂质测定,各杂质与主峰分离度良好,不同溶剂的氯化琥珀胆碱注射液降解产生不同的杂质。详见图1。
2.4 结构解析
USP标准中仅给出降解杂质琥珀酸和氯化琥珀单胆碱。氯化琥珀胆碱注射液(水溶剂)均检出2个杂质,为琥珀酸和氯化琥珀单胆碱,无未知杂质检出;氯化琥珀胆碱注射液(丙二醇溶剂)未检出琥珀酸和氯化琥珀单胆碱,检出2个含量较高的未知杂质,对其进行结构确认。经液相色谱质谱联用(LC-MS)检测,采用ESI离子源,正离子模式进行扫描。在正离子模式下,出现质荷比(m/z)为262.3碎片峰,减少相对分子质量35,推测失去Cl-;出现m/z为197.2碎片峰,推测为氯化胆碱酯键断裂后的[C7H11O5+Na-H]+碎片;m/z为297和299处有M峰和M+2峰的分子离子峰,丰度比为3∶1,符合Cl-特征峰。因此该杂质的相对分子质量为297,与杂质A的相对分子质量一致。在正离子模式下,出现m/z为197.1碎片峰,为单酯断裂的[C7H11O5+Na-H]+碎片峰;同时出现对称的m/z为139.1和255.0碎片峰,分别为对称2个酯键断裂的碎片峰,因此该杂质的相对分子质量为234,与杂质B一致。
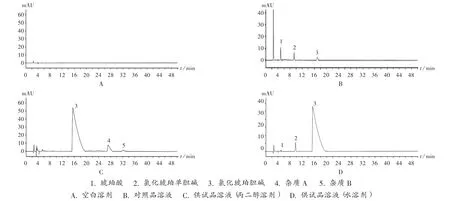
图1 高效液相色谱图
2.5 强制降解
取样品(批号为1701101),按拟订色谱条件进行强制降解试验。
未降解:取样品5支,混匀,移取2.0 mL,置10 mL容量瓶中,加流动相稀释至刻度,摇匀,进样测定。
酸降解:取样品5支,混匀,移取2.0 mL,置10 mL容量瓶中,加1.0mol/L盐酸溶液1mL,放置0.5 h,再加1.0 mol/L氢氧化钠溶液1 mL中和,加流动相稀释至刻度,摇匀,进样测定。
碱降解:取样品5支,混匀,移取2.0 mL,置10 mL容量瓶中,加0.1 mol/L氢氧化钠溶液0.5 mL,放置10 min,再加0.1 mol/L盐酸溶液0.5 mL中和,加流动相稀释至刻度,摇匀,进样测定。
氧化降解:取样品5支,混匀,移取2.0 mL,置10 mL容量瓶中,加30%双氧水1 mL,室温放置1 h,加流动相稀释至刻度,摇匀,进样测定。
光照降解:取光照样品(4 500 lx,72 h)5支,混匀,移取2.0 mL,置10 mL容量瓶中,加流动相稀释至刻度,摇匀,进样测定。
高温降解:取高温样品(40℃,1个月)5支,混匀,室温放置,移取2.0 mL置10 mL容量瓶中,加流动相稀释至刻度,摇匀,进样测定。
由试验结果(图2)可见,样品(水溶剂)中,氯化琥珀单胆碱和琥珀酸主要在酸碱及高温条件下降解产生,且均为主要降解杂质,是由本品结构中的酯键断裂形成。其他条件下,几乎无杂质降解产生。在各降解条件下,杂质之间及杂质与主峰之间的分离度良好。
2.6 重复性试验
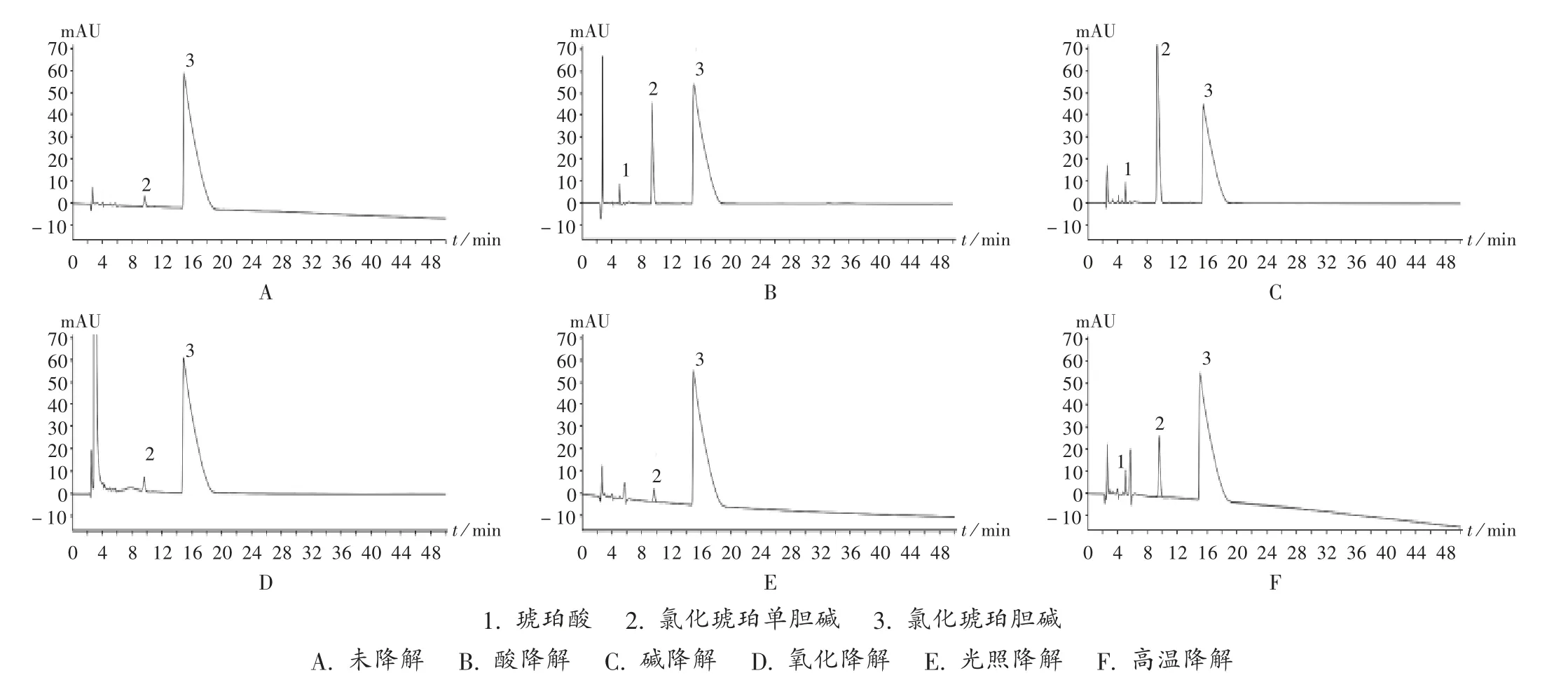
图2 供试品溶液(水溶剂)强制降解高效液相色谱图
取样品(批号为1701101)5支,混匀,移取2 mL,置10 mL容量瓶中,加流动相溶解并稀释至刻度,摇匀,作为供试品溶液,平行配制6份,精密吸取50μL,进样,记录色谱图,按外标法计算杂质量。结果供试品溶液中,琥珀酸含量平均为0.06%,氯化琥珀单胆碱平均含量为1.83%,RSD为0.21%(n=6),表明方法重复性良好。
2.7 稳定性试验
取样品(批号为1701101)5支,混匀,移取2 mL,置10 mL容量瓶中,加流动相稀释至刻度,摇匀,作为供试品溶液,放置室温条件下,分别于0,2,4,6,8 h时进样,记录色谱图,外标法计算各杂质含量。结果供试品溶液随着放置时间的延长,琥珀酸的含量均保持在0.05%,氯化琥珀单胆碱含量逐渐水解增大,在8 h内由1.88%增长至1.93%,增长了0.05%。提示供试品溶液8 h内不稳定,需临用新制。
3 讨论
琥珀酸和氯化琥珀单胆碱的检测中,改变流动相中2 mol/L硫酸溶液的加入量,分别加入10,8,0 mL,不改变其他色谱条件,分别测定流动相的pH,结果为3.09,3.20,4.90。取对照品溶液,分别在不同流动相条件下进样,结果加入硫酸溶液为0 mL时各杂质不能检出,加入10,8 mL时各杂质均有较好的分离度。根据预强制降解试验,样品溶液在酸性条件下稳定性较好,故选择加入2 mol/L硫酸溶液的量为10 mL,流动相pH约为3.1。
杂质A与杂质B为氯化琥珀胆碱注射液(丙二醇溶剂)特有的未知杂质,氯化琥珀单胆碱中的羧基与丙二醇中的醇羟基缩合得到新的杂质(杂质A);琥珀酸中的羧基继续与两分子丙二醇反应,得到新的降解杂质(杂质B)。因此,在氯化琥珀胆碱注射液(丙二醇溶剂)中未检出琥珀酸与氯化琥珀单胆碱,降解产生的琥珀酸与氯化琥珀单胆碱继续参与反应,与丙二醇溶剂脱水得到杂质A和杂质B。氯化琥珀胆碱在体内经水解酶水解后,代谢产生琥珀酸与氯化琥珀单胆碱[10],为体内代谢产物,其安全性可预知。杂质A与杂质B为丙二醇溶剂与降解杂质的反应产物,无相关文献报道其体内的代谢途径与安全性。以丙二醇为溶剂的注射液,临床安全性较低[11]。氯化琥珀胆碱注射液(水溶剂)的产品质量优于氯化琥珀胆碱注射液(丙二醇溶剂)。
