5-氟尿嘧啶卟啉锰/锌配合物的合成、光电性质及抗癌活性
2019-06-06任丽磊彭晓霞王树军肖立伟李泽强
任丽磊 彭晓霞 王树军 肖立伟 李泽强
(廊坊师范学院化学与材料科学学院,廊坊 065000)
5-氟尿嘧啶(5-FU)是临床使用的广谱抗癌药物,它能抑制胸苷酸合成酶,干扰DNA和RNA的合成,已成功应用于肠癌、胃癌、乳腺癌等实体癌的治疗[1]。但由于首过代谢显著、脂溶性低、对癌细胞选择性差,影响抗肿瘤疗效。为了降低其毒副作用,科研工作者对5-FU进行了大量的化学修饰[2-4],结果表明,将5-FU适当衍生化,可提高其选择性,降低毒副作用。
另一方面,卟啉及金属卟啉是一种重要而特殊的物质,具有独特的生物活性。对卟啉进行功能分子设计、合成,在光动力疗法[5-6]及抗癌方面[7-8]备受关注,有着十分广阔的应用前景。利用卟啉对恶性肿瘤有特殊的亲和力[7]这一特点,将其与抗癌药物相连,组成卟啉-抗癌药物的二元体系,是近年来卟啉化学的研究热点之一,这种二元体系包括卟啉-BNCT体系,卟啉-顺铂体系,卟啉-蒽醌体系[9-11]等。研究表明,组合分子的抗癌疗效远远大于2种药物同时使用时的疗效。
基于这些考虑,本文合成了一种新型的5-氟尿嘧啶卟啉化合物(L)及其锰配合物(MnL)、锌配合物(ZnL),对目标化合物的结构进行了表征,研究了它们的光、电性质和抗癌活性。以期为筛选新的抗癌药物提供一定的基础数据支持。
1 实验部分
1.1 仪器和试剂
BRUKER AVANCE 400型核磁共振仪;Agilent 6520 QTOF LC/MS质谱分析仪;Shimadzu-2550紫外-可见分光光度计;WGY-10型荧光分光光度计;Prestige-21傅立叶变换红外光谱仪;CHI660C电化学工作站。
吡咯和 1,2-二溴乙烷 (使用前重蒸),5-氟尿嘧啶(用前重结晶),所有试剂均为市售分析纯。5-邻羟基苯基-10,15,20-三苯基卟啉(A)和 5-邻(2-溴乙氧基)苯基-10,15,20-三苯基卟啉(B)参照文献[12]合成。
1.2 化合物的合成
目标化合物的合成路线如Scheme1所示。

Scheme 1 Synthetic routes of the ligand and complexes
1.2.1 5-(2-(5-氟尿嘧啶-3-基)乙氧基苯基)-10,15,20-三苯基卟啉(L)的合成
在100 mL干燥的圆底烧瓶中,加入130 mg(1 mmol)5-氟 尿 嘧 啶 和 30 mL N,N-二 甲 基 甲 酰 胺(DMF),搅拌使之溶解。加入焙烧过的无水K2CO3166 mg(1.2 mmol),于 80 ℃搅拌 1 h,使 5-氟尿嘧啶生成钾盐。然后加入88 mg(0.12 mmol)5-邻(2-溴乙氧基)苯基-10,15,20-三苯基卟啉,升温至 120 ℃,搅拌,10 h后停止。饱和NaCl溶液盐析,抽滤,蒸馏水洗涤,干燥。粗产品用柱色谱分离,用氯仿与丙酮体积比为4:1的混合液淋洗,收集第二色带,旋蒸干燥,得紫色晶体L 23 mg,产率为22%。1H NMR(CDCl3,400 MHz):δ-2.74(s,2H,Pyrrole N-H),4.10~4.12(t,2H,OCH2),4.30~4.31(t,2H,-NCH2),7.75~7.78(m,4H,ArO-o,m,p-H),7.99(s,1H,C-H in 5-FU),8.21~8.31(m,15H,Ar-H),8.81~8.83(m,8H,Pyrrole-H);HRMSESI(m/z):[M+H]+787.282 6,按 C50H35FN6O3计算值:787.282 7;UV-Vis(CHCl3):λmax/nm(ε/(L·mol-1·cm-1)):418(3.66×105),514(1.46×104),549(4.87×103),589(3.41×103),644(1.95×103);IR(KBr,cm-1):ν(NH)3 471,ν(CH)2 924,ν(CO)1 637,ν(C=C)1 517,ν(COC)1 136。
1.2.2 金属配合物MnL、ZnL的合成
在50 mL圆底烧瓶中,加入25 mg(0.032 mmol)化合物 L、20 mL二氯甲烷,再加入 63 mg(0.32 mmol)氯化锰溶于甲醇制成的饱和溶液,电磁搅拌下回流,反应1 h。冷却,蒸馏水洗涤,分液。有机层水浴蒸干。粗产品用氯仿与丙酮体积比为4∶1的混合液洗脱。收集最浓绿色带,旋蒸浓缩,干燥得绿色固体MnL 17 mg,产率为63.6%。HRMS-ESI(m/z):[M+H]+839.197 0,按C50H33FN6O3Mn计算值:839.197 3;UV-Vis(CHCl3):λmax/nm(ε/(L·mol-1·cm-1)):478(1.67×105),580(1.15×104),622(1.03×104);IR(KBr,cm-1):ν(NH)3 412,ν(CH)2 922,ν(CO)1 637,ν(C=C)1 570,ν(COC)1 240,ν(Mn-N)1 010。
按上述方法,用59 mg(0.32 mmol)乙酸锌代替氯化锰,得紫红色固体ZnL 21.8 mg,产率为80.3%。1H NMR(CDCl3,400 MHz):δ4.12~4.13(m,2H,OCH2),4.22~4.30(m,2H,-NCH2),7.60~7.64(m,4H,ArO-o,m,p-H),7.85(s,1H,C-H in 5-FU),8.18~8.24(m,15H,Ar-H),8.67~8.69(m,8H,Pyrrole-H);HRMS-ESI(m/z):[M+H]+848.188 4,按C50H33FN6O3Zn计算值:848.188 4;UV-Vis(CHCl3):λmax/nm(ε/(L·mol-1·cm-1)):419(3.83×105),547(1.48×104),583(1.23×103);IR(KBr,cm-1):ν(NH)3 471,ν(CH)2 924,ν(CO)1 637,ν(C=C)1 575,ν(COC)1 261,ν(Zn-N)997。
1.3 荧光光谱的测定
以三氯甲烷为溶剂,配制浓度为10μmol·L-1的溶液进行荧光光谱的测定。荧光光谱测试条件:室温,样品池为1 cm×1 cm×4 cm石英池,激发狭缝10 nm,发射狭缝10 nm,激发波长为420 nm,负高压:450 V,扫描范围:550~750 nm。
1.4 电化学测试
本实验中循环伏安法实验条件如下:采用三电极体系,玻碳电极为工作电极,铂电极为对电极,饱和甘汞电极为参比电极。以二氯甲烷为溶剂,样品浓度为 1 mmol·L-1,支持电解质为 0.1 mol·L-1四丁基高氯酸铵,扫描速率50 mV·s-1,测定前用高纯氩气除去体系中的氧气,在氩气气氛下进行循环伏安测试。
1.5 抗癌活性测试
胎牛血清购自北京元亨圣马生物技术研究所,RPMI-1640培养液购自Invitrogen公司,SRB购自Sigma公司,酶标仪(MD公司,M5型)。人肺癌细胞株A549、人肝癌细胞株Bel-7402和人结肠癌细胞株HCT-8均购自中国医学科学院基础研究所细胞中心。
应用磺酰罗丹明B蛋白染色法(SRB法)检测目标化合物对癌细胞(A549、Bel-7402和HCT-8)增殖生长的抑制作用。步骤如下:接种对数生长期细胞于96孔培养板中,37℃,5%(V/V)CO2培养24 h。药物处理孔加入10μL样品溶液 (终浓度:化合物为5 μg·mL-1;混合物为 50 μg·mL-1),阳性药物孔加入终浓度为5μg·mL-1的5-FU进行处理;对照孔加入含等体积溶媒的培养基,37℃,5%(V/V)CO2培养72 h。弃去培养基,轻轻加入100μL 4℃预冷的50%TCA固定细胞。先静置5 min,然后再移至4℃放置1 h。倒掉固定液,蒸馏水洗涤5次去除TCA,空气干燥1 h。每孔加入0.4%SRB溶液80μL,室温染色30 min。弃染液,1%醋酸洗涤5次充分去除未结合的SRB,空气干燥。加入150μL 10 mmol·L-1Trisbase(pH=10.5)溶解,用M5酶标仪于510 nm波长下测定OD值,以下列公式计算细胞生长抑制率(Ri):

2 结果与讨论
2.1 紫外可见吸收光谱
从实验部分紫外数据可以看出:(1)自由卟啉的紫外可见光谱有1个Soret带和4个Q带。在418 nm处的强吸收是Soret带,由电子从基态S0跃迁到最低激发单重态S2产生;在500~650 nm之间的吸收带是Q带,由电子从基态S0跃迁到最低激发单重态S1产生,这些是卟啉的特征光谱;(2)自由卟啉与Mn2+、Zn2+配位后,Q带吸收峰由4个减少到2个。这是由于当金属离子与自由卟啉配位后,形成N-M键,配合物的对称性由D2h变为D4h,且能级靠近,表现为QⅠ、QⅣ谱带消失,同时Soret带发生一定程度的位移。紫外光谱的明显变化说明金属离子与自由卟啉配位,生成了金属配合物[13];(3)与锌配合物相比,锰配合物的Soret带红移至478 nm。分析原因为:2种金属离子的相对离子半径顺序为Mn2+(88 pm)>Zn2+(74 pm), 而电负性 Mn2+(1.5)<Zn2+(1.6),因此锰对外层价电子的束缚力较弱,使得电子更易流向卟啉环,从而使卟啉环上的电子云密度升高,降低电子跃迁所需要的能量,使得Soret带红移较多[14-15]。
2.2 红外光谱
根据文献[16]对3种化合物的红外特征吸收光谱进行了经验归属,数据见实验部分。在自由卟啉中,1 637 cm-1处的吸收峰是5-FU中羰基的伸缩振动吸收峰,同时在1 136 cm-1处有醚键的特征吸收峰,这表明5-FU是以成醚的方式与卟啉侧端的乙氧链相连。而锰配合物、锌配合物的红外光谱数据中,分别在1 010和997 cm-1处出现了新的强伸缩振动吸收峰,该峰归属于卟啉环内Mn-N键和Zn-N键的振动吸收,这表明卟啉环内的2个氢原子被金属取代形成了稳定的金属卟啉配合物。
2.3 核磁共振氢谱
3种化合物的核磁共振氢谱数据列于合成部分,由数据可知:自由卟啉中环内N-H的化学位移在-2.74处,与卟啉环上苯环相连的2个-CH2的化学位移值分别是4.10~4.12和4.30~4.31,5-FU中的C-H在7.99处出现,而5-FU中的N-H由于没有处在屏蔽区,故它的δ为正,应在9以上。但由于受溶剂的影响,积分比又小,该峰未显示出来。再对比锌配合物的氢谱数据,与锌离子配位后,吡咯环内NH的化学位移消失,这是形成金属锌卟啉配合物的重要证据[17]。
2.4 荧光光谱
卟啉具有典型的双荧光性质(S2→S0和S1→S0)。通常,S2→S0荧光只有在低温和极稀的溶液中才能得到,本实验得到的是S1→S0荧光。图1只给出了自由卟啉和锌配合物的荧光发射光谱图。从图1可知,自由卟啉的发射峰位于651和715 nm处,与吸收光谱中Q带成镜像对称。而锌配合物的发射峰出现在599、645 nm处,与自由卟啉相比,荧光特征峰蓝移50~60 nm,同时荧光强度减弱,说明锌配合物具有一定的荧光猝灭性质[17]。这是由于当卟啉环与锌配位后,吡咯N原子通过σ电子的给予与Zn2+形成配位键,同时,Zn2+通过d电子的给予与N原子形成反馈π键,由于形成的反馈π键可以使卟啉环上的共轭体系的π电子密度增加,从而使荧光特征峰峰位发生改变并产生荧光猝灭效应。而具有顺磁性的锰配合物却观察不到荧光发射光谱,这是因为顺磁性金属卟啉配合物中π-π*激发单重态与中心金属的多重态之间发生较强的相互作用,使系间窜跃速率增大,导致最低激发单重态到基态的跃迁几率降低,产生荧光猝灭[18]。

图1 化合物L(a)、ZnL(b)的荧光光谱图Fig.1 Fluorescence spectra of compounds L(a)and ZnL(b)
2.5 电化学性质
为了研究金属离子对卟啉配合物电化学性质的影响,用循环伏安法测试了3种化合物的电化学性质,测定结果及循环伏安曲线分别见表1和图2。从图2可以看出,自由卟啉和锌配合物图形相似,在负电位区间,均呈现2对准可逆的氧化还原峰,对应于2个单电子还原过程。在正电位区间,自由卟啉呈现1对准可逆的氧化还原峰,而锌配合物呈现2对准可逆的氧化还原峰。由表1可以看出,化合物L和ZnL的第一氧化峰和第一还原峰的差值分别为2.24和2.14 V,这与通常用来鉴定卟啉环发生氧化还原反应的ΔE1/2=(2.25±0.15)V相一致[19],也与Zemer等[20]的分子轨道理论计算值2.18 V一致。说明自由卟啉与锌配合物具有相同的电极反应过程,电子转移反应在卟啉环上进行,被氧化成π阳离子或还原为π阴离子,并进一步还原为二价阴离子。

表1 化合物L、MnL和ZnL在CH 2Cl2溶剂中的氧化还原电势数据Table 1 Redox potentials of L,MnL and ZnL in CH 2Cl2 V

图2 化合物L(a)、MnL(b)和ZnL(c)的循环伏安曲线图Fig.2 Cyclic voltammograms of compounds L(a),MnL(b)and ZnL(c)
锰配合物MnL的循环伏安曲线形状与自由卟啉相差很大。基于中心金属离子先于卟啉环氧化还原的观点,可认为其第一还原反应发生在金属Mn上,而其它氧化还原反应发生在卟啉环上[21]。
从表1还可以看出,自由卟啉的第一还原半波电位E1/2为-1.23 V,而锰配合物与锌配合物的第一还原半波电位E1/2分别变为-1.52和-1.40 V,这是因为卟啉配体与金属离子配位后对称性增大,卟啉环更加稳定,还原较难进行,因而需要更高的负电位才能将其还原[22]。
2.6 目标化合物对肿瘤细胞的抑制活性
采用SRB法测定了3个化合物对人肺癌细胞株A549、人肝癌细胞株Bel7402和人结肠癌细胞株HCT-8的抑制活性,结果见表2。从表2可知:(1)样品浓度为10μg·mL-1时,3个化合物对Bel7402和HCT-8均有一定的抑制作用,而MnL对A549有一定抑制作用,自由卟啉和锌配合物对A549的抑制率为负值。3个化合物抑制活性均低于阳性对照药5-氟尿嘧啶,分析原因可能是目标化合物对细胞株的抑制有很强的选择性,对上述3种细胞株选择性较差,对其他细胞株的抑制活性将在后续工作中进行。(2)锰配合物对3种细胞株的抑制率明显高于自由卟啉和锌配合物,抑制率分别为24.32%、34.16%和23.54%,说明卟啉化合物的抗肿瘤活性与中心金属离子有关,锰卟啉对癌细胞的抑制活性较锌卟啉和自由卟啉要高很多,这与文献[16]所得结论一致。(3)锰配合物对人肺癌细胞株A549的抑制率最高,为34.16%,也表明卟啉化合物的抗肿瘤活性具有一定的选择性,对不同的肿瘤细胞的作用机理可能不一样。(4)与文献[16]对比,发现抑制率均低于文献值,说明当苯环上连有给电子基时对这3种细胞株的抑制率较大。与肿瘤DNA作用机制可能是:卟啉化合物优先以空间匹配及静电作用与DNA螺旋小沟中连续的AT(A=腺嘌呤,T=胸腺嘧啶)富碱基区域进行沟槽结合[23],其抗肿瘤活性与它们和DNA相互作用的强弱、结合模式及中心金属离子种类均有关。
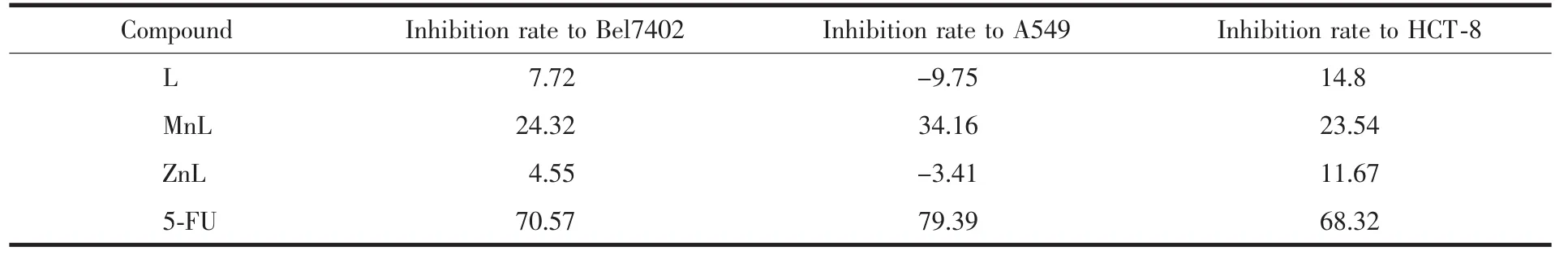
表2 化合物L、MnL和ZnL对A549、Bel7402和HCT-8的抑制率Table 2 Inhibition rates of L,MnL and ZnL to A549,Bel7402 and HCT-8%
3 结 论
通过亲核取代反应合成了5-氟尿嘧啶修饰的自由卟啉L及其金属配合物MnL和ZnL,采用现代分析测试手段表征了其化学结构。研究了目标化合物的荧光性质和电化学性质;测试了它们的抗癌活性。结果表明:金属离子对卟啉的荧光性质有显著影响,锌配合物荧光强度减弱,而具有顺磁性的锰配合物荧光信号消失;锰配合物的循环伏安曲线与自由卟啉、锌配合物不同,除了卟啉环发生氧化还原外,还发生了金属离子的氧化还原反应;锰配合物较其他2种化合物有明显的抗癌作用。
致谢:抑制活性由中国医学科学院药物研究所国家药物筛选中心测试,特此感谢。
