中国肝移植受者代谢病管理专家共识(2019 版)
2019-06-02中国医师协会器官移植医师分会中华医学会器官移植学分会肝移植学组
中国医师协会器官移植医师分会,中华医学会器官移植学分会肝移植学组
成熟的手术技术、规范的术后管理,使中国肝移植受者术后生存率逐步提高。2018 年中国肝脏移植医疗质量报告[1]显示,肝移植术后1 周内死亡率由2015 年的3.7%降至2018 年的2.2%,而良性终末期肝病肝移植受者3 年累积生存率为78.5%,符合杭州标准的肝癌肝移植受者3 年累积生存率为75.8%,可见我国肝移植术后生存率已达到国际领先水平[2]。但代谢病、慢性肾病和心血管疾病等肝移植术后慢性疾病发病率却呈逐年升高趋势。代谢病是肝移植术后常见合并症,包括糖尿病、高血压、血脂异常、高尿酸血症以及肥胖症等,代谢病常具有同时存在且互相影响的特点,而具 备糖尿病、高血压、血脂异常和肥胖症这4 项中的3 项以上者可诊断为代谢综合征。肝移植术后糖尿病发生率为30% ~ 40%[3],高血压发生率超过50%[4],血脂异常为40% ~ 66%[5],高尿酸血症为14% ~ 53%[6-9],肥胖症为18% ~ 30%[10-11],而且 随术后时间的延长呈递增趋势[12]。代谢病是肝移植术后发生慢性肾病、心血管疾病、感染和非酒精性脂肪肝的重要危险因素,在很大程度上影响受者的生存质量和长期存活[13-14],而大多数代谢病可通过早期干预进行预防和治疗。本共识旨在为中国肝移植受者术后代谢病的防治提供建议,以期改善受者的长期生存。
1 肝移植受者代谢病防治建议
有效的免疫抑制治疗是肝移植后移植物长期存活的最重要保障[14],但免疫抑制剂与代谢病存在密切联系,长期使用免疫抑制剂会加重或促进肝移植后代谢病的发生和发展。不同免疫抑制剂对代谢病具有不同影响,详见表1。
研究发现,肝移植受者使用巴利昔单抗进行免疫诱导,并使用含霉酚酸(mycophenolic acid,MPA)的无糖皮质激素或早期撤除方案,以及MPA 合并减量钙调磷酸酶抑制剂(calcineurin inhibitor,CNI)的免疫抑制方案,均能在保证免疫抑制疗效的基础上,减少免疫抑制剂所致代谢病的发生和不良影响[15-23]。因此,肝移植术后代谢病的管理,应在改善饮食结构和生活方式的基础上,根据受者个体差异选择合适的免疫抑制剂,必要时使用药物治疗。免疫抑制方案调整需肝移植随访医师参与 其中。
建议1:肝移植术后代谢病的防治应以改变饮食习惯和生活方式为基础,重视免疫抑制剂的不良影响,提倡个体化用药,巴利昔单抗联合含有MPA 类药物的无糖皮质激素或CNI 最小化方案是可行的。
1.1 糖尿病的防治:肝移植术后糖尿病(posttransplant diabetes mellitus,PTDM)包括既往存在的糖尿病和移植后新发糖尿病(new-onset diabetes mellitus after transplantation,NODAT)[15]。因部分 移植受者术前未进行规范的糖尿病诊断,故近年来以PTDM 统一表示移植后糖尿病,参照 2019 年美国糖尿病协会制定的糖尿病和糖尿病前期诊断标准[24-25]。肝移植术后PTDM 发生率为30% ~ 40%[3,26]。大多数PTDM 以胰岛素抵抗为特点,症状发展缓慢,具有2 型糖尿病的特点,但也 可出现酮症酸中毒等1 型糖尿病特征性的严重并发症[27]。PTDM 的发生增加肝移植术后排斥反应、感染、心血管事件和死亡风险[28-29]。2017 年欧洲COMMIT(consensus on managing modifiable risk in transplantation)共识推荐肝移植术后血糖控制目标:空腹血糖<6.7 mmol/L(120 mg/dl),餐后血糖 8.88 mmol/L (160 mg/dl)或糖化血红蛋白 (hemoglobin A1c,HbA1c)<7%[23]。
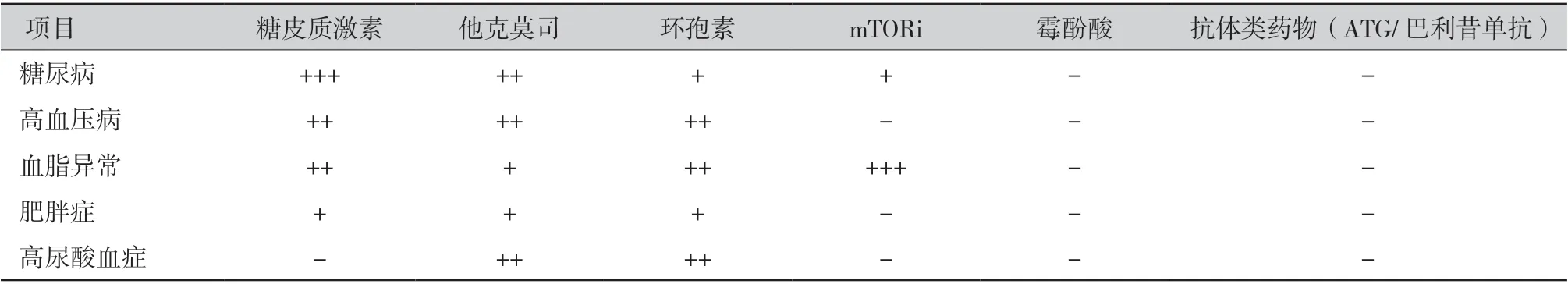
表1 免疫抑制剂对肝移植术后代谢病的不良影响
PTDM 主要发病机制包括胰岛素敏感性降低和β 细胞功能减退。多种因素与PTDM 发病相关,如丙型肝炎病毒感染、糖尿病家族史、体质量指 数(body mass index,BMI)过高和免疫抑制剂等,而免疫抑制剂中糖皮质激素、他克莫司是最重要的致病因素,而环孢素和包括西罗莫司及依维莫司在内的哺乳动物雷帕霉素靶蛋白抑制剂(mammalian target of rapamycin inhibitor,mTORi)对血糖的影响则相对不明显[3,30]。有研究指出,肝移植术后3 个月他克莫司血药浓度>8 ng/ml 是PTDM 的独立危险因素[31]。另一方面,糖尿病的分子遗传学研究越来越广泛,部分研究成果被应用于糖尿病的早期基因诊断、临床治疗和初级预防策略中。基因诊断为研究其发病机制提供了重要线索,供、受者糖尿病相关的基因多态性也被证实与PTDM 相关。 浙江大学医学院附属第一医院和上海交通大学医学院的研究分别指出,供、受者基因多态性ADIPOQ rs1501299[32]和SUMO4 rs237025[33]与PTDM 相关。
饮食疗法及改变生活方式是治疗PTDM 的基础,包括锻炼和减重(若受者肥胖),同时调整免疫抑制剂方案。有研究结果显示,泼尼松剂量每增加0.01 mg/kg,PTDM 的发生风险上升5%[34]。与传统含糖皮质激素免疫抑制方案相比,无糖皮质激素或早期撤除方案可显著降低PTDM 发生率,而巴利昔单抗和以吗替麦考酚酯(mycophenolate mofetil,MMF)为代表的MPA 类药物的使用则使无糖皮质激素或早期撤除方案安全可行[35-36]。 另有研究结果显示,合并PTDM 的受者,将他克莫司转换为环孢素后,空腹血糖和HbA1c 水平明显下降[37-38]。血糖控制不佳(餐后血糖峰 值>11 mmol/L 和HbA1c >9%)的肝移植受者,建议将他克莫司转换为环孢素,或调整为MMF 联合低剂量他克莫司[23,27]。
肝移植术后早期,当移植肝功能尚未完全恢复时,若合并明显的高血糖症状或HbA1c 明显升高,应予胰岛素治疗[39]。根据现有的证据,胰岛素作为预防性治疗策略时,术后第1 周控制平均血糖<10 mmol/L且HbA1c<8%是必要和安全的[40]。 同时大剂量使用糖皮质激素时,胰岛素治疗是最佳选择。随着肝移植术后时间的延长,胰岛素用量降至24 U/d 以下且移植肝功能正常时,可给予口服降糖药物[15]。对于若通过改变饮食习惯、加强运动以及调整免疫抑制方案等方法均未能有效控制血糖的PTDM 受者,也需给予口服降糖药物。可根据肾功能选择口服降糖药物:二甲双胍或磺酰脲可用于肾功能正常的肝移植受者,一般认为肾小球滤过率>60 ml/min 时,可安全使用双胍类药物;在肾功能受损的情况下,首选磺酰脲类药物(如格列吡嗪和格列美脲)[41]。
建议2:肝移植术后血糖控制目标:空腹血糖<6.7 mmol/L(120 mg/dl),餐后血糖<8.88 mmol/L (160 mg/dl)或HbA1c <7.0%。
建议3:糖皮质激素最小化及MPA 联合CNI减量的方案有助于减少PTDM 的发生。血糖控制不佳 (餐后血糖峰值>11 mmol/L 和HbA1c >9%)的肝移植受者,建议将他克莫司转换为环孢素。
建议4:术前进行供、受者糖尿病相关基因多态性检测以评估PTDM 发生风险。
建议5:肝移植术后静脉使用糖皮质激素以及移植肝功能未完全恢复时,建议胰岛素治疗。胰岛素用量降至24 U/d 以下,移植肝功能正常时可给予口服降糖药物。肾功能正常时可以选用二甲双胍或磺酰脲类药物,肾功能受损时首选磺酰脲类药物(如格列吡嗪和格列美脲)。
1.2 高血压的防治:肝移植术后超过50%的受者发生高血压,并随着生存时间的延长,发生率逐年上升[4]。约有47%的肝移植受者高血压发生在移植后的1 ~ 3 个月内[42]。高血压的发生是肝移植后并发肾功能不全和心血管疾病的主要危险因 素[43-44]。2017 年,欧洲COMMIT 共识推荐肝移植术后血压控制目标值为130/80 mmHg(1 mmHg=0.133 kPa,下同)[23],肾功能受损的受者高血压的控制目标为125/75 mmHg[45]。
肝移植术后高血压的病因复杂。肝移植受者伴发肥胖症或糖尿病时,术后发生高血压的风险明显增加[46-47]。免疫抑制剂的使用(如CNI 及糖皮质激素)是肝移植术后新发高血压的主要危险因素。CNI 诱发高血压的主要机制在于诱导体循环阻力增加并进一步影响肾脏血流,糖皮质激素主要通过其盐皮质激素效应增加血管阻力和心肌收缩力[14]。其他危险因素有高龄、遗传背景等[48]。肝移植术后高血压的预防应首先全面评估受者相关的危险因素,并积极干预已有的危险因素,如改变不良生活方式、限盐饮食、控制体质量和适当运动等[46]。制定个体化免疫抑制方案,通过调整免疫抑制方案可以一定程度上降低高血压发生风险,如应用最小剂量可能致高血压的免疫抑制剂(CNI 和糖皮质激素),CNI 中环孢素较他克莫司引起高血压的风险更高[49]。因此,以MMF 为代表的MPA 联合减量CNI 方案可以使肝移植术后新发高血压的风险明显下降,无糖皮质激素或早期撤除方案也能显著降低术后新发高血压的发生率[50-53]。
如果改变生活方式和调整免疫抑制方案均不能达到目标血压水平,则需要辅以降压药物治 疗[45]。常用的降压药物包括钙通道阻滞剂 (calcium channel blockers,CCB)、血管紧张素转化酶抑制 剂(angiotensin-converting enzyme inhibitor,ACEI)、血管紧张素Ⅱ受体拮抗剂(angiotensin Ⅱ receptor blocker,ARB)、β 受体阻滞剂以及利尿剂。CCB 由于可以拮抗CNI 引起的血管收缩作用, 常作为无蛋白尿高血压受者的一线用药,其中二氢吡啶类CCB(如硝苯地平、氨氯地平和尼卡地平等)与免疫抑制剂之间的相互作用相对较少,可优先选用[54]。但非二氢吡啶类CCB (维拉帕米和地尔硫)可显著增加CNI 的生物利用度,需谨慎使用。对于合并蛋白尿的高血压受者,ACEI 或ARB 类药物可作为一线用药[50],但当受者肾功能显著受损时应慎用。利尿剂治疗主要适用于移植早期循环血容量过多的受者[55]。如果单药血压控制不理想,可选择CCB 与ACEI 或ARB 联用。
建议6:肝移植术后血压控制目标为< 130/80 mmHg,伴肾功能损伤时血压控制目标为<125/75 mmHg。
建议7:糖皮质激素最小化以及MPA 联合CNI 减量的方案有助于减少肝移植术后高血压的 发生。
建议8:CCB、ACEI 和ARB 应作为一线降压药物。ACEI 和ARB 适用于合并蛋白尿的肝移植术后高血压受者。
1.3 血脂异常的防治:肝移植术后血脂异常的发生率为40%~66%,是受者罹患心血管疾病的重要危险因素之一[5]。肝移植受者血脂异常的治疗目标低密度脂蛋白胆固醇(low density lipoprotein chesterol,LDL-C)<2.6 mmol/L(100 mg/dl), 存在心血管危险因素受者目标LDL-C <1.8 mmol/L (70 mg/dl)[23]。
血脂异常的危险因素包括饮食习惯、年龄、 体质量、其他代谢病(如糖尿病、高血压和肥胖症等)、遗传因素以及药物,其中肝移植术后使用免疫抑制剂是导致血脂异常的主要因素,尤其是mTORi、CNI 以及糖皮质激素的使用[5]。不同CNI 对血脂的影响不同,环孢素对血脂的影响较他克莫司大,mTORi 对血脂的影响比糖皮质激素大。mTORi 导致血脂异常的机制为增加肝脏脂质合成、降低脂质清除以及抑制胰岛素和胰岛素样生长因子相关信号通路[56];而CNI 类主要为降低胆汁酸合成、下调LDL 受体功能、抑制胆固醇清除、诱导胆固醇合成以及促进极低密度脂蛋白转变 为LDL[5]。
肝移植术后血脂异常的治疗首选改变生活方式和饮食习惯,并调整免疫抑制方案。改变生活方式和饮食习惯包括:戒烟、限盐和限制饮酒量;减少饱和脂肪酸和胆固醇的摄入,选择能够降低LDL-C 的食物,如植物甾醇(2 g/d)、可溶性纤维 (10 ~ 25 g/d);超重或肥胖者减轻体质量5 % ~ 10%; 有规律的体力锻炼,包括足够的中等强度锻炼, 以保证每日至少消耗836.8 kJ 热量。在免疫抑制剂中,以MMF 为代表的MPA 类药物对血脂无影响。有研究表明,血脂异常的肝移植受者在MMF治疗基础上,撤除或减量CNI,总胆固醇(total cholesterol,TC)和甘油三酯(triglycerides,TG)均下降[57]。MMF 联合他克莫司的免疫抑制方案导致血脂异常发生率显著低于mTORi 联合他克莫司治疗方案[21]。难治性血脂异常(目前尚无明确定义),一般认为包括以下几种情况:TG ≥5.65 mmol/L (500 mg/dl)或(和)LDL-C ≥4.92 mmol/L(190 mg/dl); 或 经 过 规 范 降 脂 治 疗TG 或LDL 仍 升 高 者[58]。 对于难治性血脂异常或确定由免疫抑制剂导致的血脂异常,治疗上应考虑调整免疫抑制方案,可考虑停用mTORi 或将环孢素更换为他克莫司,或采用CNI 减量联合MMF 方案[15]。
若通过改变饮食习惯、加强运动,以及调整免疫抑制方案均未能有效控制血脂水平时,需要开始药物治疗。对于肝功能正常受者,可应用降脂药;而对于肝酶>正常3 倍的受者,需停用该药,监测肝功能指标,明确肝功能异常病因,再决定是否使用降脂药[5]。高胆固醇血症治疗首选他汀类药物,治疗时需警惕不良反应,尤其是潜在的肝毒性和肌病。大部分他汀类药物和CNI 类药物均经过细胞色素P450 酶代谢,因此在使用过程中,需监测免疫抑制剂血药浓度,及时调整用量。辛伐他汀与CNI 代谢相互影响较大,不推荐使用。对于胆固醇正常的高甘油三酯血症,首选鱼油治疗,如果效果不理想,可以加用吉非贝齐或非诺贝特[5]。
建议9:肝移植术后血脂控制目标为低密度脂蛋白胆固醇(LDL-C)<2.6 mmol/L(100 mg/dl),对于存在心血管危险因素的受者目标LDL-C < 1.8 mmol/L(70 mg/dl)。
建议10:存在血脂异常的肝移植受者,应考 虑减少和撤除糖皮质激素,谨慎使用mTORi,并严 密监测血脂指标。对于难治性血脂异常或确定由免疫抑制剂导致的血脂异常,应首先调整免疫抑制方案,可考虑停用mTORi 或将环孢素更换为他克莫司,或采用联合MPA 的CNI 减量方案。
建议11:高胆固醇血症药物治疗首选他汀类药物,用药前后需密切监测肝功能、肌酸激酶和免疫抑制剂血药浓度。
建议12:单纯高甘油三酯血症治疗首选鱼油。如效果不理想,可以加用吉非贝齐或非诺贝特。
1.4 高尿酸血症的防治:肝移植后高尿酸血症发病率为14% ~ 53%[6-9]。高尿酸血症可致痛风、尿酸 结石及肾功能受损,且与其他代谢病(如糖尿病、高血压和慢性肾病等)密切相关[6-7]。肝移植术后高尿酸血症导致的慢性肾病是其主要危害之 一[7]。高尿酸血症的控制目标为:对于存在心血管危险因素和合并心血管疾病者,血尿酸应长期控制在360 μmol/L 以下;对于有痛风发作者,则需将血尿酸长期控制在300 μmol/L 以下[59]。
肝移植术后高尿酸血症的发生可能与免疫抑制剂使用、移植前高尿酸血症病史以及利尿剂的使用有关[6-7]。目前证实明确与高尿酸血症有关的免疫抑制剂是CNI,其主要通过降低肾小球滤过率和增加肾小管对尿酸的重吸收,导致尿酸排泄减 少[60-61]。部分文献报道,移植后服用环孢素较服用他克莫司的受者HUA 发病率更高[61-63],但也有文献报道二者无差异[64]。
肝移植术后高尿酸血症的一般治疗包括改变不良生活方式(如低嘌呤饮食、多饮水、适当碱化尿液和多运动等),同时筛查相关并发症,与专科医师合作,积极治疗与血尿酸升高相关的代谢性及心血管危险因素[65]。尽量避免使用升高血尿酸的药物,有文献报道CNI 减量联合MMF、或将CNI 转换为mTORi、或将他克莫司由普通剂型转换为缓释剂型,血尿酸降低[66-67]。
如一般治疗未能有效控制高尿酸血症,则需要开始药物治疗,可以选用促进尿酸排泄和抑制尿酸生成的药物[65]。其中促进尿酸排泄药物苯溴马隆、非诺贝特和氯沙坦及抑制尿酸生成药物别嘌醇、 非布索坦和托匹司他均能有效降低血尿酸水平, 且目前尚无影响免疫抑制剂浓度的报道[6-8,59,68]。严重肾功能不全的患者应谨慎使用别嘌醇和苯溴马隆,可选择非布索坦或托匹司他治疗,但当肝功能严重受损时,谨慎使用非布索坦或托匹司他。氯沙坦和非诺贝特分别为降压和降脂药物,同时都具有降尿酸的作用,当高尿酸血症合并高血压或血脂异常时可优先选用[59]。
仅有观察性的研究显示降尿酸治疗后,血尿酸降低同时血清肌酐下降[6,8],降尿酸治疗是否可有效改善肝移植受者肾功能及病死率尚需进一步的研究证实。
建议13:肝移植术后血尿酸控制目标:高尿酸血症合并心血管危险因素和心血管疾病的受者,血尿酸长期控制在360 μmol/L 以下;有痛风发作的受者,血尿酸长期控制在300 μmol/L 以下。
建议14:肝移植术后CNI 减量或撤除,并联合MPA 类药物或mTORi 治疗有助于降低血尿酸 水平。
建议15:根据高尿酸血症的分型诊断标准选用促进尿酸排泄或抑制尿酸生成的药物。严重肾功能不全者可选择非布索坦或托匹司他治疗,肝功能严重受损时选择苯溴马隆治疗。合并高血压时可选择氯沙坦,合并血脂异常时可选择非诺贝特治疗。
1.4 肥胖症的防治:肝移植术后新发肥胖症的定义为肝移植术后随访过程中首次出现BMI ≥30 kg/m2[69]。 据文献报道,肝移植术后肥胖症发生率为18% ~ 30%[10-11],其中成人肝移植术后1 年、3 年肥胖症发生率分别为23.7%和30.6%[10,70],儿童受者分别为19%和18%[11]。肥胖症与肝移植预后密切相关,肥胖症受者的整体生存率会降低[71]。同时,与心血管不良事件、术后感染和呼吸衰竭的发生密切相关[69,72]。肝移植术后BMI 应控制在30 kg/m2以下,并尽量控制在25 kg/m2以内。
导致体质量增加和肥胖的机制主要由遗传、 生理、行为和环境因素的复杂相互作用驱动[73]。移植术前存在肥胖是术后出现肥胖症的一个重要危险因素[74],其他危险因素包括遗传因素、心理因素(如抑郁症)、年龄、性别、种族、饮食习惯、运动习惯和免疫抑制剂等[69,75]。免疫抑制剂中,长时间和大剂量使用糖皮质激素是影响受者体质量的重要因素[10,69],标准剂量CNI 较MMF 或mTORi 联合CNI 减量方案受者体质量增加更多[76]。有与服用他克莫司的受者相比,服用环孢素的受者肝移植术后1 年时更容易增重[70]。
肥胖症的治疗包括改变生活方式(饮食/锻炼),在适当的情况下进行药物治疗和手术,以达到BMI <25 kg/m2[23]。对高危肝移植受者建议减少或停用糖皮质激素,也可考虑早期积极将他克莫司转换成环孢素,必要时需早期引入药物治疗和减肥手术[77]。治疗肥胖症的药物可分为非中枢性减重药物(奥利司他)、中枢性减重药物(拟交感胺类药物,如芬特明;5-羟色胺能药物,如氯卡色林)以及兼有减重作用的降糖药物(如二甲双胍和利拉鲁肽)[78]。对于顽固性肥胖症的肝移植受者,仅依靠饮食、运动及药物很难取得显著效果,减重 手术是主要治疗方案,包括Roux-en-Y 胃旁路术、胃袖状切除术以及胆道胰腺分流手术等[79-80]。 此外,还可使用内镜治疗,限制摄入食物与胃肠道黏膜的接触,从而限制吸收,达到减肥的目的[77]。但手术和内镜治疗在肝移植受者中均尚未形成 规范[77,80]。
建议16:肝移植术后体质指数(BMI)控制目标为<25 kg/m2。糖皮质激素最小化和CNI 减量方案有助于控制肝移植后体质量增加,行为治疗和药物治疗无效的肥胖症受者可考虑使用外科手术 治疗。
2 肝移植受者代谢病的监测
肝移植受者需要重视代谢病的监测,根据情况及时调整免疫抑制方案的,应至少每6 个月评估 1 次,以减少药物长期不良反应,并重视可能继发的心血管事件及肾功能损害。肝移植术后需将血糖、血压、血脂、血尿酸和BMI 等代谢指标作为常规随访监测项目。对PTDM 受者而言,进行自我血糖监测是基本形式,HbA1c 是反映长期血糖控制水平的金标准[41]。对于高血压受者,同样鼓励家庭测量血压,而LDL-C、TG、TC 和血尿酸水平 是血脂异常和高尿酸血症肝移植受者的基本监测项目[15,81],肝移植术后需长期监测体质量变化。
对已诊断糖尿病、高血压、血脂异常、高尿酸血症或肥胖症的肝移植受者,除上述基础监测项目外,还需酌情进行针对性检查,详见表2。这些针对靶器官功能的检查,可及时发现和诊断可能继发于代谢病的心脑血管疾病、慢性肾病、视网膜病变和痛风性关节炎等,从而改善肝移植受者的长期生存。代谢病治疗后需要每3 个月对疗效进行评 估[82],规范化的监测需要移植科医师的重视和受者的配合。

表2 肝移植术后代谢病监测
建议17:长期生存的肝移植受者需要重视代谢病的监测。
建议18:免疫抑制方案至少每6 个月评价1 次,以减少长期不良反应,酌情进行调整。
建议19:血压、血脂、血糖、血尿酸及BMI的监测在术后第1 年每3 个月1 次,此后每年1 次。代谢病治疗后每3 个月对疗效进行评价1 次。
组长:郑树森(浙江大学医学院附属第一医院);徐骁(浙江大学医学院附属第一医院)
编审委员会成员:陈孝平(华中科技大学同济医学院附属同济医院);陈实(华中科技大学同济医学院附属同济医院);严律南(四川大学华西医院);丁义涛(南京大学医学院附属鼓楼医院);杨广顺(海军军医大学附属东方肝胆外科医院);徐骁 (浙江大学医学院附属第一医院);陈规划(中山大学附属第三医院);彭志海(厦门大学附属翔安医院);朱继业(北京大学人民医院);李波(四川大学华西医院);李玉民(兰州大学第二医院);王正昕(复旦大学附属华山医院);卢实春(中国人民解放军总医院第一医学中心);叶啟发(武汉大学中南医院);吕国悦(吉林大学第一医院);朱志军(首都医科大学附属北京友谊医院);刘军(山东省立医院);刘振文(中国人民解放军总医院第五医学中心);刘景丰(福建医科大学附属第一医院);齐海智(中南大学湘雅二院);孙倍成(南京大学医学院附属鼓楼医院);杜国盛(中国人民解放军总医院第八医学中心);李立(昆明市第一人民医院);李宁(首都医科大学北京佑安医院);李齐根 (南昌大学第二附属医院);李启勇(树兰(杭州)医院);杨家印(四川大学华西医院);时军(南昌大学第一附属医院);何晓顺(中山大学附属第一医院);张峰(南京医科大学第一附属医院);张水军(郑州大学第一附属医院);张雷达(陆军军医大学西南医院);陈知水(华中科技大学同济医学院附属同济医院);明英姿(中南大学湘雅三院);郑虹(天津市第一中心医院);郎韧(首都医科大学北京朝阳医院);夏强(上海交通大学医学院附属仁济医院);黄建钊(贵州省人民医院 );董家鸿(北京清华长庚医院);景鸿恩(青海大学附属医院);傅志仁(海军军医大学长征医院);温浩(新疆医科大学第一附属医院);窦剑(河北医科大学第三医院);窦科峰(空军军医大学西京医院); 臧运金(青岛大学附属医院);霍枫(南部战区总医院);梁廷波(浙江大学医学院附属第一医院);张珉(浙江大学医学院附属第一医院);吴健(浙江 大学医学院附属第一医院);蒋文涛(天津市第一中心医院);郭文治(郑州大学第一附属医院);汪国 营(中山大学附属第三医院);杨扬(中山大学附属第三医院);钟林(上海交通大学附属第一人民医院);牛玉坚(中国人民解放军总医院第三医学中心);卢倩(北京清华长庚医院)
执笔人:沈恬(浙江大学医学院附属第一医院);庄莉(树兰(杭州)医院);孙晓东(吉林大学第一医院);戚晓升(上海市第一人民医院);王智慧(郑州大学第一附属医院);李瑞东(复旦大学附属华山医院);常文秀(天津市第一中心医院);杨家印(四川大学华西医院);杨扬(中山大学附属第三医院);徐骁(浙江大学医学院附属第一医院)
