CT和MR联合诊断不同级别软骨肉瘤的影像特征对比分析
2019-05-28董江宁李乃玉王传彬韦树华
唐 军 董江宁* 李乃玉 王传彬 韦树华 韦 超 方 昕 曹 峰
软骨肉瘤是一类起源于软骨细胞或向软骨分化的间叶组织细胞来源恶性骨肿瘤,发病率仅次于骨肉瘤。病理学根据细胞异型性、分化程度及侵犯状况等分为低级别和中高级别软骨肉瘤[1]。不同级别软骨肉瘤治疗方法不同,且患者预后与肿瘤分级密切相关。影像学检查是软骨肉瘤主要无创性诊断方法,术前CT和MR区分不同级别软骨肉瘤,对于指导治疗及判断预后尤为重要。目前,常采用临床、影像和病理相结合综合方法判断软骨肉瘤级别[2]。本研究通过研究不同级别软骨肉瘤CT与MR联合检查的影像表现特征,探讨其区分不同级别软骨肉瘤的价值,以期提高软骨肉瘤术前诊断水平。
1 资料与方法
1.1 一般资料
回顾性搜集2012年1月至2017年12月中国科学技术大学附一院西区安徽省肿瘤医院收治的22例软骨肉瘤患者资料,其中男性12例,女性10例;年龄8~69岁,平均年龄(45.87±16.54)岁。按照病理分级分为低级别组(8例)和中高级别组(14例)。术前两组患者中15例行CT和MR联合检查,5例仅行CT,2例仅行MR检查,对两组影像学特征在高低级别软骨肉瘤分布进行统计分析。临床症状和体征主要表现为肿块或伴疼痛,部分患者病灶处局部功能障碍。患者性别、年龄及病灶最大径、个数在低级别和中高级别两组间均无显著统计学差异,具有可比性。
1.2 纳入与排除标准
(1)纳入标准:①患者CT、MR影像检查与病理大标本资料齐全;②病灶在中轴骨/扁平骨或四肢长管状骨。
(2)排除标准:①患者临床、影像和病理检查资料不全;②CT和MR图像不符合诊断标准。
1.3 仪器设备
采用Discovery CT 750 HD型64排CT(美国GE公司);MR设备为HDxt 3.0T型超导MR扫描仪(美国GE公司)。
1.4 影像检查
采用Discovery CT750 HD型64排CT,依据病变部位常规平扫或平扫加增强。扫描参数:管电压120 kV,管电流300~350 mAs,螺旋扫描模式。增强扫描前禁食6 h以上,增强采用高压注射器经肘前正中静脉注射欧乃派克75~100 ml(300 mgI/ml),注射速率2.0~2.5 ml/s,行动脉期(18~25)s、静脉期(45~65)s双期扫描。CT原始图像采用1.25 mm薄层重建,导入GE ADW4.5工作站行多平面重建及容积再现(volume rendering,VR)技术等后处理。采用HDxt 3.0型T超导MR扫描仪,依据患者病变部位选择不同的线圈,常规T1WI序列:重复时间(repetition time,TR)450~700 ms,回波时间(echo time,TE)15~20 ms,T2WI序列:TR200~4000,TE80~100 ms,T2WIfs或STIR序列:2000~4000 ms,TE50~100,TI130~150 ms,DWI:b值为800 s/mm2,激励次数1次,TR4300 ms,TE45~55 ms。加扫矢状位、冠状位T1WI、T2WIfs。增强后行矢状位或冠状位LAVA-FLex扫描,对比剂为钆-塞酸二钠(Gd-DTPA),注射速率1.5~2.0 m/s,剂量0.1 mmol/kg。
1.5 图像处理与观察评价指标
(1)所有患者CT和MR数据传至GE AW4.5工作站及PACS系统。在未知病变病理分级情况下,由2名擅长骨肌软组织影像诊断主治医师对CT、MR影像特征进行独立分析和测量。如果意见不统一,需由高级职称医师重阅协商后决定。
(2)观察分析CT、MR影像表现和特征,包括骨髓或软组织水肿、骨膨胀、皮质增厚、皮质破坏、骨膜反应、软组织肿块、边缘及分隔样强化以及片状无强化区的存在与否;分析影像钙化或软骨化的程度:①<1/3为少量钙化;②≥1/3为中、多量钙化,测量病灶的长径。
1.6 统计学方法
采用IBM SPSS 22.0软件进行统计学处理,计量资料经Kolmogorov-Smirnov检验符合正态分布,以x-±s表示,采用独立样本t检验;计数资料用率表示,采用Fisher确切概率法分析,以P<0.05为差异有统计学意义。
2 结果
2.1 两组不同级别软骨肉瘤发生部位比较
低级别组的8例患者中,发生部位为股骨5例,胫骨1例,尺骨1例,胸椎椎体1例;病理为高分化4例,不典型软骨肉瘤2例,普通型髓内软骨肉瘤1例,粘液型1例。中高级别组的14例患者中,部位为骨盆5例,骶尾部2例,肩胛骨2例,肱骨1例,股骨1例,腓骨1例,指骨1例,肋骨1例;病理为粘液型2例,余均为2~3级软骨肉瘤。
2.2 两组不同级别软骨肉瘤CT和MR影像特征比较
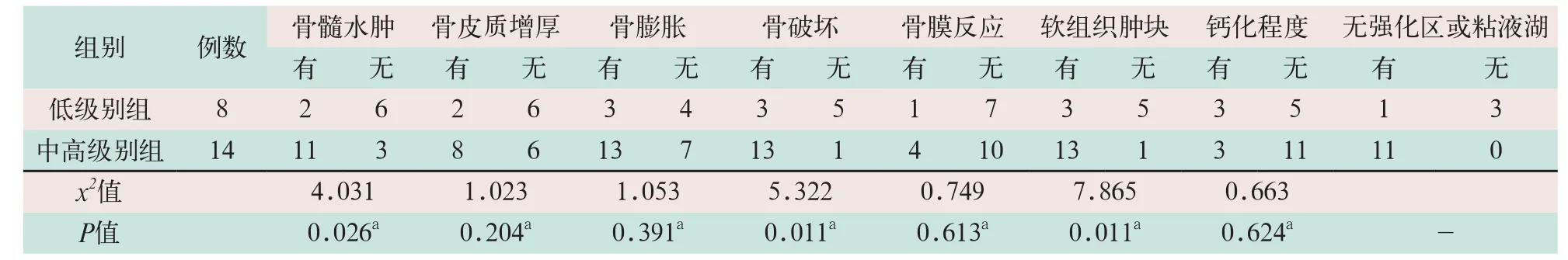
表1 两组软骨肉瘤组间CT和MR影像特征分布比较
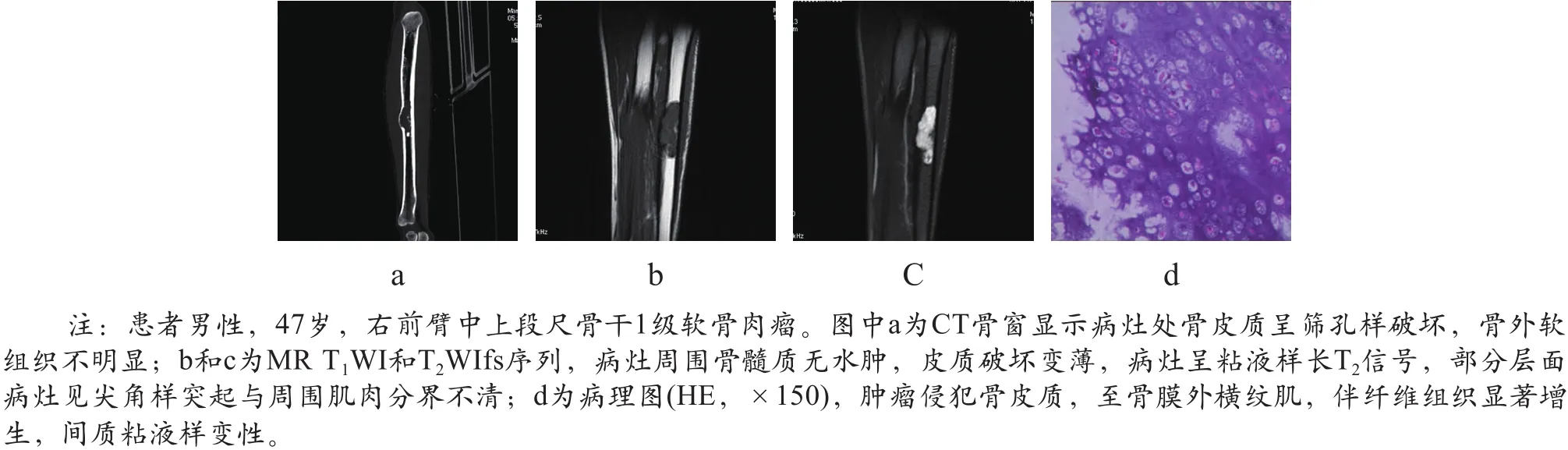
图1 右前臂中上段尺骨干1级软骨肉瘤CT和MR影像及病理图
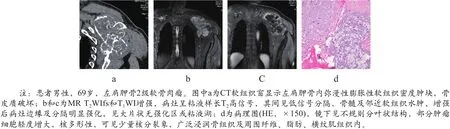
图2 左肩胛骨2级软骨肉瘤CT和MR影像及病理图

图3 左髂骨3级软骨肉瘤CT和MR影像及病理图
依据不同级别软骨肉瘤CT和MR影像特征,两组患者影像表现为软组织肿块伴骨质破坏共16例(占72.7%),低级别组3例,中高级别组13例;骨髓或软组织水肿共13例(占59.1%),低级别组2例,中高级别组11例;骨皮质增厚共10例(占45.5%),低级别组2例,中高级别组8例;骨膨胀共11例(占50.0%),低级别组4例,中高级组别7例;骨膜反应共5例(占22.7%),低级别组1例,中高级别组4例。增强检查15例,粘液湖样无强化区12例(占80.0%),低级别组1例,中高级别组11例。两组骨髓或软组织水肿、骨质破坏以及软组织肿块在软骨肉瘤之间分布差异均有统计学意义(x2=4.031,x2=5.322,x2=7.865;P<0.05),余特征在两组间无统计学差异,中高级别组软骨肉瘤均可见粘液样无强化区(见表1)。
2.3 不同级别软肉瘤CT和MR影像表现及特征对比分析
(1)MR不同级别软骨肉瘤呈稍长T1和长T2信号,CT对其骨化或钙化显示较好,不同级别软肉瘤内见不同程度骨化或钙化,增强呈不均匀较明显强化。低级别软骨肉瘤肿块、髓质或软组织水肿少见(如图1所示)。
(2)中高级别软骨肉瘤软组织肿块、骨质破坏明显及见大片无强化粘液区(如图2和图3所示)。
3 讨论
3.1 软骨类肿瘤分类及软骨类肿瘤诊断与分级
WHO(2013)骨肿瘤分类把软骨源性肿瘤分为良性、中间型和恶性[3]。目前,最常用软骨肉瘤组织病理学分级是以2013年WHO骨和软组织肿瘤分类为标准,按照软骨细胞丰富程度、软骨细胞异型程度、双核细胞和核分裂象有无和多少以及软骨基质粘液变性有无和多少评定将软骨肉瘤分为1、2、3级。但在组织学分级时,对于每一个具体病例,上述各项标准改变程度常不一致,在区分不同级别软骨肉瘤时常缺乏客观性,难免带有主观性。此外,软骨肉瘤的异质性,在同一肿瘤内常同时存在不同级别组织成分[4]。
研究已经证实,软骨肉瘤分级在预测生物学行为和预后方面有积极作用。低级别软骨肉瘤生长缓慢,很少发生转移,5年生存率可达90%;中、高级别软骨肉瘤5年生存率为40~50%。不同部位软骨肉瘤生物学特点也存在差异,位于骨盆等中轴骨的软骨肉瘤一般侵袭性较强,复发率高。低级别软骨肉瘤一般采用局部病灶切除手术;中、高级别软骨肉瘤主要采用更积极的治疗手段,以防病灶复发或转移[5]。在低级别与中、高级别软骨肉瘤的鉴别中,活检由于受到取材不充分,可能会导致软骨肉瘤级别降低的可能性。在骨肿瘤、特别是软骨类肿瘤诊疗中多学科协作越来越被强调,需要结合临床、影像和病理综合分析[6]。目前,X射线平片、CT与MR、核素成像和PET均不同程度应用于骨软骨类肿瘤诊断与分级。X射线作为常规检查,在骨肿瘤诊断和鉴别方面有其不可或缺的重要作用。但在准确界定病灶范围及周围结构侵犯方面远不如CT和MR,在骨软骨类肿瘤临床诊断与鉴别中多采用CT平扫加MR平扫或增强的检查模式[7]。
3.2 不同级别软骨肉瘤CT与MR表现特征及其病理基础
软骨性肿瘤良恶性鉴别除了依据细胞学,还需要了解肿瘤的生长方式,不同级别软骨肉瘤其生长方式也不相同,级别越高越表现出侵袭性的生长方式[8]。软骨类肿瘤病理级别可以发生进展,良性软骨肿瘤可以恶变为软骨肉瘤,低级别软骨肉瘤可以演变成中、高级别软骨肉瘤。不同级别软骨肉瘤由于临床分期和病理分级不同,表现出不同的影像学特征[9]。位于骨盆和长骨干骺段或骨干多表现为膨胀性骨质破坏,边缘可有轻度骨质硬化,骨皮质变薄、中断,骨膜反应少见。不同病例软组织肿块大小差异大,部分病灶可见骨旁或骨外软组织密度肿块形成,其内常见钙化或骨化高密度影,钙化可位于软骨小叶内和(或)分隔上,可多可少。MR一般呈长T1、长T2信号,尤其T2WI呈明显高信号,有一定的特征性。MR显示软骨小叶及其分隔有明显优势。肿瘤与邻近正常骨界面呈扇贝或花边状压迹,其病理基础与软骨小叶膨胀性生长有关。增强后软骨肉瘤周边和分隔一般明显强化,呈弓环状强化。肿瘤性粘液较明显时,软骨肉瘤小叶区呈大片状粘液湖样无强化区,彼此可融合连通,类似与恶性肿瘤中心坏死无强化区[10-11]。
在诸多影像学特征中,用于鉴别低级别与中、高级别软骨肉瘤各家文献报道结果不尽一致[12]。Douis等[13]研究表明,骨质破坏、骨膜反应、软组织肿块及肿瘤长径是区别长管骨低、高级别软骨肉瘤可靠征象,受试者工作特征下面积为0.956。本研究病例CT与MR影像学特征中,骨髓或软组织水肿、骨破坏、软组织肿块在鉴别低级别与中、高级别软骨肉瘤方面有统计学差异。其病理基础为软组织肿块伴骨破坏反映了肿瘤细胞丰富及病灶的侵袭性更大,骨髓或邻近软组织水肿表明病灶对周围结构侵犯的恶性特征,与过去研究相似。在骨膨胀或扇贝样压迹、骨皮质增厚、骨膜反应、钙化程度及病灶长径方面无统计学差异,这些征象多见于良恶性软骨类肿瘤的鉴别,在软骨肉瘤分级鉴别方面可靠性尚需要大样本研究。有些研究表明,病灶长径对在四肢长管骨中鉴别低级别与高级别软骨肉瘤有统计学意义,但本研究资料无统计学差异,可能与本研究资料纳入标准相对过宽,更反映了高级别软骨肉瘤的最主要特征有关。钙化程度在鉴别良性与低级别软骨肉瘤有统计学意义,但在中、高级与低级别软骨肉瘤鉴别上无统计学差异,可能与不同级别软骨肉瘤的钙化均较少或中等量有关。边缘及分隔样强化是软骨肉瘤特征性的影像表现之一,尤其是大片状无强化区或粘液区一般多见于中、高级别软骨肉瘤[14]。其病理基础是肿瘤细胞异形型明显,生长相对较快或伴中心区坏死,同时肿瘤间质中肿瘤血管成分丰富或分泌细胞外大量软骨粘液样基质有关。这种肿瘤性粘液变性大体呈半液态的粘液,即镜下软骨基质广泛粘液变性,软骨陷窝大部分消失,软骨细胞呈幼稚的间叶细胞样,可无明显异型性,也不一定富于细胞,但容易种植、浸润、出现血管瘤栓或远处转移,恶性程度比较高。肿瘤性粘液变性与退行性粘液性变有本质区别,后者是指因缺血、缺氧等原因软骨基质局灶性粘液变性,软骨陷窝仍存在,大体和镜下为透明软骨样而非半液态粘液,在良性内生性软骨瘤和低级别软骨肉瘤均可见[15]。本研究资料高级别软骨肉瘤均可见无强化粘液区(100%),低级别仅出现1例(25%),印证了这点。
本研究局限性在于例数较少且是回顾性研究,病例入组可能存在偏倚。本研究仅就软骨肉瘤不同级别分组讨论,未对发生在不同部位软骨肉瘤和不同组织学类型进行细分,这些都需要进一步积累资料或作一些前瞻性的后续研究。
CT与MR联合诊断在软骨肉瘤术前诊断中发挥重要作用,在诸多影像表现中,本组资料提示骨髓或软组织水肿、骨破坏、软组织肿块及片状无强化区在鉴别低级别与中、高级别软骨肉瘤的病理与分级诊断中有一定的临床指导价值。
