索磷布韦/达拉他韦治疗慢性丙型肝炎患者疗效及安全性分析:一项真实世界研究*
2019-05-08刘立李俊义杜映荣刘春云李卫昆王辉李惠敏常丽仙祁燕伟
刘立,李俊义,杜映荣,刘春云,李卫昆,王辉,李惠敏,常丽仙,祁燕伟
【关健词】 慢性丙型肝炎;索磷布韦;达拉他韦;直接抗病毒药物;治疗
近几年来,国外多项临床试验发现直接抗病毒药物(direct-acting antiviral agent,DAA)具有很强的抑制病毒复制的作用,可使治疗CHC患者的SVR自40%~70%提高到90%[1-5],尤其是2014年上市的索磷布韦(sofosbuvir,SOF)和达拉他韦(daclatasvir,DCV)有很好的临床效果,两者联合应用实现了无干扰素方案,且治疗各基因型CHC患者综合SVR可达到95%,在1型感染者甚至达到99%,SVR24则更是高达99.5%[6-9],并且在用药过程中普遍不良反应较少。艾伯维公司开发出全新的治疗CHC的3D方案(partaprevir/ritonavir and ombitasvir in combination with dasabuvir,3D),临床试验发现,对于基因la型受试者SVRl2达到95%以上[10-15]。本研究应用SOF联合DCV治疗CHC患者,现对其疗效及安全性情况总结报道如下。
1 资料与方法
1.1 研究对象 2016年5月~2017年5月就诊于我院的CHC患者515例,其中440例同意接受SOF/DCV±利巴韦林方案治疗。排除标准:存在失代偿期肝病、血肌酐清除率(creatinine clearance,CrCl)≤30 ml/min、妊娠、吸毒或同性恋者。所有受试者在研究前签署书面知情同意书,本研究经昆明市第三人民医院医学伦理委员会批准。
1.2 治疗方法 本组患者包括LC和CHC患者。129例LC患者经肝脏瞬时弹性测定≥12.5 kPa或肝组织活检为F4或有其他证据显示肝纤维化达到肝硬化,曾经PR治疗无效或停药复发36例、曾经使用其他DAA方案治疗无效或停药复发15例,给予SOF/DCV联合利巴韦林方案治疗;给予311例CHC患者SOF/DCV方案治疗。用法:SOF联合DCV【老挝 Tongmeng(Laos) Pharmaceutical£Food Co.,Ltd生产的仿制药】分别为400 mg和60 mg口服,1次/d,利巴韦林(山东齐鲁药业有限公司)10~15 mg·kg-1·d-1口服。治疗 12 w,随访 12 w。对合并艾滋病者给予高效抗逆转录病毒治疗(highly active antiretroviral therapy,HAART),DCV 减为半量,SOF 剂量不变。
1.3 统计学方法 应用SPSS 20.0统计学软件进行数据分析。计量资料以(±s)表示,采用t检验,计数资料的比较采用x2检验,采用单因素和多因素回归分析影响疗效的因素,P<0.05为差异有统计学意义。
2 结果
2.1 基线特征 在入组的440例患者中,男性250例,女性190例;年龄18~76岁,平均年龄(45.18±11.21)岁。其中合并糖尿病8例,合并慢性乙型肝炎(CHB)5例(其中2例一直服用恩替卡韦,另3例为HBV携带者),合并高血压病6例,合并慢性胃炎12例,合并艾滋病8例(均在接受HAART治疗),合并胃溃疡1例。440例患者基线特征见表1。
表1 440 例患者基线资料(n,±s)

表1 440 例患者基线资料(n,±s)
CHC(n=311) LC(n=129)性别(男/女) 171/140 79/50年龄(岁) 43.9±11.9 48.3±8.6 TBIL(μmol/L) 21.0±28.6 24.1±18.1 ALT(IU/L) 97.8±106.4 91.4±54.6 AST(IU/L) 72.5±80.8 81.1±40.5 PLT(×109/L) 180.6±56.6 124.2±58.1 HB(g/L) 146.8±16.3 145.2±26.0 WBC(×109/L) 5.6±1.3 4.8±1.3 HCV RNA(lg IU/ml) 6.2±1.3 5.9±1.2 LSM(kPa) 11.8±3.3 17.6±9.9基因型(1/2/3/6/无/混合) 56/43/116/29/65/2 16/15/65/13/20/0
2.2 生化学应答 患者接受SOF/DCV加或不加利巴韦林治疗2 w时,两组血清ALT和AST显著下降(P<0.05),LC 组血清 TBIL显著下降(P<0.05);随着治疗时间的延长,各项指标进一步下降,且生化学应答率均较好(表2)。
表2 两组生化学指标(±s)变化

表2 两组生化学指标(±s)变化
与基线比,①P<0.05
TBIL(μmol/L) ALT(IU/L) AST(IU/L)CHC组基线(n=311) 21.0±28.6 97.8±106.4 72.5±80.8治疗2 w 20.1±4.6 32.5±10.0① 32.0±6.7①治疗4 w 18.1±3.5 27.9±10.7① 29.4±6.0①治疗12 w 14.9±3.5 30.3±3.4① 27.1±6.7①停药12 w 18.9±0.5 30.4±1.0① 31.6±0.9①LC组基线(n=129) 24.1±18.1 91.4±54.6 81.1±40.5治疗2 w 20.2±3.5① 35.2±18.5① 35.1±13.2①治疗4 w 18.2±3.2① 28.4±5.9① 30.2±4.7①治疗12 w 15.7±2.7① 34.5±35.8① 43.5±7.4①停药12 w 19.0±2.3① 30.7±4.9① 31.9±2.9①
2.3 两组不同基因型感染者SVR发生率比较 治疗2周时,CHC组血清HCV RNA为(1.83±2.88)lg IU/ml,LC 组为(1.67±2.34)lg IU/ml,提示联合或不联合利巴韦林均可快速降低HCV RNA载量;停药12周时,不同基因型感染者获得SVR情况见表3。
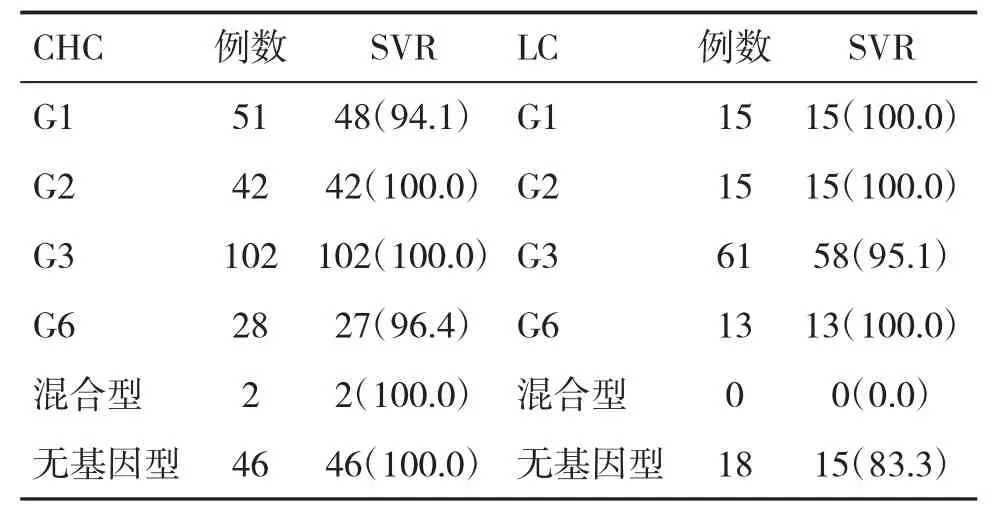
表3 两组不同基因型感染者SVR(%)比较
2.4 10例未取得SVR患者基本情况 见表4。

表4 10例未取得SVR患者特征
2.5 影响SVR的基线资料多因素回归分析 对未获得SVR的患者基线资料进行回归分析,以性别、年龄、基因型、TBIL、ALT、AST、PLT、Hb、WBC、LSM、HCV RNA水平、肝硬化或复治为自变量,行回归分析,仅血清TBIL水平、肝硬化或复治有统计学意义(P=0.029,P=0.033);行多因素回归分析,选择Forward:LR,向前逐步选择自变量,结果肝硬化或复治具有有统计学意义(P=0.042,表5)。
2.6 两组LSM水平变化 治疗12周时,CHC组LSM 水平为(8.09±0.90)kPa,LC 组为(13.32±1.47)kPa。
2.7 药物不良反应情况 在治疗期间,无因出现不良反应而退出治疗病例,出现乏力52例,头痛47例,头晕32例,皮疹12例,皮肤瘙痒6例,腹痛、腹泻8例。上述大多不良反应持续时间短暂,均在2周内消失或经对症处理后消失。

表5 影响SVR的多因素回归分析
3 讨论
云南地区慢性HCV感染率高于全国平均水平。本地区HCV基因型以3型为主。本组资料显示亦以基因3型最多见。目前,DAA治疗慢性HCV感染患者收到了很好的治疗效果。
SOF是NS5B聚合酶抑制剂,DCV是NS5A抑制剂。国外的临床研究显示[16],SOF联合DCV加或不加利巴韦林治疗基因1型CHC患者24周停药12周SVR高达99%,小样本的基因3型CHC患者在治疗24周停药12周时SVR为92%。本研究应用老挝生产的仿制药SOF/DCV加或不加利巴韦林抗病毒治疗云南地区CHC和丙型肝炎肝硬化患者,治疗2周时绝大多数患者都可以迅速获得病毒学应答(87.6%),在4周时达94.9%,12周时病毒学应答率为96.9%。持续观察停药12周时SVR仍为97.5%,表明该联合方案适用于本地区CHC人群的抗病毒治疗。
对于10例未获得SVR12的患者进行多因素回归分析,结果显示基线时肝硬化或P-R方案或其他DAA治疗无效的患者是本方案治疗不能获得SVR的高危因素。针对这样的患者,可酌情延长疗程或改用其他的治疗方案。
本研究还观察到,抗病毒治疗期间,随着病毒载量的下降,患者肝功能等各项指标亦出现相应的好转,LSM显著降低。
在不良反应的监测中,乏力出现的最多见,但适当休息均能缓解;其次为明显的头痛,但也在患者能耐受的程度内;也有少数病例出现头晕、皮疹、皮肤瘙痒、腹痛、腹泻,均经对症处理后缓解。
