应用糖皮质激素治疗核苷(酸)类似物撤药性肝炎患者临床疗效评价*
2019-05-08潘劲劲宋海燕张俊飞陈照林
潘劲劲,董 静,宋海燕,张俊飞,陈照林,刘 波
在我国,慢性乙型肝炎(chronic hepatitis B,CHB)广泛流行,目前尚无有效的临床治愈方案。研究表明[1],长期抗病毒治疗可以控制病情向肝硬化、肝癌及相关临床并发症进展,从而降低病死率,改善生活质量,延长生存时间。应用α-干扰素(interferon-α,IFN-α)和核苷(酸)类似物[nucleos(t)ide analogues,NAs]治疗是临床主要的抗病毒治疗方法,其中NAs可通过抑制乙型肝炎病毒(hepatitis B virus,HBV)复制,降低病毒载量,但不能彻底清除HBV复制过程中形成的转录模板,即共价闭合环状 DNA(covalently closed circular DNA,cccDNA),故HBV cccDNA在肝细胞内持续存在,需长时间的治疗以抑制病毒的复制。目前,各种指南均未明确CHB患者使用NAs抗病毒治疗的疗程,寻找预测NAs停药的临床指标和生物学标志仍是临床亟待解决的临床课题[2]。由于有些患者医疗卫生知识缺乏或经济原因等导致CHB患者长期治疗依从性较差,部分CHB患者擅自停用NAs,导致HBV复制反弹,激发强烈的免疫应答和免疫清除反应,造成广泛的肝组织损伤,严重者可进展为肝衰竭(liver failure,LF)。LF 导致肝脏合成、解毒、排泄和生物转化等功能发生严重障碍,病情重,预后差,病死率高[3]。故寻找有效的方法治疗撤药性肝炎(withdrawal hepatitis,WH)并阻止其向肝衰竭发展是目前临床医生面临的严峻课题。在我科收治的因停用NAs导致的WH患者中,符合《肝衰竭诊治指南(2018年版)》肝衰竭前期定义患者23例,部分患者在早期应用糖皮质激素后,病情立即好转,现报道如下。
1 资料与方法
1.1 研究对象 2017年12月~2018年12月解放军联勤保障部队第901医院感染病科收治的因停用NAs导致的WH患者23例,其中因停止拉米夫定治疗引起者8例,因停止阿德福韦引起者12例,因停止替比夫定引起者3例。符合肝衰竭前期诊断标准,服用核苷(酸)类似物32~312周,平均为(86.4±18.6)周,停药前血清 HBV DNA<1×103拷贝/毫升。CHB诊断符合2015年中华医学会制定的《慢性乙型肝炎防治指南》的标准[4],LF诊断符合中华医学会修订的《肝衰竭诊治指南(2012年版)》的标准[5]。肝衰竭前期界定标准:①极度乏力,并有明显厌食、呕吐和腹胀等严重的消化道症状;②血清丙氨酸氨基转移酶(ALT)和/或天冬氨酸氨基转移酶(AST)水平大幅升高,黄疸进行性加深(85.5μmol/L≤血清 TBIL<171 μmol/L)或每日上升≥17.1 μmol/L;③有出血倾向,40%<PTA≤50%或 INR<1.5。排除标准: ①合并 HAV、HCV、HDV、HEV、HIV 重叠感染者;②存在大量腹水、自发性细菌性腹膜炎、消化性溃疡或消化道出血者;③伴有Ⅱ期以上肝性脑病、肝肾综合征或并发细菌或真菌感染者;④存在酒精、药物和自身免疫性肝病等其他因素引起的肝衰竭前期患者;⑤有应用糖皮质激素禁忌证者。
1.2 检测方法 采用 CHEMCLIN1500化学发光法检测HBV血清标志物(美国雅培生物技术公司);采用实时荧光定量PCR法检测HBV DNA(上海复兴生物高科技有限公司,最低检测下限为1×103拷贝/毫升);使用美国Beckman BX 800全自动生化分析仪及其配套试剂检测肝肾功能指标;使用ACL200凝血分析仪检测PT。
1.3 治疗方法 将患者分为两组,所有患者在入院后均接受恩替卡韦(博路定)0.5 mg口服,1次/d,异甘草酸镁注射液、腺苷蛋氨酸和人血白蛋白或新鲜冰冻血浆等支持治疗。给予观察组氢化可的松琥珀酸钠100 mg加入生理盐水100 ml中静脉滴注,1次/d,用至血清TBIL<100 μmol/L后,减为50 mg·d-1,继续应用至血清 TBIL<50μmol/L 后,改为强的松口服,逐渐减量至停用。
1.4 统计学方法 应用 SPSS 22.0软件处理数据,计量资料以(±s)表示,采用独立样本的 t检验;计数资料的比较采用x2检验,P<0.05被认为差异有统计学意义。
2 结果
2.1 两组一般资料比较 两组一般资料比较,无显著性差异(P>0.05,表1),具有可比性。
表1 两组一般资料(%,±s)比较

表1 两组一般资料(%,±s)比较
例数 男性 年龄(岁) 病程(年) 用药时间(w) 停药时间(w)观察组 12 10(83.3) 32.1±7.8 4.9±3.2 85.4±17.3 7.9±5.8对照组 11 9(81.1) 34.2±6.9 4.2±4.6 86.9±18.9 8.6±6.4 t值 0.501 0.677 0.527 0.707 P值 0.746 0.516 0.712 0.520
2.2 转归 对照组患者在治疗6周时因病情进展至肝衰竭死亡1例,在治疗8周时死亡2例;观察组患者在治疗8周时因病情进展而死亡1例。
2.3 两组血生化、凝血功能指标和终末期肝病模型(MELD)评分的比较 观察组血清总胆红素(TBIL)水平显著低于对照组,血清白蛋白(ALB)和凝血酶原活动度(PTA)显著高于对照组,在治疗4周时观察 组患者MELD评分显著低于对照组(P<0.05,表2)。
表2 两组肝功能指标(±s)比较
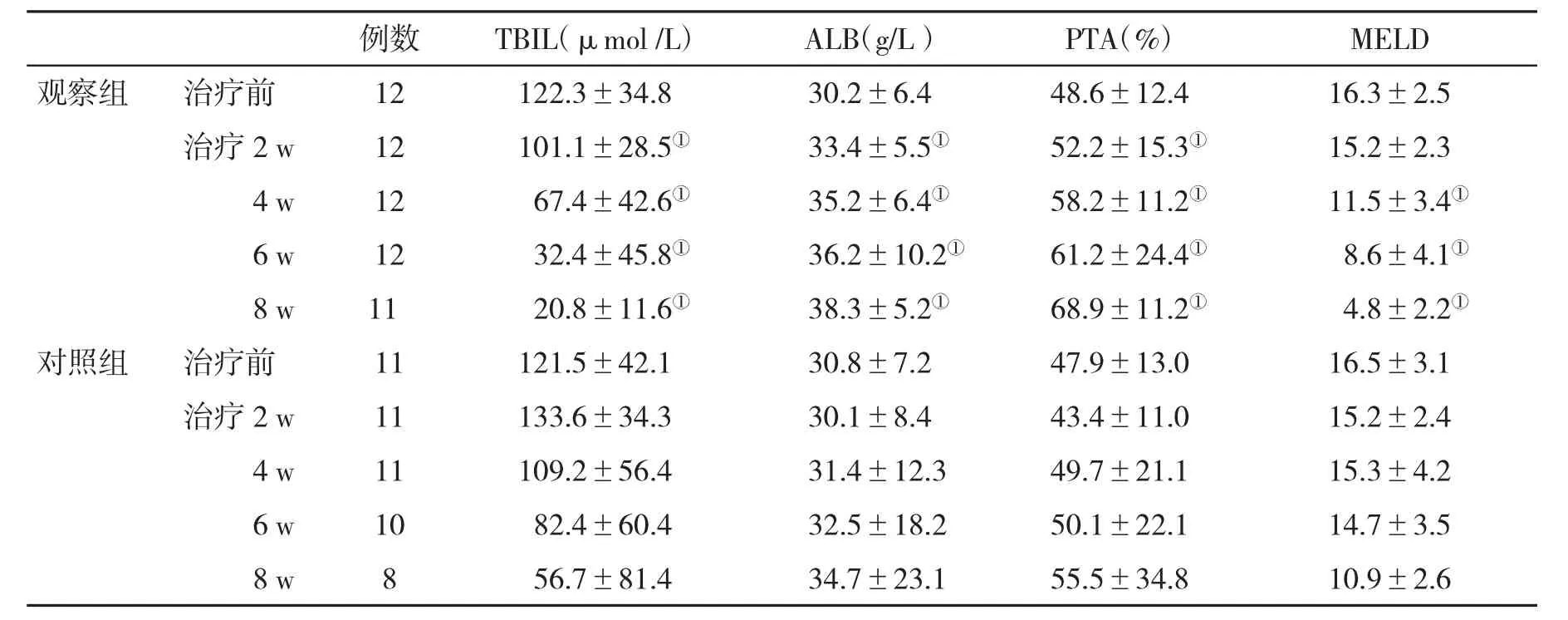
表2 两组肝功能指标(±s)比较
与对照组比,①P<0.05
例数 TBIL(μmol/L) ALB(g/L) PTA(%) MELD观察组 治疗前 12 122.3±34.8 30.2±6.4 48.6±12.4 16.3±2.5治疗2 w 12 101.1±28.5① 33.4±5.5① 52.2±15.3① 15.2±2.3 4 w 12 67.4±42.6① 35.2±6.4① 58.2±11.2① 11.5±3.4①6 w 12 32.4±45.8① 36.2±10.2① 61.2±24.4① 8.6±4.1①8 w 11 20.8±11.6① 38.3±5.2① 68.9±11.2① 4.8±2.2①对照组 治疗前 11 121.5±42.1 30.8±7.2 47.9±13.0 16.5±3.1治疗 2 w 11 133.6±34.3 30.1±8.4 43.4±11.0 15.2±2.4 4 w 11 109.2±56.4 31.4±12.3 49.7±21.1 15.3±4.2 6 w 10 82.4±60.4 32.5±18.2 50.1±22.1 14.7±3.5 8 w 8 56.7±81.4 34.7±23.1 55.5±34.8 10.9±2.6
2.4 两组血清学和病毒学指标变化的比较 在治疗4周和8周时,两组血清HBsAg和HBV DNA水平变化无显著性差异(P>0.05,表3)。
表3 两组血清HBsAg和HBV DNA水平(±s)比较
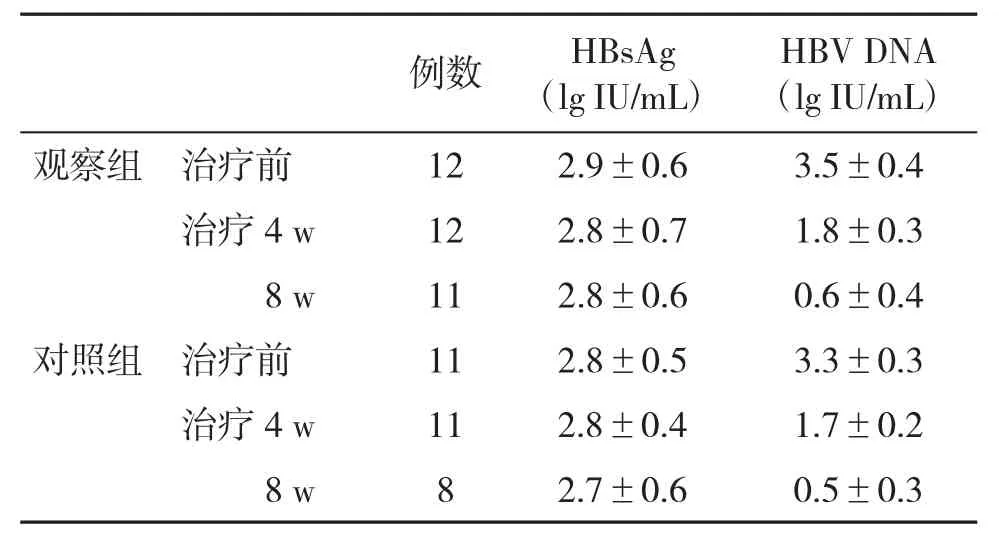
表3 两组血清HBsAg和HBV DNA水平(±s)比较
HBV DNA(lg IU/mL)观察组 治疗前 12 2.9±0.6 3.5±0.4治疗4 w 12 2.8±0.7 1.8±0.3 8 w 11 2.8±0.6 0.6±0.4对照组 治疗前 11 2.8±0.5 3.3±0.3治疗4 w 11 2.8±0.4 1.7±0.2 8 w 8 2.7±0.6 0.5±0.3例数 HBsAg(lg IU/mL)
2.5 两组并发症发生情况比较 在治疗过程中,两组均有少数患者发生院内感染,但观察组患者病情控制(指临床症状消失,血清胆红素水平开始下降,凝血功能指标稳定或好转)时间显著短于对照组,生存率显著高于对照组(P<0.05,表4)。观察组患者在治疗过程中,无消化道出血等严重并发症发生。
表4 两组病情控制(±s)和结局指标(%)比较

表4 两组病情控制(±s)和结局指标(%)比较
与对照组比,①P<0.05
例数 感染观察组 12 1(8.3)对照组 11 2(18.1)病情控制(d)22.4±9.4①36.7±13.1生存11(91.6)①8(72.7)
3 讨论
抗病毒治疗CHB患者可以有效减轻肝组织炎症、阻断肝硬化进展、预防肝癌的发生,从而改善患者生活质量,延长生存时间,是目前治疗方法的首要选择[4]。但由于各种原因,部分患者自行停药导致WH,这种情况在临床诊疗过程中日益多见。研究发现,停用抗病毒药物后,WH发生率较高[6]。部分WH患者病情迅速进展至LF,增加临床病死率。因此,有效阻止肝衰竭前期病例进展为LF是临床救治WH患者的关键。
研究发现[7,8],在 LF 患者,肝组织病理学检查显示,除有大量肝细胞坏死外,还存在炎症细胞浸润,反映了LF发生时出现的免疫攻击性损伤。在WH患者,大量HBV DNA复制可直接或通过诱发免疫损伤间接地导致肝细胞死亡,免疫损伤引起局部炎症反应。局部炎症反应可导致缺血缺氧性损伤,继而促进内毒素血症的发生,从而加速LF病情进展[9,10]。在肝衰竭前期患者,主要以免疫损伤和肝组织缺血缺氧性损伤为主,免疫处于亢进及紊乱状态,且免疫反应可能导致肾上腺皮质功能减退[11],这个时期使用糖皮质激素一方面可通过诱导免疫细胞凋亡、调节CD4+T细胞亚群比例[12]、抑制肝内细胞间黏附分子-1表达[13]等方式抑制免疫应答,进而减轻原发性肝损伤;另一方面,还能通过抑制TNF-α、IL-1、IL-6、IL-17等促炎性细胞因子的产生和释放,增强IL-10等抗炎性细胞因子的产生和释放,从而发挥强大的抗炎作用,进而减轻细胞因子过度活化引起的继发性肝损伤。另有大量研究表明[14,15],在肝衰竭前期患者,早期使用糖皮质激素有可能阻止LF的发生,降低病死率。本研究结果显示,观察组进展为LF者3例,而对照组为10例,表明在肝衰竭前期使用糖皮质激素可缓解消化道症状,有效阻止病情进展为LF,从而降低病死率。本研究亦发现早期使用糖皮质激素通过抑制免疫损伤,阻止大量肝细胞死亡导致的微循环障碍,可防止微循环障碍,进一步阻断病情进展。观察组治疗后血清胆红素下降明显,血清白蛋白和凝血酶原活动度上升。在治疗6周时,观察组血清胆红素为(32.4±45.8)μmol/L,病情控制明显。本研究显示,观察组病情控制时间为(22.4±9.4) d,对照组病情控制时间为(36.7±13.1)d,故早期使用糖皮质激素可明显缩短病情控制时间。也有学者担忧,在CHB患者使用糖皮质激素会导致HBV复制活跃,增加感染的风险,但本研究发现观察组与对照组病例血清HBsAg和HBV DNA水平变化无统计学差异,表明在恩替卡韦抗病毒治疗的基础上,使用糖皮质激素可阻止HBV复制活跃。恩替卡韦抑制病毒复制的作用强,耐药率低,近年越来越多地用于WH导致LF患者的抗病毒治疗[16-18]。本研究结果显示,观察组感染发生率为8.3%,对照组感染发生率为18.1%,说明在肝衰竭前期的撤药性肝炎患者中,早期使用糖皮质激素不增加感染的发生率。分析原因,可能是因为本研究在应用皮质激素的同时,给予强有力的基础支持治疗,保证了治疗的安全性[19],而早期使用糖皮质激素可阻止病情进展为肝功能衰竭,缩短平均住院日,也可减少感染发生的机会。
本研究观察组1例发生肺部真菌感染,而对照组发生感染者并无合并真菌感染,我们分析原因可能是观察组使用糖皮质激素,增加了合并真菌感染的风险[20]。此为应用皮质激素的最大担忧,如何防治真菌感染,仍是需要研究的课题。本研究纳入病例数少,无法对是否应用糖皮质激素及其不同疗程和剂量等进行分层分析。
综上所述,在WH患者,选择肝衰竭前期病例,早期使用糖皮质激素治疗,在肝功能指标稳定后或黄疸消退后,逐渐减量至停药,可阻断病情进展,明显缩短患者平均住院日,降低病死率。
