3,5-二硝基水杨酸法测定黄水中总糖的含量
2019-05-05宋娇娇
宋娇娇,裴 斐,马 勇,朱 青,赵 祥
(江苏洋河酒厂股份有限公司,江苏宿迁223800)
黄水是浓香型白酒主要的副产物,黄水中含有丰富的酸类、酯类、醇类等呈香呈味物质[1],同时含有大量的糖和蛋白质等大分子物质,限制了黄水的应用[2],通常将黄水经预处理后再利用,总糖含量是评价处理效果的标准之一。实验室常用的总糖检测方法是滴定法与比色法,滴定法对溶液中的总糖含量、滴定速度、滴定环境等都有要求,且个人操作上的习惯、熟练程度等都会对结果造成较大的影响[3]。黄水颜色一般为亮黄色、深黄色甚至黑色,也会干扰对滴定终点的判定。比色法常用的有苯酚-硫酸法、蒽酮-硫酸法、3,5-二硝基水杨酸法,但前两种方法用的硫酸腐蚀性较强,会造成一定的安全隐患[4]。3,5-二硝基水杨酸比色法(DNS法)是半微量定糖法,该方法操作简单、便捷,杂质干扰较少,便于批量测定,是一种常用的测糖方法[5]。该方法的原理是在碱性条件下还原糖将3,5-二硝基水杨酸中的硝基还原成氨基,生成橘红色化合物,在一定的范围内,还原糖含量与颜色成正比[6]。本试验采用盐酸将黄水中的总糖水解成还原糖,利用DNS法在最适波长下进行检测,利用吸光值与还原糖之间的线性关系计算黄水中总糖含量[7]。本研究考察显色剂添加量、显色时间、显色温度对检测结果的影响,采用正交试验确定黄水总糖水解条件,并进行方法学考察,建立3,5-二硝基水杨酸测定黄水中总糖含量的方法,以期为黄水的预处理等应用提供参考依据。
1 材料与方法
1.1 材料与仪器
黄水,取自洋河酒厂浓香车间。
重蒸酚,上海一基实业有限公司;葡萄糖、3,5-二硝基水杨酸、酒石酸钾钠、盐酸、氢氧化钠、无水亚硫酸钠均为分析纯,国药集团化学试剂有限公司。
电热鼓风干燥箱,上海左乐仪器有限公司;纯水机,上海摩勒科学仪器有限公司;水浴锅,常州市亿能实验仪器厂;UV-6000PC型紫外/可见分光光度计,上海元析仪器有限公司。
1.2 试验方法
1.2.1 试剂的配制
DNS试剂的配制[8]:称取6.3 g 3,5-二硝基水杨酸溶于262 mL 2 mol/L的氢氧化钠溶液中。将此溶液与500 mL含182 g酒石酸钾钠的热水混合,再添加5 g重蒸酚和5 g亚硫酸钠,搅拌溶解后定容至1000 mL,充分混匀,存于棕色瓶中,避光存放7 d后使用。
1 mg/mL葡萄糖标准溶液:精密称取已烘干的葡萄糖1 g,加纯水定容至1 L,充分摇匀备用。
1.2.2 检测条件优化[9]
(1)显色剂添加量对检测结果的影响
取1 mL 1 mg/mL葡萄糖标准溶液,分别添加显色剂0.5 mL、1.0 mL、1.5 mL、2.0 mL、2.5 mL、3.0 mL、3.5 mL、4.0 mL、4.5 mL、5.0 mL、5.5 mL、6.0 mL、6.5 mL,100℃水浴中显色反应10 min,自来水迅速冷却,纯水定容至25 mL,以空白为对照,在波长540 nm处检测吸光值。
(2)显色时间对检测结果的影响
取1 mL 1 mg/mL葡萄糖标准溶液,添加显色剂5 mL,100℃水浴中分别选择显色反应时间1 min、3 min、5 min、7 min、9 min、11 min、13 min、15 min、17 min、19 min、21 min,自来水迅速冷却,纯水定容至25 mL,以空白为对照,在波长540 nm处检测吸光值。
(3)显色温度对检测结果的影响
取1 mL 1 mg/mL葡萄糖标准溶液,添加显色剂5 mL,分别在40℃、50℃、60℃、70℃、80℃、90℃、100℃水浴中显色反应7 min,自来水迅速冷却,纯水定容至25 mL,以空白为对照,在波长540 nm处检测吸光值。
1.2.3 标准曲线的绘制
取6支25 mL比色管,分别添加0、0.2 mL、0.4 mL、0.6 mL、0.8 mL、1 mL的1 mg/mL的葡萄糖标准溶液,再添加纯水使总体积到1 mL,然后添加5.0 mL的DNS试剂,充分混合后在90℃中水浴7 min,取出后用自来水迅速冷却,加纯水至25 mL充分摇匀后静置。以不加葡萄糖反应液为对照,在540 nm处测定吸光值,以葡萄糖含量为横坐标,吸光值为纵坐标绘制标准曲线。
1.2.4 黄水水解条件的优化
只有黄水中总糖充分水解,总糖含量检测结果才准确,影响黄水水解的主要条件有水解时间、盐酸浓度、盐酸添加量。本试验参考液态发酵成熟醪总糖水解方法[10],选择水解温度100℃,以水解时间、盐酸浓度、盐酸添加量为变量,以吸光值为指标,采用3因素3水平,按L9(33)正交试验进行黄水水解条件的优化[11],正交试验设计因素水平表见表1。
1.2.5 样品测定

表1 L9(33)正交试验因素水平表
取1 mL黄水水解液于25 mL容量瓶中,其他步骤同1.2.4,测定样品的吸光值,并根据标准曲线计算出黄水总糖含量。
黄水浓度(mg/mL)=样品浓度×稀释倍数。
1.2.6 方法学考查
(1)精密度试验
取同一组黄水按照1.2.3与1.2.5确定的检测条件和水解条件,在540 nm波长下连续测定6次吸光值。考查方法的精密度。
(2)重复性试验
取同一批黄水6份,按照1.2.3与1.2.5确定的检测条件和水解条件,在540 nm波长下测定吸光值。考查方法的重复性。
(3)稳定性试验
按照1.2.3与1.2.5确定的检测条件和水解条件,在540 nm波长下测定吸光值,在显色反应结束90 min内,每隔10 min测定1次。考查方法的稳定性。
(4)回收率试验
取同一黄水水解液,加入不同质量浓度的葡萄糖标准溶液,参照样品检测方法对回收率进行考查。
2 结果与分析
2.1 检测条件优化
2.1.1 显色剂添加量对检测结果的影响(图1)

图1 显色剂添加量对检测结果的影响
由图1可知,当显色剂添加量小于5 mL时,溶液吸光值随着显色剂添加量的增加而增大;当显色剂添加量大于5 mL时,溶液的吸光值基本无变化。考虑到节约资源,显色剂的最佳添加量为5 mL。
2.1.2 显色时间对检测结果的影响(图2)
由图2可知,随着显色时间的延长,吸光值呈现先增加后下降并趋于稳定的趋势,显色时间为7 min时,吸光值为最大值,因此选择显色时间7 min。
2.1.3 显色温度对检测结果的影响(图3)
由图3可知,显色温度对检测结果影响较大,当显色温度达到90℃后,吸光值趋于稳定,因此选择最佳显色温度为90℃。
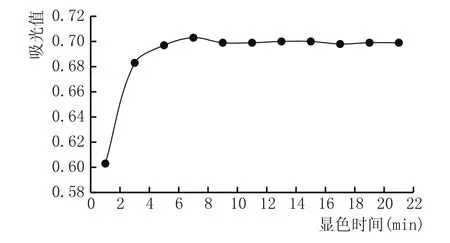
图2 显色时间对检测结果的影响

图3 显色温度对检测结果的影响
2.2 葡萄糖标准曲线的绘制(图4)
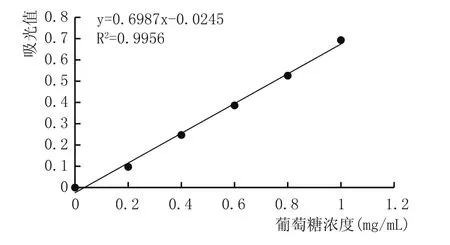
图4 葡萄糖标准曲线
由图4可知,葡萄糖标准曲线回归方程为:y=0.6987x-0.0245,线性相关系数R2=0.9956,表明葡萄糖溶液在0~1.0 mg/mL浓度范围内与吸光值呈现良好的线性关系。
2.3 黄水水解条件的优化
采用3因素3水平正交试验设计对黄水总糖水解条件进行优化,正交试验结果见表2,方差分析见表3。
由表2中的极差分析可知,RA>RC>RB,3个因素对黄水水解液吸光值的影响顺序依次为:水解时间(A)>盐酸添加量(C)>盐酸浓度(B)。由表3方差分析结果可知,水解时间对黄水水解液的吸光值影响显著(P<0.05),其他因素对结果无显著性影响(P>0.05)。根据正交试验结果与分析,水解最佳条件为A2B3C3,即水解时间30 min,盐酸浓度12 mol/L,盐酸添加量15 mL。

表2 正交试验设计与结果
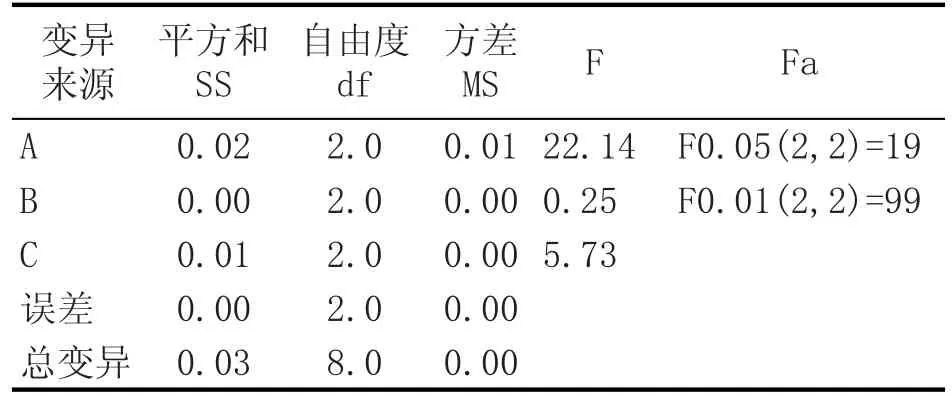
表3 方差分析
2.4 方法学考查
2.4.1 精密度试验(表4)
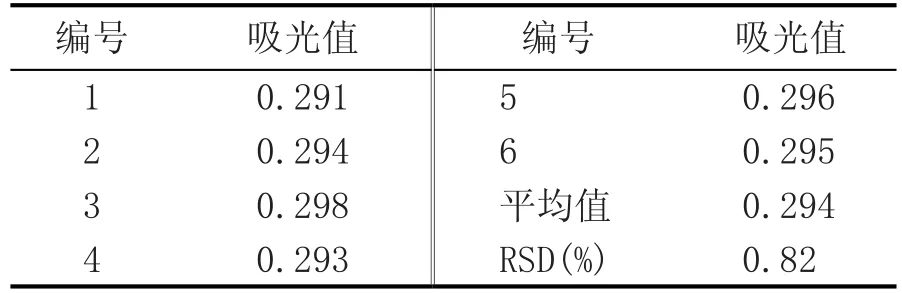
表4 精密度试验结果
由表4可知,精密度试验结果相对标准偏差RSD值为0.82%<2%,说明3,5-二硝基水杨酸法测定黄水总糖精密度良好。
2.4.2 重复性试验(表5)
由表5可知,重复性试验结果相对标准偏差RSD值为1.62%<2%,说明3,5-二硝基水杨酸法测定黄水总糖重复性良好。
2.4.3 稳定性试验(表6)

表5 重复性试验结果
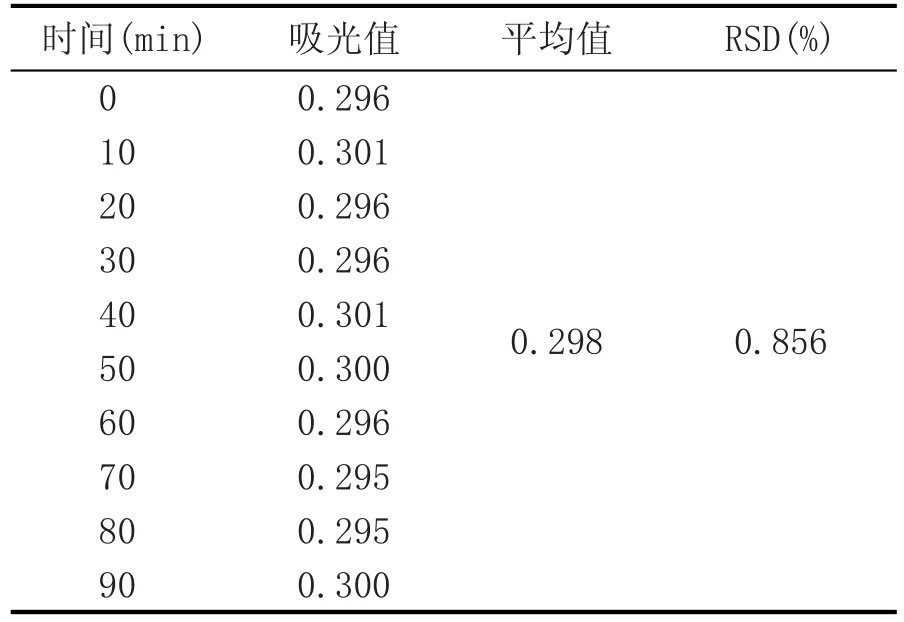
表6 稳定性试验结果
由表6可知,黄水总糖在0~90 min内吸光值基本稳定不变,相对标准偏差RSD值为1.62%<2%,说明采用3,5-二硝基水杨酸法测定黄水总糖在90 min内稳定性良好。
2.4.4 回收率试验(表7)
由表7可知,黄水中添加葡萄糖标液检测回收率在94.60%~97.60%,RSD值均小于2%,证明该方法对总糖的回收性良好,该方法准确度良好。
3 结论
本研究对3,5-二硝基水杨酸法(DNS法)测定黄水中总糖的检测条件和水解条件进行了优化,并进行了方法学考查,建立了DNS法测定黄水中总糖含量的方法。确定了3,5-二硝基水杨酸法检测黄水中总糖的检测条件为:显色剂添加量5 mL,显色时间7 min,显色温度90℃;黄水总糖水解条件为:水解时间30 min,盐酸浓度12 mol/L,盐酸添加量15 mL。该方法的精密度、重复性、稳定性良好(相对标准偏差RSD均小于2%),平均加标回收率94.60%~97.60%,RSD值均小于2%。表明该方法检测黄水中总糖准确、可靠、重现性好。该方法适用于黄水中总糖检测,可为黄水应用提供依据,也可为其他总糖的测定提供参考。

表7 回收率试验结果
