自动勾画技术在前列腺癌自适应放射治疗中的临床应用研究
2019-04-29崔志强庞廷田李文博董婷婷汪之群
崔志强 邱 杰* 杨 波 刘 峡 庞廷田 刘 楠 于 浪 李文博 董婷婷 汪之群 王 贝
当前,调强放射治疗(intensity modulated radiation therapy,IMRT)已成为治疗前列腺癌的主要方式,其在减少疾病复发和改善临床预后等方面发挥着重要的作用。调强放射治疗在靶区得到精确处方剂量分布的同时,可以更好地保护周围的危及器官(organs at risk,OAR)[1-3]。但实现这一优势的前提是必须在患者定位CT图像上,准确定义与勾画出靶区和OAR的轮廓。传统定位图像上的手工勾画占用医生临床工作的大部分时间,且易形成不同勾画者间的差异[2-5]。这已经迟缓了自适应放射治疗(adaptive radiotherapy,ART)技术快速发展的脚步[6]。
ART的特点需要在放射治疗间期更为快速、准确地进行相关结构的勾画。在这样的前提下,OAR甚至靶区的自动勾画成为研究的焦点[6-9]。因此,一些自动,半自动勾画软件应运而生,并应用于临床实践中。然而,国内外对于自动勾画技术多聚焦于头颈部肿瘤的研究,并显示出在提高勾画效率,即勾画结果的准确性较高、勾画时间明显减少、减少不同医师之间的勾画差异以及明显降低勾画误差等方面的潜力[6-10]。但对于器官位置及形态变化较大的腹腔、盆腔器官相关轮廓的勾画是该技术面临的最大挑战,且相关研究报道较少。基于此,本研究探讨前列腺癌自适应放射治疗中基于图谱集的自动勾画技术(atlasbased auto-segmentation,ABAS)对于OAR自动勾画临床应用的可行性,评价与分析Prostate和General两种算法的性能。
1 资料与方法
1.1 临床资料
1.2 仪器设备
CT模拟定位采用Brilliance CT(Big Bore)型16排大孔径螺旋CT模拟机(荷兰Philips)进行扫描;勾画工具采用ABAS自动勾画软件(瑞典Elekta);最后采用Eclipse计划系统(美国Varian)对勾画结果进行分析。
1.3 定位方法
患者均取仰卧位,为了在ART进程中更为准确的评估OAR的受量,在CT模拟定位之前要求其排空直肠;饮水充盈膀胱并利用B超评价膀胱充盈情况;热塑体膜固定。扫描参数:①CT扫描条件,扫描电压140 kV,扫描电流280 mAs;②扫描范围,从腰3椎体上缘至坐骨结节下缘,包括整个盆腔;③扫描重建,层厚5 mm。
1.4 硬件工具
ABAS(Version 2.01)为形变配准自动勾画工具,主要由图谱集(参考图像)和待勾画患者定位图像(目标图像)组成,其通过在软件中选择不同算法对两种图像进行相应的形变配准。获取参考图像的形变向量,将参考图像上的感兴趣器官的结构轮廓以非线性方式映射到目标图像上,最终完成对目标图像的自动勾画[8-10]。
1.5 勾画流程
由一名住院医师在计划系统上对所有患者两程定位CT图像上的OAR进行手工勾画,并由一名主治医师对第1程和第2程手工勾画的结果进行校对,并记录第2程定位图像上手工勾画与修改时间。以患者第1程定位图像作为参考图像,重新拷贝第2程定位图像作为目标图像,将两程图像以医学数字影像及通信(digital imaging and communication of medicine,DICOM)的格式传输至ABAS自动勾画系统中。勾画标准参考国际放射辐射单位和计量测量委员会(International Commission on Radiation Units and Measurements,ICRU)发布的62号文件。勾画的OAR包括膀胱、左右髋骨、左右股骨头及直肠。
在ABAS系统中选用单一图谱自动勾画方式下用于腹部勾画的General和Prostate两种形变配准算法,进行两种算法的自动勾画。将自动勾画结果传输至Eclipse计划系统中与医师手工勾画结果进行比对及分析(如图1所示)。
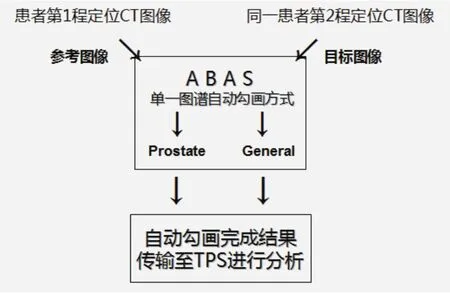
图1 自动勾画流程图
1.6 评价标准
(1)通过Eclipse计划系统,以医生手工勾画的OAR轮廓为“金标准”,评价自动勾画的OAR与手工勾画结果吻合程度。
(2)形状相似性系数(dice similarity coefficient,DSC)与交叉指数(overlap index,OI)。使用DSC和OI评价自动勾画与手动勾画OAR的重合性。其值位于0~1之间,越接近1表示自动勾画与手工勾画的重合性越好,反之则两种勾画方式无重合。在图像重合度研究中,建议DSC>0.7为重合度较好的标准[11-13]。DSC和OI计算为公式1、公式2:

式中Va为自动勾画器官的体积;Vm为手工勾画器官的体积;Va∩Vm为自动勾画与手工勾画重合的体积。
教师不但要在教学实践中对学生学习情况进行监管和引导,同时在发布各个任务之前,应该设定对应任务规划目标。在任务设计完成以后,需要开展项目分析及课程结构分析等工作。探究教学提纲以及课程框架,获取各个知识模板教学框架。同时,将各个项目任务划分为多个模块,同时各个模块均要结合对应知识点将其划分成多个部分教学内容。教师可以根据教学要求和内容实现对应教学任务的设计,将各个学习知识隐藏在各个任务中,让学生在落实各个任务时实现知识点的科学应用,提升学习能力[4]。此外,结合项目开发模板及各个学生学习特性进行小组分配,同时下发对应的学习任务,给实施环节做好准备。
(3)体积差异(volume difference,ΔV)。正值表示自动勾画高估了目标体积(过度勾画),负值表示自动勾画低估了目标体积(勾画不足),其绝对值越接近0,表明自动勾画结果变化程度越小,越接近“金标准”[10-13]。ΔV计算为公式3:

式中Va-Vm为自动勾画与“金标准”的体积差值。
(4)勾画时间比较。分别记录两种算法自动勾画,并经同一名主治医生对结果进行手工修改的时间与第2程定位图像单纯手工勾画与修改的时间。
1.7 统计学方法
采用SPSS 21.0软件对自动勾画与手工勾画相关数据进行配对样本的非参数检验--Wilcoxon符号秩检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两种自动勾画算法与手工勾画OAR结果
(1)当参考图像和目标图像为同一患者时,左右髋骨及左右股骨头自动勾画的DSC、OI值均>0.8,显示出与手工勾画具有良好的重合性。Prostate算法左右髋骨DSC值为0.85±0.06和0.84±0.09,OI值为0.84±0.11和0.83±0.17,均高于General算法,而左右股骨头在不同算法下的DSC及OI值近似。对于具有相同密度的骨性组织,左右髋骨DSC、OI值均>左右股骨头,如Prostate法左髋骨DSC为0.85±0.06,左股骨头为0.82±0.05。在ΔV中显示出近似的结果,左右髋骨ΔV的绝对值<左右股骨头。如Prostate法左髋骨ΔV为-0.11±0.10,左股骨头为-0.17±0.13。骨性组织的ΔV<0,表明自动勾画对其勾画不足(见表1)。
(2)两种自动勾画算法在左髋骨体积均值存在统计学差异。Prostate算法左髋骨体积值>General算法,且更接近手工勾画。膀胱,直肠在自动勾画器官体积、DSC及OI值均显示出统计学差异。膀胱的两种自动勾画DSC,OI结果均>0.7。Prostate算法DSC为0.76±0.08,OI为0.74±0.09,均高于General算法(见表2)。
(3)对于接受ART的前列腺癌患者,自动勾画结果在应用放射治疗计划设计之前,需进行必要的校准及修改。
2.2 两种自动勾画算法CT图像
(1)Prostate算法膀胱ΔV为0.10±0.05,绝对值<General算法,且DSC,OI均高于General算法。Prostate算法勾画结果更接近手工勾画如图2所示。

图2 Prostate算法自动勾画膀胱接近手工勾画示图
表1 两种自动勾画算法与手工勾画OAR结果
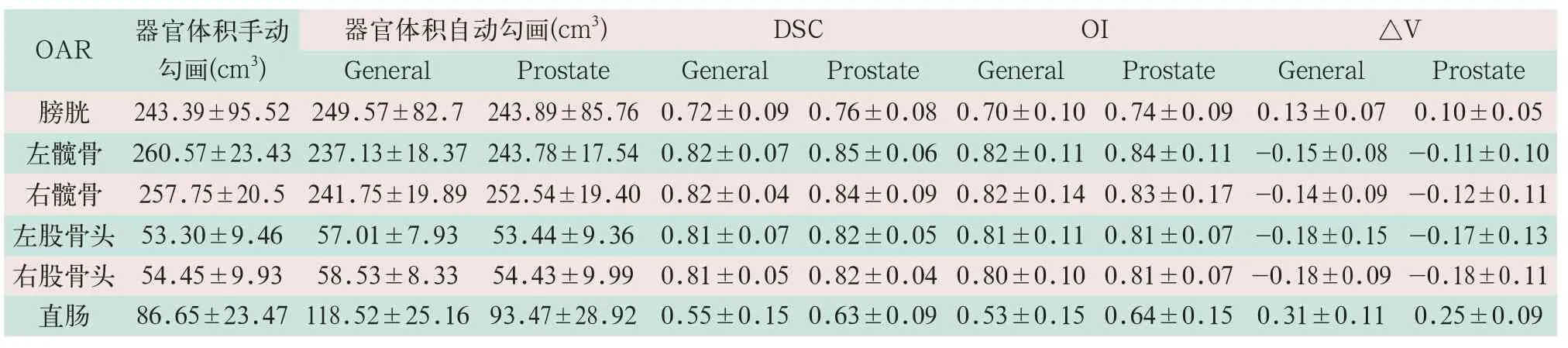
表1 两种自动勾画算法与手工勾画OAR结果
注:表中OAR为危及器官;DSC为形状相似性系数;OI为交叉指数;△V为体积差异。
?

表2 两种自动勾画算法统计结果
(2)两种自动勾画算法与手工勾画方式器官体积差异最大的是直肠,GeneralΔV为0.31±0.11,ProstateΔV为0.25±0.09。直肠手工勾画器官体积为86.65±23.47,General为118.52±25.16,Prostate为93.47±28.92,General与Prostate自动勾画器官体积均大于手动勾画结果(如图3所示)。

图3 两种自动勾画算法直肠体积勾画示图
(3)自动勾画对于像直肠及膀胱这样位置及形态不恒定的器官显示出过度勾画,ΔV值均为正值。第2程定位CT图像利用Prostate和General算法进行自动勾画,时间约为30 s。自动勾画加上手工修改平均耗时约6 min,明显少于单纯进行手工勾画平均耗时(约13 min),其时间缩短近54%。
3 讨论
由于放射治疗期间,大部分患者会发生体重减轻、肿瘤收缩、周围组织继发炎性反应等因素,以致于肿瘤和OAR体积及位置会发生相应的变化[12-14]。为了更好地发挥具有良好适形度和陡峭剂量变化梯度治疗技术的优势,需要对这些患者再次进行定位CT扫描并重新制定放射治疗计划,这就要求对同一患者进行多次相关轮廓的勾画。因此,需要自动勾画软件应用于自适放射治疗过程,以减少手工勾画靶区和OAR的时间,同时降低手工勾画出现的各种差异与误差[14-16]。
在接受前列腺癌ART的患者中,特别对于高密度的组织和器官,与周围组织形成了较为鲜明的密度差异,因而自动勾画的结果与“金标准”相比具有较高的重合性[10-13]。左右髋骨及左右股骨头DSC,OI值均>0.8。部分CT层面上经过较小范围的修改或不经修改的情况下即可满足临床要求,其结果低于彭应林等[17]报道的对于下颌骨及颞颌关节DSC(0.96;0.93)的自动勾画。考虑可能由于正常人在腹式呼吸的影响下,盆腔骨性结构位移引起的两程图像上配准误差。此外两种算法左右髋骨的DSC、OI值均高于左右股骨头,此结果也与上述的研究中下颌骨的DSC值为0.96高于颞颌关节DSC的结果0.93相一致,再次证明了影响自动勾画结果的因素除了与器官密度相关外,还与体积有关,即密度越高,体积越大,勾画效果越好。同样的情况也影响着膀胱的自动勾画。尿液的充盈所形成密度上的差异是自动勾画算法识别膀胱轮廓的基础与前提。对于本研究接受自适应放射治疗的患者,在每一程CT图像定位之前,嘱患者饮水充盈膀胱后利用便携式B超估算患者膀胱大体容积,这在一定程度上尽可能保持多次定位过程中膀胱充盈的一致性,最终在目标图像上得到了较为理想的结果DSC>0.7。由于膀胱体部得到良好的充盈,两种自动勾画结果与手工勾画形成了良好的重合度,这与膀胱顶部情况形成了巨大的反差。原因可能为近似球形的膀胱,其顶部容积减小以致增厚的膀胱壁与附近的肠管重合,导致局部勾画效果不佳。但由于Prostate算法在密度识别,修正运动器官配准差异等方面优于General算法,Prostate算法有效勾画面积(绿线)大于General算法(蓝线)[3,4,12]。
受肠内容物及肠管蠕动的影响,直肠个体间差异显著,即便同一患者随着时间的推移,在位置形态上也会产生明显的变化,由于直肠与邻近肠管结构近似,有时在CT断层图像上对于医生也很难精确的识别出分界线,以致于在手工勾画情况下不可避免的会把部分相邻肠管包入其中。观察自动勾画结果发现,往往造成直肠在头尾方向过度勾画明显要大于其他方向。定位CT图像中直肠与乙状结肠形成分界,但两种自动勾画算法(绿蓝线)无法认别。在直肠已消失的层面上,两种算法明显过度勾画。
前列腺底部与膀胱颈及其精囊腺,在远端与直肠相邻且密度接近,像这种与相邻组织缺乏明显对比度的结构必会导致自动勾画结果严重变形[3-4]。在临床实践中,可以利用MRI成像优势来提高前列腺与周围软组织对比度,所以前列腺病变最佳手工勾画方法是应用CT-MRI融合图像。但在目前,ABAS无法识别MRI图像,因此该研究排除了对前列腺癌靶区的自动勾画。
4 结语
理论上只要选择合适的参考图像,单一图谱的勾画方式可以满足临床要求。对于接受自适应放射治疗的前列腺癌患者,选用这种勾画方式主要考虑到,前后两程定位图像部分器官具有一致的解剖轮廓(如左右髋骨,左右股骨头),而且在定位之前采用了合理准备措施--排空直肠并对膀胱的充盈做到有效的估算,尽可能的保证直肠、膀胱这样的器官(随着充盈的不同处于不断变化)在两程定位图像上其轮廓的近似一致性。该研究最终得到的结果表明,Prostate算法勾画的精确程度要优于General算法。但在临床中,对于新定位的患者,由于个体的差异性的普便存在,是选择与参考图像近似的单一图谱勾画方式进行勾画,还是选择多重图谱勾画方式,即利用更多的参考图像去覆盖整个器官变化的范围,这是对类似的研究提出了新的命题。
