典型PPCPs在河流沉积物中的吸附特性
2019-04-28余绵梓李适宇胡嘉镗
余绵梓,袁 啸,李适宇,2*,胡嘉镗,2**
典型PPCPs在河流沉积物中的吸附特性
余绵梓1,袁 啸1,李适宇1,2*,胡嘉镗1,2**
(1.中山大学环境科学与工程学院,广东 广州 510275;2.广东省环境污染控制与修复技术重点实验室,广东 广州510275)
选取了咖啡因、氯霉素、卡马西平、磺胺甲噁唑和三氯生等5种PPCPs,在实验室条件下,近似模拟了自然河流的水/沉积物界面,应用中心复合实验设计,考察了温度、pH值、有机质含量和流速对PPCPs吸附比例的影响;利用多元回归方程拟合实验数据得到PPCPs吸附模型,并利用独立数据对模型进行验证,以建立适用于自然河流的PPCPs吸附模型.实验结果表明,咖啡因和卡马西平的吸附过程是放热反应,而磺胺甲噁唑、氯霉素和三氯生的吸附为吸热反应;pH值的升高对磺胺甲噁唑和三氯生的吸附能力产生抑制,但能促进咖啡因吸附,而对氯霉素和卡马西平的影响不大;有机质含量、流速和初始浓度对5种PPCPs的吸附比例变化趋势影响一致,随着各因素浓度或速度升高,PPCPs的吸附比例均随之增大,但影响程度有所不同.另外,吸附模型结果表明,5种PPCPs的吸附比例拟合值与实测值相关系数均达到0.8以上;独立数据验证结果表明,拟合值与实测值相关系数均达到0.8以上;因此,多元回归方程能较好地拟合环境因素与PPCPs吸附之间的关系,同时,在所考察的环境因素浓度范围内,多元回归方程较好地预测了PPCPs在自然河流沉积物中的吸附行为.
药物和个人护理品(PPCPs);吸附;沉积物;影响因素;多元回归方程
药物和个人护理品(PPCPs)的概念于1999年提出[1],由于使用量大、使用次数多,导致PPCPs持续不断进入河流、土壤和地下水等环境介质中,尤其是在河流中的检出率最高[2],近年来受到广泛关注.相关研究表明,PPCPs在水环境中的暴露会对水生生物产生毒害作用[3],并通过食物链累积和人类食用行为进入人体[4],对人类健康和生态系统构成极大的威胁[5].
PPCPs进入水环境中会发生扩散、降解和吸附等一系列迁移转化过程,其中PPCPs在底层水和沉积物间的吸附过程是影响PPCPs最终归趋的关键过程[6],直接影响到PPCPs在水体中的分布及其生物可利用度[7].当沉积物受到水流冲刷时,水/沉积物界面的PPCPs则会通过扩散、再悬浮等途径,重新进入上覆水体,引起水体二次污染[8].另外,PPCPs吸附到沉积物之后会发生垂向迁移过程,不仅会影响水流和溶质的运移,还对深层沉积物和地下水造成危害[9].因此,了解 PPCPs在沉积物中的吸附行为和吸附特性是一项重要的研究内容,对研究水环境中PPCPs的迁移转化和归趋有着重要意义.
研究表明,pH值[10]、有机质含量[11]和水体扰动程度[12]等因素对PPCPs的吸附结果均会产生影响.然而,目前对环境因素影响PPCPs吸附的研究多依据经济合作与发展组织化学品测试准则OECD guideline 106批实验方法,且通过单因素实验进行[13],该方法无法模拟真实河流中的水/沉积物界面,而且单因素实验难以反映自然环境下多因素构成的复杂体系,从而导致实验研究与实际测定的结果往往出现偏差[14].另一方面,关于PPCPs吸附模型,目前大多采用吸附动力学和吸附等温式模型,但上述模型均未考虑环境因素的作用[15-16],因此在实际应用中拟合结果与实际测定结果存在较大误差[17].为了考虑不同环境因素对PPCPs吸附的影响,多元回归方程的应用越来越得到重视.例如,Franco等[18]采用多元回归方程较好地拟合了有机物吸附量与辛醇水分配系数及电离常数之间的关系;Al- Khazrajy等[19]同样利用多元线性回归拟合了5种PPCPs在不同土壤中的吸附,均取得较好的拟合效果.然而,上述研究中所采用的拟合数据仅限于所研究区域的沉积物,对于环境条件不同的其它区域,模型的应用效果仍未可知.
总体而言,目前对PPCPs在河流沉积物中的吸附行为研究尚有待深入,特别是模拟真实河流环境中多种因素影响下的吸附过程,另外,适用于描述自然水体的PPCPs吸附过程的数学模型亦有待进一步建立.因此,本文选取卡马西平、三氯生、氯霉素、磺胺甲噁唑和咖啡因等5种典型PPCPs(理化性质如表1)为研究对象,在实验室条件下近似模拟自然河流的水/沉积物界面,应用中心复合实验设计(CCD),考察pH值、温度、有机质含量和流速等4种环境因素对不同性质PPCPs吸附的影响;在此基础上,利用多元回归方程对实验数据进行拟合,并结合独立数据对拟合模型进行预测和验证,以建立适用于所考察因素浓度水平内的PPCPs在河流沉积物中的吸附模型.
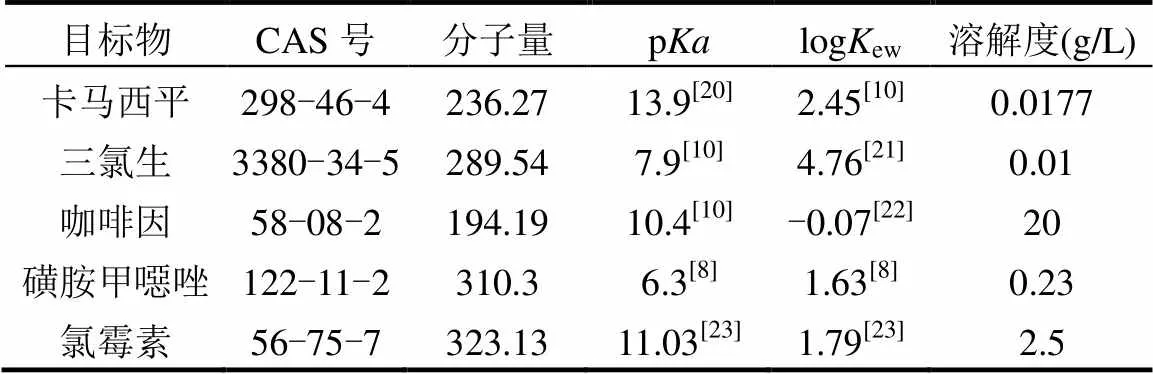
表1 目标物的理化性质
1 材料与方法
1.1 沉积物样品与实验用品
沉积物样品:样品采集自广州市石井河的表层沉积物(0~5cm),采集的沉积物样品经风干后过2mm 筛,在550℃下灼烧1h以去除有机质及咖啡因,保存在4℃下待用.
实验药品:咖啡因(CAF)纯度99.5%、氯霉素(CAP)纯度99.5%、卡马西平(CBZ)纯度99.5%、磺胺甲噁唑(SMX)纯度99.5%和三氯生(TCS)纯度99.5%均购自德国Dr. Ehrenstorfe公司.甲醇和乙腈(色谱纯)购自德国Merck公司;腐植酸(HA)购自美国Aladdin公司.
PPCPs储备液:取一定量PPCPs标准品,用甲醇溶解配成浓度为1g/L的储备液,于-18℃下保存待用.
PPCPs标准使用液:取一定体积储备液于50mL容量瓶中,用0.01mol/L CaCl2超纯水定容,加入10mmol/L NaN3以抑制微生物作用.
实验仪器:三重四极杆液相色谱-质谱联用仪(LC-MS/MS,Thermo Fisher Scientific)、SPE固相萃取装置(Automatic Science, China),pH计(Mettler Toledo, Swiss)、超纯水仪(Millipore, Germany)、氮吹仪(Anpel Scientific, China).
1.2 实验方法
吸附实验在OECD Guideline 106[13]基础上改进,以在实验室条件下近似模拟自然河流的水/沉积物界面,装置如图1所示.实验在一系列500mL烧杯中进行,取20g纯净沉积物样品平铺于干净烧杯中,加入20mL超纯水在暗处浸润24h使沉积物饱和[9].将上清液用针筒抽取去除.再用针筒缓慢加入100mL含100ng/L PPCPs溶液.溶液中含0.01mol/L CaCl2及100mg/L叠氮化钠,CaCl2用以保持PPCPs的电离度,叠氮化钠用以去除微生物影响;溶液中甲醇控制在0.1%以下以避免发生共溶现象.
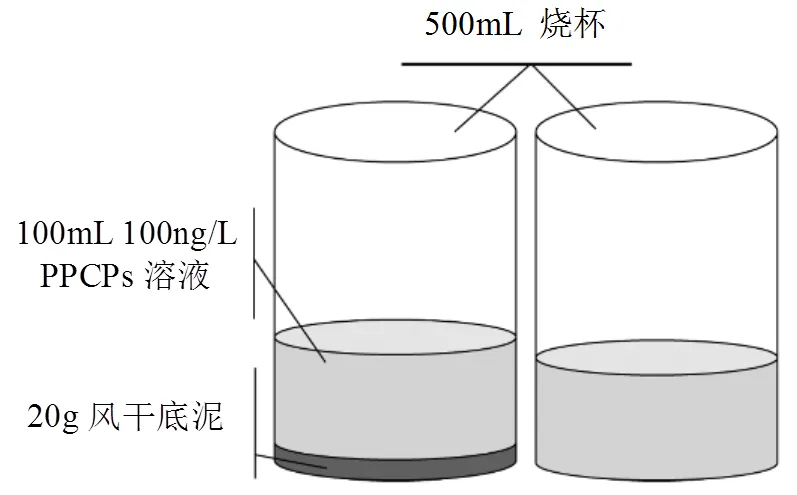
图1 吸附实验装置
实验前,洁净沉积物样品在121℃下高压灭菌15min 以去除微生物[24],并调节不同的pH值、温度、有机质含量、初始浓度和流速等条件,考察各因素对咖啡因在河流沉积物中吸附的影响.各因素的浓度水平根据响应面分析软件Design Expert 8.0.6中的中心复合实验设计确定,取值范围和大小如表2所示,得到实验设计共86组.其中,pH值通过0.1mol/L HCl或0.1mol/L NaOH调节.有机质含量通过添加HA进行调节;由于自然河流沉积物中有机质的成分复杂,在实验室条件下难以模拟,而前人研究表明,底泥中天然有机质的主要成分为HA[25-26],因此本实验中有机质含量的模拟通过在沉积物样品中添加HA进行,将一定量HA加入沉积物中,加入20mL超纯水搅拌均匀后在暗处浸润24h,使HA与沉积物充分吸附同时使沉积物饱和[9].流速与温度通过水浴恒温振荡器控制;流速大小的主要影响是改变水体的搅动状况,由于在实验室条件下难以模拟真实河流的水况,有学者将流速转换为振荡器转速以模拟自然条件下不同的水体搅动状况[12,27].本文采用王华等[28]通过大规模同步监测及泥沙悬浮实验建立的振荡器转速与水体流速之间的等量转化关系,其公式为
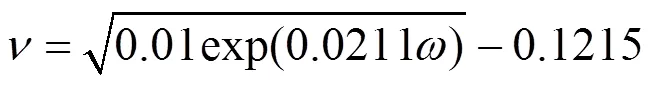
式中:为流速, m/s,为振荡器转速, r/min.
实验以不含底泥样品作为对照以考察水解、壁吸附等因素的影响,样品外裹锡纸以遮光去除光解作用.
取样后在5000r/min下离心10min,取上清液经0.22μm滤膜过滤,滤液经固相萃取和氮吹定容后进行LC-MS/MS测定.咖啡因的吸附特性通过吸附比例K表示,可通过式(2)计算:
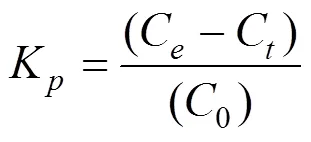
式中:K为PPCPs的吸附比例;0为PPCPs的初始浓度, ng/L;C为取样点小时实验组上清液PPCPs浓度, ng/L;C为取样时间点时对照组中咖啡因浓度, ng/L.
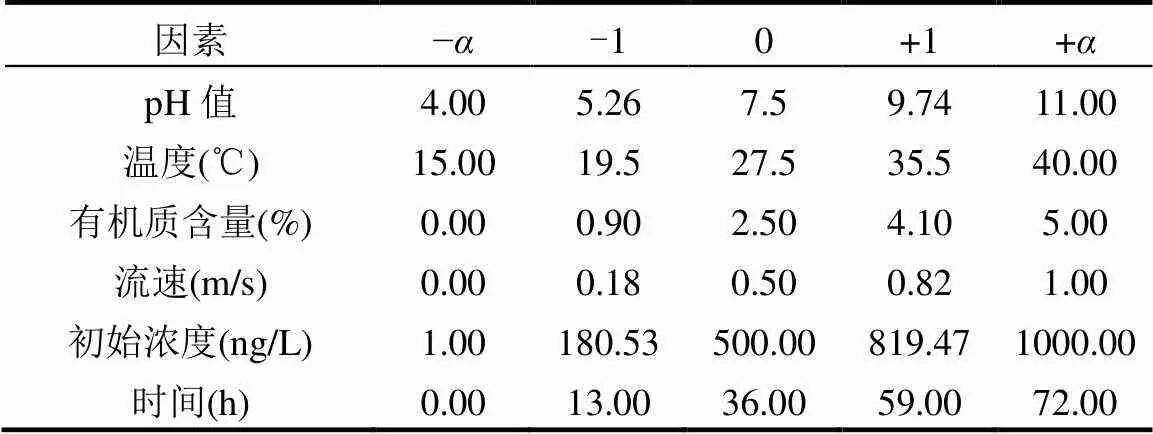
表2 影响因素的大小及范围
1.3 PPCPs测定
采用LC-MS/MS对实验样品的PPCPs浓度进行测定.流动相为0.1%甲酸水溶液:乙腈=85:15,流速为0.3mL/min,进样量为2μL,咖啡因、卡马西平、氯霉素、磺胺甲噁唑和三氯生的保留时间分别为1.55, 5.04,3.96,3.37和8.00min.
2 结果与讨论
2.1 环境因素对PPCPs吸附的影响
2.1.1 温度对PPCPs吸附的影响 由图2可知,随着温度的升高,咖啡因和卡马西平的吸附比例出现下降,磺胺甲噁唑、氯霉素和三氯生的吸附比例则上升.在pH值为7.5、初始浓度为500ng/L、有机质含量为2.5%、流速为0.5m/s、吸附时长为36h的条件下,随着温度从15℃升高到40℃,咖啡因的吸附比例下降了约10%,卡马西平的吸附比例则下降了5%;而其他3种物质的吸附比例均随之增加约5%.
从温度对PPCPs吸附比例的影响可以看出,咖啡因和卡马西平的吸附过程是放热反应,吸附程度随着温度的升高而降低;这是由于温度升高时,吸附平衡会向逆反应方向移动,同时物质的溶解度增大,从而抑制吸附反应[29];此外,温度升高还一定程度上促进了解吸过程的发生,因此,温度的升高使咖啡因和卡马西平的吸附比例降低[30].在天然河流的温度范围内(~20℃),温度变化对咖啡因吸附的影响较小,当温度大于30℃并向上递增时,咖啡因的吸附比例才出现较明显的下降趋势.由于温度的升高同样会促进分子的扩散,使得咖啡因与沉积物之间接触增多,增加吸附反应发生的机会,抵消一部分对吸附反应的抑制作用,因此温度较高时,升高温度对咖啡因吸附的抑制作用相比温度较低时更明显.研究表明,大部分PPCPs的吸附反应是放热过程,吸附程度随着温度的升高而降低.如Wang等[31]研究表明卡马西平在石墨上的吸附过程为放热反应.本研究中磺胺甲噁唑、氯霉素和三氯生的吸附比例随着温度的升高而略有增大,表明其吸附过程为吸热反应,也可能是由于分子间无规则运动即分子摆脱束缚引起的[32].王凯等[33]的研究也表明,磺胺甲噁唑的吸附是吸热反应,吸附平衡量随着温度升高而升高,但变化幅度不大.
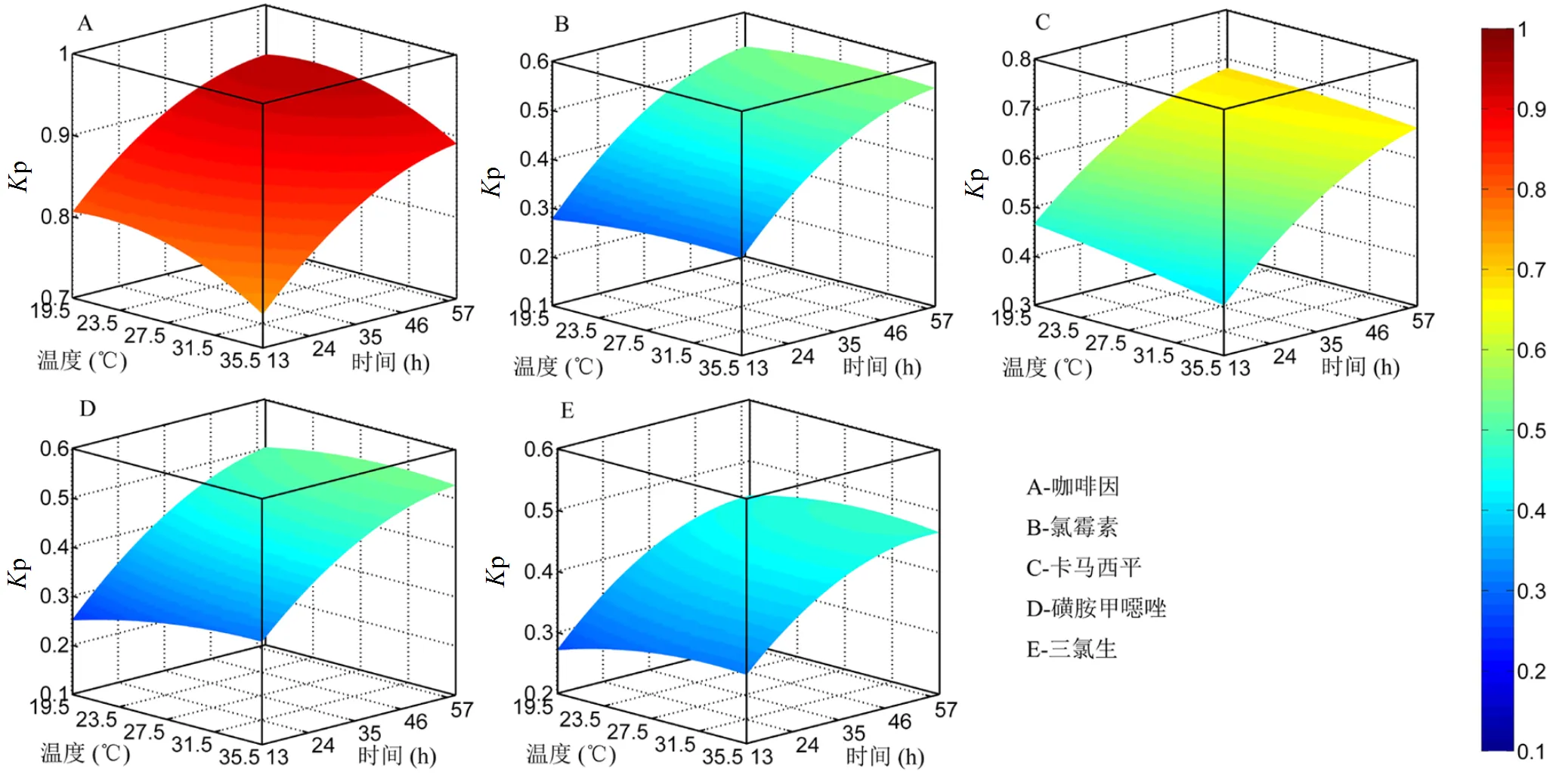
图2 温度对PPCPs吸附的影响
2.1.2 pH值对PPCPs吸附的影响 如图3所示.磺胺甲噁唑和三氯生的吸附比例随着pH值升高而降低,咖啡因的吸附比例在pH值约为10左右达到最高值,而氯霉素和卡马西平则基本不受pH值变化的影响.
pH值对PPCPs吸附的影响主要通过改变PPCPs的分子形态,进而影响其与沉积物颗粒的吸附机理从而影响吸附的程度.当pH值低于物质的p值时,酸性物质大部分保持质子态[34],比电离态更容易吸附,碱性物质则带有正电而易于吸附;随着pH值升高,酸性物质更加趋向电离带负电,吸附能力减弱,而碱性物质则水解趋向带正电,疏水性有所增大,吸附能力增强对于两性离子,pH值较低时,阳离子基团占主导,随着pH值升高,去质子化作用增强,吸附能力下降.从实验结果可以看出,与沉积物之间的静电反应是三氯生、磺胺甲噁唑和咖啡因的吸附机理之一,而卡马西平和氯霉素则基本不通过静电反应进行吸附.
三氯生的分子结构上含有一个—OH和多个Cl 基团,p= 7.8,呈弱酸性.在pH为7左右时,三氯生分子中83%~99%带正电,因此吸附能力较强[21];当pH>7.8时,三氯生主要以阴离子形式存在,因此表面带有负电荷的沉积物对其吸附效果较差[33].磺胺甲噁唑同样是一种酸性物质,在天然pH值条件下同时存在离子态和质子态[35],随着pH值变化,不同形态的磺胺甲噁唑所占比例也随之变化.离子态分子由于带有负电,与沉积物之间存在静电排斥作用而吸附能力较弱,因此磺胺甲噁唑的吸附主要依靠质子态分子的憎水反应[36].
咖啡因是一种碱性PPCPs,p值为10.4,因此在本研究pH值范围内(4~11),当pH值小于p值时,咖啡因主要呈现电离态,在水体中带正电,而沉积物颗粒带负电,因此咖啡因与沉积物颗粒之间可以通过静电反应进行吸附[37].从结果可以看出,pH值的升高咖啡因趋向于带正电,与带负电荷的沉积物颗粒之间相互作用力增强.但pH值大于pKa时,对咖啡因的水解产生抑制作用,从而降低吸附比例.
卡马西平和氯霉素的pKa值均较高(分别为13.9和11.03),为中性物质,憎水性吸附是主要的吸附机理,在本研究pH值范围内,质子态是卡马西平和氯霉素的主要形态,pH值对其影响很小[38].
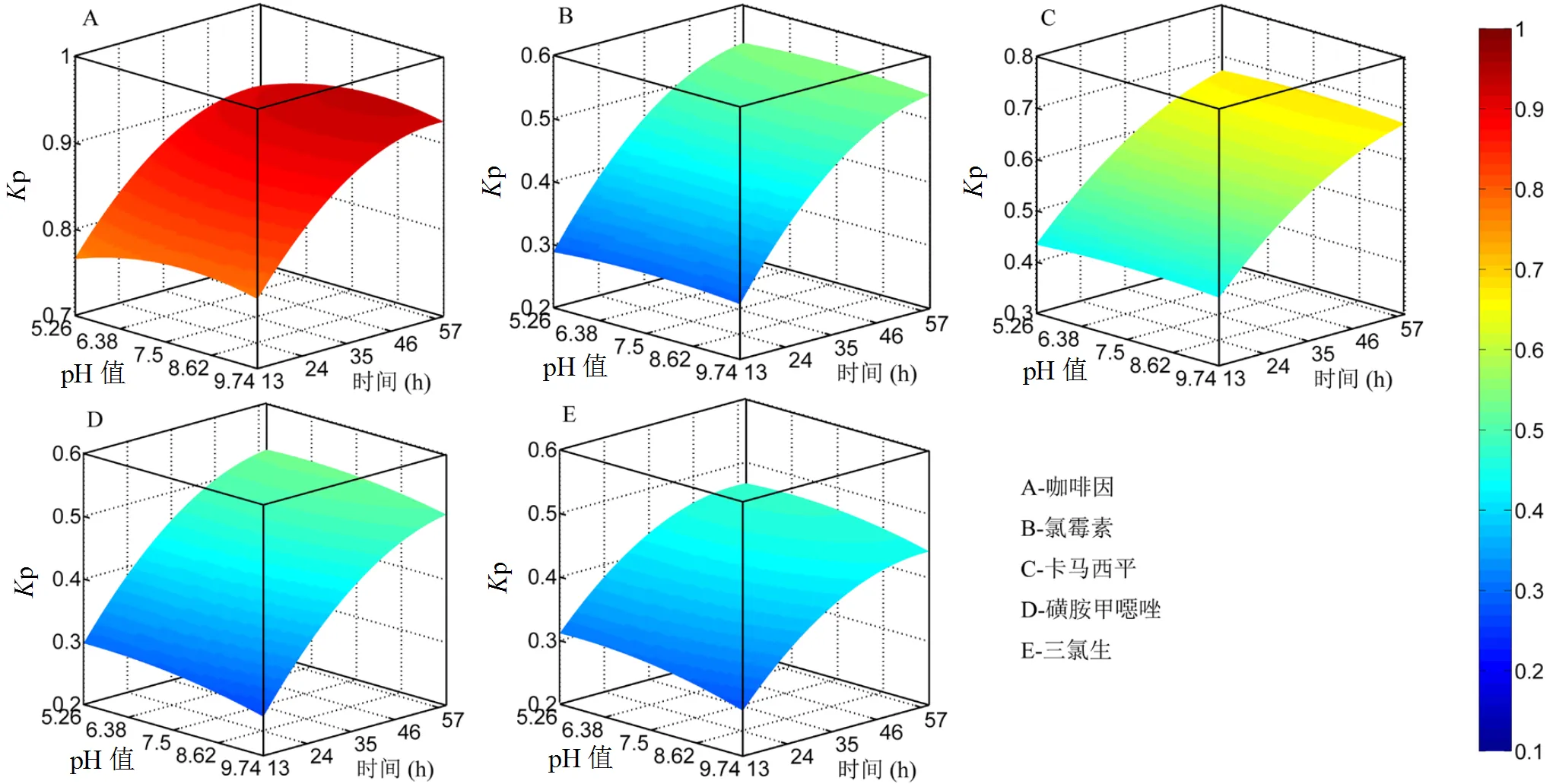
图3 pH值对PPCPs吸附的影响
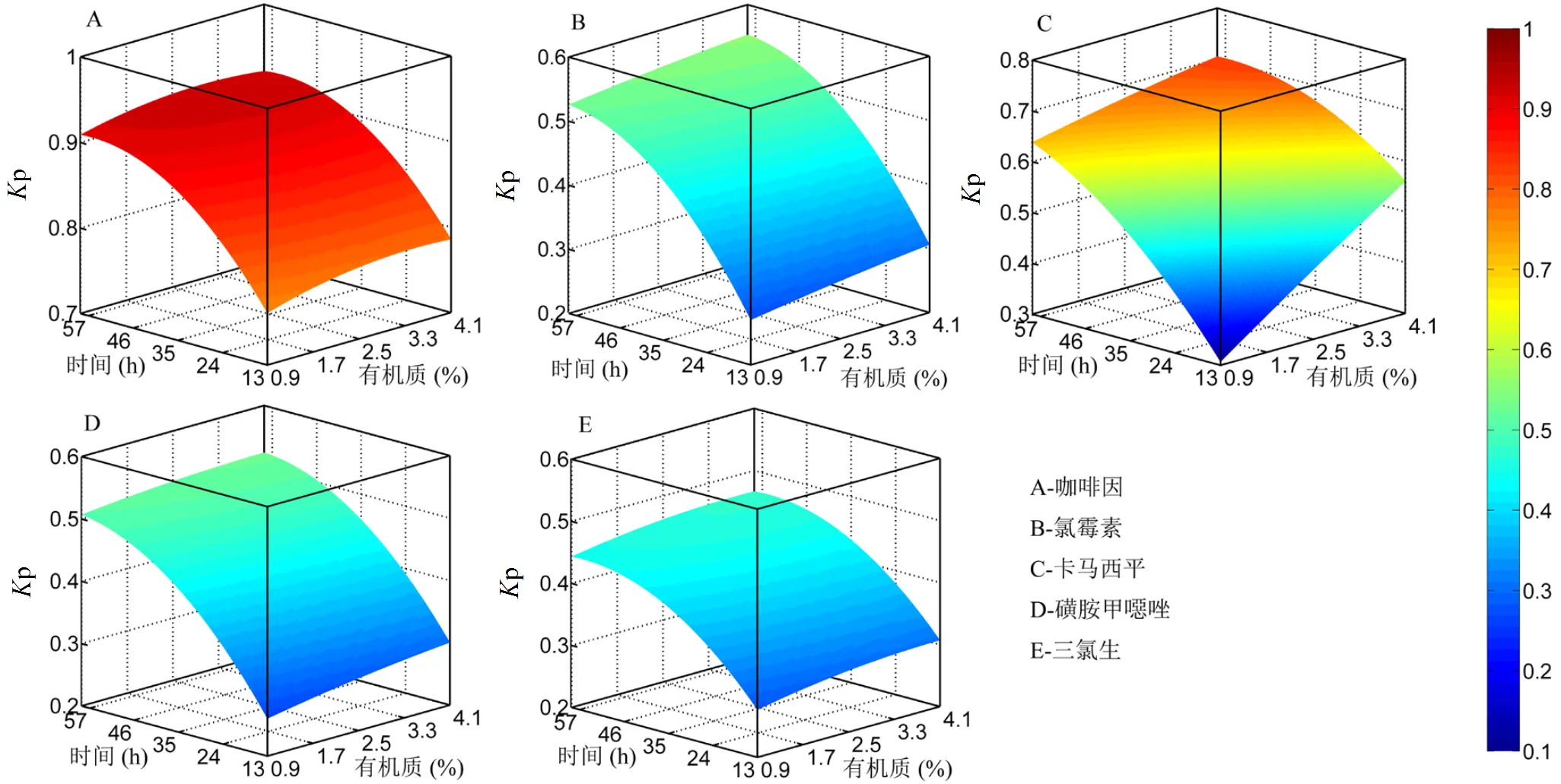
图4 有机质含量对PPCPs吸附的影响
2.1.3 有机质含量对PPCPs吸附的影响 如图4所示,有机质含量增大,在不同程度上促进PPCPs的吸附,其中影响最大的为卡马西平,在吸附进行13h未达到平衡时,有机质含量从0%升高到5%,卡马西平的吸附比例提高约40%,但随着接近吸附平衡,有机质含量变化的影响逐渐减弱.但对于其他4种PPCPs,有机质含量变化的影响程度较卡马西平小.
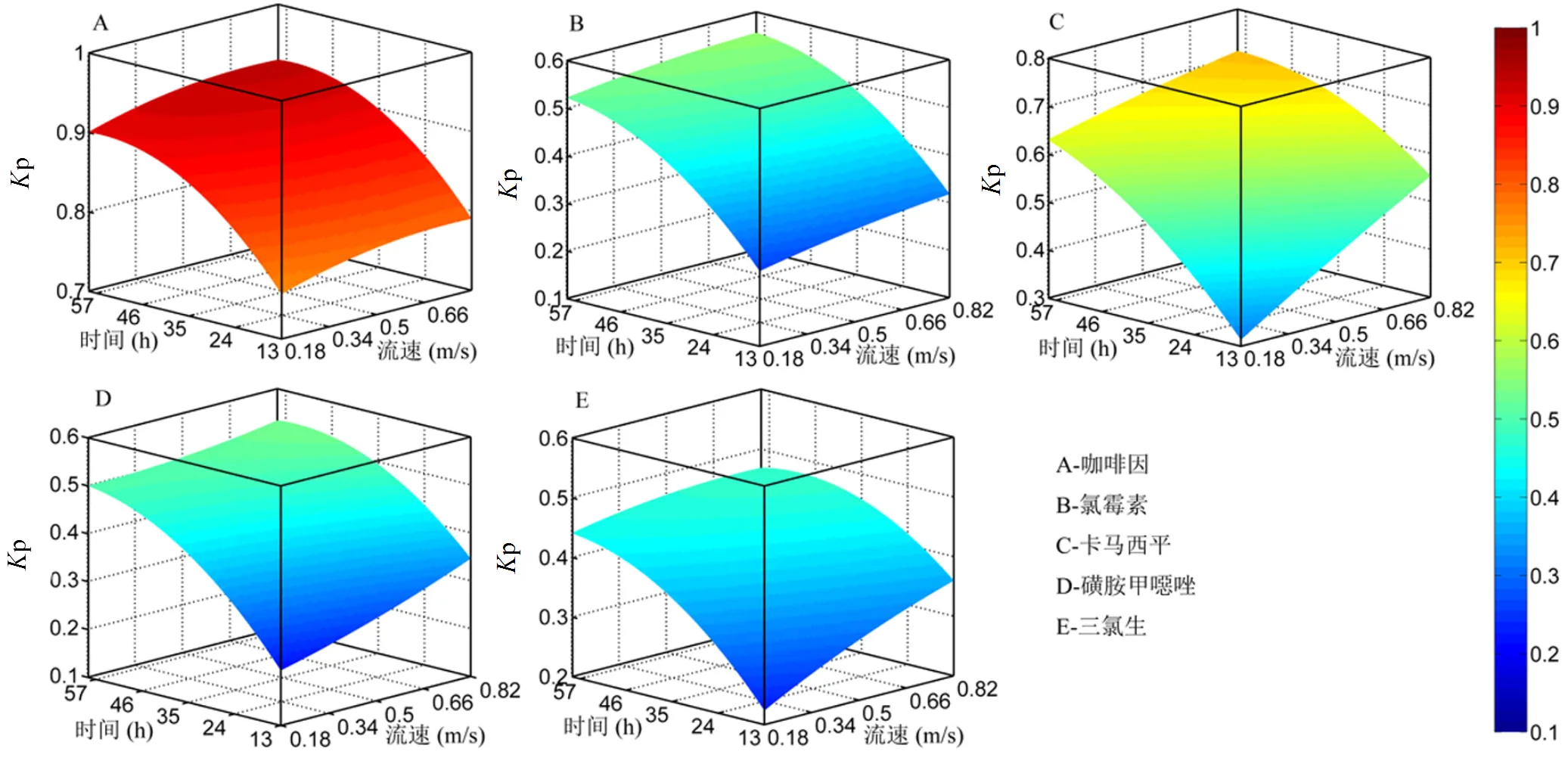
图5 流速对PPCPs吸附的影响
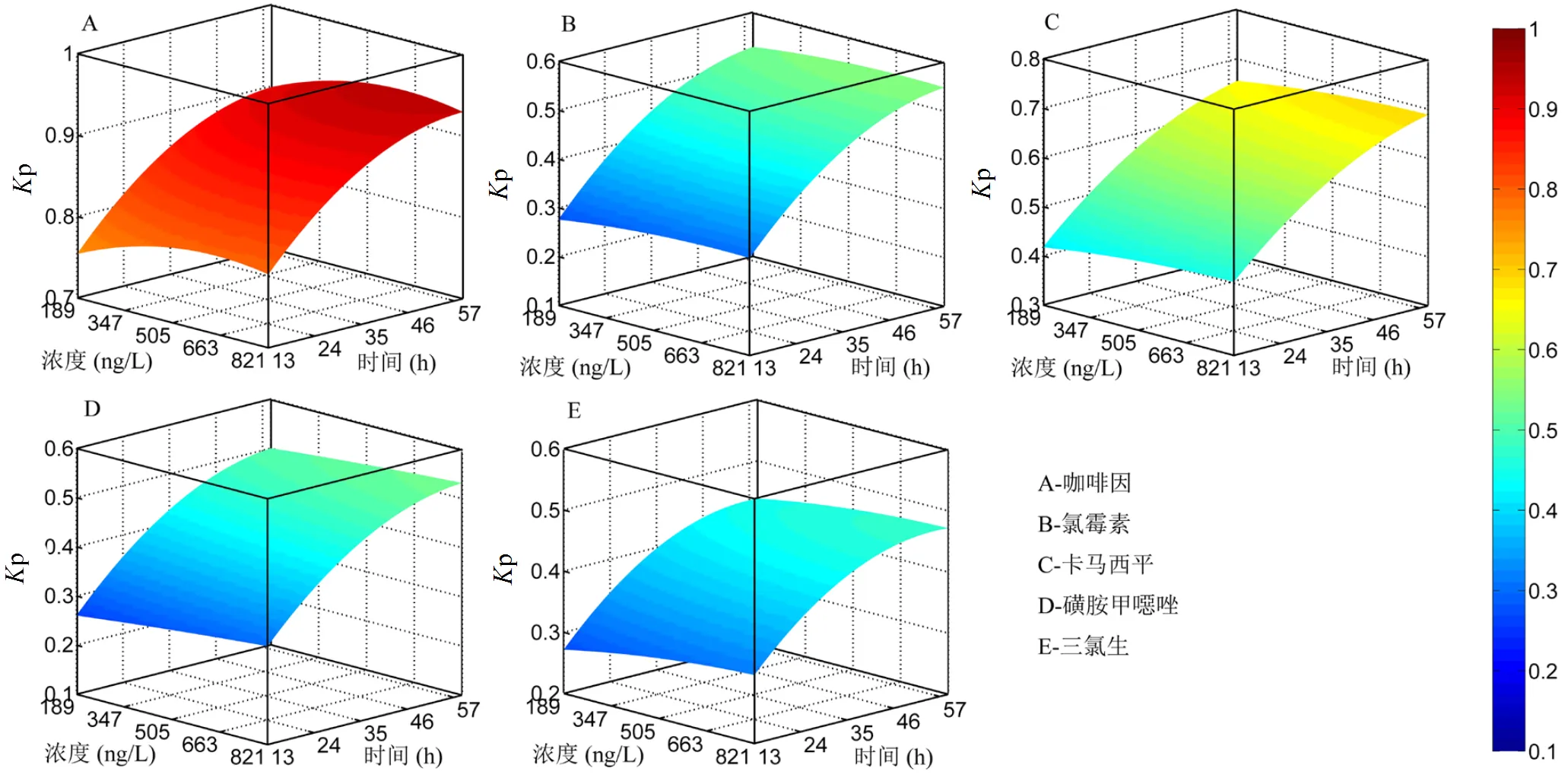
图6 初始浓度对PPCPs吸附的影响
有机质可以通过配体交换、阳离子桥接与阴离子交换等机制吸附至沉积物颗粒[39],同时一部分以溶解态形式溶于沉积物间隙水中.沉积物中的有机质与PPCPs进行结合是PPCPs吸附的途径之一,吸附态的有机质可以给PPCPs提供特异性吸附点位;此外,由于多数PPCPs带有一定的疏水性,可通过疏水反应与有机质进行吸附,然后通过有机质与沉积物颗粒的吸附间接吸附在沉积物中[40-41].从有机质含量对卡马西平吸附的影响可以看出,卡马西平和沉积物中有机质之间的反应是其主要的吸附机理,随着有机质含量的增大,能够提供更多吸附点位与卡马西平进行憎水反应[41],极性官能团数量也随之增多,可以作为π受体与卡马西平进行吸附[42].从有机质含量对其他4种PPCPs吸附的影响可以看出,其他4种物质不仅通过有机质进行吸附,还可通过范德华力、氢键作用等途径与沉积物颗粒进行吸附[10],但有机质含量的增大仍有一定的促进作用,表明与有机质进行吸附也是这几种PPCPs进行吸附的途径.
2.1.4 流速对PPCPs吸附的影响 如图5所示,随着流速的增大,5种PPCPs的吸附比例均随之增大,并且增大幅度随着反应时间的增长而减小;除卡马西平外,其余4种PPCPs吸附比例在57h后均达到最大值,而卡马西平吸附比例在57h后仍随着流速增大而有所增加.
流速是自然河流重要的水动力指标,在不同时间、河流不同区域的流速均会存在差异,改变沉积物上覆水体的搅动状况,水体的搅动会使沉积物颗粒再悬浮,增大颗粒与PPCPs之间的接触面积,更有利于吸附过程的进行[43].由于在实验室条件下难以模拟真实河流的水况,因此关于流速对吸附的影响还鲜有研究.Hajj-Mohamad等[12]通过设置静态和振荡条件,近似模拟了水体的搅动和静置状态,并对比了静态和振荡条件下4种药物的吸附差异,发现振荡条件下4种药物的吸附能力均大于静态条件;但该研究只是设置了2种条件,而没有研究不同的搅动状态对药物吸附的影响.由于流速的模拟在实验室条件下难以进行,本研究将流速大小转化为振荡器转速,有效地模拟了不同搅动水况对PPCPs吸附的影响.水体的搅动能促进PPCPs的吸附,搅动幅度越大,PPCPs的吸附比例越高;但这种促进作用随着反应时间的增长而减弱,这是由于随着反应时间增长,吸附反应已经接近平衡,且搅动情况下沉积物颗粒与水体接触,也有利于解吸的进行,因此可以从结果看到,达到吸附平衡时,流速的变化对最终吸附比例没有影响.
2.1.5 初始浓度对PPCPs吸附的影响 如图6所示,在实验条件范围内,5种PPCPs的吸附比例均随着初始浓度的增加而增大,增大幅度约为5%,但均呈现出随着吸附时间增大而幅度降低的趋势.
前人研究多用吸附等温式对不同浓度下PPCPs的吸附进行模拟,如Wang等[31]研究表明卡马西平和磺胺甲噁唑的吸附等温式更符合Langmiur模型,磺胺甲噁唑则更符合Freundlich模型;Xu等[34]通过实验分别对三氯生和磺胺甲噁唑的吸附等温式进行拟合,发现两者的吸附等温式均符合Freundlich公式,吸附能力随着初始浓度的增大而增强,但公式拟合结果中值不为1,说明2种物质的吸附等温式并不是线性的,不仅仅受到初始浓度的影响,还与其他环境因素有关.
本研究为模拟真实河流中PPCPs的浓度(ng/L级别),初始浓度的取值比一般实验室研究的浓度(mg/L)较小,因此吸附点位对于PPCPs而言相对充足[22],虽然初始浓度的增大能促进PPCPs的吸附,但其影响较小.
2.2 多元回归方程
PPCPs吸附模型的构建利用多元回归方程进行.采用多元逐步回归方法[44],考察PPCPs吸附比例与各因素之间的关系,并应用主成分分析方法筛选出各PPCPs的主要影响因素,以建立较为简化的PPCPs吸附模型.本研究模型的构建在SPSS 22.0中完成,将pH值、温度、有机质、初始浓度、流速和时间作为输入量,吸附比例K作为输出量.实验数据共86组,随机抽取其中9组作为独立验证数据,另外77组作为拟合数据;模型的可靠性通过拟合值与实测值的相关系数分析.
得到简化的PPCPs吸附模型如表3所示,式中参数乘积项表示2个因素对吸附比例的交互作用.从结果可以看出,拟合值与实测值的相关系数均大于0.8,相关性较强,表明5种PPCPs吸附模型均可以较好地拟合出环境因素与吸附比例之间的关系.从主成分分析结果可以看出,5种PPCPs吸附模型的主要影响因素分别为:咖啡因(温度、时间和流速),氯霉素(温度、初始浓度和时间),卡马西平(时间、有机质含量和流速),磺胺甲噁唑(时间和流速)及三氯生(时间和流速).可以看出,时间因素对5种PPCPs的吸附均有较大影响;除氯霉素外,其他4种PPCPs吸附的主要影响因素均包含流速;此外,温度、初始浓度和有机质含量也为主要的因素,而pH值对5种PPCPs的吸附影响程度均较小.
为检验模型的应用效果,利用所建立的模型对独立验证数据进行验证,结果如图7所示.从结果可以看出,5种PPCPs吸附模型对验证数据的拟合值与实测值相关系数均达到0.8以上,相关性较强,表明吸附模型可以很好地应用于PPCPs吸附结果的预测.
多元回归方程近年来开始被应用于吸附模型的建立.如Radka等[45]采用多元回归方程拟合7种有机物的Freundlich系数,拟合值与实测值的相关系数可达到0.97;He等[46]同样采用多元回归方程,建立五氯酚在不同土壤中的吸附模型,拟合值与实测值相关系数均达到0.8以上.但上述研究中,均未利用独立数据对模型进行验证,因而吸附模型的应用效果未知.本研究中,多元回归方程能较好地拟合环境因素与PPCPs吸附之间的关系,且利用独立数据进行验证,结果表明了多元回归方程应用于实际预测中的可行性.
注::温度(℃);:初始浓度(ng/L);:时间(h),:pH值;:有机质含量(%);:流速(m/s).
3 结论
3.1 在实验室条件下近似模拟了自然河流中的水/沉积物界面,综合考察了不同环境因素对咖啡因、氯霉素、卡马西平、磺胺甲噁唑和三氯生等5种PPCPs在沉积物中吸附的影响,并通过拟合和验证多元回归方程,得到适用于自然河流的PPCPs吸附模型.实验结果表明,咖啡因和卡马西平的吸附过程是放热反应,而磺胺甲噁唑、氯霉素和三氯生的吸附为吸热反应;pH值升高抑制磺胺甲噁唑和三氯生的吸附能力,而促进咖啡因的吸附过程,但对氯霉素和卡马西平的影响不大.随着有机质含量、流速和初始浓度值的增大,5种PPCPs的吸附比例均随之增大,但增大程度有所不同.
3.2 通过对77组实验数据进行多元回归方程拟合,5种PPCPs的吸附比例拟合值与实测值相关系数均达到0.8以上.利用模型对9组独立验证数据进行预测,拟合值与实测值相关系数也均达到0.8以上;结果表明,多元回归方程能较好地拟合环境因素与PPCPs吸附之间的关系,验证结果表明,在所考察的环境因素取值范围内,将其应用于预测自然河流中PPCPs在沉积物中的吸附是可行的.
[1] Daughton C G, Ternes T A. Pharmaceuticals and personal care products in the environment: agents of subtle change?[J]. Environmental Health Perspectives, 1999,107(Suppl 6):907-938.
[2] Dai G, Wang B, Huang J, et al. Occurrence and source apportionment of pharmaceuticals and personal care products in the Beiyun River of Beijing, China [J]. Chemosphere, 2015,119:1033-1039.
[3] Foran C M, Bennett E R, Benson W H. Developmental evaluation of a potential non-steroidal estrogen: triclosan [J]. Marine Environment Research., 2000,50(1-5):153-156.
[4] Lopes C, Persat H, Babut M. Transfer of PCBs from bottom sediment to freshwater river fish: a food-web modelling approach in the Rhône River (France) in support of sediment management. [J]. Ecotoxicology & Environmental Safety, 2012,81:17-26.
[5] Kemper N. Veterinary antibiotics in the aquatic and terrestrial environment [J]. Ecological Indicators, 2008,8(1):1-13.
[6] Zhou J, Broodbank N. Sediment-water interactions of pharmaceutical residues in the river environment [J]. Water Research, 2014,48:61-70.
[7] Maeng S K, Sharma S K, Abel C D T, et al. Role of biodegradation in the removal of pharmaceutically active compounds with different bulk organic matter characteristics through managed aquifer recharge: Batch and column studies [J]. Water Research, 2011,45(16):4722- 4736.
[8] Ying G, Zhao J, Zhou L, et al. Fate and occurrence of pharmaceuticals in the aquatic environment (surface water and sediment [J]. Comprehensive Analytical Chemistry, 2013,(62):453-557.
[9] Fenet H, Mathieu O, Mahjoub O, et al. Carbamazepine, carbamazepine epoxide and dihydroxycarbamazepine sorption to soil and occurrence in a wastewater reuse site in Tunisia [J]. Chemosphere, 2012,88(1):49-54.
[10] Karnjanapiboonwong A, Morse A N, Maul J D, et al. Sorption of estrogens, triclosan, and caffeine in a sandy loam and a silt loam soil [J]. Journal of Soils and Sediments, 2010,10(7):1300-1307.
[11] Lin A Y, Lin C, Tung H, et al. Potential for biodegradation and sorption of acetaminophen, caffeine, propranolol and acebutolol in lab-scale aqueous environments [J]. Journal of Hazardous Materials, 2010,183(1-3):242-250.
[12] Hajj-Mohamad M, Darwano H, Duy S V, et al. The distribution dynamics and desorption behaviour of mobile pharmaceuticals and caffeine to combined sewer sediments [J]. Water Research, 2017,108: 57-67.
[13] Oecd. Adsorption - Desorption Using a Batch Equilibrium Method [M]. OECD Guideline for the Testing of Chemicals, Paris: Organization for economic Cooperation and Development, 2000:1-44.
[14] Zhou J, Broodbank N. Sediment-water interactions of pharmaceutical residues in the river environment [J]. Water Res. 2014,48:61-70.
[15] Ho Y S. Review of Second-Order Models for Adsorption Systems [J]. Journal of Hazardous Materials, 2006,136:681-689.
[16] Samaraweera M, Jolin W, Vasudevan D, et al. Atomistic prediction of sorption free energies of cationic aromatic amines on montmorillonite: a linear interaction energy method [J]. Rapid Communications in Mass Spectrometry, 1993,7(7):163-166.
[17] Nguyen T H, Goss K, Ball W P. Polyparameter linear free energy relationships for estimating the equilibrium partition of organic compounds between water and the natural organic matter in soils and sediments [J]. Environmental Science & Technology, 2005,39(4): 913-924.
[18] Franco A, Trapp S. Estimation of the soil-water partition coefficient normalized to organic carbon for ionizable organic chemicals [J]. Environmental Toxicology & Chemistry, 2008,27(10):1995.
[19] Al-Khazrajy O S A, Boxall A. Impacts of compound properties and sediment characteristics on the sorption behaviour of pharmaceuticals in aquatic systems [J]. Journal of Hazardous Materials, 2016,317:198- 209.
[20] Zhang W, Ding Y, Boyd S A, et al. Sorption and desorption of carbamazepine from water by smectite clays [J]. Chemosphere, 2010, 81(7):954-960.
[21] Revitt D M, Balogh T, Jones H. Sorption behaviours and transport potentials for selected pharmaceuticals and triclosan in two sterilised soils [J]. Journal of Soils and Sediments, 2015,15(3):594-606.
[22] Martínez-Hernández V, Meffe R, Herrera S, et al. Sorption/desorption of non-hydrophobic and ionisable pharmaceutical and personal care products from reclaimed water onto/from a natural sediment [J]. Science of The Total Environment, 2014,472:273-281.
[23] Liao P, Zhan Z, Dai J, et al. Adsorption of tetracycline and chloramphenicol in aqueous solutions by bamboo charcoal: a batch and fixed-bed column study [J]. Chemical Engineering Journal, 2013, 228:496-505.
[24] 余绵梓,袁 啸,李适宇,等.咖啡因在河流沉积物中吸附的影响因素及模拟研究[J]. 环境科学学报, 2018,38(2):560-569. Yu M Z, Yuan X, Li S Y, et al. Laboratory and simulation study on the adsorption of caffeine onto river sediments and the influencing factors [J]. Acta Scientiae Circumstantiae, 2018,38(2):560-569.
[25] Nguyen L M. Organic matter composition, microbial biomass and microbial activity in gravel-bed constructed wetlands treating farm dairy wastewaters [J]. Ecological Engineering, 2000,16(2):199-221.
[26] Stevenson F J. Humus chemistry: genesis, composition, reactions. [J]. Soil Science, 1994,135(2):129-130.
[27] Gaullier C, Dousset S, Billet D, et al. Is pesticide sorption by constructed wetland sediments governed by water level and water dynamics? [J]. Environmental Science and Pollution Research, 2017, 25(4):1-12.
[28] 王 华,逄 勇.藻类生长的水动力学因素影响与数值仿真[J]. 环境科学, 2008,29(4):884-889. Wang H, Pang Y. Numerical simulation on hydrodynamic character for algae growth [J]. Environmental Science, 2008,29(4):884-889.
[29] Zeng G, Zhang C, Huang G, et al. Adsorption behavior of bisphenol A on sediments in Xiangjiang River, Central-south China [J]. Chemosphere, 2006,65(9):1490-1499.
[30] Cheng D, Liu X, Wang L, et al. Seasonal variation and sediment-water exchange of antibiotics in a shallower large lake in North China [J]. Science of The Total Environment, 2014,476-477:266-275.
[31] Wang C, Li H, Liao S, et al. Coadsorption, desorption hysteresis and sorption thermodynamics of sulfamethoxazole and carbamazepine on graphene oxide and graphite [J]. Carbon, 2013,65:243-251.
[32] 茶丽娟.卡马西平在云南典型土壤上的吸附研究[D]. 昆明:昆明理工大学, 2012. Cha M J. Sorption of carbamazepine in yunnan soils [D]. Kunming: Kunming University of Science and Technology, 2012.
[33] 王 凯,李侃竹,周亦圆,等.河流沉积物对典型PPCPs的吸附特性及其影响因素[J]. 环境科学, 2015,36(3):847-854. Wang K, Li K Z, Zhou Y Y, et al. Adsorption characteristics of typical PPCPs onto river dediments and its influencing factors [J]. Environmental Science, 2015,36(3):847-854.
[34] Xu J, Wu L, Chang A C. Degradation and adsorption of selected pharmaceuticals and personal care products (PPCPs) in agricultural soils [J]. Chemosphere, 2009,77(10):1299-1305.
[35] Hebig K H, Groza L G, Sabourin M J, et al. Transport behavior of the pharmaceutical compounds carbamazepine, sulfamethoxazole, gemfibrozil, ibuprofen, and naproxen, and the lifestyle drug caffeine, in saturated laboratory columns [J]. Science of The Total Environment, 2017,590-591:708-719.
[36] Kay P, Blackwell P A, Boxall A B. Column studies to investigate the fate of veterinary antibiotics in clay soils following slurry application to agricultural land [J]. Chemosphere, 2005,60(4):497-507.
[37] Fairbairn D J, Karpuzcu M E, Arnold W A, et al. Sediment-water distribution of contaminants of emerging concern in a mixed use watershed [J]. Science of the Total Environment, 2015,505:896-904.
[38] Schaffer M, Boxberger N, Börnick H, et al. Sorption influenced transport of ionizable pharmaceuticals onto a natural sandy aquifer sediment at different pH [J]. Chemosphere, 2012,87(5):513-520.
[39] 王 磊,应蓉蓉,石佳奇,等.土壤矿物对有机质的吸附与固定机制研究进展[J]. 土壤学报, 2017,54(4):805-818. Wang L, Ying R R, Shi J Q, et al. Advancement in study on adsorption of organic matter on soil minerals and its mechanism [J]. Acta Pedologica Sinica. 2017,54(4):805-818.
[40] 鲍艳宇,周启星,万 莹,等.土壤有机质对土霉素在土壤中吸附-解吸的影响[J]. 中国环境科学, 2009,29(6):651-655. Bao Y Y, Zhou Q X, Wang Y, et al. Effect of soil organic matter on adsorption and desorption of oxytetracycline in soils [J]. China Environmental Science, 2009,29(6):651-655.
[41] Yamamoto H, Nakamura Y, Moriguchi S, et al. Persistence and partitioning of eight selected pharmaceuticals in the aquatic environment: Laboratory photolysis, biodegradation, and sorption experiments [J]. Water Research, 2009,43(2):351-362.
[42] Ahmed M B, Zhou J L, Ngo H H, et al. Chloramphenicol interaction with functionalized biochar in water: sorptive mechanism, molecular imprinting effect and repeatable application [J]. Science of The Total Environment, 2017,609:885-895.
[43] 王 鹏,冯 燕,蔡赟杰.水动力条件对太湖底泥吸附苯胺性能的影响[J]. 环境科学与技术, 2013,36(5):117-123. Wang P, Feng Y, Cai Y J. Aniline adsorption properties on taihu lake sediment under different hydrodynamic conditions [J]. Environmental Science & Technology, 2013,36(5):117-123.
[44] Arulsudar N, Subramanian N, Muthy R S. Comparison of artificial neural network and multiple linear regression in the optimization of formulation parameters of leuprolide acetate loaded liposomes [J]. Journal of Pharmacy Sciences, 2005,8(2):243-258.
[45] Radke M, Lauwigi C, Heinkele G, et al. Fate of the antibiotic sulfamethoxazole and its two major human metabolites in a water sediment test [J]. Environmental Science & Technology, 2009,43(9): 3135-3141.
[46] He Y, Xu J, Wang H, et al. Detailed sorption isotherms of pentachlorophenol on soils and its correlation with soil properties [J]. Environmental Research. 2006,101(3):362-372.
致谢:中山大学环境科学与工程学院樊青娟老师对本研究中PPCPs的测定提供了帮助,刘广州和徐闯同学在现场采样过程中提供了帮助,在此一并表示感谢!
Experimental and modeling study of sorption characteristics of selected PPCPs onto river sediments.
YU Mian-zi1, YUAN Xiao1, LI Shi-yu1,2*, HU Jia-tang1,2**
(1.School of Environmental Science and Engineering, Sun Yat-sun University, Guangzhou 510275, China;2.Guangdong Province Key Laboratory of Environmental Pollution Control and Remediation Technology, Guangzhou 510275, China)., 2019,39(4):1724~1733
A water/sediment interface was roughly simulated in laboratory, and a central composite design was applied to investigate the influence of temperature, pH, organic content, and velocity on the sorption proprotion of five selected PPCPs (caffeine, chloramphenicol, carbamazepine, sulfamethoxazole and triclosan). Based on the experimental data, multiple regression equations were fitted and calibrated to establish favorable sorption models for PPCPs in the river systems. The results showed that the sorption process of caffeine and carbamazepine were exothermic reaction, and the sorption of sulfamethoxazole, chloramphenicol and triclosan were endothermic reaction. The increase of pH inhibited the sorption capacity of sulfamethoxazole and triclosan, but it could promote the sorption of caffeine, while it had little effect on the sorption of chloramphenicol and carbamazepine. The organic content, velocity and initial concentration had consistent effect on the sorption ratio of PPCPs. With the increase of the values of the factors, the sorption ratio of the five PPCPs increased with different degrees. The fitting and calibration results showed that the correlation coefficients between fitted and measured values of PPCPs sorption proportions were both above 0.8. Therefore, within the ranges of concentration of the investigated factors, the multiple regression equations were able to reasonably model and predict the sorption of PPCPs onto rivers sediment.
PPCPs;sorption;sediment;parameters;multiple regression equation
X522
A
1000-6923(2019)04-1724-10
2018-08-03
广东省自然科学基金资助项目(2018A030313135);中央高校基本科研业务费(20133800031650007);国家重点研发计划项目(2016YFC0502803)
*责任作者, 教授, eeslsy@mail.sysu.edu.cn; 副教授, hujtang@mail.sysu. edu.cn
余绵梓(1993-),男,广东潮州人,中山大学硕士研究生,主要从事PPCPs吸附模拟研究.发表论文1篇.
