动态高压微射流制备玉米芯可溶性膳食纤维工艺及功能特性研究
2019-04-11曹慧慧赵海涛邢希双项爱丽张立田段晓然汤思凝吴兆举杜瑞焕孙淑玲
曹慧慧,王 磊,赵海涛,邢希双,项爱丽,齐 彪,张立田,周 鑫,段晓然,张 鑫,汤思凝,林 田,吴兆举,肖 琎,杜瑞焕,孙淑玲*
(1.唐山市食品药品综合检验检测中心,河北唐山 063000;2.河北省农产品质量安全检测技术创新中心,河北唐山 063000;3.唐山市农业广播电视学校,河北唐山 063000;4.唐山市农机技术推广站,河北唐山 063000)
膳食纤维是指不能被人体胃肠道中消化酶所消化的,不被吸收利用的多糖类物质。 在消化系统中有吸收水分的作用,在胃肠中占据较大空间,使人有饱腹感,利于减肥;膳食纤维有吸水膨胀性,可刺激胃肠道消化液的分泌,使胃肠蠕动增强,推动进食,减少食物残渣在胃肠道停留的时间,增加粪便量,促进粪便排泄,改善肠道菌群,为益生菌的增殖提供能量和营养[1-3]。膳食纤维是健康饮食不可缺少的,具有清洁消化壁和增强消化功能,促进铅等重金属及有毒物质的吸附和排泄,预防重金属中毒。膳食纤维可减缓消化速度和最快速排泄胆固醇,可以通过延缓胃排空,改变肠运转时间等使糖的吸收减慢,防止饭后血糖骤升[4-7]。
我国作为玉米种植大国,每年均产生大量的副产物——玉米芯(约为2 000万t),除少量被用做饲料外,绝大部分被焚烧或遗弃,造成严重的环境污染和资源浪费,然而玉米芯中含有丰富的可溶性膳食纤维(SDF),是制备SDF的理想原料。目前有关玉米芯SDF提取方法主要有酶解法[8]、超声波碱解法[9]和微波法[10]。动态高压微射流(DHPM)技术是集输送、超微粉碎、混合、膨化、加压加温等多种单元操作为一体的技术,其理论基础包括流体力学理论、超高压理论及撞击流理论3种。高压的推动作用可使流体混合物物料瞬时通过,当压力发生变化时,产生的巨大压力可使流体混合物物料受到剧烈的高速碰撞、剪切、高频振荡、粉碎等综合作用,使物料受到较好的超微化、均一化和微乳化作用,进而影响物料的理化性质和结构[11-13]。为进一步研究玉米芯中SDF的功效,充分利用玉米芯资源,笔者以SDF提取率为考察指标,对DHPM制备玉米芯中SDF的工艺条件进行优化,确定其最佳提取工艺,并对玉米芯中SDF提取物的功能特性进行分析。
1 材料与方法
1.1材料玉米芯由唐山润泽粮油食品有限公司提供。
DHPM-SDF:称取30 g玉米芯,加入一定量的去离子水,混合均匀,用胶体研磨机处理2次,利用动态高压均质超微粉碎设备处理一定次数,调节pH为5~6,添加2%纤维素酶,在50 ℃恒温水浴摇床中反应30 min,酶解液于95 ℃灭酶5 min,冷却至室温,高速离心分离。沉淀物经干燥得水不溶性膳食纤维(IDF);上清液经旋转蒸发浓缩至原体积的1/8,用4倍体积的75%乙醇沉淀20 min,真空抽滤,滤渣于60 ℃鼓风干燥得到SDF。
Control-SDF:称取30 g玉米芯,加入一定量的去离子水,混合均匀,用胶体研磨机处理2次,调节pH为5~6,添加2%纤维素酶,在50 ℃恒温水浴摇床中反应30 min,酶解液于95 ℃灭酶5 min,冷却至室温,高速离心分离。沉淀物经干燥得IDF;上清液经旋转蒸发浓缩至原体积的1/8,用4倍体积的75%乙醇沉淀20 min,真空抽滤,滤渣于60 ℃鼓风干燥得到SDF。
盐酸、水杨酸、亚硝酸钠、乙醇等均为分析纯(北京化学试剂公司);JK1002电子分析天平(北京朗科兴业称重设备有限公司);TD5B台式离心机(盐城凯特实验仪器有限公司);XD-3000BDQ旋转蒸发仪(上海贤德实验仪器有限公司);DR889-1电热恒温鼓风干燥箱(苏州达瑞电热设备有限公司);HH-1水浴恒温振荡器(常州国华电器有限公司);JM-65 胶体磨(上海多源机械制造有限公司);M-110EH高压微射流均质机(美国必宜DeBEE公司)。
1.2方法
1.2.1DHPM制备玉米芯SDF工艺条件的选择。
1.2.1.1料液比。高压均质压力为60 MPa,均质次数4次,分别选择玉米芯与水的比例为1∶2、1∶3、1∶4、1∶5、1∶6、1∶7、1∶8(g∶mL),考察料液比对SDF提取率的影响,每个水平3次重复。
1.2.1.2均质压力。高压均质次数为4次,料液比1∶6,分别选择均质压力为20、40、60、80、100 MPa,考察均质压力对SDF提取率的影响,每个水平3次重复。
1.2.1.3均质次数。高压均质压力为60 MPa,料液比1∶6(g∶mL),分别选择均质次数为2、4、6、8、10次,考察均质次数对SDF提取率的影响,每个水平3次重复。
1.2.2可溶解性(WS)的测定。依据李伦[14]的方法,略有修改。称取1 g左右样品于离心管,按1∶10的比例加入蒸馏水,混合均匀后,室温下静置1 h,3 000 r/min离心10 min,收集上清液和残渣,分别干燥,称重。
WS=(干燥后上清液质量/样品粉质量)×100%
1.2.3持水力(WHC)的测定。依据陈菊红[15]的方法,略有修改。准确称取1 g样品于50 mL离心管中,加入20 mL去离子水,混合均匀后置于4 ℃条件下放置24 h,4 200 r/min离心15 min,称重。
WHC(g/g)=(样品被水饱和后质量-样品粉质量)/样品粉质量
1.2.4持油力(OHC)的测定。依据陈菊红[15]的方法,略有修改。准确称取1 g样品于50 mL离心管中,加入10 mL橄榄油,混合均匀后置于4 ℃条件下放置1 h,4 200 r/min离心15 min,称重。
OHC(g/g)=(样品被油饱和后质量-样品粉质量)/样品粉质量
1.2.5膨胀力(SC)的测定。依据李伦[14]的方法,略有修改。准确称取0.2 g样品置于刻度试管中并记录其体积,加入5.0 mL蒸馏水,混合均匀后在4 ℃条件下放置18 h,记录样品吸水后的体积。
SC(mL/g)=(溶胀后样品体积-样品粉体积)/样品粉质量
1.2.6·OH清除率的测定。依据汤小明[16]的方法,略有修改。在反应体系中(水杨酸-乙醇溶液9 mmol/L,Fe2+9 mmol/L,H2O28.8 mmol/L)加入具有清除·OH能力的物质,便会与水杨酸竞争·OH,而使有色物质生成量减少。采用固定反应时间法,在相同体积的反应体系中加入不同浓度的膳食纤维(DF),并用蒸馏水作为空白对照,在波长510 nm处测量加入不同浓度DF后的吸光度,代入清除率计算公式便可计算出不同浓度的DF清除·OH自由基的能力。
·OH清除率=[1-(A1-A2)/A3]×100%
式中,A1为0.5 mL水杨酸-乙醇 + 1.0 mL DF + 0.5 mL Fe2++ 5.0 mL H2O2吸光度;A2为0.5 mL水杨酸-乙醇 + 1.0 mL DF + 0.5 mL 蒸馏水+ 5.0 mL H2O2吸光度;A3为0.5 mL水杨酸-乙醇 + 1.0 mL 蒸馏水 + 0.5 mL Fe2++ 5.0 mL H2O2吸光度。
1.2.7O2·-清除率的测定。依据汤小明[16]的方法,略有修改。取0.05 mol/L Tris-HCl缓冲液(pH 8.2)4.0 mL,置于25 ℃水浴中预热20 min,分别加入1 mL待测液和1 mL 25 mmol/L 邻苯三酚溶液,混匀后于25 ℃水浴中反应5 min,加入8% HCl溶液100 μL终止反应,波长320 nm处测定吸光度(A),以1 mL蒸馏水代替待测液做空白试验。
O2·-清除率 =[1-(A1-A2)/A3]×100%
式中,A1为4 mL Tris-HCl + 1.0 mL DF + 2 mL 邻苯三酚吸光度;A2为4 mL Tris-HCl + 1.0 mL DF + 2 mL 蒸馏水吸光度;A3为4 mL Tris-HCl + 1.0 mL 蒸馏水+ 2 mL 邻苯三酚吸光度。
1.2.8DPPH自由基清除率的测定。依据汤小明[16]的方法,略有修改。DPPH自由基在95%乙醇溶液中是一种稳定的自由基,在波长517 nm处有吸收峰,呈紫色。当自由基清除剂存在时,DPPH的孤对电子被配对,颜色变浅,在最大吸收波长处吸收度变小,且颜色变化与配对电子数呈化学计量关系,因此可用来评价自由基的清除情况。将4 mL待测液加入2 mL 0.2 mmol/L DPPH自由基溶液,于25 ℃水浴中反应20 min后于517 nm处测定吸光度(A),以蒸馏水代替待测液做空白试验。
DPPH自由基清除率=[1-(A1-A2)/A3]×100%
式中,A1为4 mL DF + 2.0 mL DPPH自由基吸光度;A2为4 mL DF + 2.0 mL 95%乙醇吸光度;A3为4 mL 蒸馏水 + 2.0 mL DPPH自由基吸光度。
1.2.9总酚含量的测定。依据汤小明[16]的方法,略有修改。取样品粉末1 g于锥形瓶中,按1∶30(W/V)的比例加入70%乙醇溶液,于30 ℃的恒温水浴摇床中(800 r/min)振荡提取24 h。提取完成后,3 000 r/min离心10 min,并用原溶剂定容至50 mL。用棕色瓶装好放入-20 ℃的冰箱中待测。取一定浓度的样品0.5 mL,加入2.5 mL 0.2 N Folin-Ciocalteu 试剂,振荡30 s后反应5 min,再加入2 mL 7.5%(W/V)的Na2CO3溶液,振荡20 s后反应2 h,在760 nm处测定吸光度,空白对照以去离子水代替样品进行反应。总酚含量以没食子酸当量(Gallic Acid Equivalent,mg/g,干基)表示。
1.3数据处理采用Design-Expert 7.0进行试验设计和数据处理。
2 结果与分析
2.1DHPM制备玉米芯SDF工艺条件
2.1.1料液比。由图1可知,当玉米芯与水的比例为1∶7时,SDF/IDF和SDF提取率均达到最大值,随着液料比的增加,底物和酶被稀释,SDF的提取率和SDF/IDF比值会有所减少。分析其原因,由酶促反应动力学可知,在酶浓度不变时,当底物浓度较低时,反应速率的增加与底物浓度的增加成正比,随底物浓度的增加,反应速率的增加逐渐减少;最后,当底物浓度增加到一定量时,反应速率达到最大值,不再随底物浓度的增加而增加,液料比的增大相当于减少了底物浓度,因而使SDF的提取率在1∶7时达到最佳,随后逐渐下降。
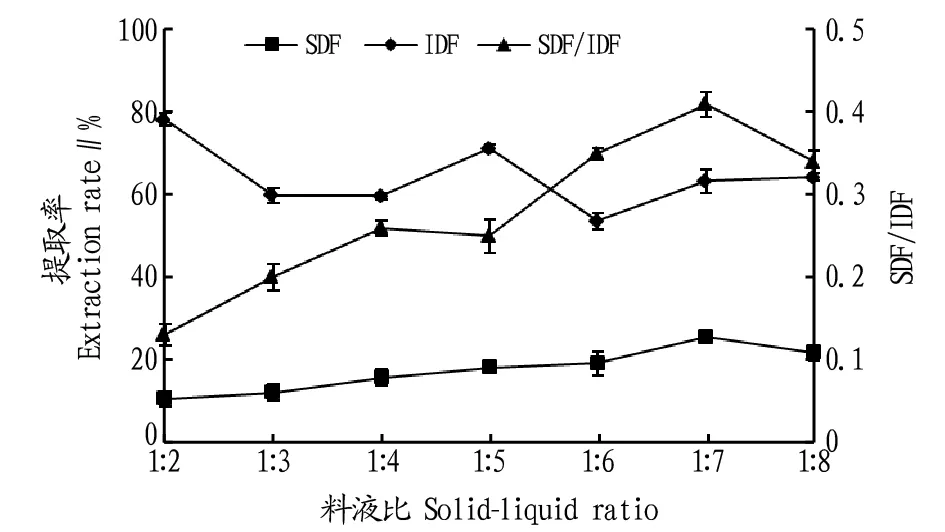
图1 料液比对SDF、IDF提取率及SDF/IDF比值的影响Fig.1 Effects of solid-liquid ratio on the SDF, IDF extraction rate and SDF/IDF
2.1.2均质压力。由图2可知,SDF/IDF和SDF的提取率比值随着压力增加而增大,IDF的提取率随着压力增加而减小。研究证明,瞬时高压作用可使SDF含量有所增加,其所受压力越大,可溶性成分增加越多。另外,膳食纤维的微观结构、平均粒径和官能团随瞬时高压作用的压力变化而变化,随着压力的增大,暴露更多的酶解结合位点,有利于纤维素酶水解IDF,从而提高SDF的提取率[17]。由于高于60 MPa处理时SDF提取率提高并不显著,而IDF提取率下降显著,说明60 MPa处理后,部分SDF聚合度降低,不能被乙醇沉淀,故选择60 MPa作为最佳处理压力。

图2 处理压力对SDF、IDF提取率及SDF/IDF比值的影响Fig.2 Effects of pressures on the extraction rate and SDF/IDF
2.1.3均质次数。由图3可知,SDF/IDF比值与SDF提取率随处理次数的增加先增大后减小,在处理8次时达到最大,分别为1.080、43.49%;IDF提取率随处理次数的增加而减小,8次以上基本趋于平衡,故而选择处理8次作为最佳处理次数。

图3 处理次数对SDF、IDF提取率及SDF/IDF比值的影响Fig.3 Effects of times on the SDF,IDF extraction rate and SDF/IDF
2.2DHPM制备玉米芯SDF理化特性从表1可以看出,玉米芯SDF经DHPM处理后其理化特性均有所提高。Control-SDF的溶解性、持水力、持油力、膨胀力为2.15%、7.63 g/g、7.73 g/g、10.35 mL/g;DHPM-SDF提高到3.85%、14.98 g/g、15.25 g/g、15.85 mL/g。DHPM处理时,一些结构组织如纤维素、半纤维素等物质被破坏,使得果胶类等可溶性膳食纤维暴露溶出,含量增加,水分子结合能力得到提高;SDF颗粒的数量增加,溶于水后体积膨胀、产生更大的伸展容积,从而导致改性后SDF的溶解性、持水力、膨胀力增大[18]。

表1 DHPM处理对玉米芯SDF理化特性的影响
注:同列数据后小写字母不同表示差异显著(P< 0.05)
Note:Different small letters within the same column mean significant differences(P<0.05)
2.3玉米芯SDF抗氧化能力自由基本身也是人体在代谢过程中产生的一种活性物质,如果自由基过量,就会攻击细胞膜、蛋白质、DNA等,造成衰老和引发慢性病。机体在代谢过程中产生的自由基有羟自由基、超氧阴离子自由基、 氢过氧自由基。可溶性膳食纤维中的多糖、多酚类物质具有清除自由基的能力,在治疗老年性痴呆症和心血管病方面独具疗效。SDF中总酚含量在DHPM处理后得到一定程度的增加,Control-SDF和DHPM-SDF中总酚含量分别为2.623、5.173 mg/g。而总酚含量的多少可间接反映抗氧化能力的大小。DHPM处理后的玉米芯SDF对DPPH、O2·-和·OH清除率明显高于未处理样品,这可能是由于物料经DHPM处理后,提取剂与SDF中抗氧化成分接触表面积增大、接触更加充分,且经过DHPM处理后物料细胞壁被破坏,活性成分较易溶出,很多不溶性活性成分转变成小分子可溶性物质,其提取率也相应增加。
由图4可知,在浓度为2~12 mg/mL内,·OH清除率与SDF浓度呈线性关系,Control-SDF和DHPM-SDF线性方程分别为y=10.029 0x+8.266 7(R2=0.999 6)和y=12.689 0x+7.840 0(R2=0.999 1),根据线性方程得IC50(清除50%自由基时SDF的质量浓度)分别为4.16、3.32 mg/mL。
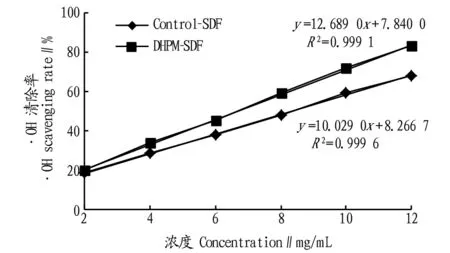
图4 DHPM对·OH清除能力Fig.4 ·OH scavenging capacitiy with DHPM
由图5可知,在浓度2~12 mg/mL内,O2·-清除率与SDF浓度呈线性关系,Control-SDF和DHPM-SDF线性方程分别为y=10.206 0x+8.280 0(R2=0.999 1)和y=12.729 0x+9.433 3(R2=0.999 7),根据线性方程得IC50(清除50%自由基时SDF的质量浓度)分别为4.09、3.19 mg/mL。

图5 DHPM对O2·-清除能力Fig.5 O2·- scavenging capacitiy with DHPM
由图6可知,在浓度2~12 mg/mL内,DPPH清除率与SDF浓度呈线性关系,Control-SDF和DHPM-SDF线性方程分别为y=5.048 6x+10.113 0(R2=0.999 3)和y=13.037 0x+9.686 7(R2=0.999 2),根据线性方程得IC50(清除50%自由基时SDF的质量浓度)分别为7.90、3.09 mg/mL。

图6 DHPM对DPPH清除能力Fig.6 DPPH scavenging capacitiy with DHPM
3 结论
(1)DHPM制备玉米芯SDF最佳工艺条件为料液比为1∶7(g∶mL),均质压力为60 MPa,均质次数为8次。
(2)Control-SDF和DHPM-SDF的溶解性分别为2.15%和3.85%,持水力分别为7.63、14.98 g/g,持油力分别为7.73、15.25 g/g,膨胀力分别为10.35、15.85 mL/g。DHPM处理提高了玉米芯SDF的溶解性、持水力、持油力和膨胀力。
(3)Control-SDF和DHPM-SDF的总酚含量分别为2.623和5.173 mg/g,·OH、O2·-和DPPH的清除能力IC50分别为4.16和3.32 mg/mL、4.09和3.19 mg/mL、7.90和3.09 mg/mL。DHPM处理提高了膳食纤维的抗氧化活性。
