荧光微球免疫层析技术定量检测抗缪勒氏管激素方法的确定
2019-04-10李思慧林伟强魏赵延吴凯
李思慧,林伟强,魏赵延,吴凯
(江苏正大天创生物工程有限公司,江苏泰州 225300)
抗缪勒氏管激素(anti-Mullerian hormone,AMH)又称为缪勒氏管抑制物(Mullerian inhibiting substance,MIS),是男女性腺功能重要的标志,在性腺的发育过程中起着重要作用。对于男性而言,AMH产生于睾丸支持细胞,抑制缪勒氏管的发育,从而产生诱导男性生殖管道[1];对女性而言,AMH由卵巢的窦前和小窦状卵泡的颗粒细胞产生,其可抑制始基卵泡的启动,并抑制窦卵泡对卵泡刺激素(follicle-stimulating hormone,FSH)的敏感性,对卵泡的发育进行调节[2]。
AMH能在月经周期中相对稳定存在,且不受激素和避孕药的影响,其检测便于临床应用[3-5]。抗缪勒氏管激素水平检测能更早且准确地反映卵巢储备功能,从而预测绝经年龄,同时在卵巢相关疾病(例如卵巢早衰、多囊卵巢综合症、卵巢颗粒细胞瘤等的诊断)和儿童性别发育异常的诊断及辅助生殖技术(ART)中有重要意义[6]。常用的方法有免疫细胞化学检测、放射免疫分析技术和ELISA检测技术,这几种检测技术都有着明显的缺陷[7]。本文中采用免疫层析技术与荧光微球标记技术相结合的方式制备了能定量检测抗缪勒氏管激素的免疫荧光层析试纸条,兼具胶体金试纸条与荧光标记技术检测的优点,能够方便携带、即时检测且灵敏度高,便于在基层医院进行推广。
1 材料和仪器
AMH抗原、标记抗体抗缪勒氏管激素(AMH)单克隆抗体、捕获抗体抗缪勒氏管激素(AMH)单克隆抗体及羊抗鼠IgG多克隆抗体购自杭州博茵生物,硝酸纤维素膜(包被垫)、玻璃纤维素膜(标记物垫)、吸水纸、PVC底板购自上海捷宁生物,EuropiumChelate微球购自Bangs/深圳市纽邦生物科技有限公司,各类缓冲液(包括样品垫处理液、封闭液、保存液、复溶液、划膜稀释液等)试剂均为国产分析纯,HM3030型三维划膜喷金仪购自上海金标生物科技有限公司,干式荧光免疫分析仪为苏州和迈精密仪器有限公司,电化学发光法检测AMH试剂盒来自罗氏。
2 方法
2.1 荧光微球标记物的制备
样品垫预处理:用XYZ三维划膜喷金仪将样品垫处理液喷于玻璃纤维长条上,喷量为4 μL/cm,喷后将玻璃纤维放置于烘箱内,干燥温度37 ℃,过夜干燥。取0.2 μm微球1 mL加入1 mg NHS和1 mg EDC,室温反应3 h,加入300 μg标记抗体抗缪勒氏管激素(AMH)单克隆抗体,反应1 h以上。加入90 μL BSA封闭液,反应1 h以上。14 000 r/min,4 ℃,离心10 min,弃上清,加入300 μL 0.01 mol/L的磷酸缓冲溶液(pH=7.4)复溶沉淀,4 ℃保存。然后用荧光微球标记的抗缪勒氏管激素单克隆抗体溶液喷涂经预处理的样品垫,喷量为4 μL/cm,喷后将样品垫放置于烘箱内,干燥温度37 ℃,过夜干燥,干燥结束后,收集密封保存。
2.2 膜处理
将另一株捕获抗体抗缪勒氏管激素(AMH)单克隆抗体及羊抗鼠IgG多克隆抗体分别用磷酸盐缓冲溶液进行稀释,用划膜喷金仪在NC膜上按照1 mg/mL的浓度进行划膜,含有捕获抗体抗缪勒氏管激素(AMH)单克隆抗体的作为检测线(T线),含有羊抗鼠多克隆抗体的作为质控线(C线),然后在37 ℃,湿度<30%的环境下过夜干燥,待用。
2.3 组装
将样品垫、制备标记垫、制备的硝酸纤维素膜、吸水纸依次粘贴在PVC底板上,切裁制得宽3~5 mm的检测试纸卡;最后将检测试纸卡装入卡壳制得检测试剂盒。
3 性能评估
3.1 灵敏度实验
取赋值的AMH企业标准品稀释配制不同浓度的AMH校准品(0.05 ng/mL、0.1 ng/mL、0.2 ng/mL、0.5 ng/mL、1 ng/mL、2 ng/mL、5 ng/mL、10 ng/mL、15 ng/mL、20 ng/mL),用制备的抗缪勒氏管激素试纸条进行依次测定,每个浓度重复5次,以0 ng/mL作为空白对照。以抗缪勒氏管激素浓度为横坐标,荧光读数仪检测信号为纵坐标,建立标准曲线。
3.2 精密度
抽取3个批次的AMH检测试纸条,分别用浓度为0.5 ng/mL、4 ng/mL、8 ng/mL的质控品进行检测,每个浓度点平行测定15次,计算3个批号检测试纸条的批内变异系数和批间变异系数。
3.3 特异性(交叉试验)
分别用含200.0 IU/L FSH、200.0 IU/L LH的0 ng/mL的AMH液进行检测,了解与AMH有无交叉反应。
3.4 稳定性
将成品试剂条放置在干燥的库房中保存,每个月测试浓度为2 ng/mL(±30%)和8 ng/mL(±30%)的企业质控品,测试期为14个月。
3.5 临床样本检测
在医院采集50份检测AMH的全血样本,用罗氏的电化学发光法检测AMH试剂盒与本试剂盒进行比较,对两种方法检测结果进行相关性和一致性分析。
4 结果与分析
本试纸条通过将免疫层析技术与荧光微球标记技术相结合的手段,利用双抗体夹心法原理,检测血清中AMH的浓度,试纸条结构示意图如图1所示。利用抗缪勒氏管激素(AMH)单克隆抗体作为标记抗体,另两个抗缪勒氏管激素(AMH)单克隆抗体作为捕获抗体,样本中的AMH首先分别与标记的抗缪勒氏管激素(AMH)单克隆抗体结合,然后经过硝酸纤维素膜的层析作用,与包被在硝酸纤维素膜检测线上的抗缪勒氏管激素(AMH)单克隆抗体结合,样本中AMH浓度与荧光信号强度成正比,通过标准曲线即可获得样本中AMH的浓度。
4.1 灵敏度
抽取3个批次的AMH检测试纸条,分别对浓度用0.05 ng/mL、0.1 ng/mL、0.2 ng/mL、0.5 ng/mL、1 ng/mL、2 ng/mL、5 ng/mL、10 ng/mL、15 ng/mL、20 ng/mL的AMH质控品进行检测,本试剂盒对0.05 ng/mL的样品可以部分检出,对0.1 ng/mL的样品全部检出,其最低检出限≤0.1 ng/mL。由图2看出,在0.1~20 ng/mL的范围具有良好的线性,线性相关系数r≥0.990,T线颜色的深浅与样品中抗缪勒氏管激素浓度成正比。
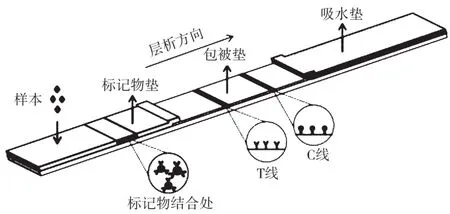
图1 AMH免疫荧光层析试纸条结构示意图
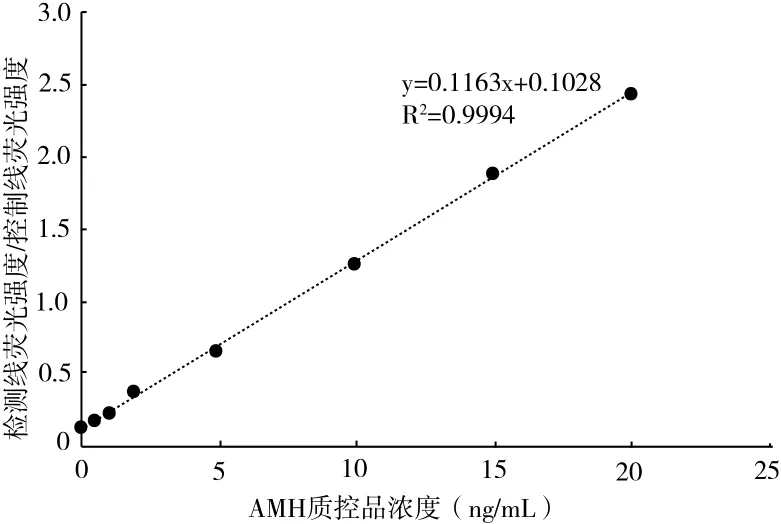
图2 标准曲线
4.2 精密度
抽取3个批次的AMH荧光微球免疫分析试纸条,分别用浓度为0.5 ng/mL、4 ng/mL、8 ng/mL的质控品进行检测,从表1中可以看出批间和批内变异系数均小于15%,说明AMH荧光免疫试纸条的精密度较高。
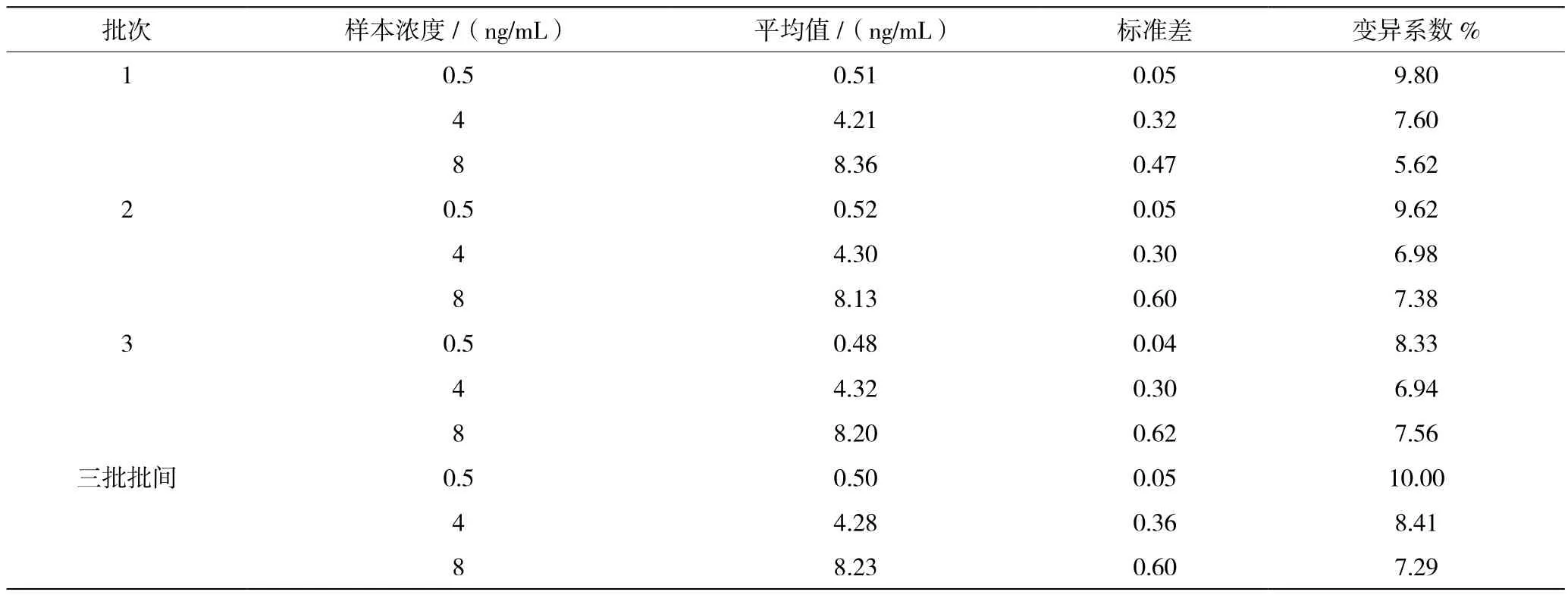
表1 试纸条精密度分析
4.3 特异性
AMH免疫荧光层析试纸条测得的特异性结果如表2所示,分别用含200.0 IU/L FSH、200.0 IU/L LH的0 ng/mL的AMH液进行检测,均小于0.1 ng/mL,表明FSH、LH与AMH之间不存在交叉反应,本试纸条的特异性强。
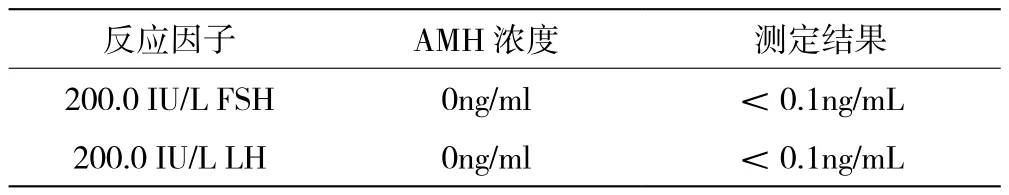
表2 试纸条的特异性分析
4.4 稳定性
AMH免疫荧光层析试纸条稳定性测试结果如表3所示,在 14个月内检测的浓度为2 ng/mL(±30%)和8 ng/mL(±30%)的企业质控品,各浓度质控品的测定结果的相对偏差均小于20%,表明该AMH试纸条有较好的稳定性,该产品有效期大于12个月。
4.5 临床样本检测
用本试纸条和罗氏AMH试剂盒分别检测50例临床样本,分析检测结果的相关性,如图3所示,回归方程为Y=0.9957X+0.0019,R2=0.9997,平均相对偏差小于10%,结果符合临床分析的要求,适用于临床检测。
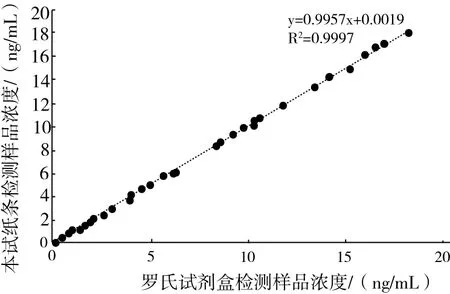
图3 AMH测定结果的相关性
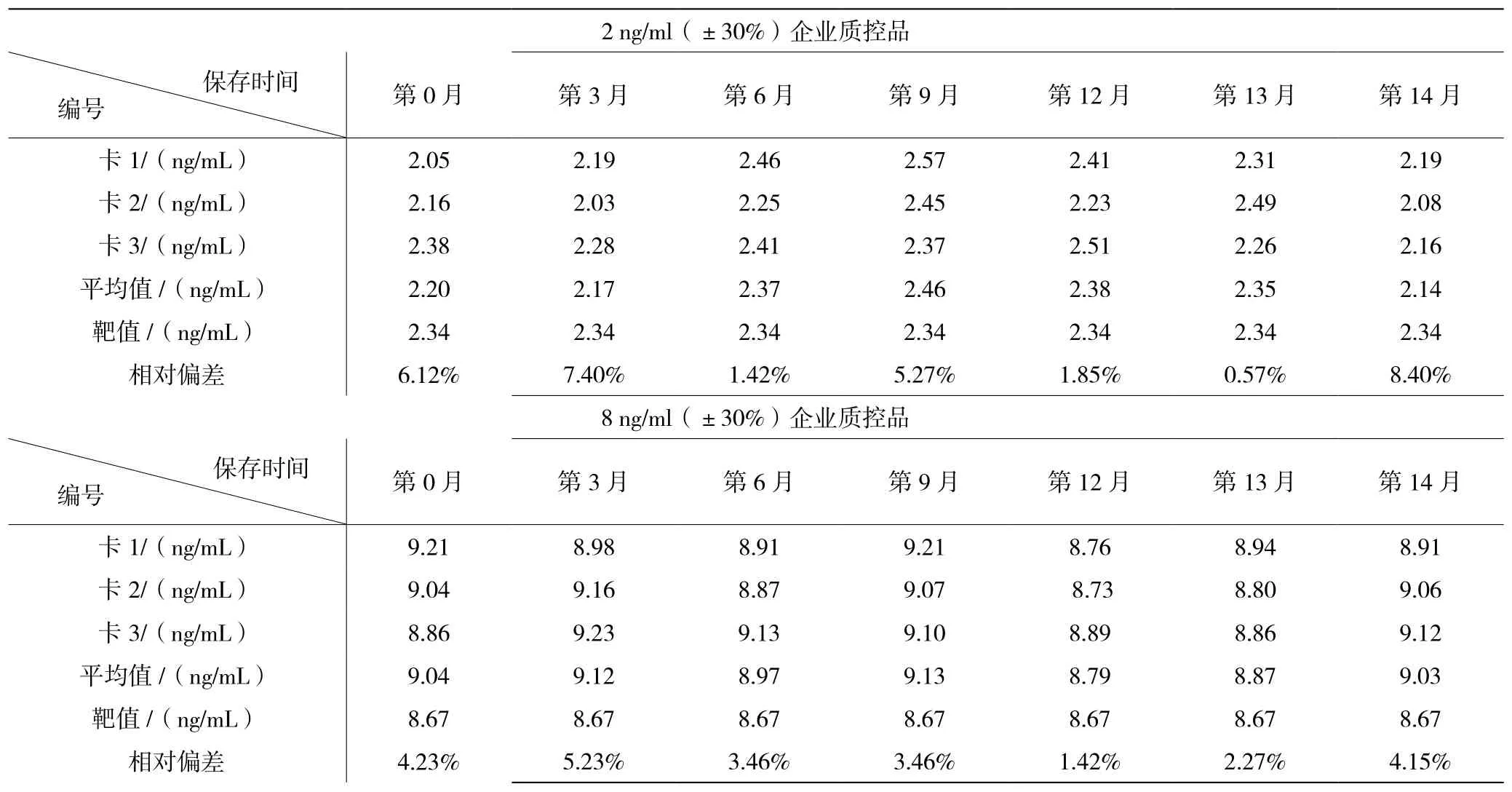
表3 试纸条的稳定性分析
5 讨论
AMH检测在临床上的应用极具意义,目前,AMH是评估卵巢刺激治疗效果及预测卵巢反应的理想标志物。通过检测AMH的水平可获得整个生命周期中卵泡的活性应用,灵敏及特异性地预测卵巢反应[8],指导生产预后,找出存在卵巢过度刺激综合征风险女性,并提升体外受精的安全性和有效性。同时为儿童性别发育异常和卵巢相关疾病的诊断提供重要的参考依据,此外,可通过对AMH的检测预测绝经期,从而为生育能力的保留提供个体化设计,帮助制定相应的生育计划。综上所述,AMH在临床诊断中发挥着越来越重要的作用[6]。
本研究以荧光微球作为示踪标记物,成功地建立了一种能够定量检测AMH 的荧光微球免疫层析试纸条。在试纸条中设置质控线,可增加检测结果的可靠性,若C线无荧光信号,无论T线有无荧光信号,其结果都视为无效。试纸条的最低检测限最低检出限≤0.1ng/mL,具有较高的精密度和特异性。稳定性检测结果表明,连续14个月内检测两种AMH质控品[2 ng/mL(±30%)和8 ng/mL(±30%)],各浓度质控品检测结果的相对偏差均在允许范围内(小于20%),表明试剂盒的有效期大于12个月,与罗氏电化学发光法检测AMH试剂盒相比具有很高的一致性。此外,用该方法检测AMH,成本低且操作简单,能够在社区基层医院中广泛推广,而且还能够满足大型医院内因病患流量大而需快速检测的要求,是一种临床上检测抗缪勒氏管激素便捷可靠的方法。
