类风湿关节炎并发感染性关节炎的临床特点
2019-04-10杨云娇俞建钰费允云曾小峰张奉春
杨云娇,俞建钰,吴 迪,尹 月,李 菁,费允云,曾小峰,张奉春
类风湿关节炎(Rheumatoid Arthritis,RA)是一种慢性非感染性炎症性关节炎,以小关节受累为主,大关节也可受累[1]。而感染性关节炎(septic arthritis,SA)则指由细菌、病毒、真菌、螺旋体等微生物感染引起的关节炎症。单独SA常以单个关节受累为主,诊断相对简单。而当RA并发SA时,则诊断难度增加,容易漏诊或延迟诊断,目前国内仅有少数RA并发SA的个案报道[2-3]。本文旨在分析北京协和医院RA并发SA住院患者的临床特点,以提高临床医生对RA并发SA的认识。
1 对象与方法
1.1 对象
1997年1月至2017年1月北京协和医院住院治疗RA患者1256例,其中同期明确病原菌的并发SA患者共9例。RA诊断符合 1987年美国风湿病协会(ACR)[4]或2010年美国风湿病学会/欧洲抗风湿联盟修订的分类标准[1]。SA诊断主要依据临床表现、典型影像学表现及病原学证据,诊断SA的“金标准”仍然为病原学[5-6]。
1.2 方法
回顾分析RA并发SA患者基本信息、关节感染病程、临床表现、实验室检查和影像学检查,治疗及转归等。
1.3 统计学处理
采用描述性方法进行统计学分析,计量资料用均值±标准差表示,计数资料用率表示。
2 结果
2.1 一般情况
近17年来北京协和医院住院患者中RA并发SA共9例,占同期RA住院患者的0.7%(9/1 256),年龄19~56岁,平均(43.3±14.8)岁。男性3例,女性6例,男女比例1∶2。同期住院患者RA患者男女比例为1∶2.9。男女比例差异无统计学差异。并发SA时RA病程6月~24年,平均(8.4±8.8)年。
2.2 RA相关治疗
9例RA患者均在病程中长期使用缓解病情的抗风湿药物(disease-modifying antirheumatic drugs,DMARDs)控制病情,其中3例患者接受了肿瘤坏死因子拮抗剂的治疗;4例患者曾在单关节炎加重后,局部抽取积液同时,接受了局部注射糖皮质激素,但治疗后局部症状缓解不明显,局部注射与关节感染相关性尚不明确(表1)。
8例患者均在长期慢性多关节肿痛的基础上出现单关节炎的加重,7例感染性关节炎均为急性起病,其中1例关节结核感染患者慢性起病;9例患者中1例患者以“多关节肿痛伴发热”起病,诊断RA时即发现右膝关节及周围软组织感染。
2.3 关节感染部位
关节感染部位为单个膝或髋关节(表1)。所有患者入院后评估均处于RA活动期,伴随其他部位关节炎。膝关节感染的SA患者关节红、肿、热、痛症状突出,髋关节感染以疼痛和活动障碍为突出表现。其中3例膝关节及1例髋关节感染患者伴关节周围软组织肿胀、结构破坏和明显积液(图1、2)。
2.4 感染病原菌学和其他感染部位
6例(66.7%)单关节炎加重时伴有低热,另外3例不伴发热。所有患者均进行了关节腔穿刺(表1),9例患者关节液均为浑浊或脓性,病原学均为阳性,3例为非耐甲氧西林金黄色葡萄球菌(有1例合并全身败血症,血培养阳性,病原学与关节液培养一致)。2例为结核分枝杆菌,1例为铜绿假单胞菌,1例为产气肠杆菌,1例为伤寒沙门菌,1例为缓症链球菌。4例并发关节周围软组织脓肿,2例为葡萄球菌,且关节结构破坏迅速。另外1例为铜绿假单胞菌,1例为沙门氏菌。
2例关节结核菌感染患者无关节外其他部位活动性结核感染的证据,且均不伴发热,其中1例单关节炎加重病程为2月,另外1例患者加重病程为24月。
3例患者并发关节外的其他感染,1例先后并发带状疱疹及血流感染, 1例患者住院期间发生肺炎及巨细胞病毒感染,另外1例并发肺炎。
2.5 辅助检查
所有患者ESR及CRP均显著增高,有不同程度的贫血,3例患者白细胞增高。白细胞(white blood cell,WBC)平均值为(9.3±3.5)×109/L,血红蛋白(hemoglobin,HGB)平均值为(102.6±27.7)g/L,血小板(platelet,PLT)平均值为(323.7±98.0)×109/L。血沉(erythrocyte sedimentation rate,ESR)平均值为(100.1±32.3)mm/1 h;超敏C反应蛋白(hypersensitivity C-reactionprotein,hsCRP)为(78.5±60.8)mg/L。2例结核感染患者外周血淋巴细胞培养+干扰素测定(A+B)高滴度阳性。

表1 9例类风湿关节炎合并感染性关节炎患者临床资料Table 1 The clinical characters of rheumatoid arthritis complicated by septic arthritis
MSSA:甲氧西林敏感金黄色葡萄球菌,Tb:结核分枝杆菌,MRI:核磁共振,ND:未做/无数据
所有RA并发SA患者感染部位关节均进行了X线或核磁共振检查,核磁共振表现为滑膜炎、骨髓水肿、关节积液、周围软组织肿胀、脓肿等,X线检查可见关节间隙狭窄(表1、图1)。
6例患者行关节镜检查,5例可见滑膜组织增生、充血明显,纤维素样组织。另外1例髋关节葡萄球菌感染患者可见大量脓液涌出,探查可见多个脓腔,已失去关节正常结构。关节镜病理结果为关节急慢性或慢性炎(表1)。
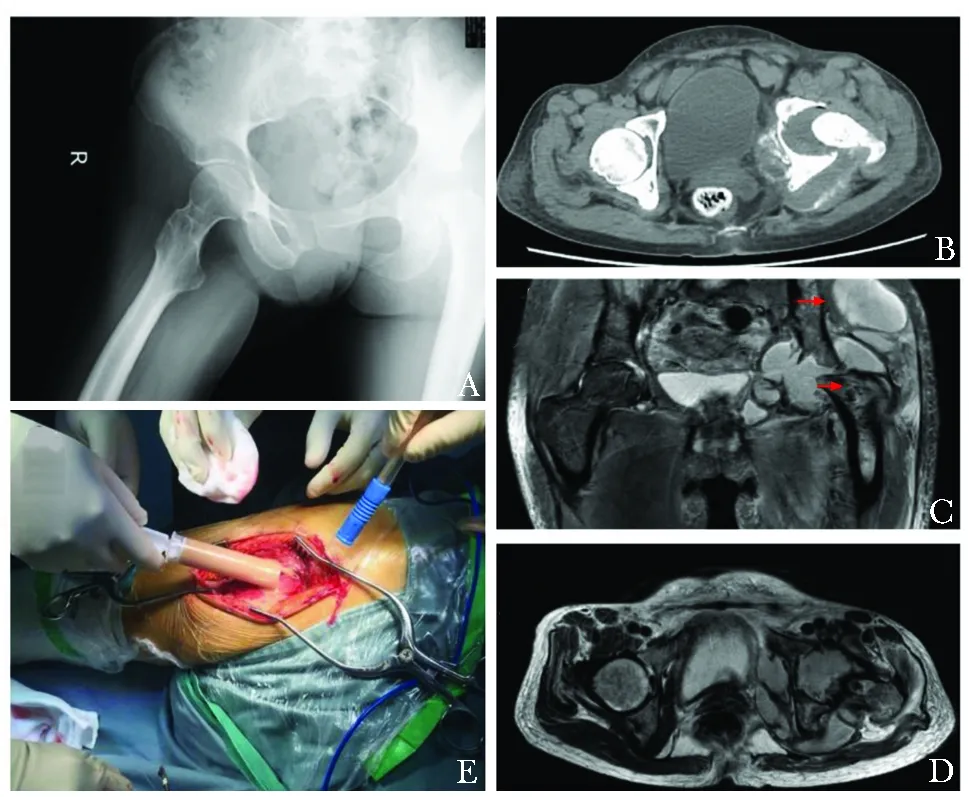
图 1 类风湿关节炎并发左髋感染性关节炎(例7),X线提示左髋关节结构破坏消失(A),CT提示左髋关节异常(B),髋关节MRI提示左髋结构破坏及周围软组织脓肿(C、D),外科术中关节周围软组织大量脓液涌出(E)Fig 1 Rheumatoid arthritis complicated by septic arthritis of left hip(The seventh case),X-ray showed structural damage of left hip(A),CT Findings of abnormal left hip Joint(B),MRI of hip joint revealed structural damage and soft tissue abscess (C,D),Surgical findings of massive pus outflow from periarticular soft tissue(E)

图 2 类风湿关节炎并发右膝关节及周围软组织感染(例9),右膝关节MRI的T2WI压脂相右膝关节间隙狭窄、滑膜增厚、关节积液、软组织水肿(A、B)Fig 2 Rheumatoid arthritis complicated by infection of right knee joint and surrounding soft tissue(The ninth case),MR imaging of the right knee on T2WI with stenosis,synovial membrane thickening,joint effusion and soft tissue edema(A、B)
2.6 治疗和预后
所有患者均根据关节感染的病原学进行了积极抗感染治疗,疗程3~12月,6例患者同时进行了关节镜清洗、引流等外科干预,其中1例患者由于关节受累范围广泛进行了负压封闭引流。除了2例结核菌关节感染患者,另外7例葡萄球菌、沙门氏菌、产气肠杆菌、绿脓杆菌及缓症链球菌关节抗感染治疗疗程为3~4月,1例髋关节感染患者为口服,其他为静脉抗生素后续贯口服抗生素治疗(表1)。
2例患者抗结核长达1年,由于所有患者均并发RA活动,故继续使用DMARDs药物。随访所有患者症状均得到缓解。9例患者均遗留感染关节活动障碍,1例拟行髋关节置换。
3 讨论
所有关节炎患者中,SA发生率为19%[7]。而RA本身即是SA的常见易感因素[8],RA并发SA的概率为正常人群的4~15倍[9],研究表明RA并发SA概率远高于普通人群,国外报道SA并发RA发生率为0.68%[10],与本研究发生率类似。目前国内多为个案报道,尚缺乏关于RA并发SA的大规模研究和报道。RA与SA均为关节炎,全身和局部表现可类似,由于其临床表现的相似性,给RA并发SA的诊断带来困难,应提高对此类疾病的警惕。
本研究中8/9例患者的感染性关节炎均在原有慢性关节炎基础上出现单个关节炎加重,仅有部分患者伴随低热。因此对于那些已经确诊RA的患者,出现单关节炎明显加重,应警惕RA并发SA,尤其是外周大关节如膝、髋关节,这与其他文献报道[9]相符。RA并发SA患者的受累关节往往有较其他关节更加严重的关节狭窄、破坏,并且和单纯RA不同的是,常伴随关节周围软组织肿胀、甚至局部脓肿,破坏范围更广泛、更快(图1、2)。由于RA患者为免疫异常人群,常使用糖皮质激素及DMARDs药物,可能会掩盖全身发热、畏寒等全身炎症反应的症状,因此无发热患者也不能排除SA,尤其是结核等慢性感染。
病原学是明确膝关节感染性关节炎的金标准,一旦怀疑关节感染, 就应该尽快行关节穿刺抽液。但关节液病原学假阴性率高,有研究报道可高达78%[11],对于临床高度怀疑SA的患者应反复行关节液培养以提高阳性率,并辅助局部超声、X线、核磁共振等检查,必要时行关节镜检查。RA并发SA国外文献报道的病原菌多为金黄色葡萄球菌[9]、也有肺炎链球菌、沙门菌[12-14]等的报道。而关节感染的途径主要为血源性途径或临近关节的骨髓、皮肤软组织直接入侵,本文9例患者3例为常见葡萄球菌,与国外相关研究类似,其中1例伴全身菌血症,为血源性感染。部分关于RA并发SA的研究认为使用肿瘤坏死因子拮抗剂容易并发沙门氏菌的感染[15-16],本研究中3例使用肿瘤坏死因子拮抗剂的患者,1例为沙门氏菌感染;另2例患者明确为结核感染,国外文献罕见报道,这可能与国内结核发病率较高相关,这2例关节结核感染患者无关节外其他部位结核感染证据。 RA并发SA的病原学各不相同,对于高度怀疑感染性关节炎的RA患者,应积极取得病原学证据,方能针对性进行抗感染治疗。
RA并发SA的机制尚不明确,易患因素包括关节局部细菌定植、RA疾病本身、DMARDs和生物制剂的使用以及关节局部注射等。英国一项关于药物对RA患者罹患SA的影响的研究,基于13万余人并持续观察15年,研究表明RA患者感染SA的概率是普通人群的12.9倍,且随着病程延长而概率增加[10]。药物中糖皮质激素、DMARDs增加SA的发病率[17],但MTX并不增加SA发病率。也有关于全身或局部使用生物制剂导致SA的报道,但难以证明其直接相关性[14,16,18-19],一项历经35年的回顾性研究认为生物制剂并未增加SA的概率[15]。局部注射也可能与RA的关节感染相关[14]。因此对于尚不能确定是否并发SA的患者,应尽量避免局部关节腔内注射。RA并发SA的相关影响因素仍需进一步大规模前瞻性队列研究。
RA并发SA的治疗主要包括积极内科抗感染治疗和外科手术干预,抗感染可根据药敏并兼顾关节软组织药物分布浓度选择药物,此外,需加强局部关节清创、引流、功能锻炼,其中关节镜是首选[20-21],可帮助诊断及充分冲洗引流。感染充分控制后,仍有功能障碍者,可选择关节置换。
综上所述,RA并发SA并不少见,且临床往往容易漏诊,诊断困难,具体影响因素及机制尚不清楚,对于关节炎再发加重或出现与全身症状不平行的单个外周大关节受累为主的患者,需警惕是否并发SA,应积极行关节穿刺等筛查,明确病原学以及时进行针对性治疗。