四川烟草主栽区根际促生菌筛选及促生菌系构建
2019-04-09甘炳成黄忠乾谢丽源彭卫红
吴 翔,甘炳成*,唐 亚,谭 昊,黄忠乾,谢丽源,彭卫红,唐 杰,周 洁,陈 影
1. 四川省农业科学院土壤肥料研究所 农业部西南区域农业微生物资源利用科学观测实验站/农业部西南山地农业环境重点实验室,成都市外东狮子山路4 号 610066
2. 四川大学建筑与环境学院,成都市一环路南一段24 号 610065
植物根际促生菌(Plant growth-promoting rhizobacteria,PGPR)是指定殖于根系,能直接或间接促进植物生长的微生物[1]。虽然根际促生菌的促生机制尚不明确,但它具有产吲哚乙酸(Indole-3-acetic acid, IAA)[2-3]、产铁载体[4-6]、产氰化物[7-10]、溶磷[11-14]及抑制病原菌生长[15-16]的功能。目前,PGPR 的研究主要集中在小麦[7,9]、水稻[17]、玉米[18]等主要粮食作物上,其他作物研究较少。植物生长素IAA 被当作筛选PGPR 的重要指标,根际促生菌通过分泌IAA 来促进植物合成生长调节物质,从而促进植物的生长发育[19-20]。
烟草是我国重要的经济作物,种植广泛。攀枝花市、宜宾市、泸州市、凉山州和广元市是四川省5 大烟草种植区。目前,四川省烟草主栽区根际土壤促生菌的研究鲜见报道。为此,从四川省5大烟草种植区采集烟草根际土壤,从中分离、筛选高效的促生菌,旨在丰富促生菌资源,为烟草促生生物肥料的研发提供基础。
1 材料与方法
1.1 土壤样品的采集及根际微生物的分离
去除植株根际约5 cm 厚的表层土壤后,采集1 kg 土壤样品,立即带回实验室进行微生物分离。微生物分离采用稀释平板法[21],培养基为牛肉膏蛋白胨培养基、高氏1 号和PDA 培养基。对分离到的菌株进行编号,编号规则:①细菌编号,样品编号-B-菌株号;②放线菌编号,样品编号-A-菌株号;③真菌编号,样品编号-F-菌株编号。每个菌株接种到3 支试管中,4 ℃冰箱保藏,用于功能菌株的筛选。
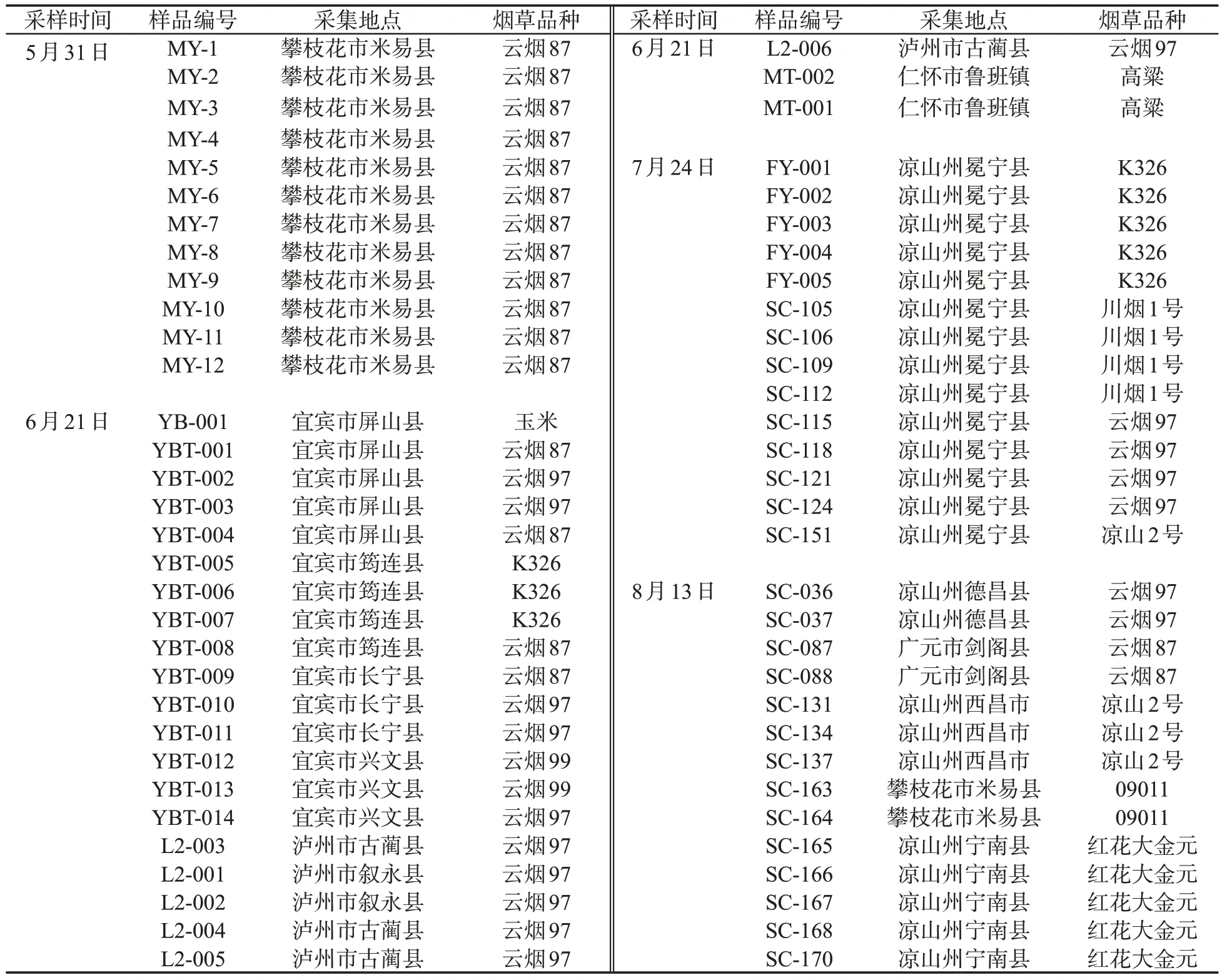
表1 样品采集信息Tab.1 Basic sample information
牛肉膏蛋白胨培养基:牛肉浸膏3.0 g,蛋白胨5.0 g,NaCl 5.0 g,琼脂20.0 g,蒸馏水1 L,pH 6.8~7.2。
高氏1号 :KNO31.00 g,K2HPO40.50 g,MgSO4·7H2O 0.50 g,NaCl 0.50 g,FeSO4·7H2O 0.01 g,可溶性淀粉20.00 g,琼脂20.00 g,蒸馏水1.00 L,pH 7.2~7.4。
PDA 培养基:土豆200.0 g,葡萄糖20.0 g,琼脂18.0 g,蒸馏水1.0 L,pH 自然。
1.2 促生微生物IAA 初筛
参照席琳乔等[22]的方法对促生微生物进行IAA 初筛。取50 μL 菌悬液滴于白色陶瓷板上,同时 加50 μL Salkowski 比色液 。 以 加50 μL IAA(50 mg/L)溶液为阳性对照,以加LB 培养基为阴性对照。菌悬液变红的程度高于阴性对照则表示微生物能够产IAA,根据变红的程度可初步判断其产IAA 能力的大小。
Salkowski 比色液:35.0% HClO450.0 mL,0.5 mol/L FeCl31.0 mL。
LB 液体培养基:胰蛋白胨10.0 g,酵母提取物5.0 g,NaCl 10.0 g,蒸馏水1 L,pH 7.4。
为把改进成果纳入标准化,须把各种设计资料、图纸整理存档,纳入本单位标准化管理工作中,制定《柱塞总成的操作规程与维护规定》,以文件形式下发到了各班组,并纳入检修规程中。同时重点要做好以下工作:
1.3 产IAA 能力的检测
使用UVmini-1240 型分光光度计(日本岛津公司)测定不同浓度IAA 溶液在530 nm 处的吸光值,以IAA 浓度为横坐标,OD530为纵坐标,绘制标准曲线。将初筛菌株接种于LB 液体培养基中,培养24 h,4 000 r/min 离心15 min。取4 mL 上清液在530 nm 处进行吸光度测定,并计算IAA 产量,每个菌株重复3 次。标准曲线的制作和菌液中IAA 浓度的测定参照Glickmann 等[23]的方法。标准曲线的空白对照为蒸馏水∶Salkowski 比色液=1∶1 的混合液,菌液检测的空白对照为LB 液体培养基∶Salkowski 比色液=1∶1 的混合液。
1.4 产铁载体能力的鉴定
将初筛菌株接种于铁载体检测培养基,以不接菌的检测培养基为空白对照。根据检测培养基上菌落周围是否产铁载体晕圈判定其是否具有产铁载体的能力[24]。铁载体检测培养基的配置:将无菌的50 mL 0.l mol/L 磷酸缓冲溶液、无菌的50 mL CAS 染液直接加入到1 L 铁载体检测基础培养基中,混匀。
CAS 染液 :l.0 mmol/L 铬天青S,0.1 mmol/L FeC13,4.0 mmol/L 十六烷基三甲基溴化铵(CTAB)。
铁载体检测基础培养基:0.5 g KCl,0.5 g MgSO4,4.0 g 葡萄糖,5.0 g 酪蛋白胨,15.0 g 琼脂,1.0 L 蒸馏水,pH 7.0~7.2。
0.1 mol/L 磷酸缓冲液 :0.590 5 g NaH2PO4·2H2O,2.427 0 g Na2HPO4·12H2O,0.250 0 g NH4Cl,0.075 0 g KH2PO4,0.125 0 g NaCl,100.00 mL蒸馏水。
1.5 产氰化氢(HCN)能力的鉴定
参 照Lorck[25]的方法检测菌株产HCN的能力。将初筛菌株接种于添加4.4 g/L 甘氨酸的牛肉膏蛋白胨培养基上后,再用浸过2%碳酸钠、0.5%苦味酸溶液(2,4,6-三硝基苯酚)的Whatman1 号滤纸覆盖,(28±2)℃培养4 d。滤纸颜色由橘黄色转为红色说明有HCN 产生,根据转红的程度判断菌株产HCN的效果。以不接菌的培养基为空白对照。
1.6 促生菌系的构建
将复筛后的促生菌株进行组合,不同组合的菌株接种到装有LB 液体培养基的三角瓶中,30 ℃ 、180 r/min 培 养24 h。利用IAA测定方法(1.3 节)检测并计算各组合IAA 的产量,以不接菌的LB 液体培养基为对照,每个组合重复3 次。
1.7 菌株16S rDNA序列的测定及系统发育树构建
参照细菌基因组DNA 提取试剂盒(杭州博日科技有限公司)的说明书提取细菌基因组DNA。参照张飞官等[26]的方法扩增菌株16S rDNA。PCR 产物在生工生物工程(上海)有限公司进行测序。将测得的16S rDNA 序列提交到GenBank,获得各菌株的登录号。参照张越己等[15]的方法构建系统发育树。
1.8 种子发芽试验
将促生菌株和构建的促生菌系分别接入LB液体培养基中,30 ℃、180 r/min 培养24 h。菌悬液的终浓度为107cfu/mL,以未接菌的LB 液体培养基为空白对照。挑选红花大金元、MS 云烟85和MS 云烟87(由四川省烟草公司攀枝花市公司米易分公司惠赠)个体饱满、大小一致的裸种,每个品种20 粒种子,均匀播于铺有2 层滤纸的无菌培养皿中,每个品种3次重复。每个培养皿加入4 mL制备好的菌悬液和10-1倍浓度的LB 液体培养基,每种菌液3 次重复,置于人工智能气候箱中培养。培养条件:光强70%、光照12 h、温度25 ℃、相对湿度70%,每隔1 d 补充1 mL 无菌水,以确保种子正常萌发,于第3、第7 天统计发芽率。
发芽率=(发芽种子数/检测种子总数)×100%
2 结果与分析
2.1 根际微生物的分离
从不同地点、不同取样时间的63 个土壤样品中,共分离出923 株微生物,其中细菌583 株、放线菌234 株、真菌106 株,基本情况见表2。
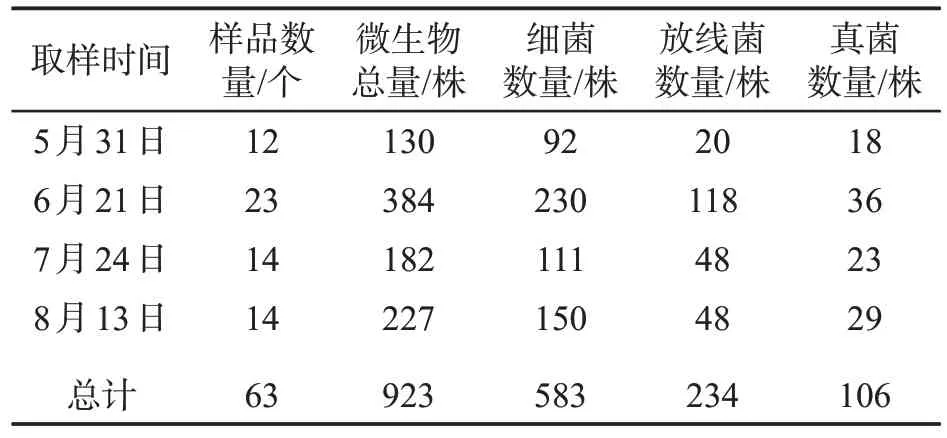
表2 样品微生物的分离情况Tab.2 Microorganism isolation results
2.2 促生菌的筛选
从923 株菌株中,初筛到具有较好产IAA 能力的菌株66 株,包括62 株细菌,占比为93.94%,4 株放线菌,占比为6.06%。通过测定菌株IAA 的产量、是否产铁载体和HCN 进行复筛。结果(表3)表明,初筛的66 株菌株IAA 的产量在2.65~42.99 μg/mL 之间,其中菌株L2-001-B-16 产IAA 的能力最强。IAA 产量排前10 的菌株:L2-001-B-16>MT-002-B-12>FY-001-B-9>YBT-003-B-5>YB-001-B-8>L2-001-B-14>L2-002-B-2>L2-006-B-16>L2-004-B-2>SC-118-B-1。对66 株菌株是否具有产铁载体、HCN 的能力进行检测发现,24 株菌株具有产铁载体能力(表3),11 株菌株具有较好产HCN的能力(表3)。以同时具有较好产IAA、铁载体和HCN 能力的菌株为复筛菌株,包括L2-001-B-16、MT-002-B-12、FY-001-B-9、YBT-003-B-5、YB-001-B-8。
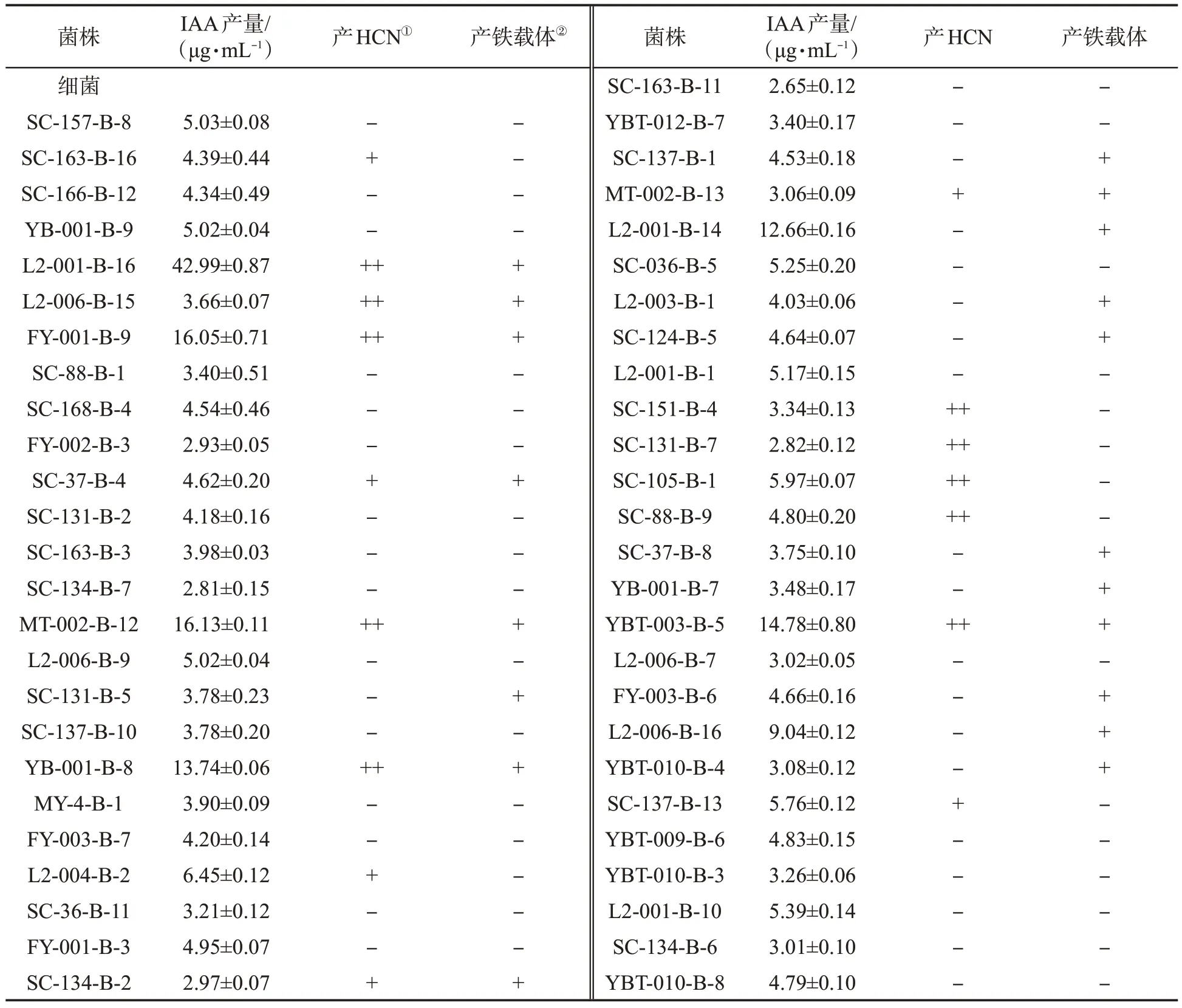
表3 初筛菌株促生能力的检测Tab.3 Promoting ability results from first-screening strains
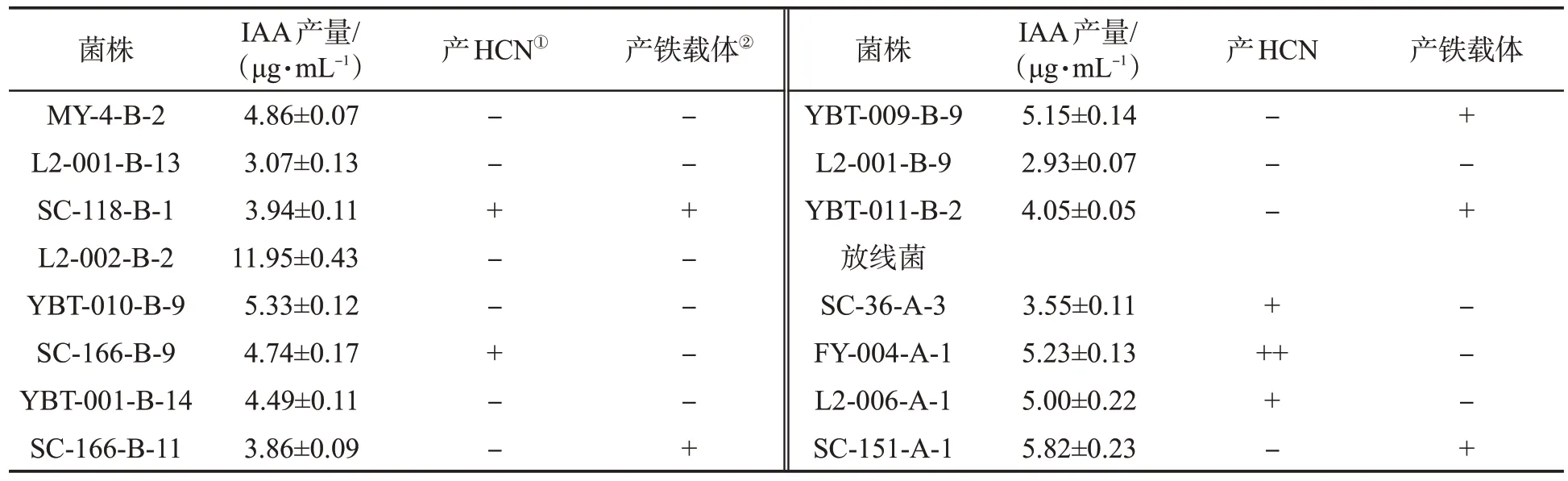
表3(续)
2.3 促生菌系的构建
将5 株复筛菌株进行组合,共31 个组合,测定这些组合产IAA 的能力(表4)。在2 个菌株的组合中,组合45 IAA 的产量最高;在3 个菌株的组合中,组合134 IAA 的产量最高。在31 个组合中,组合1345 产IAA 的能力最高,其IAA 的产量为51.27 μg/mL,极显著优于其他组合。因此,组合1345 为最优促生菌系。

表4 促生菌系产IAA 能力的检测①Tab.4 IAA yields of different growth-promoting rhizobacteria groups
2.4 16S rDNA 序列分析
进一步分析组合1345 的4 株菌株16S rDNA序列。菌株MT-002-B-12、FY-001-B-9 和YBT-003-B-5 的16S rDNA 序列长度分别为1 402、1 354、1 516 bp,在GenBank中的登录号分别为KT119350、KT119349、KT223830。根据系统发育与菌株形态特征,判定菌株MT-002-B-12 属于克雷伯氏菌属的Klebsiella variicola,菌株FY-001-B-9 属于肠杆菌属的Enterobacter xiangfangensis,菌 株YBT-003-B-5 属于芽孢杆菌属的Bacillus tequilensis。
菌株L2-001-B-16 的16S rDNA 序列长度为1 510 bp。系统发育分析结果(图1)表明,菌株L2-001-B-16 属于肠杆菌科(Enterobacteriaceae),与Enterobacter cloacae subsp. Dissolvens 的发育关系最近,二者16S rDNA 序列相似性为92.2%;其次是Klebsiella pneumoniae subsp. pneumoniae,16S rDNA序列相似性为91.9%;与肠杆菌科其他菌株的相似性均小于91.8%。因此,推测菌株L2-001-B-16 是肠杆菌科(Enterobacteriaceae)的新类群。
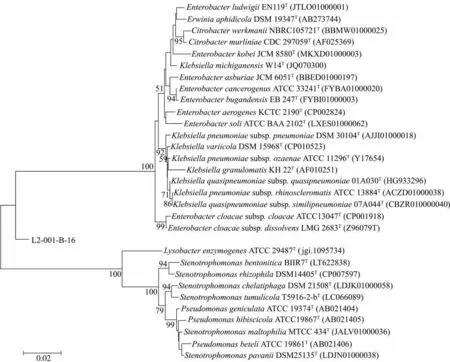
图1 菌株L2-001-B-16 的系统发育树Fig.1 Phylogenetic tree of strain L2-001-B-16 based on 16S rDNA
2.5 对种子萌发的影响
由表5 可知,与对照相比,不同菌株处理下,3 个烟草品种种子第3 天的发芽率均极显著升高。第7 天,菌株YBT-003-B-5 对红花大金元种子、菌株MT-002-B-12 对MS 云烟87 种子发芽率的影响均不显著;其余菌株处理下,3 个烟草品种种子的发芽率均极显著升高。第3 天和第7 天,在组合1345 的处理下,3 个烟草品种种子的发芽率均高于其他菌株,促进烟草种子发芽的效果明显。
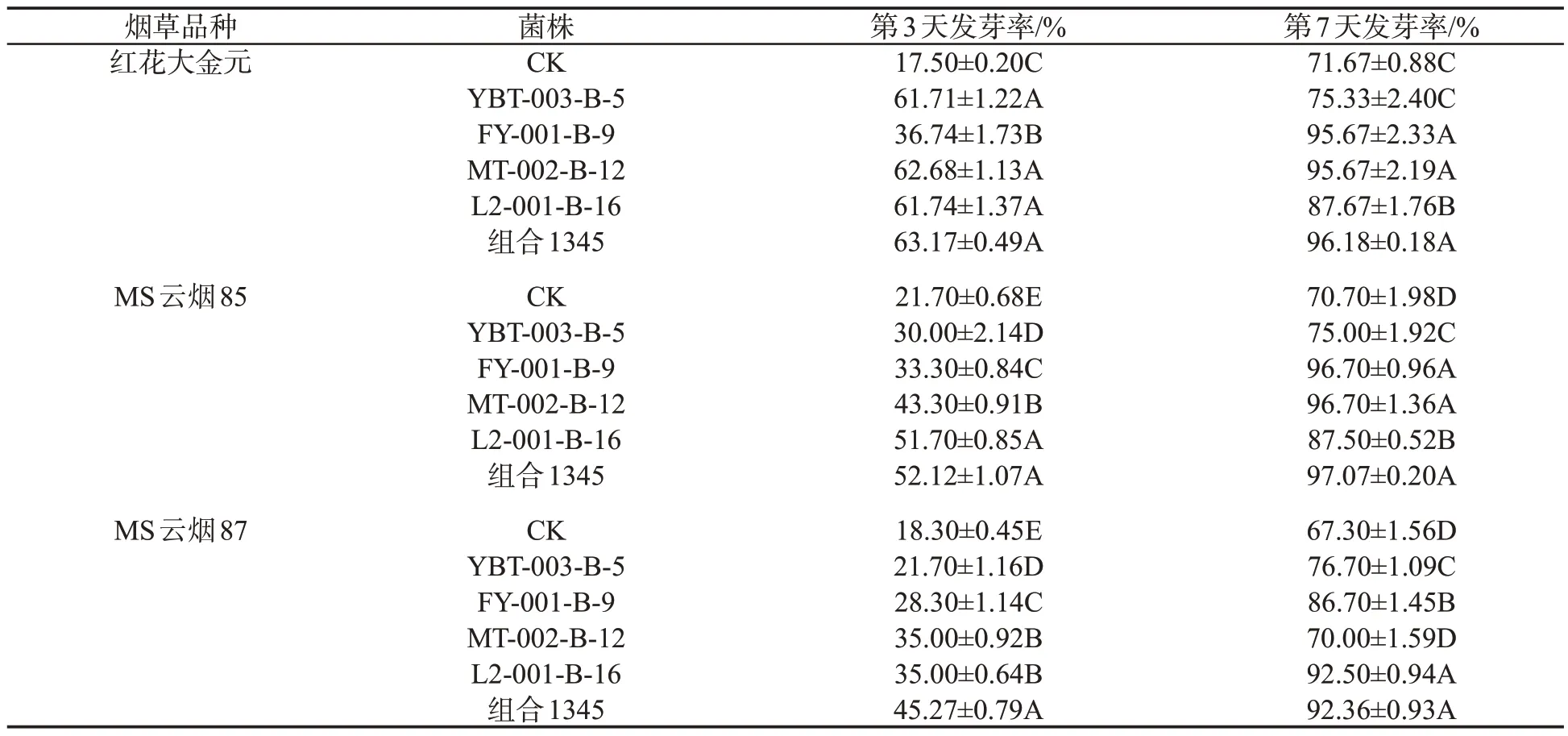
表5 不同促生菌对烟草种子发芽率的影响Tab.5 Effects of different growth-promoting rhizobacteria on germinating rates of tobacco seeds
3 讨论
席琳乔等[22]从棉花根际土壤中分离到8 株根际促生固氮菌,其IAA 的产量在6.62~22.83 μg/mL之间;刘静洋[27]筛选到29 株棉花根际细菌,其IAA的产量在0.15~22.87 mg/L 之间;徐明双[28]发现31株内生菌分泌IAA的产量为1.00~5.49 mg/L;郑文波等[29]发现菌株ZH5 IAA的产量为43.18 mg/L。从四川省烟草主栽区的根际土壤中分离到5 株(YBT-003-B-5、YB-001-B-8、FY-001-B-9、MT-002-B-12、L2-001-B-16)促生菌,所构建的促生菌系(MT-002-B-12、L2-001-B-16、FY-001-B-9 和YBT-003-B-5)IAA产量可达51.27 mg/L,高于已报道的促生菌产IAA 的能力[22,27-29],并且该促生菌系还能显著提高烟草种子的发芽率。
促生菌系中的菌株MT-002-B-12、FY-001-B-9和YBT-003-B-5 分 别 属 于Klebsiella variicola、Enterobacter xiangfangensi 和 Bacillus tequilensis。K. variicola 具有ACC 脱氨酶活性[30]、固氮[31-32]、解钾[33]等促生功能;E. xiangfangensis 具有产组胺的能力[34];B. tequilensis 具有促生[35]、产拮抗病原菌活性物质的能力[36-37]。但目前还没有关于这3 种细菌产IAA、铁载体和HCN 能力的报道。另外,菌株L2-001-B-16 可能属于肠杆菌科(Enterobacteriaceae)的新类群。本研究中,获得的促生菌株丰富了促生微生物的种类,为利用微生物研制烟草生物肥料提供了更多的选择。
4 结论
①从四川省5 个烟草主栽区的烟草根际土壤中分离到923 株微生物,其中细菌583 株、放线菌234 株、真菌106 株;②初筛筛选到具有较好产IAA能力的菌株66 株,复筛筛选出5 株具有较好产IAA、产铁载体和产HCN 能力的菌株;③将菌株MT-002-B-12、L2-001-B-16、FY-001-B-9 和YBT-003-B-5 构建成促生菌系,该促生菌系能极显著促进3个烟草主栽品种种子的萌发。
