新型阿尔茨海默症Tau蛋白PET显像剂18F-T807的合成
2019-03-07王治国张国旭石庆学张宗鹏吴锐先
王治国 左 峰 张国旭* 石庆学 张宗鹏 吴锐先
阿尔茨海默病(Alzheimer's disease, AD)是老年痴呆的主要原因,脑区和大脑皮层的纤维蛋白沉积是其特征性病理性改变,细胞内多聚Tau蛋白的沉积及细胞外间隙的β淀粉样蛋白(β amyloid,Aβ),两者在病理形态学上分别体现为神经纤维缠结(neurofibrillary tangles,NFTs)及老年斑(SP)[1]。Tau蛋白是体内含量最高的微管相关蛋白,在外周和中枢神经系统中含量丰富,Tau的病理发展过程与AD认知损伤程度密切相关,有可能作为AD潜在的治疗靶点[2]。脑内特定部位Tau蛋白沉积的无创检查对疾病早期预测及诊断很有帮助。正电子发射断层显像(positron emission tomography, PET)是一种无创分子探针成像方法,可对人脑生物学进程进行广泛的半定量分析。
近年来,研究者们研发的多种Tau蛋白PET显像剂用于观察脑内神经疾病的病理改变显像,其中包括18F-3-(6-[18F]氟吡啶基)-5氢-吡啶并[4,3-b]吲哚(18F-T807)、THK-5117和PBB3[3-4]。利用Tau蛋白放射性示踪剂PET实现对局部以及全身Tau蛋白显像,这项检查技术的发展将为临床提供及时、准确的鉴别诊断,并且在监测疾病进展和实验性临床治疗上提供有力帮助[5-6]。随着18F标记的放射性显像剂在PET显像技术中的应用,对18F标记显像剂的合成与开发提出更高的要求。本研究旨在探讨Tau蛋白显像剂18FT807的合成方法。
1 材料与方法
1.1 材料与试剂
采用minitrace加速器(美国GE公司);18F-FPPI前体(江苏华益公司);合成用QMA柱、K222、碳酸钾水溶液、乙腈以及乙醇均为德国ABX公司;分离用乙醇(色谱纯,国药化学试剂有限公司);盐酸(国药分析质检中心);二甲基亚砜(dimethyl sulfoxide,DMSO)99.9%超干溶剂(北京百灵威科技有限公司),C18柱(美国Waters公司);富18O水(日本大阳日酸株式会社);Oasis HLB型固相萃取(solid-phase extraction,SPE)柱(美国Waters公司);0.22 μm液体滤膜(Millex-GS)及空气滤膜(Millex-25)均为德国默克公司。
1.2 合成方法
18F离子由minitrace加速器生产,轰击束流45 μA,轰击时间40 min,轰击结束由氦气作为载气传输到TRACERLAB FXFN合成器靶水瓶内。合成器示意如图1所示。
(1)自动化合成主要有以下步骤:①18F离子的柱分离纯化及蒸馏干燥;②原料的18F离子亲核取代反应;③在线溶剂转换;④产品经高效液相色谱(high performance liquid chromatography,HPLC)分离纯化;⑤C18柱再次纯化。
(2)合成器的具体步骤:①18F离子由18O(p,n)18F反应制得,并经过靶水线(FROM TARGET)传送到靶水瓶,后由11号QMA固相萃取(由1 ml乙醇,2 ml水活化)分离柱捕获;②18F离子(753±7.53)mCi(1 Ci=3.7×1010Bq)由1号瓶内加入的15 mg K222溶于1 ml乙腈溶剂及1.5 mg的K2CO3溶于0.5 ml水的混合溶剂冲洗入V12号反应瓶;③混合液在氮气吹拂下于85 ℃减压蒸馏8 min,再于110 ℃氮气吹拂4 min;④加入V3号瓶内的前体(1 mg溶于1.2 ml的DMSO溶剂)并加热到130 ℃,V24关闭,反应瓶加热反应10 min;⑤反应瓶降温到50 ℃,开V24,V25恢复大气压,然后加入V5号瓶内的10 ml水;⑥反应后混合液经由V5和V6内的1.5 ml的HPLC流动相(28%乙醇水溶液,调整pH值至2.0)分别冲洗到V26阀门下收集瓶内,打开V26在N2气压力下经由Fluid进入HPLC进样环,在Fluid控制下进样环旋转,进入HPLC半制备柱(X-Select HSS T3,250×10.00 mm,5 μl),流动相以5 ml/min的流速通过柱子分离。流动相以紫外(UV,λ=254 nm)和放射计数器监测。18F-T807的保留时间为21.5 min;⑦正常HPLC分离出产品即可满足质量要求,放射化学纯度>95%,也可以通过V18阀门将产品收集到V18阀门下圆底烧瓶,圆底烧瓶内装有2 ml 8.4%的K2CO3和20 ml无菌注射用水;经16号位置的Oasis HLB SPE柱(以5 ml乙醇和10 ml水活化)纯度将提高>98%;⑧产物会挂在柱子上,然后V7号瓶内预装的10 ml水冲洗柱子,可以冲掉盐、乙腈和氟离子;⑨SPE柱经由V8号瓶内的0.8 ml乙醇冲洗进入产品羊角瓶,产品瓶内装有8 ml、0.9%生理盐水,然后产品经由V16和产品管线在N2气压力下经过0.22 μm液体滤膜过滤进入分装室的收集瓶。
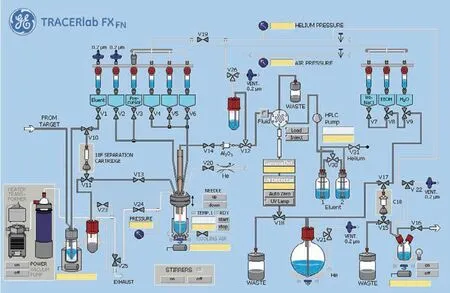
图1 TRACERLAB FXFN合成器示意图
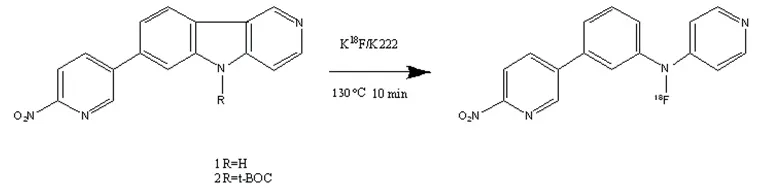
图2 18F-T807合成化学方程式示图
产品分析质量控制经由分析HPLC与标准品分别及混合进样确认产品。如果用于人体按相关质量控制标准进行质量控制。18F-T807合成化学方程式如图2所示。
2 结果
2.1 合成结果
18F-T807合成用时63 min,使用普通原料产量37.7 mCi(1 Ci=3.7×1010Bq),未校正产率5%,使用叔丁氧羰基(t-Butyloxy carbonyl,BOC)保护的原料产率会提高至15%。经过SPE柱滞留在柱子上的大部分是未反应的18F离子。
2.2 合成产物质量控制检测
对3批连续生产的产物进行质量控制。HPLC分析结果放射化学纯度和化学纯度合格。HPLC分析柱(Ultimate C-18,4.6×250 mm,5 μm),流动相是50%甲醇/水[pH=2,盐酸(HCl)调]流速1.3 ml/min,紫外检测器(UV,λ=254 nm),6 h后pH值为5.5,活度计测得半衰期为109.7 min,不包含长半衰期核素(>5 d),细菌内毒素实验合格。气相色谱结果显示,残留丙酮、乙腈、DMSO等溶剂都在检测线下。各项结果表明产品符合人体使用标准。
3 讨论
合成及分离产物时间从加速器轰击结束开始共(63±5)min,放射化学产率经过衰减校正后为(15±5)%(n=20),化学纯度>95%,放射化学纯度>99%,产品的无菌及无热原要求均符合规定。
反应总产率较低(15%),使用t-BOC保护后产率得到提高,推测原因是合成温度较高(130 ℃),原料N原子上的H还原性更高,易发生不良反应,而使用t-BOC保护后活性降低,相应不良反应极大降低。
神经显像剂显像效果受杂质影响较大,故提高放射化学纯度有实际意义,本研究通过V18阀门将产品收集到V18阀门下圆底烧瓶,圆底烧瓶内装有2 ml,8.4%的K2CO3和20 ml无菌注射用水;经16号位置的Oasis HLB SPE柱(以5 ml乙醇和10 ml水活化)纯度将提高>98%。
在GE TRACERLAB FXFN合成器上使用一步法合成的18F-T807,由HPLC纯化,使用SPE柱再次纯化保证纯化效果。合成后进行各种质量控制检测均显示符合质量控制标准。该合成方法简便易行,适合医院及各中心的Tau蛋白显像剂的合成。
