腹股沟疝修补术后补片相关感染的处理
2019-02-26金杰波江志鹏陈双
金杰波,江志鹏,陈双
(1.玉溪市人民医院胃肠外科,云南 玉溪 653100;2.中山大学附属第六医院胃肠、疝与腹壁外科,广东 广州 510000)
无张力疝修补术已经取代传统手术成为腹股沟疝修补的首选术式,但是,术后补片感染为无张力疝修补的特有并发症[1],一旦发生感染,处理非常棘手。为了探讨无张力疝修补术后补片感染的治疗及预防,我们选取2015年1月至2017年12月在中山大学附属第六医院接受手术的20例腹股沟疝补片修补术后补片感染病人为研究对象,探究有效的治疗及预防方法,现报告如下。
资料与方法
一、一般资料
腹股沟疝修补术后补片感染病人20例,男性18例,女性2例,年龄范围为19~79岁,平均年龄为56岁。合并高血压3例,糖尿病2例。20例中原发疝17例,其中1例行经腹腹膜前腹腔镜腹股沟疝修补术(laparoscopic transabdominal preperitoneal hernia repair,TAPP),其余16例行开放腹股沟疝无张力疝修补术;复发疝3例,其中1例开放修补,1例腹腔镜腹腔内补片置入术(intraperitoneal onlay mesh,IPOM),1例为多次开放手术修补(第一次未放补片,第二次三合一补片,第三次网塞+平片),修补材料为聚丙烯或聚酯补片。20例感染病人中,感染出现时间为术后2 d~8年,症状持续时间为7 d~5年,临床表现为窦道形成18例,脓肿2例(1例浅表脓肿,入院后切开引流后二期取补片,1例为术后反复抽液后的深部脓肿,抗感染治疗后腹腔镜取补片)。复杂病例4例,1例补片侵蚀膀胱;1例补片侵蚀膀胱及回盲部;1例并发盲肠皮肤瘘;1例为外院3次疝修补、多块补片置入。病人一般情况见表1。
二、手术方法
17例开放病人按照以下流程实施手术:术前备皮,采取硬膜外连续麻醉,窦道口注入美蓝,使脓腔及感染的补片充分染色,按原切口切开,剪开腹外斜肌腱膜,提起腱膜向两侧分离,注意保护精索及腹壁下血管,由于解剖结构不清,补片挛缩,精索、血管等粘连致密、瘢痕形成,极易误伤输精管和血管,沿美蓝标记可将补片提起后紧贴补片锐性分离,边分离补片边清除感染及坏死组织、增生的瘢痕组织,尽可能将感染补片切除干净。注意将缝合补片的缝线一并取出。分离网塞时应特别注意不要切破腹膜而损伤肠管,用生理盐水和双氧水、聚维酮碘反复冲洗创面,彻底止血后根据感染的脓腔大小及创面渗出情况,对12例创面渗出较少病人采用创面放置一根小号引流管或引流条,一期缝合伤口,5例病人伤口敞开放置负压封闭引流(vacuum sealing drainage,VSD),术后冲洗引流,视伤口情况再行二期缝合,其中1例合并盲肠皮肤瘘行盲肠皮肤瘘切除、补片取出,1例补片侵蚀膀胱、回盲部行膀胱切开取补片、回盲部切除吻合,17例均未再放置补片。3例病人腹腔镜下切开腹膜,自后入路完整取出补片,1例补片侵蚀膀胱的同时行膀胱部分切除、修补,1例取补片后再次IPOM。
三、术后处理
术后常规使用广谱抗生素,术区定期换药,一期缝合病人术后切口明显渗液者予拆线、敞开引流。术后一期敞开引流者,待创面渗出少,肉芽组织新鲜,再行二期缝合。
结 果
所有病人均手术取出补片。20例中17例病人开放手术取补片,其中12例一期缝合伤口,5例敞开、VSD后二期缝合伤口;一期缝合病人中,6例愈合,6例感染,感染率为50%,其中1例补片残留再次取补片后敞开、放置VSD、多次取残留补片后二期缝合。3例腹腔镜取补片病人,2例一期愈合,1例取补片后IPOM,术后补片感染再次取补片、敞开、放置VSD、多次取残留补片后二期缝合。目前均在随访中,随访时间为3~29个月,平均随访15个月,1例术后3个月复发,于术后1年TAPP修补。(表1)
讨 论
腹股沟疝是临床上的常见病和多发病,现无张力疝修补技术被广泛应用于临床,补片相关感染是疝修补术后常见并发症,一旦出现感染很难处理,因此如何防治补片相关感染是临床关注的重点。国外有关腹股沟疝术后补片相关感染的相关临床研究,结果存在较大差异,其发生率在0.001%~10%[2-3]。我国补片感染率相关报道较少,陈涛等[4]的研究补片感染率约为0.3%。感染可发生于疝修补术后数月、数年,甚至术后十余年,就目前文献报道,大部分补片感染发生于腹股沟疝修补术后1年左右[5]。其中发生于术后30 d内者为早期感染,超过此期限者为迟发型感染[6],本组20例病人出现补片感染时间为术后2 d~8年不等。
本研究所有补片相关感染病人均为外院转入,具体的补片感染原因不得而知,但也有共同点。感染者多为中老年病人,本研究中感染病人平均年龄为56岁,高龄病人可能为补片相关感染的高危人群。老年病人身体素质相对较差,在伴有免疫功能低下、糖尿病等情况下,易出现术区继发感染累及补片。笔者认为,对于高龄伴有基础疾病特别是糖尿病病人,预防性应用抗生素是必要的,可选择腹腔镜手术,其相对于开放手术具有更低的感染率。若病人切口术后出现持续疼痛,行彩色超声探查是必要的,如果感染,早期的切口敞开有利于后期的恢复。术后阴囊、腹股沟区积液应避免盲目穿刺,容易继发感染。本研究中1例病人术后因局部肿痛反复穿刺抽液导致迟发性补片感染、深部脓肿形成。这种情况应尽量避免。
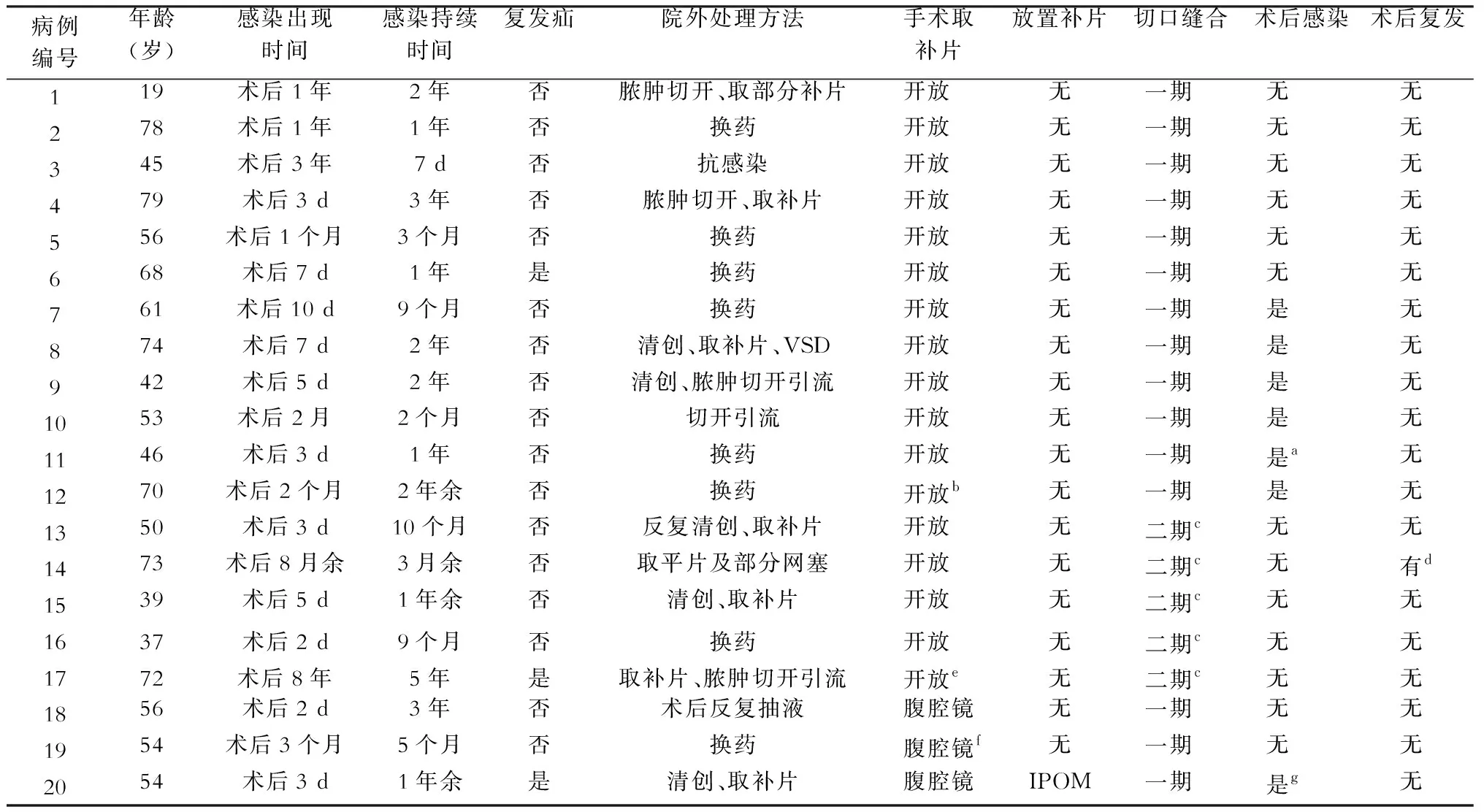
表1 腹股沟疝修补术后补片感染病人一般情况、处理及术后情况
补片、缝线选择同样重要。聚丙烯补片具有较大的孔径(>75 μm),允许纤维母细胞穿过,能较好地与组织结合,而聚四氟乙烯补片孔径较小(<10 μm),纤维母细胞无法穿过,虽然降低了组织粘连及脏器侵蚀的风险,但这种相对不透性却增加了局部血清肿的发生概率。细菌(直径约1 μm)可穿过聚四氟乙烯补片,而巨噬细胞多核白细胞(直径约10 μm)却无法穿过,因此增加了感染的风险。此外,多股纤维结构的补片(如聚四氟乙烯补片)较单股纤维结构的补片(如聚丙烯补片)具有更高的感染率,因其具有更大的表面积供细菌黏附,编织纤维间的缝隙不仅更容易藏匿细菌,同时也使免疫细胞难以到达,使用多股缝线固定补片亦可能增加补片感染的概率[7-8],术中尽量选用可吸收的缝线或Prolene 线,在将补片平展的基础上,尽量少打结。
腹股沟疝术后补片一旦感染,经反复多次清创换药及根据分泌物细菌培养及药敏实验使用敏感抗生素后未愈合的[9-10],应尽早取出感染的补片。术前须窦道造影、必要时磁共振检查了解感染程度、脓腔大小以及波及的范围,为进一步制定手术方案提供依据。术中先自皮肤窦道口注入美蓝使补片染色,了解感染补片的层次、范围,沿补片边缘仔细分离,在争取完整取出补片、清除坏死组织的同时,避免损伤腹壁下血管、精索结构,避免分破腹膜,甚至损失肠管。
补片移位、与腹腔脏器长期直接接触,可导致补片侵蚀膀胱、肠管[11-12]。本研究中,2例补片侵蚀膀胱,1例合并瘘,需在大的疝中心,由经验丰富的疝专家,联合多学科综合诊治。本研究2例病人腹腔镜取补片后痊愈,相对于前入路手术,腹腔镜下,腹股沟区骨性标志、血管解剖清楚,并可查看补片与腹腔脏器尤其是膀胱、肠管的关系,避免副损伤。
取出补片后,是否一期再次置入补片修补,存在争议。由于补片植入后的炎症反应,使得局部纤维瘢痕组织形成,局部解剖结构已得到加固,此时取出网片也不容易导致疝的复发,但是如果脓腔的形成造成原有腹壁结构薄弱,不排除有疝复发的可能。Rehman等[13]统计了40例行网片取出的病人资料,平均随访时间26个月,有2例复发。Fawole等[14]在其报道中发现在补片感染的中远期随访结果中,小于5%的病人出现复发疝。在创面污染严重的前提下,放置补片术后再次感染率非常高,取出补片同时进行再修补并不是最佳治疗方案,在本次研究中,20例再次手术病人,其中19例切除感染组织及取出感染补片后未再补片修补,术后1例复发;1例为补片感染合并疝复发,取出感染补片后,因腹壁缺损明显,同期放置补片修补,但因腹膜缺损,无法行TAPP术,放置Proceed补片(IPOM术),术后因感染再次取补片。不推荐在行清创、取补片的同时植入新的聚丙烯等材料的补片,对于取出补片后腹股沟区存在薄弱者,可用非吸收缝线(Prolene线)适当加固。生物补片是无细胞的天然组织支架,主要成分是胶原,植入后启动内源性再生,利用宿主自身的细胞逐渐完成组织重建和血管再生,从而达到完全修复腹壁缺损的目的,它兼有抗感染,提供组织修复张力的优点。对于腹壁缺损明显的,可考虑生物补片修补[15-16]。术后出现腹股沟疝复发的病人,至少半年后可再次行腹股沟疝修补术。本研究一期缝合切口的12例病人,6例术后切口感染,感染率为50%,补片感染周围组织因长期炎症刺激、瘢痕形成,血供欠佳,取补片后创面容易渗液继发感染,所以手术医生需根据病人创面的情况,必要时暂时敞开伤口,引流后二期缝合,可自制VSD装置:首先评估伤口并清创,彻底暴露感染区。根据伤口大小修剪敷料海绵并将其嵌入伤口中,将修剪好侧孔的胃管放入海绵中间,另一端连接负压,冲洗管放置在海绵底部,用半透明贴膜封闭伤口,持续冲洗引流效果佳[17]。
在行腹股沟疝无张力修补术后,及时有效的防治是控制感染的有效途径,一旦发生感染,早期发现并进行个体化治疗,才能减轻病人的心理负担和经济负担。
