高热剂实现电路毁伤的试验探究
2019-02-25段英杰王建华刘玉存于雁武袁俊明
段英杰,王建华,刘玉存,于雁武,袁俊明
(中北大学 环境与安全工程学院, 太原 030051)
随着科技的进步,电子产品的运用也越来越广泛,目前电子设备在武器中的运用十分常见,因此只要破坏敌目标的电子设备,使其控制系统瘫痪,就能够达到在减少人员伤亡的情况下实现毁伤的效果。随着含能材料研究的发展,由一种金属或者多种金属或金属与非金属的混合物在冲击碰撞过程中可自身发生反应(铝热剂、金属间化合物)或与空气发生剧烈燃烧而释放能量的高密度活性材料成为了各国学者研究的热点[1]。由于铝热剂能够产生高热,因此在日常生活中通常用于焊接铁轨、制备复合陶瓷管以及放射性废物固化等领域[2]。而吴建坤等人运用铁-铝铝热剂完成了对弹药的销毁[3]。贾栓柱等人采用干法制粒技术制备可用于销毁未爆弹药的金属基高热剂[4]。电路板上常见的电子元件主要有:集成电路、电容、电阻、二极管等。绝大多数集成电路的基本原材料是单晶硅片,主要成分为硅,熔点约为1 414 ℃,而电容、电阻、二极管等元件不耐高温。因此以Al粉、Fe2O3粉以及SiO2粉为原料,按一定比例混合制备A、B高热剂,将干燥后的高热剂药粉压成药柱进行点火试验,观察药柱的燃烧对电路板线路及各种元件的破坏效果,并通过红外测温仪测量燃烧温度,分析其高热剂燃烧对电路元件造成的毁伤效果,探究高热剂对电路造成毁伤的可行性。
1 高热剂的选择
高热剂是指由金属粉和能与该金属粉起反应的金属氧化物混制而成,能产生铝热反应的这一类燃烧剂。高热剂的燃烧过程区别于其他燃烧剂的特征是[5]:
1) 没有气体反应生成物,因而燃烧时没有火焰;
2) 燃烧反应的温度较高,大多数高热剂的温度在(2 000~2 800 ℃)范围内;
3) 燃烧时形成熔融的红渣。大多数高热剂的燃烧温度都在2 000~2 800 ℃之间,更有甚者在3 000~4 000 ℃之间,能形成高温液态产物[6]。常见的高热反应主要是能产生高温生成熔渣的铝热反应、镁热反应,以及少量的金属间化合反应。
在常见的这些高热反应中,由于镁热反应过于剧烈甚至会发生爆炸,而金属间化合反应的反应发条件较高,因此选用相对安全又较易诱发反应的铝热反应。其在一定温度下发生反应的放热量可以由式(1)计算得出:
(1)
目前,关于铝热剂的研究很多主要有Al-CuO、Al-MoO3、Al-Fe2O3等。Al-CuO在加热时能发生激烈的反应,当在1 100 K的条件下发生反应时,根据式(1)计算其放热量能达到1 249.72 kJ,根据《实用无机物热力学数据手册》[7]查得Cu单质的蒸发点为2 574 ℃,高放热量能使生成的Cu单质发生气化,因此不利于熔渣的生成,同时还有发生爆炸的危险。Al-MoO3在1 100 K下发生反应时能够产生的热量由式(1)计算为1 011.856 kJ,产生的热量足够多,但是单质Mo的熔点为2 618 ℃,因此想要通过产生的热量使得Mo单质全部熔化形成熔渣是比较困难的。
Al-Fe2O3为最常用的铝热剂,根据手册查得单质Fe的熔点为1 536 ℃、沸点为2 862 ℃,因此在发生铝热反应产生高温的时候不会生成气态铁,从而生成铁熔渣。二氧化硅在高温的条件下能够与铝发生氧化还原反应[8],在铝热剂中加入SiO2会适当减缓反应的速率,同时生成熔点为1 410 ℃的Fe-Si合金熔渣在反应体系的高温下具有一定的流动性。
纯铝热剂反应方程式为式(2):

(2)
铝热剂中加入SiO2可能发生的反应主要为式(3)~式(5)所示:

(3)

(4)

(5)
根据手册查得当T=1 100 K时,所需数据如表1所示。
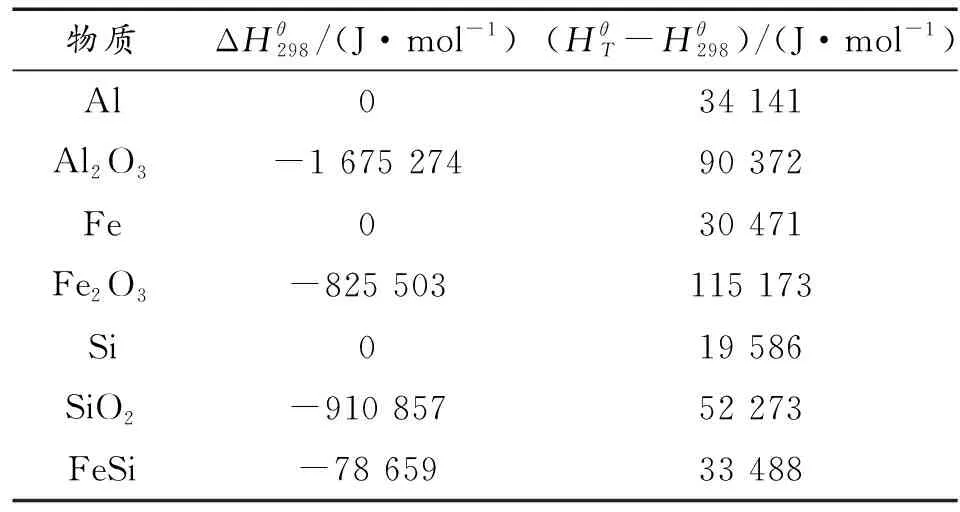
表1 各物质热力学数据
由指定温度下反应放热量的计算式(1),计算得Al+Fe2O3的理论放热量约为Q1=881.912;Al+Fe2O3+SiO2的理论放热量约为Q2=760.137
可以看出Al+Fe2O3+SiO2的理论放热量较Al+Fe2O3的放热量偏小,因此在反应过程中Al+Fe2O3+SiO2的燃烧温度会相对Al+Fe2O3偏低。
2 点火性能试验
2.1 高热剂的制备
高热剂的主要成分为Al粉、Fe2O3粉末、SiO2粉末,按以下两种不同的比例制备高热剂:
Al∶Fe2O3=1∶2制备A配方
Al∶Fe2O3∶SiO2=1∶1∶2制备B配方
选取粒度为微米级的Al粉、Fe2O3粉末、SiO2粉末,其显微镜下测得粒度如图1、图2、图3所示,Al粉为球形粒径为1~3 μm,Fe2O3粉末团聚在一起,单粒直径均为500 nm、SiO2粉末为块状直径在50~200 μm之间。

图1 Al粉SEM图
按照比例称取Al粉、Fe2O3粉用于制备A配方高热剂30 g;以及Al粉、Fe2O3粉末、SiO2粉末用于制备B配方高热剂30 g。分别放入行星式球磨机,倒入适量的无水乙醇以湿混的方式研磨混合30 min,混合好后的药粉取出放入50 ℃恒温干燥箱干燥4 h后得到图4、 图5所示的混合药剂,其中A配方高热剂中各组分外观无明显变化,两种粉末混合均匀;B配方高热剂中SiO2粉末直径明显变小,3种粉末混合均匀。

图2 Fe2O3粉SEM图

图3 SiO2粉SEM图

图4 配方A混合粉末SEM图

图5 配方B混合粉末SEM图
将混合好的药粉中加入5%黏结剂,分别称取10 g药粉放入直径20 mm的压药模具压成高15 mm的药柱备用,如图6所示。
2.2 点火性能试验
由于铝热剂燃烧需要的点火温度较高,在实验过程中无法直接点燃,因此采用导火索来引燃药剂,同时在药柱下放少许的散装药粉,保证点火的顺利进行如图7和图8所示。

图6 成型药柱

图7 配方A点火性能实验

图8 配方B点火性能实验
在点火性能试验的过程中,记录下燃烧反应的过程以及结果如图9、图10和图11所示。

图9 配方A燃烧过程

图10 配方B燃烧过程

图11 配方B燃烧后结果(正背面)
由以上试验过程可以看出配方A和配方B的燃烧过程有着明显的区别,在相同的点火条件下,配方A的燃烧过程更加剧烈,已经接近爆燃,而配方B的燃烧相对来说平缓一些。粗略统计实验结果,配方A燃烧后对电路的毁伤效果并不明显,而配方B燃烧后生成熔渣的质量为12.62 g,电路板正面熔渣毁伤面积最大为30 cm×45 cm,其中有效毁伤面积为15 cm×20 cm,烧毁电路元件包含电容器、电阻、三极管、电位器等共17个。背面灼伤面积为10 cm×13 cm,电路板无法正常工作,达到毁伤的目的。
在点火性能试验的过程中采用红外测温仪测得两种药剂在反应过程的温度变化数据,并将测得的数据采用origin画成曲线如图12、图13所示。
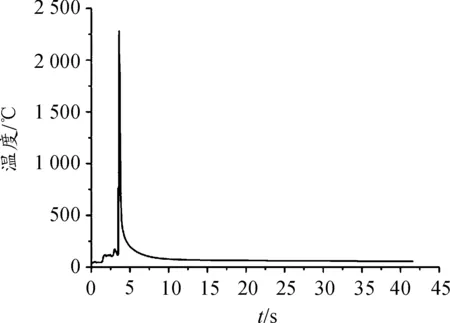
图12 配方A燃烧时间-温度曲线

图13 配方B燃烧时间-温度曲线
由两种试剂燃烧反应的时间-温度曲线可以看出:配方A的燃烧过程中温度升高和降低都非常快,进一步说明了反应的剧烈,在反应的过程中测温仪只捕捉到了爆燃一瞬间的温度,当反应结束温度也随之降低,因此配方A燃烧后对于电路板的毁伤效果并不明显。而配方B的燃烧过程相对平缓一些,在反应开始时温度迅速升高,随后由于熔渣的生成使得温度的降低变得缓慢。同时从曲线中能看出:加入SiO2后会使整个反应体系的温度有所降低,但基本维持在2 000 ℃左右,超过了Fe-Si合金的熔点(1 410 ℃),能使得合金熔渣融化。因此配方B燃烧后电路元件长时间与高温熔渣接触,使得电路元件遭到了破坏,达到了毁伤的目的。
3 结论
1) 往铝热剂中加入适量二氧化硅有利于熔渣的生成,而且形成的Fe-Si合金熔点较低,能使得生成的熔渣具有一定的流动性。
2) 同时加入二氧化硅会对铝热剂反应产生的热量有一定的影响,也会使得反应能够达到的最高温度有所降低,但是仍然保持在2 000 ℃以上。
3) 运用加入二氧化硅的铝热剂作为高热剂来破坏电路系统,一方面能够产生高温烧伤电路,另一方面产生的固体熔渣具有导电性能够造成电路短路以及断路,均能破坏电路系统。
