氨氮、苯酚在褐煤表面的单组分和双组分吸附特性
2019-02-19涂亚楠杨国枢薛继峰曹振宁徐志强
涂亚楠,杨国枢,郭 辉,周 燕,薛继峰,曹振宁,徐志强
(中国矿业大学(北京) 化学与环境工程学院,北京 100083)
现代煤化工技术主要包括煤的液化、气化和焦化、煤制烯烃、煤制醇醚等[1]。焦化废水是煤制焦工艺中产生的一种典型的高浓度、高污染、有毒难降解的煤化工工业废水[2]。煤化工废水组分复杂是其处理困难的主要原因之一,利用GC/MS法检测出焦化废水中的主要污染物包括酚类、氨类化合物,多种芳香族和多环芳烃化合物及其衍生物,少量硫化物和氰化物等数十种污染物[3,4]。上述物质具有较大的毒性和稳定的化学结构,直接采用微生物降解或化学氧化方式处理的效率较低。传统工艺通过“针对性的物化预处理—生物处理—深度处理”的方式[5]实现出水的达标排放或循环利用,工艺较为复杂。吸附法对工业废水中各种污染物都有较好的处理能力,但也存在吸附剂成本高、吸附后污染物难处理等问题[6,7]。利用具有天然多孔特性的廉价煤作为吸附剂以吸附废水中的污染物,并将吸附污染物后的煤制备为水煤浆用以燃烧获得热能或作为气化原料进行进一步的转化,是可替代的方法之一。此方法路径可避开活性炭回收存在的吸附剂回收耗能、二次污染等问题。
褐煤含有丰富的官能团和发达的孔隙结构,对废水中的污染物具有良好的吸附能力。目前有关利用煤吸附处理焦化废水中污染物的研究集中在以下几个方面:表面官能团和吸附反应条件对吸附性能的影响[8,9];通过红外光谱等表征手段解释污染物吸附的反应机理[10,11];通过表面改性提升褐煤的吸附性能[11,12]。但目前关于废水中有机和无机化合物在吸附过程中的相互影响机制的探究和分析却鲜见报道。
本文以焦化废水中的主要污染物苯酚和氨氮为研究对象,利用褐煤煤粉进行单组份和两组分吸附实验,设置不同的吸附变量考察其对吸附效果的影响,通过紫外分光光度计法对吸附过程进行定量检测,结合吸附动力学和热力学分析单一污染物和多组分同时吸附特性的差异,以及各污染物之间在褐煤表面的相互作用。
1 材料与试验方法
1.1 试验材料
煤样为内蒙古东部锡林郭勒盟褐煤,煤质分析见表1。原煤经空气干燥后用颚式破碎机破碎至3mm以下,投入球磨机中研磨10min,筛分出0.5~1mm样品,经105℃干燥脱除水分后作为吸附剂进行吸附试验。研究中所采用的试剂与纯度见表2。采用低温氮吸附法测量得该试验用吸附剂的单点比表面积为2.9257m2/g,低于一般的商业活性炭。

表1 褐煤的工业分析和元素分析
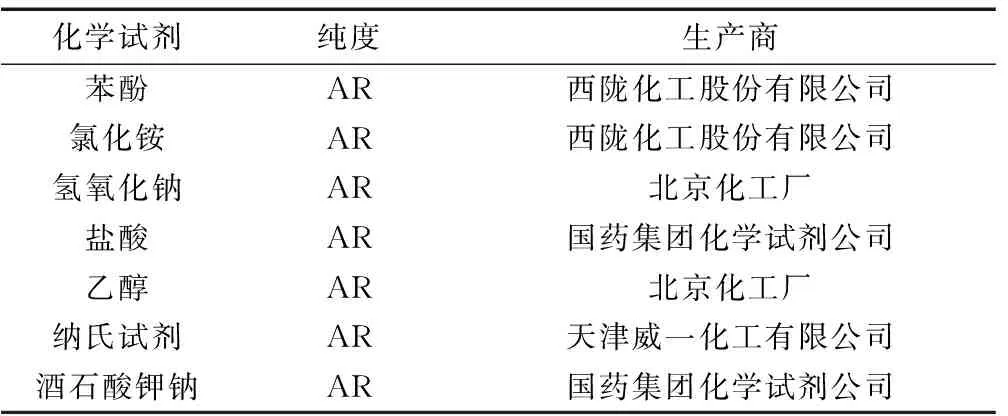
表2 本试验主要的试剂清单
1.2 试验方法
1.2.1 吸附试验方法
所有试验未调整溶液初始pH。单组分吸附试验时,用去离子水将氯化铵和苯酚分别溶解为10~70mg/L的溶液,获取模拟单组分氨氮和苯酚废水。称取1.0000±0.0002g吸附剂于100mL带塞锥形瓶中,分别加入50mL一定浓度的模拟废水,在25℃、32℃、40℃下恒温振荡不同时间后,利用针筒过滤器(孔径为0.45μm)取上清液测量溶液中氨氮和苯酚的浓度,观察不同温度、不同反应时间和不同浓度下氨氮和苯酚的煤吸附量变化。
多组分吸附试验中,将氯化铵和苯酚混合溶解为不同浓度作为双组分混合模拟废水,并设定氨氮(或苯酚)的浓度为30mg/L,而调整苯酚(或氨氮)的浓度为10~50mg/L。称取1.0000±0.0002g吸附剂于100mL带塞锥形瓶中,分别加入50mL上述溶液,在25℃下恒温震荡90min后,利用针筒过滤器取上清液测量溶液中氯化铵和苯酚的浓度,观察双组分条件下氨氮或苯酚的吸附特性。
1.2.2 组分浓度的测量和吸附量的计算
氯化铵浓度测定采用纳氏试剂分光光度法。苯酚浓度测量采用紫外可见分光光度法,通过建立269nm波长吸光度标准曲线的方式获得相应值进行计算得到。对双组分混合溶液进行浓度测量时,由于未经显色处理的氯化铵溶液在269nm波长处的吸光度对苯酚测量无干扰,因此可以直接测量苯酚溶液在此处的吸光度,进而对应标准曲线获得苯酚的浓度值。测量完成后,再通过纳氏试剂法测量氨氮的浓度。此外,测量时的参比样品为由去离子水与煤的混合悬浮液经相同搅拌浸泡时间的上清液,以剔除煤溶出物对光谱的影响。
根据式(1)和式(2)计算吸附量和去除率。
式中,Qt为t时刻组分在吸附剂上的吸附量,mg/g;Ct为t时刻溶液中组分的浓度含量,mg/L;C0为液体中组分的初始浓度,mg/L;V为溶液的体积,L;m为吸附剂的干粉质量,g;R为相应组分的去除率,%。
1.2.3 吸附动力学与热力学分析方法
采用准一级(式(3))、准二级(式(4))与颗粒内部扩散模型(式(5))[13]对吸附反应进行动力学分析,以解析反应的反应速率、平衡吸附量等参数。采用Langmuir(式(6))和Freundlich(式(7))模型[14]对吸附反应进行等温吸附热力学分析,以解析反应的主控因素和最大吸附量等参数。对不同温度条件下的吸附反应进行热力学计算(式(8)—(10)),解析吸附反应的熵变、焓变和吉布斯自由能。
ln(Qeq-Qt)=lnQeq-k1t
(3)
Qt=k3t0.5+m
(5)
ΔG=ΔH-TΔS
(9)
式中,Qt为t时刻的吸附量,mg/g;Qeq为平衡吸附量,mg/g;t为吸附反应时间,min;k1、k2、k3分别为准一级、准二级、颗粒内扩散模型参数;m,颗粒内扩散模型的参数;Ceq为吸附反应平衡时吸附质在液相中的浓度,mg/L;KL为Langmuir等温吸附模型参数;KF、1/n为Freundlich等温吸附模型吸附平衡常数;ceq为吸附反应平衡时吸附质在液相中的质量浓度,mg/g;k0为平衡分配系数;ΔG为吉布斯自由能,kJ/mol;ΔH为反应函变,kJ/mol;ΔS为反应熵变,J/(K·mol);R为理想气体常数,取8.314J/(Kmol);T为反应温度,K。
2 结果与讨论
2.1 单组分吸附试验
2.1.1 吸附动力学分析
室温条件(25℃)下,氨氮、苯酚的吸附量和去除率随反应时间的变化如图1所示。可见,吸附过程基本可以分成快速吸附、慢速吸附、稳定吸附三个阶段。其中,0~30min为快速吸附阶段:此过程中,褐煤表面含有大量空吸附位点,吸附反应易发生,吸附反应速率高。30~90min为慢速吸附阶段:此时,褐煤表面的大部分位点均被占据,吸附速率大于脱附速率,因此吸附量缓慢增加;90min以后为稳定吸附阶段:此时,吸附速率≈脱附速率,反应达到动态平衡,吸附量不再随吸附时间的增加而变化。可见,在反应时间达到90min后,氨氮和苯酚的吸附反应均达到了平衡。此时,氨氮的吸附量约为0.75~0.77mg/g,去除率约为51%~52%;苯酚的吸附量约为0.84~0.85mg/g,去除率约为56%~57%。
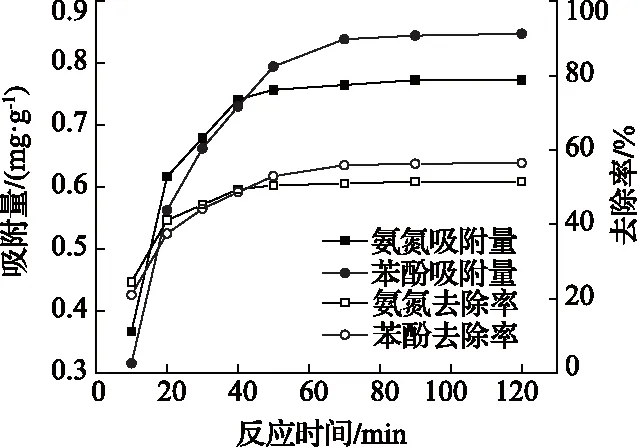
图1 反应时间对氨氮、苯酚吸附的影响
利用式(3)—(5)对图1数据进行拟合,拟合结果见表3。可知,准二级动力学方程更为适合氨氮和苯酚在褐煤表面的吸附,且氨氮的吸附速率常数要明显高于苯酚。颗粒内部扩散模型的拟合优度低,且k3均较小,且m≠0表明氨氮和苯酚的吸附受颗粒内扩散,液膜扩散和颗粒表面扩散的共同作用控制。

表3 单组分吸附动力学分析
注:Qeq(exp)为平衡吸附量实验值;Qeq(calc)为平衡吸附量计算值。
2.1.2 等温吸附分析与热力学计算
氨氮和苯酚的平衡吸附量随各自初始浓度的变化如图2所示。
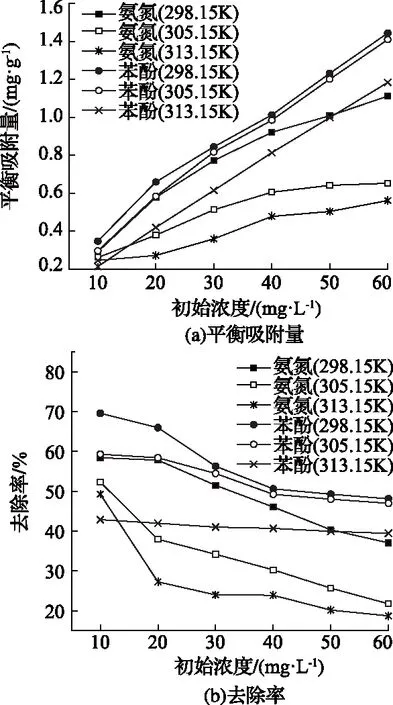
图2 不同温度条件下废水初始浓度对氨氮、苯酚吸附的影响
可见,随溶液初始浓度逐渐增大,苯酚和氨氮的去除率逐渐降低,而平衡吸附量逐渐增加。这是由于初始浓度的增加提高了吸附质在液相和固相中的浓度差,提高了吸附质向褐煤表面的迁移推动力,
增大了褐煤的吸附能力。但吸附剂的表面积有限,有效吸附位点数量也有限,因此去除率随浓度增加其去除率逐渐降低。
利用式(6)、(7)对图2数据进行拟合,拟合结果见表4。可见,在所选温度条件下,苯酚的饱和吸附量均高于氨氮,说明褐煤对苯酚的吸附能力要更高。而Freundlich模型显然具有更好的拟合优度,更加适宜描述苯酚和氨氮的吸附过程。此外,1/n的值均在0.5~1之间,说明褐煤对它们的吸附反应均较易发生。
由图2还可以看出:随着温度升高,NH4+和苯酚的分子热运动加剧,进而提高了两者的脱附速率,并使平衡吸附量下降。利用式(8)—(10)对图2(a)和表4中的数据进行计算,结果见表5。可见,褐煤对苯酚和氨氮的吸附反应的ΔG,ΔH,ΔS均小于0。其中,ΔG<0说明在以上三种反应温度下,褐煤对两组分的吸附反应均能自发进行。而|ΔG|可以反映吸附过程的推动力大小,|ΔG|越大,吸附过程的推动力越大[15]。可见,随着温度的升高,氨氮和苯酚吸附过程的|ΔG|逐步下降,且苯酚下降得更为显著,表明苯酚吸附反应对温度更为敏感。ΔH<0表明吸附过程均为放热反应,温度升高不利于反应的进行。此外,苯酚的ΔH绝对值均达到了70kJ/mol以上,表明苯酚在褐煤表面的吸附反应存在化学吸附。ΔS<0表明氨氮和苯酚被吸附到褐煤表面后运动受到限制。

表4 单组分等温吸附分析

表5 单组分吸附热力学计算结果
2.2 双组分等温吸附试验
双组分环境中,氨氮初始浓度对苯酚平衡吸附量的影响如图3所示。双组分环境中,苯酚初始浓度对氨氮平衡吸附量的影响如图4所示。可见,苯酚在双组分吸附中的平衡吸附量均高于其单组分吸附,而氨氮低于其单组分吸附。此外,图3表明氨氮初始浓度的提高对苯酚的吸附具有促进效应,而图4表明苯酚初始浓度的提高对氨氮的吸附体现为整体下降,但平衡吸附量无显著变化。双组分体系中,煤表面含氧官能团、氨氮和苯酚主要存在以下反应平衡:
R—OHR—O—+H+

C6H5OHC6H5O++H+

图3 氨氮浓度对苯酚吸附的影响
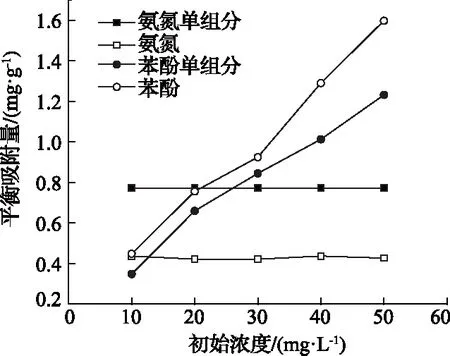
图4 苯酚浓度对氨氮吸附的影响
尽管苯酚电离出的H+有利于NH4+水解反应平衡左移,但同时也抑制了褐煤表面—OH和—COOH的电离,减少了离子交换位点,因此氨氮的平衡吸附量降低。试验过程中,各反应完成后的体系pH均在5.9~6.2之间,变化很小,说明电离平衡的左移是有限的,因此氨氮的平衡吸附量仅表现出整体的下降,而并没有随着苯酚浓度的增加而进一步减小。而NH4+会降低褐煤表面负电性,减弱了苯酚分子与褐煤表面间的静电斥力,有利于苯酚的吸附,因此导致平衡吸附量随着氨氮浓度的提高而增加。可见在双组分吸附过程中,氨氮和苯酚并非发生了吸附位点的争夺,而是各自对褐煤表面性质的整体性影响造成了各自平衡吸附量的变化。
3 结 论
1)苯酚和氨氮在褐煤表面的吸附更符合准二级动力学方程,吸附过程受颗粒内扩散,液膜扩散和颗粒表面扩散的共同作用控制。
2)随溶液初始浓度逐渐增大,苯酚和氨氮的去除率逐渐降低,而平衡吸附量逐渐增加。褐煤吸附苯酚和氨氮的过程更符合Freundlich模型,且吸附反应均较易发生。褐煤对苯酚和氨氮的吸附反应为自发、放热及熵减反应,且苯酚在褐煤表面的吸附存在化学吸附。

