负载型CoP NW/NF催化剂的制备及催化硼氢化钠水解制氢性能研究
2019-02-14代一凡
代一凡


摘要:以泡沫镍为载体材料,采用化学气相浴沉积法(CVD)制备了CoP NW/NF催化剂。采用能量色散X射线谱仪(EDS)、场发射扫描电子显微镜(SEM)、X 射线衍射(XRD)、化学吸附仪(BET)等手段对催化剂微观物理结构进行表征,对产氢速率进行了测定。同时,考察了硼氢化钠质量分数、反应温度、氢氧化钠质量分数、循环使用对催化剂性能的影响。研究表明:当硼氢化钠质量分数为15%时,产氢速率高达 13393mL/(min·g)(30℃),此时催化剂性能最佳;反应温度对产氢速率的影响较大,产氢速率与反应温度基本呈正比;氢氧化钠质量分数在20%时,产氢速率最高;该催化剂经过四次循环使用,活性仍保持在初始活性的 82.5%%,显示此催化剂具有良好的稳定性,应用前景较好。
关键词:CoP NW/NF催化剂;化学气相浴沉积法;硼氢化钠;水解制氢
由于可开采利用资源的逐渐减少和环境污染等问题[1-3]的日益严峻,迫切需要寻找一种储量丰富的环保新能源。而氢气作为高热值能源(热值120MJ·kg-1)[4],是石油热值的3 倍,且燃烧后产物为水,是最能满足社会经济可持续发展及对环境友好的清洁新能源[5-7],因而其有效开发和利用成为新能源领域的热点课题[8]。但氢气的高效、安全存 储或在温和条件下快速制氢是氢能应用必须攻克 的关键技术.
近年來,制氢的方式多种多样,可以通过化学方法对化合物进行重整、分解、光解、水解等途径获得[9-10],也可以通过电解水制氢,或者利用产氢微生物进行发酵,或光合作用来制得氢气。在众多制氢技术中,硼氢化钠(NaBH4)水解制氢因储氢密度高、产氢纯度高、反应温和、启动快速、易于调控、安全性高、副产物可回收利用等突出的优势[11],近年来备受关注,世界上许多研究 机构和公司都开展了对这一技术的研发工作。目前,用于硼氢化钠水解制氢的催化剂主要有两类:一 类是贵金属催化剂,如:Pt、Ru、Pt - Ru/LiCoO2 [12-13]等;另一类是非贵金属 催化剂,如 CoCl2、Ni - B、Co - B等[14],研究表明,贵金属催化剂对硼氢化物水解有较好的催化活性,然而贵金属价格昂贵,资源稀缺限制了其广泛使用,而过渡金属催化剂对硼氢化物水解有较好的催化活性,且不使用任何 贵金属,成本低廉[15],因此研究开发高性能的廉价实用催化剂具有重要的现实意义和研究价值[16-17]。
本研究以泡沫镍为载体,采用化学气相浴沉积方法制备了负载型 CoP 催化剂,并借助XRD、SEM、EDS、ICP、XPS 等表 征手段,分析了CoP NW/NF催化剂在 NaBH4 水解制氢过程中微观结构和表面组分的变化,研究了反应温度、硼氢化钠浓度、反 应 pH、催化剂循环使用素对其催化效率 的影响。剖析了催化剂在循环使用过程中的性能稳定的原因。
1实验部分
1.1实验试剂
泡沫镍,400 g /m2,深圳海波绿色公司;硝酸钴水合物(Co(NO3)2·6H2O,99%);氟化铵(NH4F,99%),;尿素;硼氢 化 钠(NaBH4,99%)氢 氧 化 钠(NaOH,97%),麦克林试剂公司;乙醇(CH3CH2OH,99%);盐酸(HCl,36%),北京化工厂。实验过程中所用 均为去离子水。
1.2 CoP NW/NF 催化剂的制备
采用化学气相浴沉积(CUT),以硼氢化钠为还原剂制备 CoP NW/NF催化剂,制备过程如下:
1.2.1实验选用泡沫镍为催化剂载体.剪取尺寸为 50 mm(L)× 20 mm(W)× 1.4 mm(H)的泡沫镍片用浓度为3mol/L稀盐酸超声预处理,再用去离子水洗涤后烘干。称量六水合硝酸钴(Co(NO)3·6H2O)0.5948g、氟化铵(NH4F)0.186g、尿素(CO(NH2)2)0.75g溶于35ml水中,在充分搅拌后,将溶液转移到聚四氟乙烯反应釜里,随后将泡沫镍倾斜放入,将反应釜放入鼓风干燥箱中(设置温度为120°C设置时间8h)。
1.2.2磷化
取出反应釜中已吸附纳米线的泡沫镍超声预处理,将其与已称量的1.5g次磷酸钠放入瓷舟中。将瓷舟放入管式炉通入N2(气体流动速度为35mol/L)做保护气,通过化学气相浴沉积法(CVD)磷化,煅烧300℃,2h。
1.3泡沫镍载 CoP催化剂的表征
用德国布鲁克公司的 Bruker D8 X 射线衍射仪对样品进行物相分析,入射光源为 CuKα 射线(λ=0.154 18 nm)连续扫描扫描速度 10(° /min)得XRD图(图2a);用扫描电子显微镜(SEM,日本日立公司的 HITACHI S -4800),加速电压 5 kV对样品进行形貌分 析(图1);用透射电子显微镜日立H-8100观察(TEM)图像(图2b、);用场发射扫描电子显微镜(EDX)(Nova Nano SEM 450,荷兰产)分析样品的元素成份(图2c、d)。
(此处是否需要补充物相分析及表面形貌分析?)
1.4 产氢速率的测定
催化剂对硼氢化钠产氢速率的测定通过排水法收集气体得到。该反应的方程式为 BH - 4 + 2H2O = BO - 2 + 4H2↑
为了确保测试数据的准确性,每个条件下的测试均重复 3 次,产氢速率通过单位时间内每 克Co 产 生的氢气体积计算,即对测量得到的气体体积与时 间的坐标图进行线性拟合,得到的斜率除以催化剂 中 Co 的质量,产氢速率的单位为 mL /(min·g)。本 文所使用的 CoP NW/NF 催化剂为片状结构,平均每片质 量约 45 mg,包括泡沫镍、金属 Co 以及少量杂质的 质量。在稳定性循环测试的实验过程中,由于存在 催化剂少量脱落的现象,质量会有 1 ~ 2 mg 的偏差。
2.硼氢化钠水解反应的影响因素
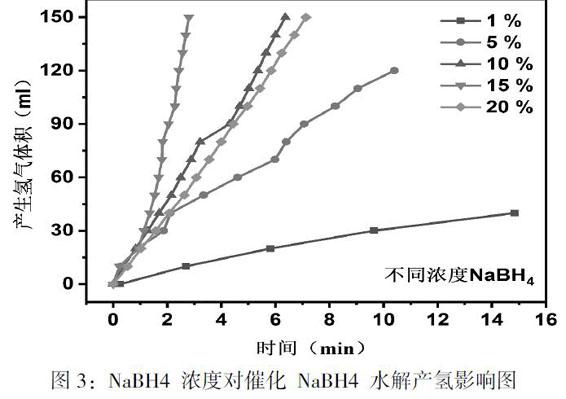
2.1 NaBH4浓度对催化 NaBH4 水解产氢的影响
首先固定反应温度为30℃NaOH质量分数为 5%,催化剂的加热时间为8h,考察不同质量分数的NaBH4(1%、5%、10%、15%、20%)对水解速率的影响。具体结果如图3所示。
当硼氢化钠质量分数为1%时,对应体系的 HGR 为 860mL/(min·g),说明在这个较低的反应物质量分数下,催化剂尚存在未被利用的活性区域[14-17]。当 NaBH4 质量分数分别为 5%、10%、15%时,对应体系的 HGR 分别为 4545mL/(min·g)、5890mL/(min·g)、13393mL/(min·g),由此可见,当其质量分数在此范围增加时,HGR数值有明显提升,说明此范围内增加反应物 浓度对 NaBH4 水解过程有促进作用。而当 NaBH4 质量分数增加至为 20%时,对应体系的 HGR则 为 5257mL/(min·g),此时 HGR值明显低于质量分数为15%的值。之所以幅度下降,研究发现是由于液体黏度大、离子扩散阻力大、反应副产物吸附累积等问题的存在所导致,按照这一趋势,继续增加 NaBH4 质量分数也很难提升水解产氢速率[14-17]。综上研究发现,当 NaBH4 质量分数为 15%,体系的 HGR 最高,催化剂性能最佳。所以,在后续的研究中,我们一直选用质量分数为15%的硼氢化钠。
2.2 Na OH浓度对催化 NaBH4 水解产氢的影响
固定硼氢化钠质量分数为15%、的 20 mL 水溶液,反应温度为30℃、催化剂的加热时间为8h。不断调整NaOH质量分数,使其分别为0%、1%、5%、10%、15%、20%、25%、30%,研究其浓度变化对水解速率的影响,具体结果如图 4所示。
当氢氧化钠质量分数为0%和1%时,对应体系的 HGR 分别为 1176mL/(min·g)和1644mL/(min·g),此时反应速率极低。当 Na OH质量分数分别提升至 5%、10%、15%、20%时,对应体系的 HGR 分别为 9415mL/(min·g)、4880mL/(min·g)、9954mL/(min·g)、37500mL/(min·g);当 NaOH 质量分数为 25% 和30%时,对应体系的 HGR 分别为 35714mL/(min·g)、31250mL/(min·g)。研究发现:在一定可控条件下,虽存在一定误差,但产氢氯基本上随 NaOH浓度的增加而提升。而当 NaOH 质量分数增加至 25% 及和30%时,此时 HGR值有所降低,表明产氢速率减小。之所以会呈现下降趋势,是由于NaOH浓度过高时会增加溶液黏度,在一定程度上抑制 NaBH4水解,降低产氢速率。综上研究发现:当Na OH质量分数为20%时,产氢速率最高。所以,在后续的研究中,我们一直使用此浓度的Na OH溶液进行实验。
2.3反应温度对催化 NaBH4 水解产氢的影响
图5 展示了不同反应温度(30℃、40℃、50℃、60℃)对体系 HGR 的影响。研究中,我们对数据点进行线性拟合得到,在反应温度分别为30℃、40℃、50℃、60℃时,体系的 HGR 分别为 4196mL/(min·g)、6445mL/(min·g)、15873mL/(min·g)、56085mL/(min·g),由图 5 可知:随着温度升高,NaBH4催化水解反应速率增加,反应温度为60 ℃ 时的反应速率比 30 ℃ 时产氢速率将近增 加 12 倍。由此可见,隨着反应温度的提高,单位时间内氢气的生成量明显提升,表明反应温度对 NaBH4水解反应的影响十分显著,升高温度有利于促进 NaBH4 水解速率,这与文献中的 结果一致。
2.4催化剂稳定性的测试
催化剂的稳定性是衡量催化剂性能的重要因素之一。图 6 是CoP NW/NF 催化 NaBH4 水解制氢第1至4次循环催化后的催化行为对比图。从图中明显看出,经过 四次循环使用后,CoP NW/NF的催化活性略有衰减,氢气的总产量没有发生较大变化,催化剂的催化活性没有明显下降,仍保留了相当于第一次 82.5%催 化 活 性。研究发现化学气相浴沉积方法制备的CoP NW/NF催化剂中,载体与 Cop 之间有更强的相互作用而使得后者结合紧密,分散良好,不易流失,催化剂整体上具有较好的稳定性。
这说明CoP NW/NF 作 NaBH4水解制氢的催化剂有着较好的稳定性和循环使用的性能。
3 结论
(1)采用化学气相浴沉积法成功制备了催化剂CoP NW/NF,并用于 硼氢化钠水解制氢反应。
(2)考察硼氢化钠质量分数对 NaBH4 溶液水解制氢的影响,研究表明:在一定范围内增加反应物浓度对 NaBH4 水解过程有促进作用。但浓度过高时,会因为液体黏度大、离子扩散阻力大、反应副产物吸附累积等问题而降低产氢速率。当 NaBH4 质量分数为 15%,体系的 HGR 最高,催化剂性能最佳。此外,还考察了反应温度和NaOH浓度变化对催化剂活性的影响,研究表明:体系温度与产氢速率呈正相关;而NaOH浓度对产氢速率的影响为在一定可控条件下,产氢氯基本上随 NaOH浓度的增加而提升,但浓度过高时会增加溶液黏度,在一定程度上抑制 NaBH4水解,降低产氢速率。
(3)对CoP NW/NF催化剂循环使用四次,测试结果表明:催化剂活性仍保持在初始活性的 82.5%%,表明载体与 Cop 之间有更强的相互作用而使得后者结合紧密,分散良好,不易流失,因而此催化剂具有较强的稳定性,应用前景较好。
参考文献
[1]PANWAR N L,KAUSHIK S C,KOTHARI S. Role of renewable energy sources in environmental protection:A revierw[J]. Renew Sust Energ Rev,2011,15(3):1513 - 1524.
[2]ZHANG X,WEI Z H,GUO Q J,et al. Kinetics of sodium borohydride hydrolysis catalyzed via carbon nanosheets supported Co/Zr [J]. J Power Source,2013,231(1):190 - 196.
[3]DUBEY P K,SINHA A S K,TALAPATRA S,et al. Hydrogen generation by water electrolysis using carbon nanotube anode[J]. Int J Hydrogen Energy,2010,35(9):3945 - 3950
[4]JIANG H L,XU Q. Catalytic hydrolysis of ammonia borane for chemical hydrogen storage[J]. Catal Today,2011,170(1):56 - 63.
[5]杨兰,罗威,程功臻. 氨硼烷水解制氢的研究进展[J]. 大学化学,2014,29(6):1 - 10.
[6]GHOSH T K,PRELAS M A. Energy Resources and Systems:Renewable Resources(Volume 2)[M]. Columbia:Springer,2011:495-629.
[7]LU J,ZAHEDI A,YANG C S,et al. Building the hydrogen economy in China:Drivers,resources and technologies[J]. Renew Sust Energ Rev,2013(23):543 - 556.
[8] Marrero-Alfonso E Y,Beaird A M,Davis T A,et al. Ind.Eng. Chem. Res.,2009,48(3):3703-3712
[9] 吴川,张华民.化学制氢技术研究进展 [ J] .化学进展,2005,17(3):423-428.
[10] 周洁,郑颖平,谢吉虹.制氢技术研究进展及燃料电池中的应 用前景[ J] .化工时刊,2007,21(5):71-75.
[11] Eberle U,Felderhoff M,Schuth F. Angew. Chem. Int. Ed.,2009,48(36):6608-6630
[12]Li Y H,Zhang Q,Zhang N W,Zhu L H,Zheng J B,Chen B H. Ru-RuO2/C as an efficient catalyst for the sodium borohydride hydrolysis to hydrogen [J]. International Journal of Hydrogen Energy,2013,38(30):13360-13367
[13]Su Runhua(苏润华),Xiao Hui(肖慧),Lin Jianbiao(林坚标). Hydrogen generation from hydrolysis of sodium borohydride with platinum catalysts loaded on nickel foam [J]. Chinese Journal of Power Sources(电源技术),2010,34(9):919-923
[14]Xu D Y,Wang H Z,Guo Q J,Ji S F. Catalytic behavior of carbon supported Ni-B,Co-B and Co-Ni-B in hydrogen generation by hydrolysis of KBH4 [J]. Fuel Processing Technology,2011,92(8):1606-1610
[15]Tian H J,Guo Q J,Xu D Y. Hydrogen generation from catalytic hydrolysis of alkaline sodium borohydride solution using attapulgite clay-supported Co-B catalyst [J]. Journal of Power Sources,2010,195(8):2136-2142
[16] Huang X K,Wu D F,Cheng D J. Porous Co2P nanowires as high efficient bifunctional catalysts for 4-nitrophenol reduction and sodium borohydride hydrolysis [J]. J Colloid Interf Sci,2017,507:429-436.
[17] Wei Y S,Huang X K,Wang J Y,et al. Synthesis of bifunctional non-noble monolithic catalyst Co -W-P/carbon cloth for sodium borohydride hydrolysis and reduction of 4-nitrophenol[J]. Int J Hydrogen Energ,2017,42(41):25860-25868.
[18]Wei Y S,Wang R,Meng L Y,et al. Hydrogen generation from alkaline NaBH4 solution using a dandelion-like Co -Mo -B catalyst supported on carbon cloth[J]. Int J Hydrogen Energ,2017,42(15):9945-9951.
[19]王濤,张熙贵,李巨峰,等.硼氢化钠水解制氢的研究[J].燃料化 学学报,2004,32(6):723-728.
[20]朱秋 灵,司 崇 殿,高 洪 涛.钴催化硼氢化 钠水解制氢研究 [J].电源技术,2011,35(1):55-58
