宫腔镜手术治疗子宫内膜息肉不孕症患者的临床疗效分析
2019-02-10张丽娟
张丽娟
(首都医科大学附属北京妇产医院妇科,北京 100026)
子宫内膜息肉是一种常见的妇科疾病,多发生在育龄期的女性,是由于子宫内膜局部过度增生所致,出现突出于子宫腔内长短不一的单个或多个光滑肿物[1~2]。目前,子宫内膜息肉的病因尚不明确,可能与人体的内分泌紊乱密切相关,雌激素水平过高会促使子宫内膜增生,长期妇科炎症、分娩、流产和手术等因素的刺激都会引起子宫内膜息肉的发生。临床上,子宫内膜息肉可以引起各种异常子宫出血,甚至会导致不孕[3-4]。去除子宫内膜息肉以往常使用刮宫术治疗,但医生只能根据临床经验来操作,可能会造成子宫内膜的创伤,破坏子宫功能[5]。近年来,随着医疗水平的不断提高,宫腔镜手术技术也取得了较大的进步,宫腔镜技术能清晰地观察宫腔内的各种改变,医生能够明确做出诊断,且对子宫内膜创伤小,术后恢复快[6]。然而,目前临床上关于宫腔镜手术治疗子宫内膜息肉不孕症的相关报道较少。因此,本研究旨在探讨宫腔镜手术治疗子宫内膜息肉不孕症的疗效。现报告如下。
1 资料与方法
1.1 一般资料
回顾性分析首都医科大学附属北京妇产医院2016年1月至2017年12月接诊的子宫内膜息肉不孕症患者108例临床资料,按照治疗方式不同分为观察组和对照组,每组各54例。对照组中,年龄25~40岁,平均(28.25±2.34)岁;病程10个月~5年。观察组中,年龄26~38岁,平均(27.53±2.17)岁;病程12个月~7年。纳入标准:(1)符合《子宫内膜息肉的治疗研究进展》[7]诊断标准;(2)均经检查确诊为不孕症;(3)超声检查子宫内有异常的回声;(4)无严重心、肾、肝等功能障碍者。排除标准:(1)合并子宫肌瘤、卵巢肿物、宫腔粘连、子宫畸形、排卵障碍者;(2)输卵管因素、男性因素引起不孕者;(3)存在凝血功能障碍者;(4)术前3个月服用过激素药物者。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法
1.2.1 对照组 给予刮宫术治疗,在宫腔镜下观察子宫内膜息肉大小、位置、数目等,采用刮匙将息肉刮除,取出后,对宫腔进行负压吸引,确保息肉刮除干净。
1.2.2 观察组 给予宫腔镜手术治疗,在月经干净后3~7 d进行手术,术前禁食。对血液和心肺功能进行检查,采用奥林巴斯医疗设备公司出品的宫腔镜电视系统,静脉麻醉,膨宫压力保持90~110 mmHg,灌流速度为250 mL/min,采用膀胱截石位,常规消毒和铺巾之后,使宫颈扩张,置入宫腔镜对子宫颈内口、前后壁、宫底等部位进行全面检查。观察息肉大小、位置、数量及蒂部宽度,将电凝输出功率调整为80~100 W,在宫腔镜直视下进行定位,切除息肉旁的子宫内膜,取出息肉后,再次使用宫腔镜进行复查,确认息肉完全彻底切除。
1.3 观察指标
观察记录两组患者手术时间、术中出血量、平均动脉压、心率和血氧饱和度。术后进行1~2年的随访,详细记录月经量、月经周期和月经改善情况(月经量减少恢复至正常状态、月经周期规律,为月经改善)。术后使用超声、宫腔镜检查患者子宫内膜息肉复发情况,随访妊娠情况。
1.4 统计学分析
2 结果
2.1 两组患者手术情况比较
观察组患者的手术时间短于对照组,且术中出血量少于对照组(P<0.05)。见表1。

表1 两组患者手术情况比较
2.2 两组患者月经情况比较
治疗前,两组患者月经情况比较,差异无统计学意义(P>0.05);治疗后,两组患者月经情况明显改善,且观察组月经量多于对照组,差异有统计学意义(P<0.05)。见表2。
表2 两组患者月经情况比较
*P<0.05,与治疗前相比。
2.3 两组患者平均动脉压、心率及血氧饱和度比较
治疗后,观察组患者平均动脉压、心率和血氧饱和度均高于对照组,差异有统计学意义(P<0.05)。见表3。

表3 两组患者平均动脉压、心率及血氧饱和度比较
*P<0.05,与治疗前相比。
2.4 两组患者复发率、妊娠成功率比较
治疗后,观察组患者复发率显著低于对照组,且妊娠成功率明显高于对照组(P<0.05),见表4。
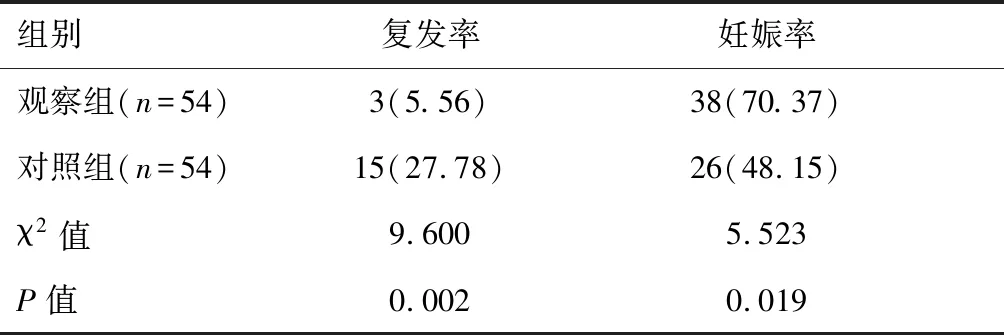
表4 两组患者复发率、妊娠成功率比较[n(%)]
3 讨论
子宫内膜息肉最常见的类型是内膜肿物突出于子宫腔内,多出现在子宫和输卵管相结合部位,是由于子宫局部内膜不断受到激素刺激导致内膜过度增生引起宫腔内突出,形成炎性息肉,造成对输卵管的堵塞,使精子、卵子不能及时结合,是导致妇女不孕的主要原因之一,也是常见的妇科疾病[8-9]。较小的子宫内膜息肉无明显的临床症状,大型息肉表面常有出血坏死,炎症容易引起感染,临床表现出现月经间期出血、月经过多和恶臭的血性分泌物。子宫内膜息肉长在子宫颈管内,阻碍了精子进入宫腔,影响胚胎的发育,导致患者不孕[10]。子宫内膜息肉不孕症不仅会对患者的身体健康造成严重的影响,还会严重影响到患者家庭。
临床上,治疗子宫内膜息肉不孕症以往主要采用药物治疗和刮宫术,但其药物治疗周期长,临床疗效不理想,很多学者也不推荐药物治疗[11]。另一方面,医生行刮宫术时看不见子宫里面,只有根据临床经验来操作,导致不能明确是否刮净,也不能做到完全刮除息肉根部。此外,刮宫手术会破坏子宫内膜功能层,刮匙不能刮到宫底及宫角部分,导致息肉残留,引起子宫内膜息肉再次复发[12]。近年来,随着医疗水平的不断提高,宫腔镜手术也被运用到妇科疾病中。宫腔镜能够清晰地观察到宫腔内的任何变化,可以对子宫内的疾病进行准确的诊断和治疗[13]。宫腔镜不仅能直接检查出子宫腔内病变,还能对息肉表面的组织结构进行细致的观察,确定出息肉位置、大小和外观。临床医生可以直接通过宫腔镜定位,去除子宫内膜息肉,大大提高了对子宫内膜息肉的准确性和成功率。宫腔镜手术还具有创伤小、出血少、可有效控制复发的优点,而且手术时间短,去除息肉的同时,也不会对子宫带来损伤,在临床上得到了广泛运用[14-15]。
本研究结果显示,采用宫腔镜手术治疗的患者妊娠成功率高达70.37%,明显高于使用刮宫手术治疗的患者,且采用宫腔镜手术治疗的患者的复发率为5.56%,明显低于使用刮宫手术治疗的患者。这提示,宫腔镜手术治疗对子宫创伤小,可以有效降低术后复发率,提高妊娠率。本研究结果还显示,采用宫腔镜手术治疗的患者手术时间、术中出血量均低于刮宫手术治疗的患者,说明宫腔镜手术治疗不但能确保子宫内膜完整,而且还可有效的减少手术时间和术中出血量。这可能是因为宫腔镜手术治疗能够准确的判定息肉的位置,从而将息肉完全清除,有效的保护了子宫内膜,从而保留患者生育功能[16]。
本研究发现,采用宫腔镜手术治疗的患者平均动脉压、心率和血氧饱和度均明显性高于刮宫手术治疗的患者。这提示在宫腔镜定位下能够切除息肉蒂部附着处的基底层,保持盆底正常解剖结构,可以改善患者的平均动脉压、心率和血氧饱和度,提高治疗效果。崔婷等[17]研究发现,采用宫腔镜手术治疗疗效显著,可以有效提升治疗准确性,且复发率较低,与本研究结果相似。这说明采用宫腔镜手术治疗子宫内膜息肉不孕症效果明显优于刮宫术,能够更精确的根除子宫内膜息肉,保证子宫内膜的完整性,疏通输卵管,有效控制月经量,从而提高了妊娠成功率,减少复发率[18]。
综上所述,宫腔镜手术治疗子宫内膜息肉不孕症患者的疗效显著,可以有效改善患者的月经情况,改善手术指标,提高妊娠率。
