D001型阳离子交换树脂吸附Cr(Ⅲ)的平衡特性及动力学
2019-01-29张学峰谈定生谢昀映李增辉丁伟中
张学峰,谈定生,2,谢昀映,李增辉,丁伟中,2
(1.上海大学 材料科学与工程学院,上海 200444;2.上海大学 省部共建高品质特殊钢冶金与制备国家重点实验室,上海 200444)
不锈钢酸洗、制革和电镀等行业产生的废水中常含有大量Cr(Ⅲ)。Cr(Ⅲ)的毒性比Cr(Ⅵ)的毒性小很多,约为1/300[1],且微量Cr(Ⅲ)对包括人类在内的哺乳动物,能起到调节身体血糖水平和控制代谢等有益作用[2],但人体内过量Cr(Ⅲ)的存在会破坏红血球、降低人体免疫力[3-4];废水中的Cr(Ⅲ)在一定条件下又有可能被氧化为毒性很大的Cr(Ⅵ)[5-6]:因此国家对含铬废水的排放有严格限制,允许排放的废水中总铬质量浓度不超过1.5 mg/L。
降低废水中Cr(Ⅲ)浓度有多种方法。化学沉淀法目前应用较广,但该法产生的含铬污泥仍属于危废固体,需要进行二次处理[7]。液膜萃取、物理吸附和生物吸附、电化学处理、离子交换等方法均能不同程度地去除Cr(Ⅲ)[8-12],其中离子交换法因具有操作简便、树脂可再生循环利用、铬离子可富集回收的特点而得到广泛重视[13-15]。
试验选用D001型阳离子交换树脂,通过静态吸附试验研究树脂对Cr(Ⅲ)的吸附效果,考察Cr(Ⅲ)在树脂上的吸附平衡和动力学行为,确定该类型树脂在含Cr(Ⅲ)废水治理中的作用。
1 试验部分
1.1 试剂与仪器
主要试剂:D001树脂(上海逊尔化工科技有限公司);硝酸铬、氢氧化钠、盐酸和1,5-二苯基碳酰二肼等,均为分析纯(国药集团化学试剂有限公司)。
主要仪器:pHS-3C型pH计(上海精密科学仪器有限公司),722型可见分光光度计(上海精密科学仪器有限公司),超级数显恒温水浴(上海浦东荣丰科学仪器有限公司),循环水式多用真空泵(上海豫康科教仪器设备有限公司)。
1.2 分析方法
采用高锰酸钾氧化-二苯碳酰二肼分光光度法测定Cr(Ⅲ)质量浓度,即在酸性介质中,用高锰酸钾将三价铬氧化成六价铬,六价铬与二苯碳酰二肼反应生成紫红色化合物,在波长540 nm处以分光光度法测定[16]。
1.3 试验方法
1.3.1树脂预处理
离子交换树脂用去离子水浸泡,待充分溶胀后,用8倍树脂体积的盐酸(1 mol/L)、去离子水、氢氧化钠(1 mol/L)、去离子水、盐酸(1 mol/L)依次淋洗转化为H型,之后再用去离子水洗至中性,抽滤后备用。
1.3.2静态吸附试验
准确称取(1.00±0.01) g湿树脂于250 mL烧瓶中,加入由硝酸铬(Cr(NO3)3·9H2O)配制的Cr(Ⅲ)质量浓度一定的溶液200 mL,在一定温度、300 r/min条件下充分混合,定时分析吸附后溶液中Cr(Ⅲ)质量浓度,计算Cr(Ⅲ)在树脂上的吸附量(q)和吸附去除率(r)。
(1)
(2)
式中:q—树脂对Cr(Ⅲ)的吸附量,mg/g;V—溶液体积,L;m—树脂质量,g;ρ0—吸附前溶液中Cr(Ⅲ)质量浓度,mg/L;ρ—吸附后溶液中Cr(Ⅲ)质量浓度,mg/L。
2 试验结果与讨论
2.1 吸附时间对树脂吸附Cr(Ⅲ)的影响
在溶液中Cr(Ⅲ)质量浓度1 027.4 mg/L、25 ℃、溶液pH=1.0条件下,吸附时间对树脂吸附Cr(Ⅲ)的影响试验结果如图1所示。
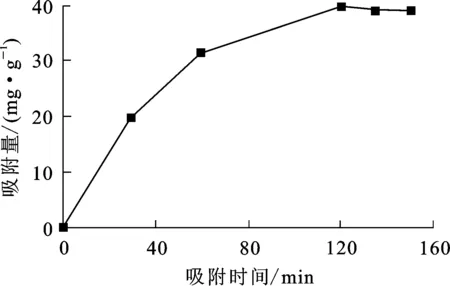
图1 吸附时间对树脂吸附Cr(Ⅲ)的影响
由图1看出:树脂对Cr(Ⅲ)的吸附量随吸附时间延长而提高;60 min内,Cr(Ⅲ)吸附量提高较快,而后提高较慢;120 min后吸附趋于平衡,平衡吸附量为39.14 mg/g。
2.2 吸附平衡等温线
吸附等温线是离子交换达到平衡时,离子在树脂相浓度和溶液相浓度相互关系的具体描述。在25 ℃、溶液pH=1.0、Cr(Ⅲ)初始质量浓度57.53~430.7 mg/L条件下,吸附等温线如图2所示。
②河道堤防:在满足河道防洪要求的条件下,改变堤顶同高、边坡均同的河堤设计方式。在满足水利规范要求的堤身宽度、高度、边坡范围内,充分利用天然堤防、自然地形等条件,形成微地形堤防,亦可将防洪堤暗藏在绵延起伏的高尔夫地形中,满足景观要求。
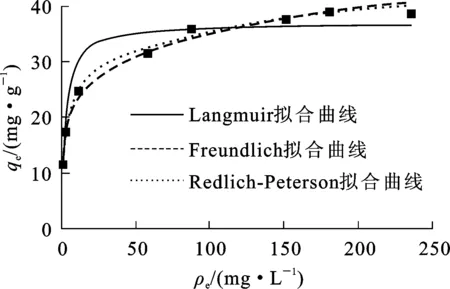
图2 树脂吸附Cr(Ⅲ)的等温线及吸附模型拟合曲线
由图2看出,树脂对Cr(Ⅲ)的平衡吸附量随溶液中Cr(Ⅲ)质量浓度增大而提高,直至Cr(Ⅲ)在树脂上达到吸附饱和。
为描述Cr(Ⅲ)在树脂相和溶液相之间的平衡关系,分别采用Langmuir、Freundlich和Redlich-Peterson吸附等温模型对图2数据进行拟合,相应方程为:
Langmuir模型,
(3)
Freundlich模型,
(4)
Redlich-Peterson模型,
(5)
式中:qe—树脂对Cr(Ⅲ)的平衡吸附量,mg/g;ρe—吸附平衡时溶液中Cr(Ⅲ)质量浓度,mg/L;qm—树脂对Cr(Ⅲ)的饱和吸附量,mg/g;kL—Langmuir平衡常数,L/mg;kF—Freundlich常数,mg(1-1/n)·g-1·L1/n;n—Freundlich吸附特征常数,量纲一;kR—Redlich-Peterson平衡常数,L/g;αR—Redlich-Peterson常数,(L/mg)β;β—Redlich-Peterson指数,量纲一。
3种模型的拟合曲线如图2所示,相应参数及相关系数(R2)见表1。可以看出,试验条件下,Redlich-Peterson模型与试验数据拟合度最好(R2=0.991 8),Freundlich模型拟合度次之(R2=0.979 1),Langmuir模型拟合度最差(R2= 0.880 7)。

表1 D001树脂吸附Cr(Ⅲ)的模型参数
Freundlich方程是描述离子在树脂上吸附平衡的经验方程,n为衡量树脂和离子亲和力的参数,n>1表明吸附容易进行[19]。拟合结果得到n=5.491,表明树脂吸附Cr(Ⅲ)为优惠吸附,与Langmuir模型拟合得出的结论一致。但树脂吸附Cr(Ⅲ)是非均匀吸附,所以采用适合非均匀吸附的Freundlich模型拟合效果优于Langmuir模型。
由图2看出:Redlich-Peterson吸附等温线能对试验数据进行很好的拟合。该模型是3参数经验方程,它结合了Langmuir和Freundlich方程的特点,同时又克服了前者受高浓度和后者受低浓度适用条件的限制[20-21],因而能更好地描述试验条件下树脂吸附Cr(Ⅲ)的平衡关系。
2.3 吸附热力学特性
热力学参数可以判断离子交换自发进行的可能性及了解温度对交换反应的影响。热力学参数计算公式如下:
(6)
(7)
ΔG=ΔH-TΔS。
(8)
式中:ΔH、ΔG、ΔS分别为离子交换吸附过程的焓变(kJ/mol)、吉布斯自由能变(kJ/mol)和熵变(J/(mol·K));kD为吸附平衡时Cr(Ⅲ)在树脂相和溶液相的分配系数,L/g;T为热力学温度,K;R为气体常数,8.314 J/(mol·K)。
由不同温度下的试验数据绘制lnkD与1/T之间的关系曲线,如图3所示,并进行直线拟合。根据式(6),ΔH、ΔS分别由直线斜率和截距求得,不同温度下的ΔG按式(8)计算,所得结果见表2。
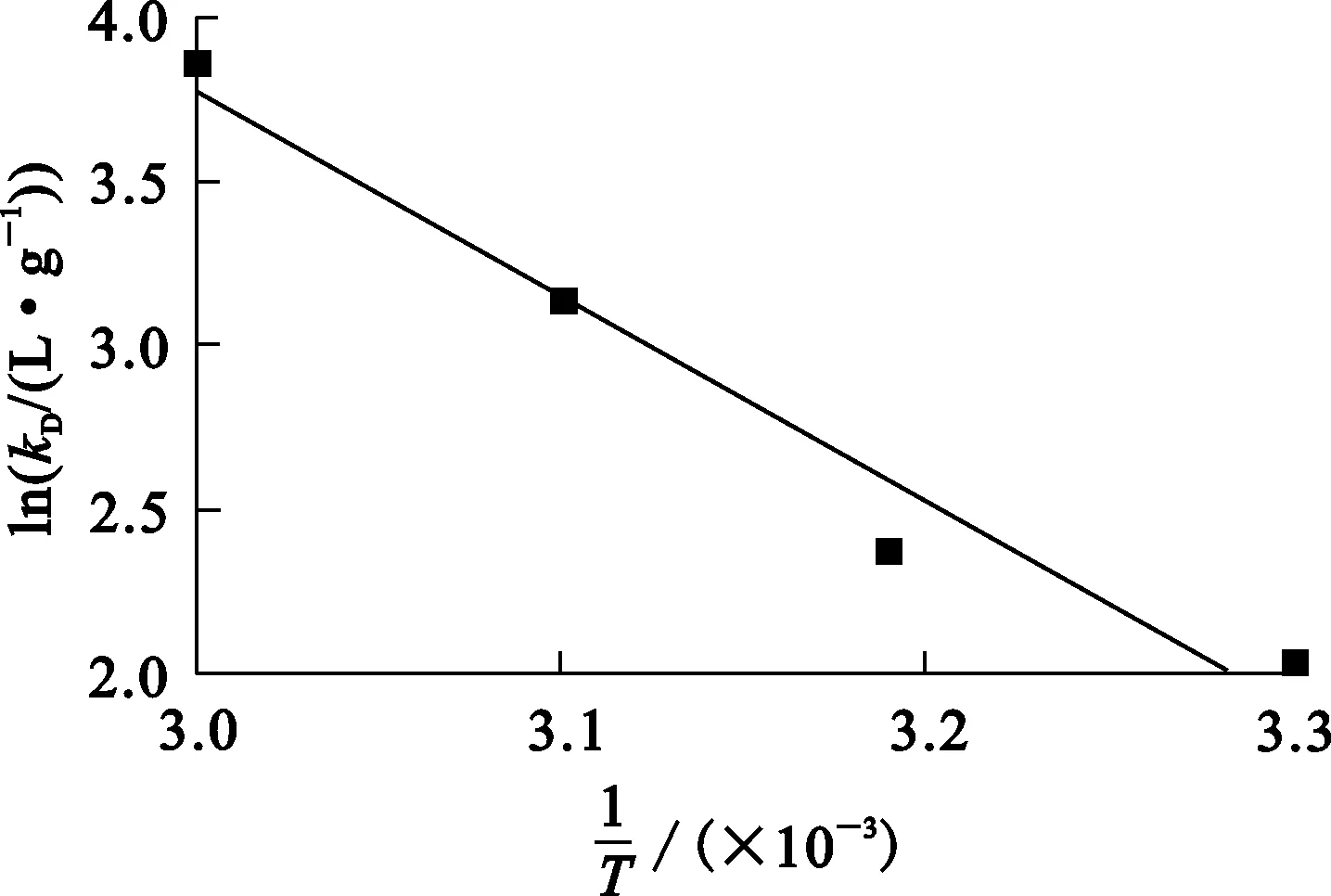
图3 树脂吸附Cr(Ⅲ)的lnkD与1/T之间的关系曲线

T/KΔG/(kJ·mol-1)ΔH/(kJ·mol-1)ΔS/(J·mol-1·K-1)303-4.77313-6.65323-8.53333-10.4152.21188.06
由表2看出:试验条件下,ΔG均为负值,表明Cr(Ⅲ)的交换吸附可自发进行;而且随温度升高,ΔG绝对值增大,表明较高温度加大了Cr(Ⅲ)吸附过程的自发程度;ΔH>0,表明树脂吸附Cr(Ⅲ)过程中吸热,升高温度有利于吸附进行;ΔS>0,是因为选择性较高的Cr(Ⅲ)交换出选择性较低的H+后,一方面树脂收缩,释放出部分水化水到溶液相,使水的熵值增大,另一方面1个三价离子交换释放出3个H+到溶液相,H+自由度增大[22]。尽管Cr(Ⅲ)从液相到树脂固相后自由度有所降低,但整个体系的自由度还是增加的。
2.4 吸附动力学
2.4.1离子交换过程的反应级数
描述离子交换的吸附动力学模型有多种,其中准一级和准二级动力学模型应用更广泛[21]。2个模型的线性化方程分别为:
ln(qe-qt)=lnqe-k1t;
(9)
(10)
式中:qt为吸附时间t时的吸附量,mg/g;k1为准一级速率常数,min-1;k2为准二级速率常数,g/(mg·min)。
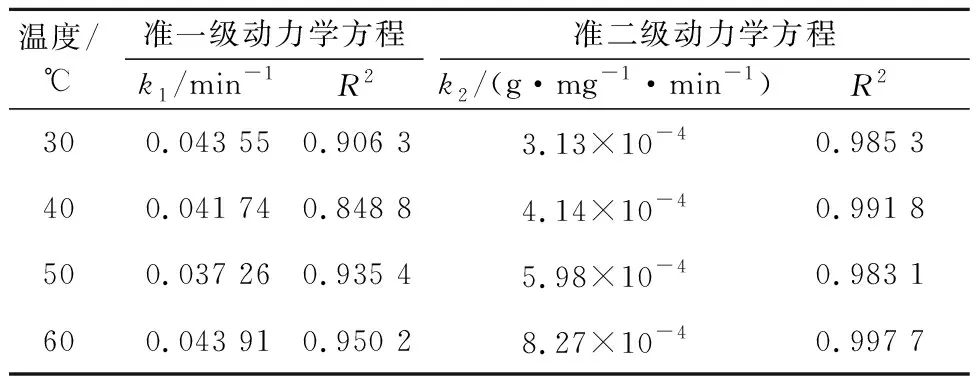
分别将不同温度下的试验数据按式(9)(10)进行准一级和准二级动力学模型线性拟合,结果如图4、5所示。D001树脂吸附Cr(Ⅲ)的动力学参数见表3,直线的斜率和截距分别为速率常数和相关系数(R2)。
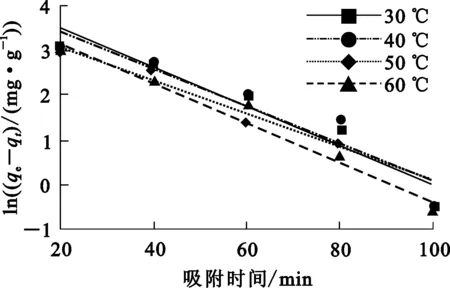
图4 树脂吸附Cr(Ⅲ)的准一级动力学拟合曲线

图5 树脂吸附Cr(Ⅲ)的准二级动力学拟合曲线
温度/ ℃准一级动力学方程k1/min-1R2准二级动力学方程k2/(g·mg-1·min-1)R2300.043 550.906 33.13×10-40.985 3400.041 740.848 84.14×10-40.991 8500.037 260.935 45.98×10-40.983 1600.043 910.950 28.27×10-40.997 7
不同温度下,准一级动力学模型的R2均小于准二级动力学模型的R2,表明树脂吸附Cr(Ⅲ)的动力学特征能更好地用准二级反应动力学模型描述。准二级动力学模型基于Cr(Ⅲ)吸附在树脂上包含有化学反应过程[23],即Cr(Ⅲ)和H+发生了离子交换反应。
根据阿伦尼乌斯公式,
(11)
以lnk2对1/T作图(图6),线性拟合相关系数R2=0.988 3,直线斜率为-3 302,计算求得树脂吸附Cr(Ⅲ)的反应活化能为27.45 kJ/mol。

图6 树脂吸附Cr(Ⅲ)过程中lnk2与1/T之间的线性关系
2.4.2交换过程的控制步骤
离子交换过程一般经历4个步骤:1)溶液中的金属离子扩散到树脂表面的液体薄膜边界层(本体扩散);2)金属离子扩散通过液体薄膜到达树脂表面(外扩散);3)树脂表面的金属离子向树脂内部扩散(颗粒内扩散);4)进入树脂内部的金属离子与树脂上的可移动离子进行化学交换反应。
在静态离子交换吸附过程中,搅拌强度足够大时,可以忽略本体扩散的影响。离子交换反应一般进行得较快,因此,外扩散或颗粒内扩散通常是交换过程的速率控制步骤[24]。
交换过程的速率控制步骤可以用Weber和Morris经验公式[25]来判断。
(12)
式中:kid为颗粒扩散速率常数,mg/(g·min1/2);I为反映薄膜边界层影响程度的参数。qt和t1/2之间呈线性关系,则离子在颗粒内扩散是离子交换过程的速率控制步骤,否则为混合控制步骤。
将试验数据按式(12)作图并进行线性拟合,结果如图7所示。

图7 颗粒扩散方程拟合曲线
由图7看出:不同初始Cr(Ⅲ)质量浓度下,qt与t1/2基本都呈直线关系,表明颗粒扩散是树脂吸附Cr(Ⅲ)的速率控制步骤;但低初始Cr(Ⅲ)质量浓度下的I(截距)大于高初始Cr(Ⅲ)质量浓度下的I,说明初始Cr(Ⅲ)质量浓度较低时,薄膜边界层影响程度较大[24],因为较低的初始Cr(Ⅲ)质量浓度在离子通过薄膜边界层扩散时推动力较小。
3 结论
用D001阳离子交换树脂可从废水中吸附Cr(Ⅲ),吸附过程更符合Redlich-Peterson模型。D001树脂吸附Cr(Ⅲ)的过程可自发进行,同时吸热和增熵。动力学研究表明,Cr(Ⅲ)在树脂上的吸附符合准二级动力学方程,吸附反应的活化能为27.45 kJ/mol,吸附过程的速率控制步骤为颗粒扩散。
