宫颈癌螺旋断层放疗与静态调强技术的剂量学比较
2019-01-28刘娟李双双高山宝闫婧侯震朱丽晶
刘娟,李双双,高山宝,闫婧,侯震,朱丽晶
1.南京大学医学院附属鼓楼医院肿瘤中心,江苏南京210000;2.东南大学生物科学与医学工程学院生物电子学国家重点实验室、医学电子学实验室,江苏南京210096
前言
宫颈癌是最常见的妇科恶性肿瘤,其发病率非常高,占我国女性恶性肿瘤之首[1]。放疗作为宫颈癌的主要治疗手段,在改善局部控制率及提高总生存时间上是得到肯定的[2-3]。常规放疗技术多采用二维模式,照射区内的正常组织受照面积过大,易引起严重急性反应或远期症状。调强放射治疗(IMRT)和容积旋转调强放疗(VMAT)的应用使宫颈肿瘤照射更加精确,正常组织能得到很好的保护。尤其是螺旋断层放射治疗(Helical Tomotherapy,HT)的出现,其整合IMRT、影像引导放疗(Image-Guided Radiation Therapy,IGRT)和剂量引导放疗为一体,是目前世界高端的肿瘤放疗设备之一,结合CT影像引导行360°聚焦式的断层照射,对肿瘤患者进行精准、安全、高效的治疗,无疑给宫颈癌患者带来了新的曙光。本研究对25例宫颈癌盆腔照射患者分别采用HT与七野-静态调强放疗(7F-IMRT)治疗技术比较剂量学差异,旨在为HT技术进一步深入运用于宫颈癌外照射提供参考数据。
1 材料与方法
1.1 临床资料
收集南京大学医学院附属鼓楼医院2015年3月~2017年10月期间接受HT治疗的25例宫颈癌盆腔外照射的患者;均有病理诊断;患者年龄35~88岁,中位年龄55岁;患者一般情况较好,KPS评分≥70分。
1.2 主要设备
美国螺旋断层放射治疗系统(Helical Tomotherapy,Hi-ART),Hi-Art Version 5.1.1三维治疗计划系统(HT组),Philips公司的Pinnacle39.10三维治疗计划系统(7F-IMRT组),Philips公司的Brilliance CT6模拟定位机(CT-SIM),美科PBSV4.1膀胱超声扫描仪,德国LAP移动激光灯,碳纤维俯卧位定位板、头枕及体膜、金点等。
1.3 定位方法
(1)定位前准备:定位前1 h嘱咐患者排空膀胱,饮用800 mL约10%浓度CT造影剂使肠道显影,自感膀胱充盈后,用超声膀胱扫描仪检测尿量;(2)定位固定:采用俯卧位,确保腹盆部自然垂入俯卧位定位板的方孔内,双臂上举交叉置于额下,并保证患者身体正中矢状面与定位板中垂线一致、背部与定位板平行,体膜固定,利用激光灯在皮肤和体模上均做标记,并在膜上贴金点;(3)影像获取:扫描范围一般自第1腰椎上缘至盆腔下缘5~10 cm处,120 kV,250 mAs,层厚5 mm,平扫+增强扫描;(4)后续工作:将数据传输至Pinnacle39.10计划系统,在患者皮肤标记“十”字处贴上保护膜,记录好数据,由双人审核签字。
1.4 靶体积及危及器官的勾画
根据ICRU 62和83号报告,由妇科肿瘤放疗医师勾画靶区与危及器官。肿瘤体积(GTV)包括MRI、CT显示的宫颈病灶和肿大淋巴结;临床靶体积(CTV)包括子宫颈体、宫旁及盆腔淋巴引流区域;计划靶区(PTV)在CTV基础上外放5~8 mm生成。危及器官包括小肠、结肠、直肠、膀胱及双侧股骨头等。由物理师创建不同剂量梯度的剂量限制环Ring及辅助限量区域Avoid,并将图像和勾画轮廓传输至TOMO计划系统。
1.5 治疗计划设计
采用Hi-Art Version 5.1.1和Philips Pinnacle39.10治疗计划系统对每例患者分别进行HT组和7FIMRT组两种计划设计。处方剂量:46~50 Gy/23~25 f(根据患者实际治疗剂量确定,保证每个患者两种计划处方剂量一致)。要求95%的PTV应获得100%的处方剂量。剂量限定如表1所示。
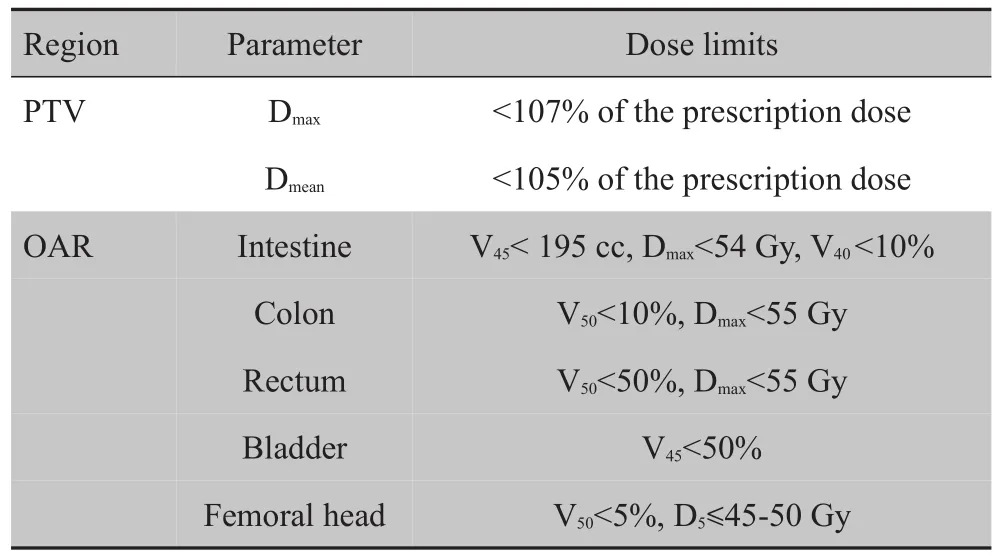
表1 靶区及正常组织剂量限定Tab.1 Dose limits for PTV and OAR
1.5.1 HT计划设计 计划模式为逆向调强,6 MV X线,剂量率864 MU/min,64对多叶准直器(MLC);设定靶区处方剂量、剂量计算网格为Fine、射野的宽度选2.5 cm、螺距(Pitch)设定0.43、调制因子初设2.0,根据优化情况进行调整,一般都不超过2.8,设定各剂量限定的优先权重(优化中时时调整)进行优化,得到最佳的剂量分布,然后进行Get Full Dose运算以考虑散射的完全剂量计算,最后进行Final Dose计算,得到最终计划。
1.5.2 7F-IMRT计划设计 调强方式为静态调强(step and shot),采用逆向设计,七野共面射野,6 MVX线,剂量率为560 MU/min,40对MLC;入射角度为0°、50°、100°、155°、205°、260°、310°,根据靶区剂量和危及器官剂量规定设置优化目标。子野数量限定60个,最小子野面积9 cm3,最小子野机器输出跳数5 MU,进行计划优化,通过反复调整优化条件或目标函数的权重,以获得较理想的剂量分布,最后进行剂量归一(95%的PTV达到处方剂量)。
1.6 评价指标
计划评价是基于各断面的剂量分布及剂量体积直方图(DoseVolume Histogram,DVH)进行各参数比较。(1)靶区剂量参数:D1(1%体积的PTV受到的最大剂量)、D2、D98(98%体积的PTV受到的最小剂量)、D95、平均剂量(Dmean)和中位剂量(D50);(2)PTV 适形度指数(Conformity Index,CI)[4]:用来评价等剂量线与靶区PTV的适形度,CI=(TVRI/TV)×(TVRI/VRI),其中TVRI为处方剂量线包绕的靶体积,TV为靶体积,VRI为处方剂量包绕的体积,CI的范围为0~1,其值越接近1表示靶区适形度越好[5];(3)靶区均匀性指数(Homogeneity index,HI)[6]:用来反映靶区内的剂量分布均匀性,HI=D2-D98/D50,其值越接近0表示均匀性就越好,数值越大表示剂量分布越不均匀[7-8];(4)两种计划危及器官比较,包括小肠、结肠、直肠和膀胱的最大剂量(Dmax)、Dmean和30、40、50 Gy 剂量受照射的体积(V30、V40、V50);双侧股骨头Dmax、Dmean、股骨头接受25 Gy受照的体积(V25)及5%的体积受照的剂量(D5)。
1.7 统计学方法
应用SPSS 22.0统计软件,数据用均数±标准差表示,采用配对t检验对两种治疗计划的剂量学进行差异分析,P<0.05为差异有统计学意义。
2 结果
25例患者均能配合治疗,未出现严重的不良反应,顺利完成治疗。
2.1 靶区剂量分布与DVH图比较
图1为某例患者两种计划中心截面的剂量分布,包括横断面、矢状面和冠状面。图2为该患者两种计划的DVH图。与7F-IMRT计划比较,HT计划处方等剂量线对靶区包绕更好,而且靶区的CI和HI更优,剂量分布更理想。

图1 两种治疗计划中心截面的等剂量分布Fig.1 Isodose distribution in the central section of two treatment plans
2.2 两种治疗计划的PTV剂量参数比较
本研究剂量分布显示,HT和7F-IMRT两种放疗计划中靶区的覆盖均能满足临床剂量要求。HT计划PTV的D1、D2分别为(51.19±2.12)Gy、(50.99±2.11)Gy,比7F-IMRT计划(52.44±2.18)Gy、(52.34±2.19)Gy低(P<0.001,P<0.001);HT计划和7F-IMRT计划的Dmean分别是(50.25±2.00)Gy、(50.47±1.97)Gy(P=0.048),D98分别是(47.85±1.98)Gy、(47.03±1.81)Gy(P<0.001),D95分别是(48.68±1.95)Gy、(48.39±1.86)Gy(P=0.015)。结果表明HT技术在尽可能保证靶区的最小剂量接近处方剂量,同时降低靶区内的热点区,使靶区的剂量线梯度越陡直;HT计划和7F-IMRT计划的CI分别为0.898±0.017和0.834±0.013(P<0.001),HT计划的CI值更接近于1,适形度优于7F-IMRT;HT计划和7F-IMRT计划的HI分别为0.062±0.012和0.109±0.019(P<0.001),HT计划的HI值更接近于0,靶区剂量分布更均匀。具体参数如表2所示。
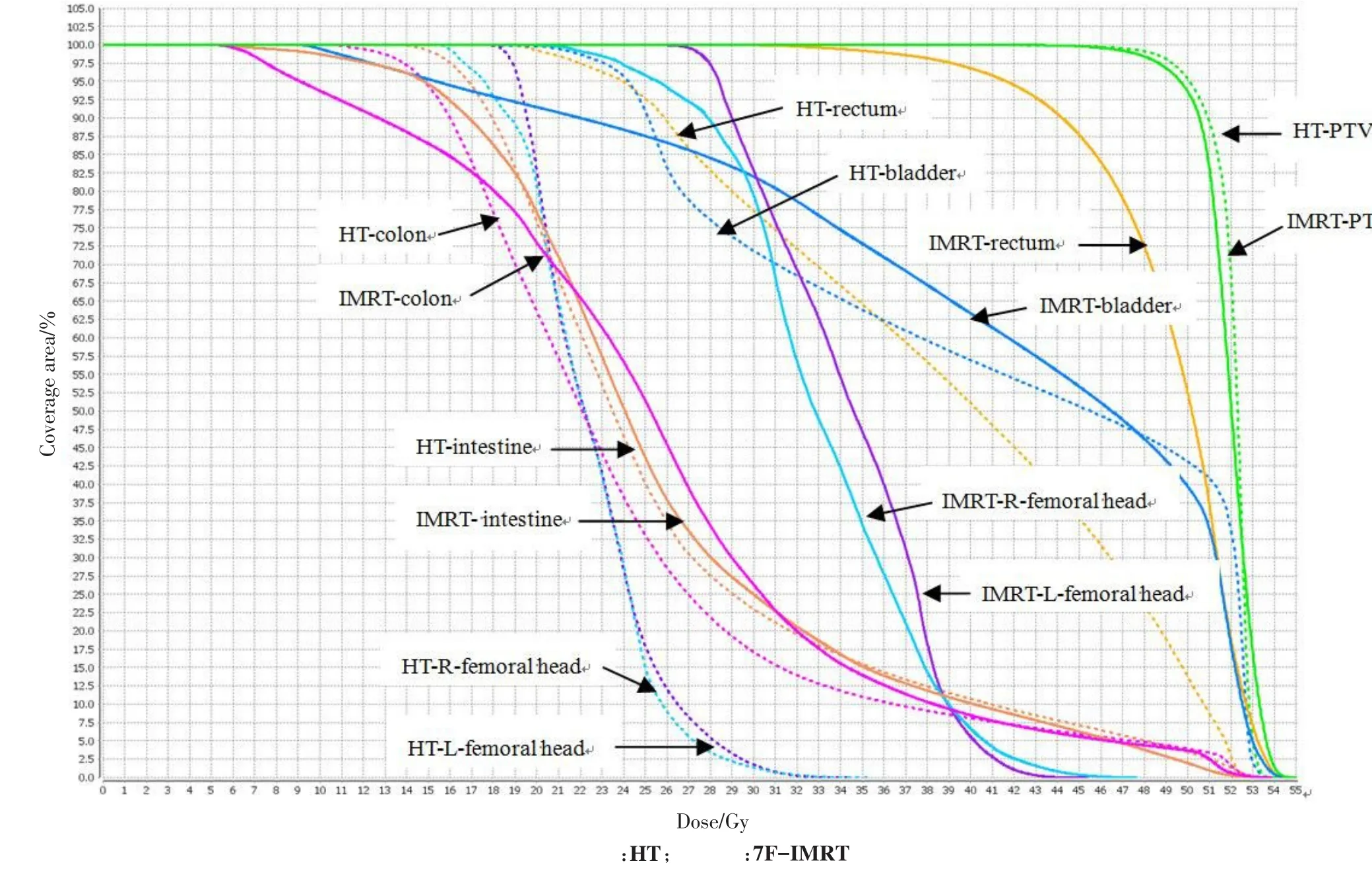
图2 同例患者两种治疗PTV和危及器官DVH图比较Fig.2 Dose-volume histogram comparison of PTV and OAR in two treatment plans of the same patient
表2 HT计划和7F-IMRT计划的PTV剂量参数比较(±s)Tab.2 Comparison of dose parameters in planning target volume between HT plan and 7F-IMRT plan(Mean±SD)

表2 HT计划和7F-IMRT计划的PTV剂量参数比较(±s)Tab.2 Comparison of dose parameters in planning target volume between HT plan and 7F-IMRT plan(Mean±SD)
CI:Conformity index;HI:Homogeneity index
Plan HT 7F-IMRT P value D98/Gy 47.85±1.98 47.03±1.81<0.001 CI 0.898±0.017 0.834±0.013<0.001 HI 0.062±0.012 0.109±0.019<0.001 Dmean/Gy 50.25±2.00 50.47±1.97 0.048 D1/Gy 51.19±2.12 52.44±2.18<0.001 D2/Gy 50.99±2.11 52.34±2.19<0.001 D95/Gy 48.68±1.95 48.39±1.86 0.015
2.3 两种治疗计划危及器官的剂量参数比较
对于小肠,两组比较除了V50无统计学意义(P=0.130),Dmax、Dmean、V30和V40均有统计学意义(P<0.001,P<0.001,P<0.001,P=0.001),HT组均优于7F-IMRT组;对于结肠除了V50无统计学意义(P=0.051),Dmax、Dmean和V30全部有统计学意义(P<0.001,P<0.001,P<0.001),HT组和7F-IMRT组的V40分别为(11.00±8.73)%、(11.82±1.64)%(P=0.006)。具体参数如表3所示。
对于直肠,HT 组的 Dmax、Dmean、V30和 V40分别为(51.14±2.10)Gy、(40.61±5.44)Gy、(80.58±19.76)%、(55.70±17.56)%均显著低于7F-IMRT组(P<0.001,P<0.001,P<0.001,P<0.001),HT组和7F-IMRT组的V50分别为(15.93±16.90)%、(25.85±24.99)%(P=0.006);对于膀胱,除了V50无统计学差异(P=0.309),HT组的Dmax、Dmean、V30和 V40均明显低于 7F-IMRT 组(P<0.001,P<0.001,P<0.001,P<0.001)。具体参数如表4所示。
对于双侧股骨头,HT组的D5、Dmean、Dmax和V25均明显低于7F-IMRT组(P<0.001,P<0.001,P<0.001,P<0.001)。具体参数如表5所示。
表3 HT计划与7F-IMRT计划小肠和结肠的剂量参数比较(±s)Tab.3 Comparison of dose parameters in small intestine and colon between HT plan and 7F-IMRT plan(Mean±SD)
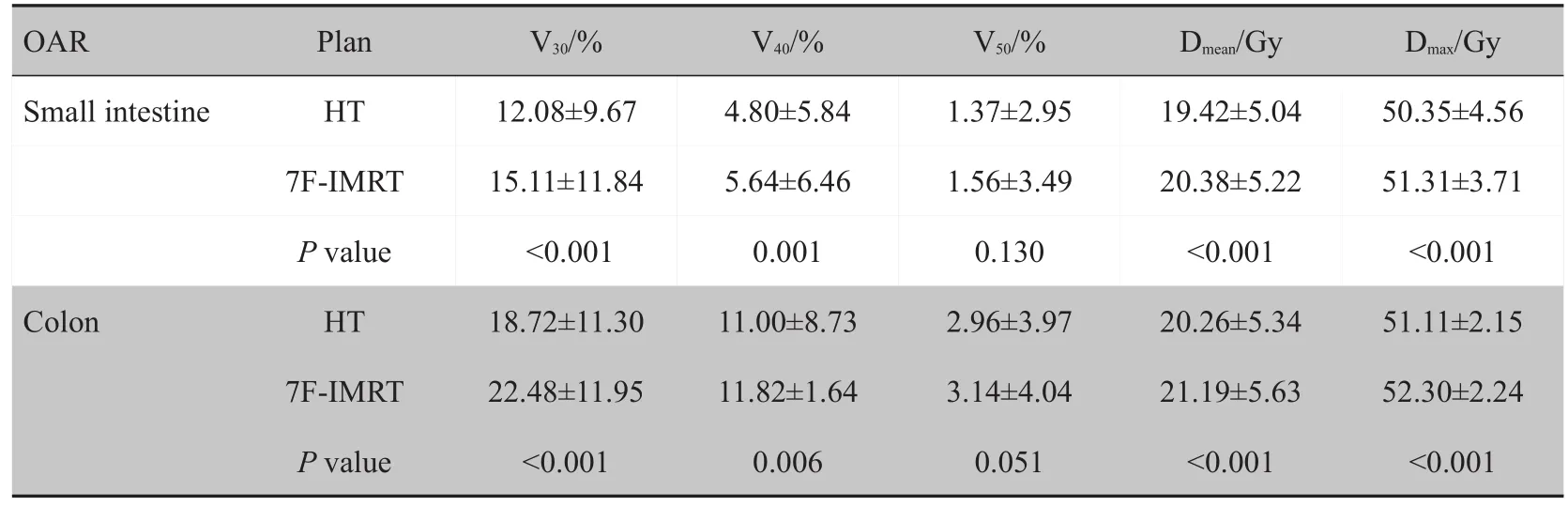
表3 HT计划与7F-IMRT计划小肠和结肠的剂量参数比较(±s)Tab.3 Comparison of dose parameters in small intestine and colon between HT plan and 7F-IMRT plan(Mean±SD)
OAR Small intestine Colon Plan HT 7F-IMRT P value HT 7F-IMRT P value V30/%12.08±9.67 15.11±11.84<0.001 18.72±11.30 22.48±11.95<0.001 V40/%4.80±5.84 5.64±6.46 0.001 11.00±8.73 11.82±1.64 0.006 V50/%1.37±2.95 1.56±3.49 0.130 2.96±3.97 3.14±4.04 0.051 Dmean/Gy 19.42±5.04 20.38±5.22<0.001 20.26±5.34 21.19±5.63<0.001 Dmax/Gy 50.35±4.56 51.31±3.71<0.001 51.11±2.15 52.30±2.24<0.001
表4 HT计划与7F-IMRT计划直肠和膀胱的剂量参数比较(±s)Tab.4 Comparison of dose parameters in rectum and bladder between HT plan and 7F-IMRT plan(Mean±SD)
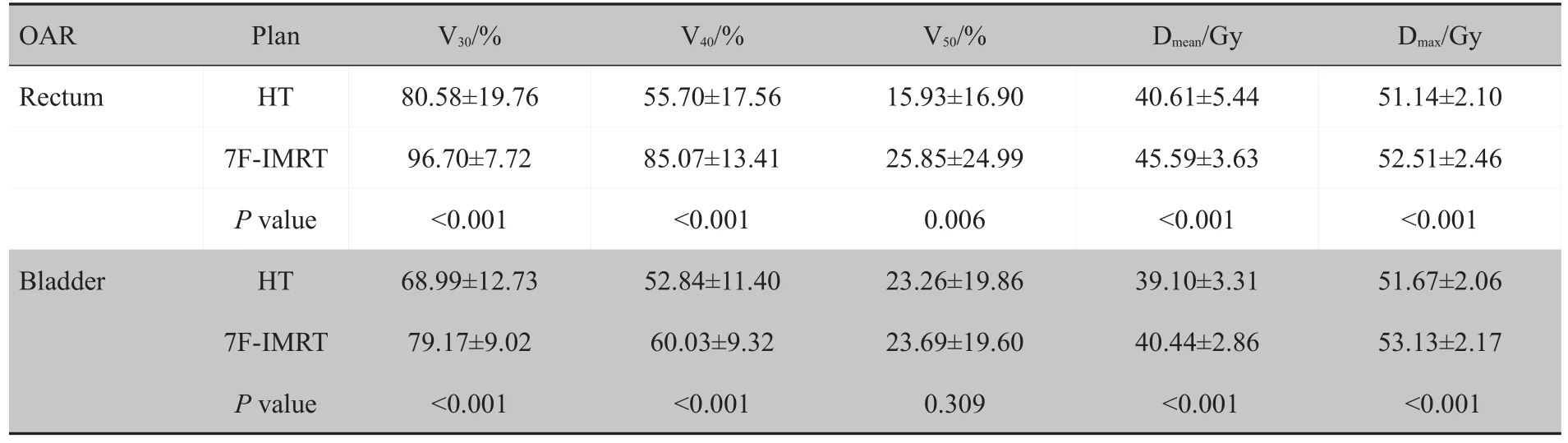
表4 HT计划与7F-IMRT计划直肠和膀胱的剂量参数比较(±s)Tab.4 Comparison of dose parameters in rectum and bladder between HT plan and 7F-IMRT plan(Mean±SD)
OAR Rectum Bladder Plan HT 7F-IMRT P value HT 7F-IMRT P value V30/%80.58±19.7655.70±17.5615.93±16.9040.61±5.4451.14±2.10 96.70±7.7285.07±13.4125.85±24.9945.59±3.6352.51±2.46<0.001<0.0010.006<0.001<0.001 68.99±12.7352.84±11.4023.26±19.8639.10±3.3151.67±2.06 79.17±9.0260.03±9.3223.69±19.6040.44±2.8653.13±2.17<0.001<0.0010.309<0.001<0.001 V40/%V50/%Dmean/Gy Dmax/Gy
表5 HT计划与7F-IMRT计划左右股骨头的剂量参数比较(±s)Tab.5 Comparison of dose parameters in left and right femoral heads between HT plan and 7F-IMRT plan(Mean±SD)
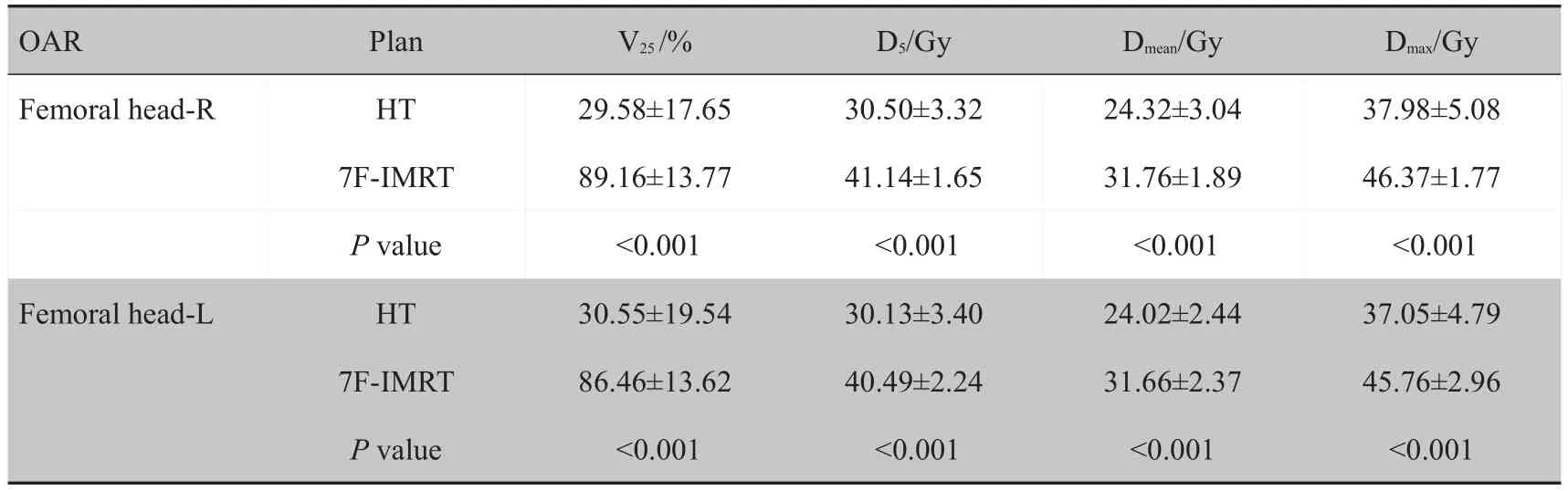
表5 HT计划与7F-IMRT计划左右股骨头的剂量参数比较(±s)Tab.5 Comparison of dose parameters in left and right femoral heads between HT plan and 7F-IMRT plan(Mean±SD)
OAR Femoral head-R Femoral head-L Plan HT 7F-IMRT P value HT 7F-IMRT P value V25/%29.58±17.6530.50±3.3224.32±3.0437.98±5.08 89.16±13.7741.14±1.6531.76±1.8946.37±1.77<0.001<0.001<0.001<0.001 30.55±19.5430.13±3.4024.02±2.4437.05±4.79 86.46±13.6240.49±2.2431.66±2.3745.76±2.96<0.001<0.001<0.001<0.001 D5/Gy Dmean/Gy Dmax/Gy
2.4 机器输出跳数
HT计划与7F-IMRT计划的机器输出量分别为(5 702±1 124)MU、(808±131)MU,HT计划相对于7F-IMRT计划的机器跳数平均增加了7.1倍(P<0.001),延长了治疗时间,降低了射线利用率。
3 讨论
放射治疗在宫颈癌的综合性治疗中有着重要的地位,但是常规放疗可能会导致较为严重的消化系统和泌尿系统的并发症,不仅严重影响了生活质量,也影响了疗效[9]。随着放疗技术的不断发展,三维调强放疗技术日臻完善,宫颈癌IMRT技术在临床上已应用十余年,其优势主要表现在对正常组织的保护和毒性反应的降低,最大可能提高疗效,减低副作用,缓解患者的痛苦[10-12]。
近几年,旋转断层调强技术的出现与发展,有效改善了放射治疗的效能,如HT、VMAT及质子治疗等[13-14]。HT技术结合加速器与CT螺旋断层扫描,是一种较新的调强模式,具有旋转照射、螺旋式照射、MVCT-IGRT等多种放疗技术优势。既往研究结果显示,HT技术在肿瘤治疗中显示出更优的靶区适形度、均匀性及对危及器官保护等优势,在肿瘤放疗中取得更好的治疗效果,并且放疗相关副反应耐受良好[15-18]。本研究对HT与7F-IMRT的剂量学优势进行全面的比较,结果显示在HT计划中,其改善了放疗计划的CI和HI,显著改善了剂量分布,同时满足了剂量限制的需求,具有显著的剂量学优越性,明显好于7F-IMRT计划,为提高肿瘤治疗的疗效提供保障;在危及器官保护方面,HT计划对小肠、结肠、膀胱、直肠及股骨头等的保护均优于7F-IMRT计划,与既往杨宗霞等[19]研究结果类似。
HT是当前唯一采用放疗与验证CT同源的图像引导系统,成像精度非常高,高达±0.1 mm,在每次治疗前进行图像配比,可依据肿瘤部位逐日的变动情况及时调整照射剂量、角度和范围。由于盆腔肿瘤照射过程中存在小肠、结肠不自主运动,受膀胱充盈和直肠扩张的影响较大,使得肿瘤位置随之改变,即便在一次治疗开始与治疗中都有可能因大便或尿液的积聚而不同,所以我们在每次治疗前使用超声膀胱测量仪检测膀胱容量,直肠处于排便后状态,尽可能跟定位时状态保持一致。由于HT技术采用的是螺旋断层治疗,机器输出量较高,MU数较多,治疗时间延长,低剂量辐射区域较大,对射束的利用率不高,其风险还需要进一步评估[20]。
HT计划可减少宫颈癌放疗中危及器官的受量,满足剂量限制的需求,对小肠、股骨头及直肠的保护尤其突出,并且放疗计划的CI和HI明显提高,改善剂量分布,从而优化治疗计划。本研究也有一定的缺陷,比如病例数目过少、未跟后装内照射进行剂量叠加后的评估等,后续会继续扩大样本量,进一步分析剂量分布与相关毒副作用及治疗近、远期疗效。
