DART-Q-Orbitrap MS法快速检测豆制品中碱性橙Ⅱ和金胺O
2019-01-22迟鸿悦赵彩秀郭云龙刘淑莹
刘 喆,迟鸿悦,赵彩秀,黄 鑫,郭云龙,刘淑莹,2
(1.长春中医药大学,吉林省人参科学研究院,吉林 长春 130117;2.中国科学院长春应用化学研究所,长春质谱中心,吉林 长春 130022)
腐竹、干豆腐、豆皮等豆制品中含有丰富的蛋白质等多种营养成分,是颇受欢迎的传统食品。碱性橙Ⅱ(C12H12N4HCl)和金胺O(C17H21N3HCl)均属于偶氮工业染料,主要用于腈纶、纺织品、纸张、皮革、家具等的染色,该染料可致癌、致畸,对人体健康具有严重的危害。碱性橙Ⅱ和金胺O等染料在中性和偏碱性的条件下与蛋白质结合牢固,不易褪色且成本低廉。一些食品生产商非法添加该类染料使豆制品颜色鲜亮,严重损害了消费者的身体健康。《中华人民共和国食品添加剂使用卫生标准》及《中华人民共和国食品卫生法》规定,禁止碱性橙Ⅱ和金胺O作为食品添加剂。
目前,检测豆制品中碱性橙Ⅱ和金胺O的方法主要有光谱法、高效液相色谱法(HPLC)和高效液相色谱-质谱法(HPLC-MS)[1-6]等。虽然研究人员不断优化检测方法,但在实际操作中仍存在前处理使用的试剂种类复杂,检测前需要液相分离,检测步骤繁琐耗时等问题。
敞开式离子化质谱(ambient ionization mass spectrometry, AIMS)是由Cooks等[7]于2004年首次提出的一种新型离子化技术,即在大气压环境下,在开放实验室环境中,在不改变被分析物本身性质的条件下,直接完成对样品的离子化以及进样分析的技术方法[8]。实时直接分析(DART)是AIMS中一种典型的离子化技术,主要优点是可以在几秒钟内实现液体、气体、固体样品材料表面的痕量或少量化合物的离子化质谱分析[9]。四极杆-静电轨道高分辨质谱仪(Q-Exactive)采用先进的信号处理技术,依靠其高分辨的优势可将检测数值精确到小数点后两位,有效避免假阳性结果的出现。该仪器对定性和定量的程序进行了重新定义,具有称为确证定量“quanfirmatiom”的新功能,对化合物的鉴定、定量和确证,都可在一次分析中同时完成,是针对食品安全中的一些非法添加及有机污染物定性或定量分析的理想筛选平台[10]。
本研究拟采用DART-Q-Orbitrap MS联用技术对豆制品中非法添加的碱性橙Ⅱ和金胺O染料进行快速检测分析,通过优化分析方法,希望建立一种简单、快捷、准确、高效、绿色的定性和定量分析方法,并为其他食品中非法添加的染料检测提供参考依据。
1 实验部分
1.1 仪器与试剂
DART 离子源:包括自动滑轨、载样熔点孔载样器、玻璃滴管液体载样模块(Dip-it),美国 Ion Sense 公司产品;Q-Exactive Orbitrap 质谱仪(包括Xcaliber工作站)、移液枪:均为美国Thermo-Fisher公司产品;Waters Purifier-R-M220 超纯水机:长春莱博特公司产品;KQ-500DA 数控超声波清洗器:昆山市超声仪器公司产品;高速万能粉碎机:北京市永光明医疗仪器有限公司产品;离心机:德国Eppendorf公司产品。
碱性橙Ⅱ和金胺O标准品:纯度均大于80%,上海源叶生物科技有限公司产品;豆制品样品:购自本地市场;乙腈:色谱纯,美国Thermo-Fisher公司产品;高纯氮气、氦气:纯度 99.999%,长春巨洋氧厂产品。
1.2 标准品溶液配制
精密称取各5 mg碱性橙Ⅱ和金胺O标准品,分别置于10 mL容量瓶中,加入乙腈溶解,摇匀,并用乙腈定容,配制成0.5 g/L的标准品工作溶液,于4 ℃冰箱储存,备用。
1.3 样品制备
将市售豆制品样品粉碎,过60目筛,精密称取1 g(精确至0.01 g)样品,置于50 mL离心管中,加入10 mL 80%乙腈水溶液[6],超声提取30 min,以5 000 r/min离心5 min,转移上清液于另一50 mL离心管中,作为样品溶液,于4 ℃冰箱中保存,备用。将空白豆制品样品粉碎,依照上述方法制成空白基质溶液,于4 ℃冰箱保存,备用。
1.4 实验条件
1.4.1DART条件 离子化气体为氦气,待机气体为氮气,气体压力0.3 MPa,离子化温度300 ℃,毛细管温度250 ℃,其他参数采用仪器默认设置,应用正离子模式采集,Dip-it方式进样,载样器传输速度2 mm/s。
1.4.2质谱条件 质量扫描范围m/z50~500,分辨率70 000 FWHM,AGC target 3×10-6,正离子模式,扫描方式为Full MS-SIM/Targeted-MS2,碎裂电压为50~55 eV,DART离子源与质谱仪接口之间的距离为3.2 cm。
2 结果与讨论
2.1 DART-MS参数的优化
2.1.1工作气体的选择 为提高检测性能,达到更好的检测效果,对DART的实验参数进行系统性优化。实验发现,工作气体类型和温度是影响信号强度的重要因素。根据文献报道,DART离子源的工作气体多为He[11-13],这是因为N2作为离子化试剂时会发生副反应,产生的信号峰相对杂乱,且这种气体的激发态粒子能量较低,为8.5~15.0 eV;而23S激发态的氦原子具有比氮更高的能量,其内能可达到19.8 eV,能够使更多种类的化合物被电离,且不产生过多的碎片离子[14-15]。因此,本实验选用氦气作为工作气体。由于氦气的价格约为氮气的15倍,实验待机过程中选用N2作为待机气体,既可防止离子源污染又可节约成本。
2.1.2工作气体温度的选择 分别取适量的碱性橙Ⅱ和金胺O标准品工作液,用基质溶液稀释至10 mg/L,以熔点管进样方式分别在100、150、200、250、300、350、400 ℃下检测碱性橙Ⅱ和金胺O在质谱中的响应值与载气温度的关系。由于高温激发态有利于待测物质去溶剂化并转移到气相中[16],故在一定范围内升高温度。在达到最大离子信号前(金胺O为350 ℃,碱性橙Ⅱ为300 ℃),离子信号的强度随温度升高而不断增强,超过最高温度范围后离子信号明显减弱。这是由于过高的温度会使样品分解、碳化,因此信号强度随温度升高而下降[13]。综合考虑载气温度对各检测值的影响,最终选定最佳温度为300 ℃。
2.1.3其他参数优化 待测物通过由DART 软件控制的滑动轨道上的Dip-it管尖端引入质谱仪。通过检测发现,载有待测物的Dip-it管尖的移动速度与离子流图的峰宽密切相关,减慢速度有利于提高离子化效率,但速度过慢会使离子流图的峰宽过宽。综合考虑,本实验选择传输速度为2 mm/s,DART离子源孔与质谱仪接口之间的距离为3.2 cm。
2.2 碱性橙Ⅱ和金胺O的定性分析
碱性橙Ⅱ和金胺O在溶液中以正离子形式存在,根据其结构,选择正离子模式进行扫描[18],用熔点管分别蘸取碱性橙Ⅱ和金胺O标准品的乙腈溶液(10 mg/L),得到Full MS下的一级质谱图,示于图1。碱性橙Ⅱ(C12H12N4·HCl)的相对分子质量为248.082 9,在DART-MS正离子模式下,得到质子化的准分子离子峰m/z213.114 2[C12H12N4+H]+,与理论值的质量偏差为3.23×10-6。金胺O(C17H21N3·HCl)的相对分子质量为303.150 2,得到质子化的准分子离子峰m/z268.181 1[C17H21N3+H]+,与理论值的质量偏差为1.12×10-6。通过Targeted-MS2扫描,分别对碱性橙Ⅱ和金胺O进行二级质谱碎裂,发现碱性橙Ⅱ在碰撞电压为50 eV时,得到的主要碎片离子有m/z77.04、105.04、121.06;金胺O在碰撞电压为55 eV时,主要碎片离子有m/z79.05、107.07、122.10、147.09、252.15。两种化合物的二级质谱图和碎裂途径示于图2。
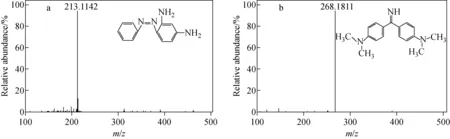
图1 碱性橙Ⅱ(a)和金胺O(b)的一级质谱图Fig.1 Full mass spectra of Basic Orange Ⅱ(a) and Auramine O (b)

图2 碱性橙Ⅱ(a)和金胺O(b)的二级质谱图Fig.2 DART tandem mass spectra of Basic Orange Ⅱ (a) and Auramine O (b)
本实验对阳性豆制品样品进行直接检测。将空白豆制品样品分别浸泡在不同浓度梯度的碱性橙Ⅱ和金胺O的80%乙腈标准溶液中,取出后用氮气吹干。剪取小片腐竹、干豆腐和豆皮(约2 cm×0.5 cm×0.3 cm,大小没有严格的要求,可放入离子源与质谱仪接口间并留有一定空隙即可),分别置于DART 离子源与质谱仪接口之间,按照1.4节条件对阳性样品进行一级质谱检测。结果表明,浸泡在浓度为0.2 mg/L碱性橙Ⅱ标准溶液和浸泡在浓度为0.5 mg/L金胺O标准溶液中的豆制品均可直接在DART质谱仪中检出相应的染色剂。
2.3 碱性橙Ⅱ和金胺O的定量分析
借助电喷雾离子化(electrospray ionization, ESI)和基质辅助激光解吸离子化(matrix-assisted laser desorption/ionization, MALDI)等软电离质谱,通过被测物质的准分子离子信号实现定量检测[18-19],为质谱用于直接定量分析奠定了基础。迄今为止,已经相继开发了20余种能够用于质谱直接定量分析的离子化技术[20]。虽然它们的结构原理不尽相同,但均能将气、液和固态样品直接离子化,可用于复杂样品(如中药、代谢物、非法添加物质等)的快速定量分析[21-24],并可利用质谱自身的筛选功能对分析物进行含量测定,实现快速在线原位分析,缩短检测周期,且具有良好的准确性和稳定性。本实验采用定量分析方法进行方法学考察,并得到了豆制品中非法添加染料碱性橙Ⅱ和金胺O的含量。
由于熔点管无法准确控制载样量,因此选用Dip-it管进样方式来控制载样量的相对统一。取少量配制好的母液进行混合并梯度稀释至0.1 mg/L,将不同浓度的碱性橙Ⅱ和金胺O标准品混合基质溶液置于1.5 mL EP管中,统一液面高度为1.5 cm,用Dip-it管蘸取相同液面高度的混合基质溶液于载样熔点孔载样器上,蘸取时间约3 s。然后将其固定在DART离子源与四极杆-静电场轨道阱质谱仪之间的滑动轨道上,按照1.4节条件进行检测,得到该方法对碱性橙Ⅱ和金胺O的检出限(LOD)均为0.2 mg/L。
2.4 精密度实验
分别蘸取5.0 mg/L碱性橙Ⅱ和金胺O标准品基质溶液,按1.4节条件进行检测,重复测定6次,分别提取碱性橙Ⅱ和金胺O的离子流图,以峰面积计算。结果表明,碱性橙Ⅱ、金胺O的相对标准偏差(RSD)值分别为9.2%、14.0%,表明该仪器的精密度良好。
2.5 重复性实验
分别按1.3节方法将碱性橙Ⅱ和金胺O标准品用基质溶液稀释成10、20和50 mg/L的标准品,同一浓度配制6份。按照1.4节条件进行检测,分别以碱性橙Ⅱ和金胺O提取离子流图的峰面积计算。结果表明,碱性橙Ⅱ的RSD 分别为 7.0%、9.8%和5.3%,金胺O的RSD 分别为13.7%、7.3%和5.7%,表明该方法重复性良好。
2.6 线性关系考察
精密吸取适量标准品储备液,分别以基质溶液稀释成质量浓度为1.0、2.0、5.0、10.0、20.0、50.0、100.0 mg/L的标准品溶液,每个浓度配制6份,按照1.4节条件进行检测,取每个浓度的平均值。结果表明,在1.0~20.0 mg/L浓度范围内,碱性橙Ⅱ和金胺O的线性关系良好。当浓度为50和100 mg/L时,由于浓度过高,对轨道阱检测器造成饱和效应,不能获得良好的线性关系。以峰面积(y)和标准品质量浓度(x)进行回归分析,得到碱性橙Ⅱ和金胺O的回归方程分别为y=14 130x+534.74,R2=0.994 1;y=26 601x+2 629.2,R2=0.990 7,二者的线性关系曲线示于图3。

图3 碱性橙Ⅱ(a)和金胺O(b)的线性关系曲线Fig.3 Corresponding relation curves of peak area vs.the concentration of Basic Orange Ⅱ (a) and Auramine O (b)
2.7 标准曲线绘制
采用五味子醇甲为内标,分别以碱性橙Ⅱ和金胺O与五味子醇甲提取离子流图的峰面积比为纵坐标,碱性橙Ⅱ和金胺O基质溶液的浓度为横坐标绘制标准曲线。碱性橙Ⅱ和金胺O标准溶液的浓度梯度分别为1.0、2.0、5.0、10.0、20.0 mg/L,五味子醇甲的浓度均为5 mg/L。得到碱性橙Ⅱ和金胺O的回归曲线分别为y=0.124x+0.162 9,R2=0.994 5和y=0.258 4x+0.147 5,R2=0.998 9,示于图4。由于敞开式离子源存在一定的不稳定性,进样量无法保证完全一致,而内标法定量与进样量无关,只需被测物质和内标物出峰,且分离度符合要求即可。因此,为使定量分析结果更加准确,本实验选择内标法进行定量。需要注意的是,在实验过程中必须保证内标物与样品混合均匀。
2.8 市售样品检测
各取5组市售的腐竹、干豆腐、豆皮样品,编号为Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ,按照1.4节条件,将统一大小的样品小片分别置于离子化区域内直接检测,发现Ⅱ、Ⅴ号腐竹中出现碱性橙Ⅱ的准分子离子峰[C12H12N4+H]+,Ⅰ号豆皮样品中出现金胺O的准分子离子峰[C17H21N3+H]+,分别对其进行二级质谱碎裂,其谱图与图2相同。按1.3节方法进行提取,并按上述方法定量,测得腐竹Ⅴ号的碱性橙Ⅱ含量为1.59 mg/kg,Ⅱ号样品的峰面积比值低于线性范围而无法定量,但不影响定性。Ⅰ号豆皮中的金胺O含量为1.26 mg/kg。干豆腐样品以及其他的腐竹和豆皮样品中,均未检出两种染料。
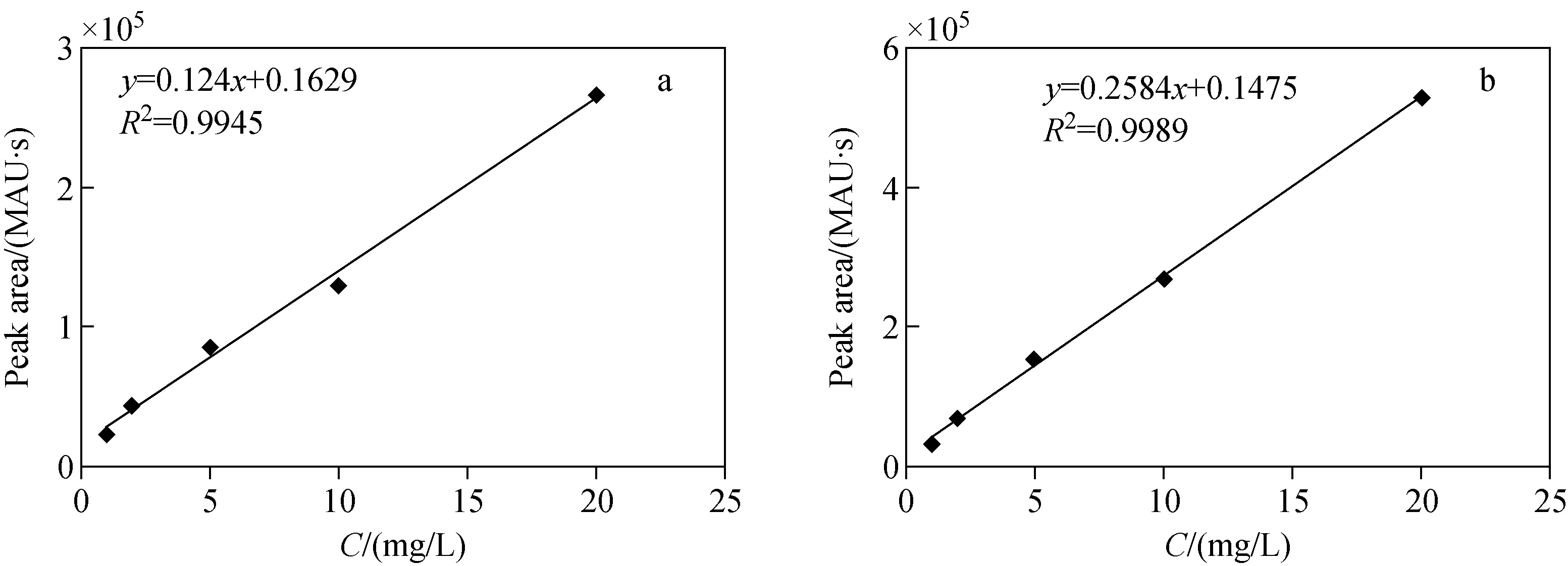
图4 峰面积比值与碱性橙Ⅱ(a)和金胺O(b)浓度的线性关系曲线Fig.4 Corresponding relation curves of peak area vs. the concentrations of Basic Orange Ⅱ (a) and Auramine O (b)
3 结论
本实验采用DART-Q-Orbitrap高分辨质谱联用技术快速定性和定量分析豆制品中可能添加的碱性橙Ⅱ和金胺O。该方法可直接将脱水后的豆制品置于离子化区域内进行定性检测,整个过程只需3 s。与常规的色谱法相比,DART质谱技术可大大减小溶剂和其他复杂基质的干扰,使检测过程更加快速、方便、准确。
在定量分析中,该方法具有良好的精密度与重复性,定量结果虽然比传统的色谱方法略微逊色,但其具有简单、快捷、高效、绿色等优点,可为食品的高通量筛查、快速定性、定量分析以及质量鉴定提供方法参考。
