应用XAD大孔树脂与阴阳离子交换树脂串联技术探究不同腐解时期鱼粪溶解性有机质组分差异
2019-01-19杨淇茹吴胜春李雨桐
杨淇茹 吴胜春 李雨桐
摘要:随着我国渔业的快速发展,高密度网箱、网围精养等集约型养殖模式在我国海洋养殖中被广泛采用。生产过程中,养殖生物所产生的大量排泄物会使周边水体中溶解性有机质(DOM)及氮、磷等营养盐含量增加,造成水体富营养化和藻华的发生等环境问题。利用傅里叶红外光谱仪对浙江省舟山市岱山县桐盘湾某石斑鱼养殖场的鱼粪便中的DOM进行结构分析,得出羟基、甲基、羧基为主要官能团,并对DOM结构构象有重要影响。同时,通过XAD树脂与阴、阳离子交换树脂建立了鱼粪便中DOM亚组分的纯化分离方法,将其按极性分成6种组分,并探究在不同腐解时期鱼粪便DOM各组分变化规律。研究发现,疏水性有机组分在整个腐解阶段所占比例逐渐减少。其中疏水性酸、疏水性碱性有机物是鱼类粪便DOM的主要组成成分,约占组分的55.8%~72.7%;亲水性有机组分随着腐解时间的增加,占比由8.0%提高至28.1%。
关键词:鱼粪;溶解性有机质;红外光谱;组分分离
中图分类号: X171.4 文献标志码: A 文章编号:1002-1302(2019)22-0303-04
近海环境中的天然有机质(NOM)是全球碳循环中的重要组成部分,对水生生态系统结构与功能及全球生物地球化学循环起着至关重要的作用。其中溶解性有机质(DOM)占天然有机质的97.1%,是各种环境介质中的重要化学组分,是生态系统中物质与能量循环的重要物质[1]。DOM在操作层面被定义为能通过0.1~0.7 μm滤膜、且具有不同结构和分子量的有机物,如游离氨基酸、酶、多酚、碳水化合物、有机酸和腐殖质等[2-3]。在水生生态系统中,DOM还含有 —CH2、—CH3、—OH、—COOH、—CO、—NH2等多种官能团,可作为天然的载体或配体与水体中许多生物活性金属元素如铜、汞、镉、锌、铅、钴、铁等产生强烈的相互作用,从而影响它们的氧化还原行为、化学形态、生物有效性和毒性[4]。
在自然条件下,由于DOM浓度较低及大量无机盐离子的存在,其元素分析、官能团分析等大大受阻[5]。尽管有些表征手段可以对DOM的特征进行一定程度的表征,但得到的结果往往不够精确。因此,为了更好地认识DOM与金属离子之间的相互作用机制,对DOM亚组分的分离、提纯和结构表征显得格外重要。近年来,随着DOM组分纯化分离技术的日渐成熟,根据DOM各组分的极性分类,XAD大孔树脂与阴阳离子交换树脂串联分离方法被广泛应用。本试验根据需要对XAD分离技术进行改良和调整,并利用该技术对新鲜鱼粪在水体中腐解时,水体中DOM各亚组分的浓度、所占百分比和主要官能团的变化规律进行讨论,以期为进一步深入研究鱼粪的环境效应及其与重金属离子的络合机制提供参考。
1 材料与方法
1.1 样品采集与处理
供试鱼粪便采自浙江省舟山市岱山县桐盘湾某石斑鱼养殖场(30°19′34.9″N,122°11′11.6″E)。在夏季对1年龄鱼苗进行新鲜粪便收集,为提高收集量,于喂食后在鱼排底部张细纱网收集。将采好的新鲜粪便立刻保存在4 ℃恒温箱内带回实验室进行冷冻干燥,并充分混合均匀,备用。
试验时间与地点:本试验于2018年6—8月在浙江省土壤污染生物修复重点实验室完成。
1.2 试验方法
1.2.1 前期准备 称取已处理好的鱼粪10.0 g,置于5 L烧杯中,加入3 L 0.3% NaCl溶液(模拟海水)模拟腐解试验。在试验开始后0、5、10、20、30、60、90、120 d将鱼粪便分别捞出,进行再次冷冻干燥,待其性状稳定后研磨过100目筛。DOM的提取采用水浸提的方法,将过筛后的鱼粪与超纯水按照质量比为1 ∶ 10的比例进行混合,在黑暗条件下恒温(25 ℃)振荡24 h后高速离心,取上清液过0.45 μm玻璃纤维滤膜,获得的产物即为DOM样品,置于4 ℃冰箱内保存备用。
投入使用前的Amberlite XAD大孔树脂需用2~4 BV的95%甲醇以1~2 BV/hr的速度过柱(须赶走气泡),接着用蒸馏水以1~2 BV/hr的速度淋洗至流出液的溶解性有机碳浓度近乎为0;而阴、阳离子交换树脂则需以60 ℃热水反复清洗至浸洗水不带褐色,且几乎无泡沫为止。水洗后阳离子交换树脂用3 BV浓度为3%~5%的HCl、NaOH溶液以2 BV/hr的流速按照酸-碱-酸的进液次序进行2次处理,阴离子交换树脂的酸碱用量及流速与阳离子交换树脂相对应,用3 BV浓度为3%~5%的NaOH、HCl溶液以2 BV/hr的流速清洗树脂,进液次序为碱-酸-碱。处理完成的树脂置于密封罐中,备用。
采用总有机碳分析仪测定不同腐解时间DOM中溶解性有机碳浓度(TOCDOM),并根据Leenheer的方法[6-7]提取DOM,经冷冻干燥获得各组分固体样本,计算DOM回收率,具体计算公式为
式中:MHOA为疏水酸性物质量;MHOB为疏水碱性物质量;MHON为疏水中性物质量;MHIA为亲水酸性物质量;MHIB为亲水碱性物質量;MHIN为亲水中性物质量;TOCDOM为测得的溶解性有机碳浓度;VDOM为离心液体积。
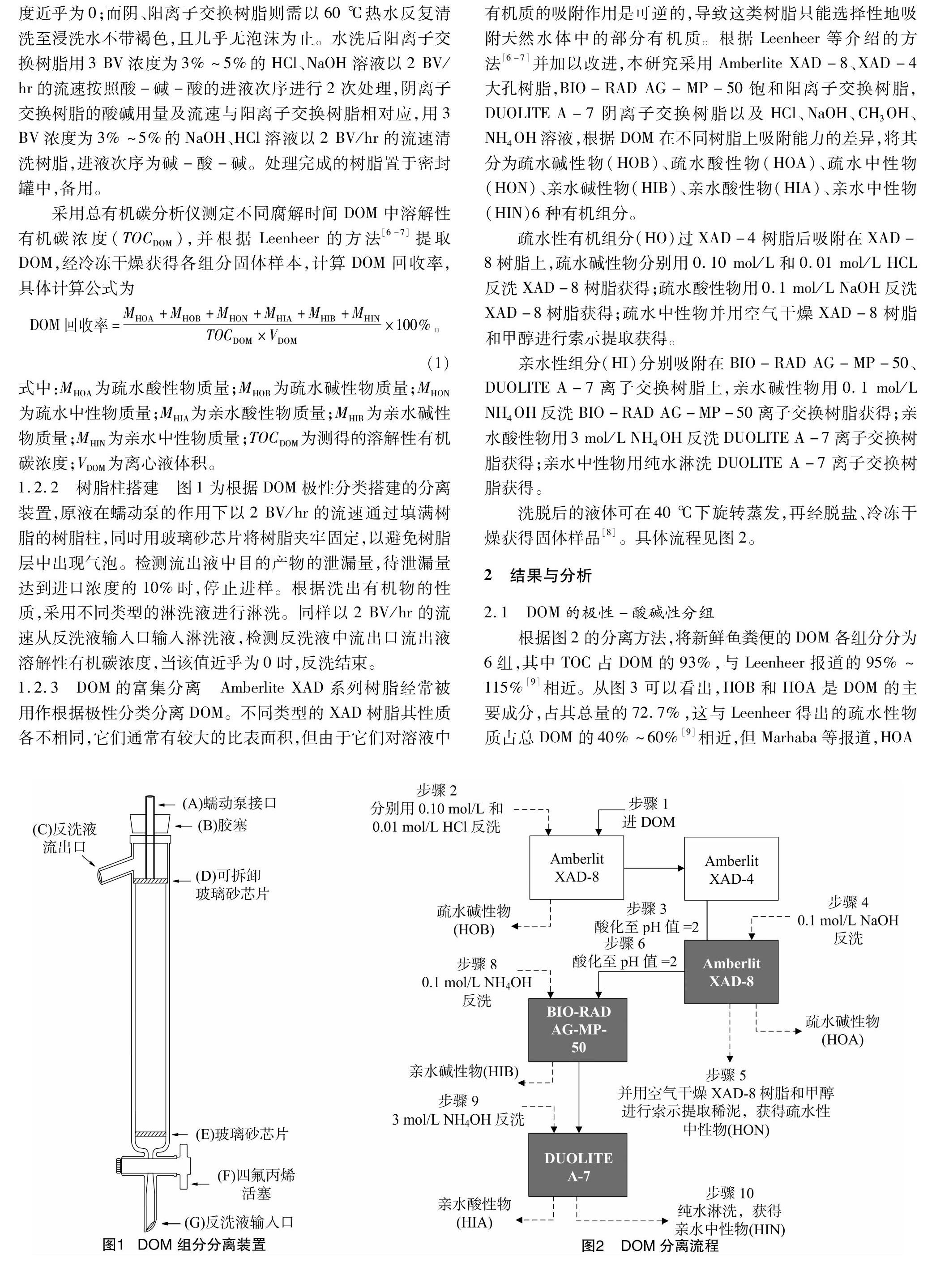
1.2.2 树脂柱搭建 图1为根据DOM极性分类搭建的分离装置,原液在蠕动泵的作用下以2 BV/hr的流速通过填满树脂的树脂柱,同时用玻璃砂芯片将树脂夹牢固定,以避免树脂层中出现气泡。检测流出液中目的产物的泄漏量,待泄漏量达到进口浓度的10%时,停止进样。根据洗出有机物的性质,采用不同类型的淋洗液进行淋洗。同样以2 BV/hr的流速从反洗液输入口输入淋洗液,检测反洗液中流出口流出液溶解性有机碳浓度,当该值近乎为0时,反洗结束。
1.2.3 DOM的富集分离 Amberlite XAD系列树脂经常被用作根据极性分类分离DOM。不同类型的XAD树脂其性质各不相同,它们通常有较大的比表面积,但由于它们对溶液中有机质的吸附作用是可逆的,导致这类树脂只能选择性地吸附天然水体中的部分有机质。根据Leenheer等介绍的方法[6-7]并加以改进,本研究采用Amberlite XAD-8、XAD-4大孔树脂,BIO-RAD AG-MP-50饱和阳离子交换树脂,DUOLITE A-7阴离子交换树脂以及HCl、NaOH、CH3OH、NH4OH溶液,根据DOM在不同树脂上吸附能力的差异,将其分为疏水碱性物(HOB)、疏水酸性物(HOA)、疏水中性物(HON)、亲水碱性物(HIB)、亲水酸性物(HIA)、亲水中性物(HIN)6种有机组分。
疏水性有机组分(HO)过XAD-4树脂后吸附在XAD-8树脂上,疏水碱性物分别用0.10 mol/L和0.01 mol/L HCL反洗XAD-8树脂获得;疏水酸性物用0.1 mol/L NaOH反洗XAD-8树脂获得;疏水中性物并用空气干燥XAD-8树脂和甲醇进行索示提取获得。
亲水性组分(HI)分别吸附在BIO-RAD AG-MP-50、DUOLITE A-7离子交换树脂上,亲水碱性物用0.1 mol/L NH4OH反洗BIO-RAD AG-MP-50离子交换树脂获得;亲水酸性物用3 mol/L NH4OH反洗DUOLITE A-7离子交换树脂获得;亲水中性物用纯水淋洗DUOLITE A-7离子交换树脂获得。
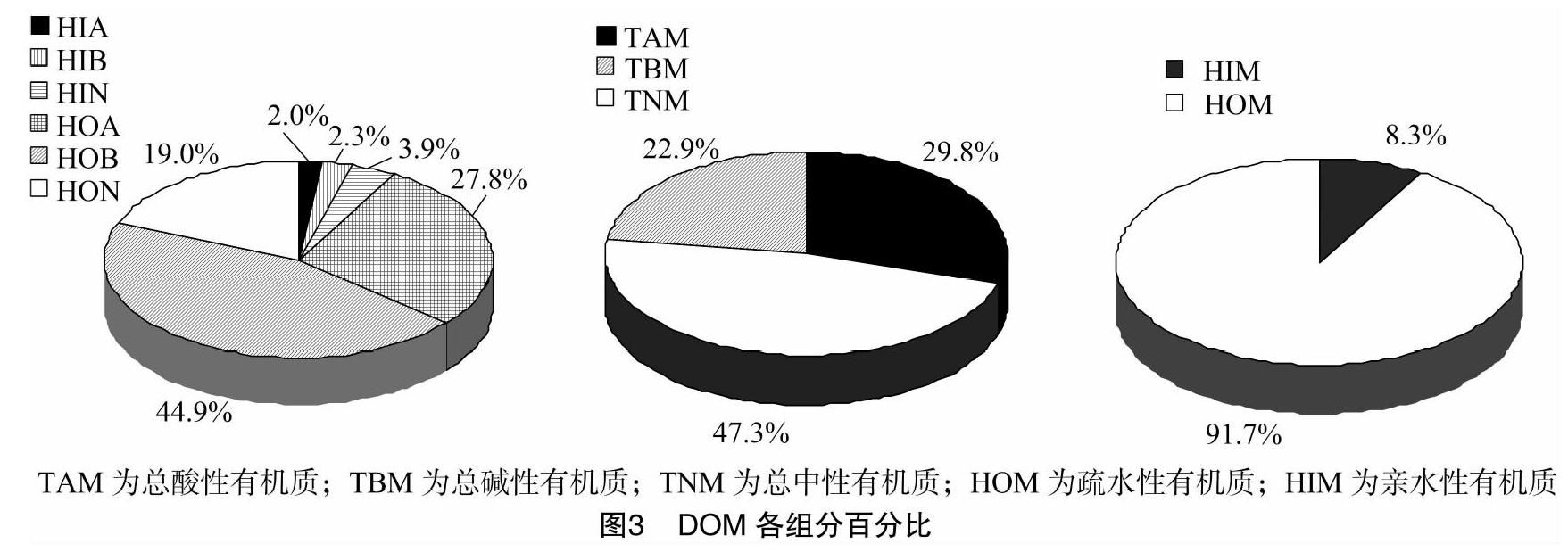
洗脱后的液体可在40 ℃下旋转蒸发,再经脱盐、冷冻干燥获得固体样品[8]。具体流程见图2。
2 结果与分析
2.1 DOM的极性-酸碱性分组
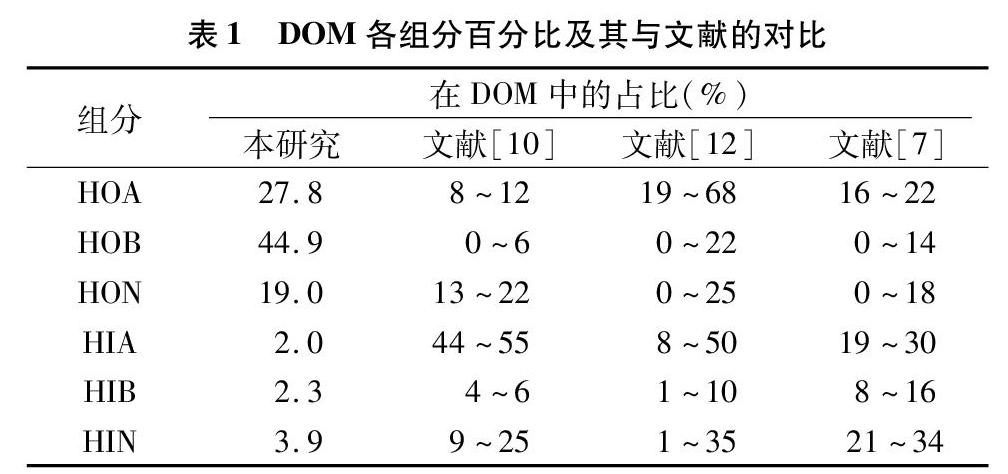
根据图2的分离方法,将新鲜鱼粪便的DOM各组分分为6组,其中TOC占DOM的93%,与Leenheer报道的95%~115%[9]相近。从图3可以看出,HOB和HOA是DOM的主要成分,占其总量的72.7%,这与Leenheer得出的疏水性物质占总DOM的40%~60%[9]相近,但Marhaba等报道,HOA的含量不会超过12%[10]。HON含量为19%;HIM总含量为8.3%, 与Swietlik报道的该值不会超过15%[11]相吻合。 与已有文献中的试验结果[7,10,12]相比,不同有机质组分占比不同(表1)。
2.2 DOM官能团组成及其光谱学特征
DOM是含有低分子质量化合物(游离氨基酸和糖)和酶、氨基糖复合物、多酚和HS的混合物,细微的条件改变均可导致其结构发生变化,采用传统的化学分析方法容易在测定过程中改变其原有性质,因此DOM成分的确定是极其困难的。
根据Sierra等对DOM红外光谱的解析发现[13-15],从图4可以看出,本研究中鱼粪DOM含氧官能团含量相对较高,峰值出现在波长3 400 cm-1处,O—H伸缩振动,存在键合和非键合羟基;峰值出现在3 000~2 850 cm-1处,C—H伸缩振动,可存在脂肪族亚甲基;峰值出现在1 600~1 550 cm-1处的COO—反对称伸缩及1 410 cm-1处的COO—对称伸缩说明羧酸占比较高;峰值出现在1 000、680~610 cm-1处,表明存在C—O的伸缩振动及S—O伸缩振动,说明可能有无机化合物合物的碳酸盐矿物和硫酸盐。说明未经腐解的DOM各官能团显性明显,随腐解时间的增长各基团含量减少并于 30 d 后趋于稳定。
综上,DOM上的羟基、甲基、羧基等官能团的相互作用可对DOM构象产生影响。当这些官能团均带有负电荷时,因其相互排斥,使得DOM结构相对疏松[16-17]。因此,某些环境因素的改变(如pH值、温度等),若对官能团的电荷产生较大影响,将改变官能团之间的相互作用,进而改变DOM的微观构象。
2.3 不同腐解时期DOM各组分变化
由式(1)可计算出不同腐解时期DOM溶解性有机碳浓度,由表2可知,由于腐解初期鱼粪便有机物质向水体扩散,TOCDOM随着腐解时间的增加而逐渐减少并于60 d后趋于平稳。同时,TOCDOM的降低,在一定程度上增大了DOM的回收误差。
由图5可知,疏水性有机物在整个腐解阶段始终占有较大比例,为69.8%~91.7%。其中,HOA在腐解前5 d约占溶解性有机质总质量(MDOM)30%左右,随着腐解深入,在第10天、第20天发生突跃,MHOA/MDOM最高可达46%,随后趋于平稳。HOB在腐解前5 d所占份额最多,约为44%。其余时期基本稳定,数值在30%左右。HON受腐解时间影响并不明显,占各个时期MDOM的20%左右。由图6可知,亲水性有机物各组分在整个腐解期间浓度变化相差不大,并没有因鱼粪中有机物质向水中释放,使亲水性有机物浓度降低,也正因为此原因,亲水性有机物质量占MDOM的比例会随着腐解的进行逐渐升高,最高可达28.1%。在整个腐解过程中亲水性有机物各组分占比表现为MHIN>MHIB>MHIA。
3 结论
近海网箱养殖鱼类粪便DOM主要由羧基、羟基、甲基等官能团组成,环境因素的改变可影响这些官能团的相互作用,以致DOM的微观构象发生变化。
利用XAD树脂和阴、阳离子交换树脂串联技术,对近海網箱养殖鱼类粪便DOM加以富集分离,分为HOB、HOA、HON、HIA、HIB和HIN 6种有机组分,其中疏水性碱、疏水性酸是主要的组成成分,约占组分的72.7%。
随着腐解的进行,疏水性有机物在DOM中的占比有所下降但始终占有较大份额,但HOA在腐解的10~20 d产出增大,随后趋于平稳;亲水性有机物在DOM中的占比则从8.0%升至28.1%,并且整个过程始终是MHIN>MHIB>MHIA。
参考文献:
[1]Frimmel F H,Abbt‐Braun G. Dissolved organic matter (DOM) in natural environmentse[M]//Biophysico-chemical processes involving natural nonliving organic matter in environmental systems,2009.
[2]Jones M N,Bryan N D. Colloidal properties of humic substances[J]. Advances in Colloid & Interface Science,1998,78(1):1-48.
[3]Post W M,Peng T H,Emanuel W R,et al. The global carbon cycle[J]. American Scientist,1990,78(1):310-326.
[4]Santos P S M,Otero M,Duarte R M B O,et al. Spectroscopic characterization of dissolved organic matter isolated from rainwater[J]. Chemosphere,2009,74(8):1053-1061.
[5]Baker A,Spencer R G M. Characterization of dissolved organic matter from source to sea using fluorescence and absorbance spectroscopy[J]. Science of the Total Environment,2004,333(1/2/3):217-232.
[6]Leenheer J A,Huffman E W D.Classification of organic solutes in water by using macroreticular resin[J]Journal of Research of the US Geological Survey,1976,4(6):737-751.
[7]Chefetz B,Hader Y,Chen Y. Dissolved organic carbon fractions formed during composting of municipal solid waste:properties and significance[J]. Clean-Soil Air Water,2010,26:172-179.
[8]Swietlik J,Dabrowska A,Raczyk-stanislawiak U,et al. Reactivity of natural organic matter fractions with chlorine dioxide and ozone[J]. Water Res,2004,38:547-58.
[9]Leenheer J A. Comprehensive approach to preparative isolation and fractionation of dissolved organic carbon from natural waters and wastewaters[J]. Environmental Science & Technology,1981,15:578.
[10]Marhaba T F,Van D,Lippincott R L. Changes in NOM fractionation through treatment:a comparison of ozonation and chlorination[J]. Ozone-Science & Engineering,2000,22(3):249-266.
[11]S′wietlik J,Dbrowska A,Raczyk-stanisawiak U,et al. Reactivity of natural organic matter fractions with chlorine dioxide and ozone[J]. Water Research,2004,38:547-558.
[12]Korshin G V,Benjamin M M,Sletten R S. Adsorption of natural organic matter (NOM) on Iron oxide:Effects on nom composition and formation of organo-halide compounds during chlorination[J]. Water Research,1997,31(7):1643-1650.
[13]Sierra M M,Giovanela M,Parlanti E,et al. Structural description of humic substances from subtropical coastal environments using elemental analysis,FT-IR and C-13-solid state NMR data[J]. Journal of Coastal Research,2005,21(42):370-382.
[14]Huo S L,Xi B D,Yu H C,et al. Characteristics of dissolved organic matter (DOM) in leachate with different landfill ages[J]. Journal of Evivronmental Sciences,2008(4):492-498.
[15]Kim H C,Yu M J,Han I. Multi-method study of the characteristic chemical nature of aquatic humic substances isolated from the Han River,Korea[J]. Applied Geochemistry,2006,21:1226-1239.
[16]吳济舟. 溶解性有机质分组及各组分对芘的生物有效性及其吸附解吸的影响研究[D]. 天津:南开大学,2012.
[17]张耀玲. 近海环境中天然有机质的分离与表征[D]. 上海:华东师范大学,2013.
