活动期克罗恩病IFX维持治疗期间发生失应答的相关危险因素研究
2018-12-17索日娜史伟东
索日娜 刘 洁 史伟东 李 凤
炎症性肠病是慢性非特异性肠道炎症疾病,临床以克罗恩病、溃疡性结肠炎最常见。据报道[1],近年来克罗恩病(Crohn disease, CD)发病率呈升高趋势,引起关注。CD的病因和发病机制尚不明确,目前认为与遗传因素、环境因素、免疫反应等有关[2]。英夫利西单克隆抗体(infliximab, IFX)是首个被批准用于临床治疗特发性炎症性肠病的生物制剂,对糖皮质激素、免疫抑制剂治疗无效或无法耐受的患者,具有良好效用[3]。有报道称[4],IFX虽可使多数克罗恩病患者获得诱导缓解和维持缓解,但部分患者仍存在继发性失应答的情况。继发性失应答是指CD患者经初始诱导治疗达临床缓解后在维持治疗阶段再次复发CD相关症状。目前,继发性失应答的确切原因并不明确,目前主要认为是血清中IFX有效浓度不足引起[5],继发性失应答的相关影响因素分析也较为缺乏。本研究以本院收治的90例CD患者为例,探讨活动期CD患者发生IFX继发性失应答的危险因素,现报告如下。
资料与方法
一、一般资料
1. 纳入标准
①符合《炎症性肠病诊断与治疗的共识意见》[6]中CD诊断标准;②使用IFX治疗(治疗次数≥4次)的门诊或住院患者;③临床资料完善。
2. 排除标准
①伴中重度心力衰竭者;②合并神经系统脱髓鞘病变者;③伴肝炎、巨细胞病毒感染等其他感染疾病者;④入组前3个月内有过疫苗接种史者;⑤对IFX过敏者;⑦精神病患者;⑧妊娠或哺乳期妇女。
3. 研究对象
选取本院2015年6月至2018年6月收治的符合上述纳入与排除标准的90例CD患者。其中,男61例,女29例;年龄25 ~ 62岁,平均(36.14±5.21)岁。
二、方法
1. 治疗方案
所有患者均于第0、2、6周时静脉滴注IFX(西安杨森制药有限公司生产,批准文号:注册证号S20120012,规格:100 mg/支),5 mg/kg,作为诱导治疗;后每间隔8周予相同剂量的IFX进行维持治疗。每次静脉滴注IFX前肌内注射25 mg盐酸异丙嗪预防过敏。
2. 实验室指标的检测
所有患者入组后均常规测定体质量指数[(体重(kg)/身高(m)2],采集5 mL肘静脉血检测C反应蛋白、血红蛋白、白蛋白;另于第4次静脉滴注IFX前2 h内再次采集5 mL肘静脉血,检测血清C反应蛋白、血红蛋白、白蛋白及IFX谷浓度。其中C反应蛋白采用散射比浊法测定,IFX谷浓度采用ELISA法测定,血红蛋白与白蛋白采用比色法测定。
3. 继发性失应答的定义与分组
从第4次静脉滴注IFX开始,每间隔8周采用简化克罗恩病活动指数评分法对患者进行1次评估,至2018年7月,以患者停用IFX或发生继发性失应答作为随访终点。将符合以下任一条件的患者纳入失应答组:①需通过增加IFX剂量和(或)缩短IFX输注间隔时间以维持缓解;②加用免疫抑制剂以维持缓解;③因IFX无法维持缓解而换用其他药物治疗;④IFX诱导缓解后疾病再次活动(经内镜证实或简化克罗恩病活动指数评分 > 4分)。随访结束仍应用IFX治疗的CD患者纳入持续应答组。
4. 研究方法
比较失应答组与持续应答组的性别、发病年龄、病程、吸烟、病变部位、阑尾切除史、体质量指数、C反应蛋白、血红蛋白、白蛋白水平。
三、统计方法
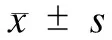
结 果
一、治疗结果
90例患者中,3例(3.33%)患者治疗初始无应答,其余87例(96.67%)患者均应答,其中70例(80.46%)至随访结束持续应答,纳入持续应答组,另外17例(19.54%)发生继发性失应答,纳入失应答组。
二、失应答组与持续应答组的临床资料比较
失应答组与持续应答组性别、发病年龄、病程、体质量指数、吸烟、病变部位、阑尾切除史、治疗前C反应蛋白、治疗前血红蛋白、第4次注射IFX前的血红蛋白、治疗前白蛋白、第4次注射IFX前的白蛋白水平的差异均未见统计学意义(P> 0.05);失应答组第4次注射IFX前的C反应蛋白≥3 mg/L患者的占比与第4次注射IFX前的IFX谷浓度≤3.5 μg/mL患者的占比明显高于持续应答组,差异有统计学意义(P< 0.05),见表1。
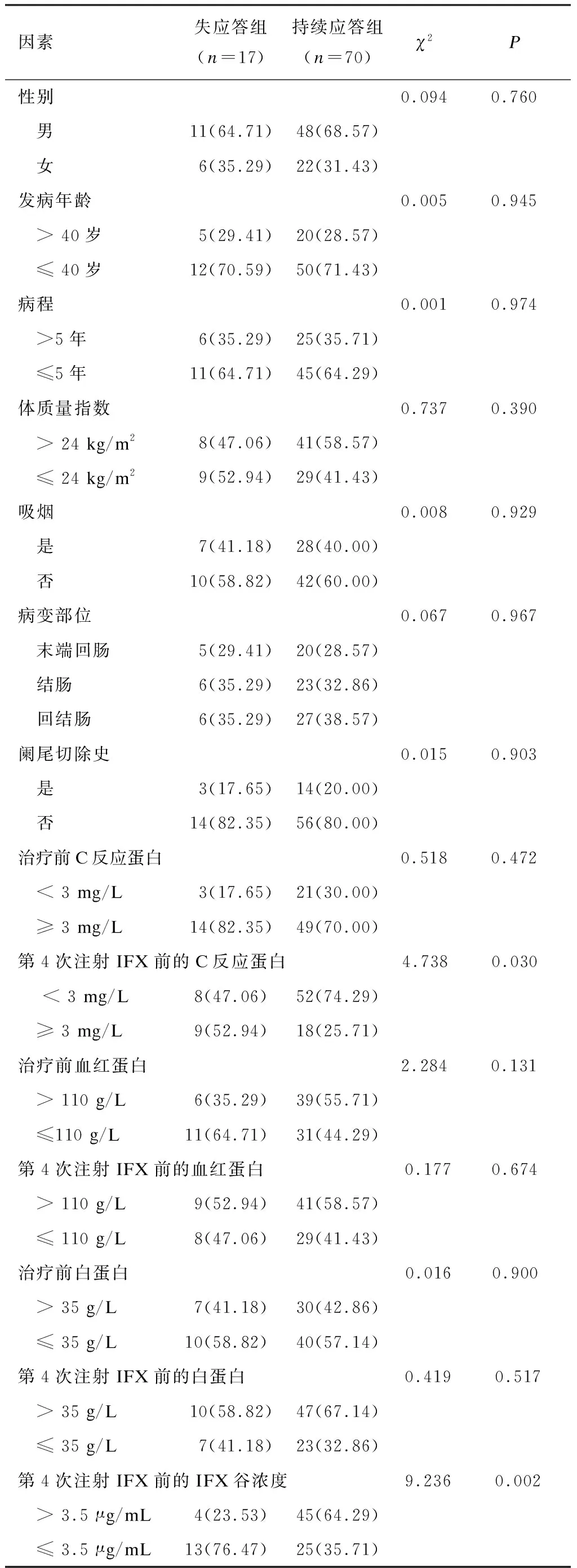
表1 失应答组与持续应答组的临床资料比较 [n(%)]
三、继发性失应答的Logistic回归多因素分析
将单因素分析具有统计学意义的自变量纳入Logistic回归多因素分析,最终第4次注射IFX前的C反应蛋白与第4次注射IFX前的IFX谷浓度入选,赋值:①第4次注射IFX前的IFX谷浓度:≥3 mg/L=1, < 3 mg/L=0;②第4次注射IFX前的IFX谷浓度:≤3.5 μg/mL=1,> 3.5 μg/mL=0。多因素Logistic回归分析显示,第4次注射IFX前的C反应蛋白与第4次注射IFX前的IFX谷浓度为活动期CD患者IFX维持治疗期间发生继发性失应答的独立危险因素(P< 0.05),见表2。
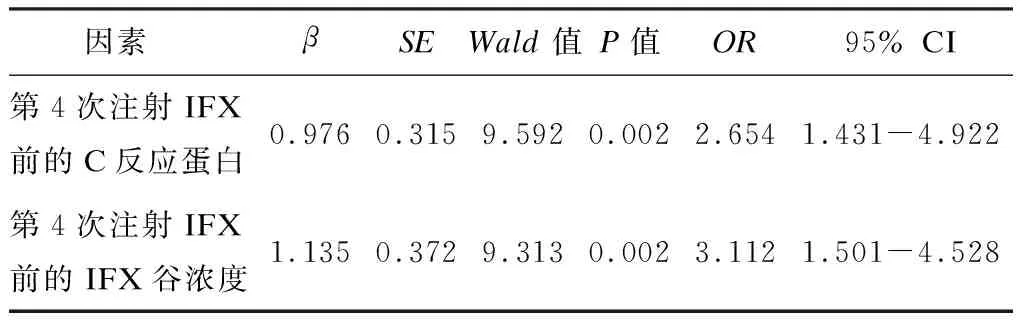
表2 继发性失应答的多因素Logistic回归分析
讨 论
CD的治疗药物包括糖皮质激素、免疫抑制剂、氨基水杨酸制剂、IFX等,其中IFX是一种人鼠嵌合体IgG1单克隆抗体,在糖皮质激素和免疫抑制剂治疗无效、无法耐受激素、重度难治性CD患者中,CD的临床应用发挥了巨大作用,为CD的临床治疗取得了阶梯性进步,已成为CD的一线治疗药物[7]。但其中出现的继发性失应答问题也逐渐引起重视,成为当前主要研究方向之一[8]。
本研究90例CD患者中,87例初始应答,在后续的随访过程中,17例(19.54%)于初始应答后出现继发性失应答,继发性失应答率与相关报道相符。单因素分析结果发现,失应答组与持续应答组仅第4次注射IFX前的C反应蛋白与第4次注射IFX前的IFX谷浓度存在差异,并最终经多因素Logistic回归分析证实上述2个因素均为活动期CD患者IFX维持治疗期间发生失应答分危险因素,成为本研究的关注重点。
IFX维持治疗阶段药物浓度的监测早已引起临床重视,多项证据表明[9-11],失应答患者的血清IFX浓度明显偏低。谷浓度指下次用药前药物浓度的最低点,也称最低有效药物浓度。研究显示[12],低于检测下限的CD患者1年内失应答的风险明显更高。目前认为[13],当IFX血液浓度维持在3 μg/mL以上才可持续有效控制疾病。也有研究发现[14],IFX治疗CD患者第14周的谷浓度大于>5.1 μg/mL预示持续临床应答良好。本研究中所选取的临界点为3.5 μg/mL,是失应答组与持续应答组患者的均值,可能会受到失应答组患者较少的因素影响,有待进一步确定。虽然较高血清IFX水平的CD患者总体上可获得更好的预后,但临床上仍有部分患者血清中IFX药物浓度低于治疗水平,但仍可维持临床缓解,与本研究结论不一致。笔者认为,这一问题的原因在于检测的时点不同,维持治疗前期间IFX浓度的检测意义可能不如在维持治疗之前的检测意义大,具体原因可能仍需进一步讨论分析。
C反应蛋白为机体受到炎性刺激时由肝脏合成的一种时相蛋白,可反映体内炎性反应程度,是CD疾病活动度的重要生物学标志物。张玲的研究认为[15],感染或其他疾病引起的炎性反应是CD患者继发性失应答的主要原因之一。IFX主要通过特异性结合肿瘤坏死因子α、白细胞介素-6等细胞因子来抑制免疫损伤和炎性反应,促进肠道黏膜修复[16]。而C反应蛋白水平的升高往往提示体内炎性反应的存在,可能会对肿瘤坏死因子α、白细胞介素-6水平造成影响从而增加继发性失应答的风险。也有证据表明[17],应用IFX前,C反应蛋白水平>5 mg/L的患者的IFX应答率可达76%,而C反应蛋白正常患者的IFX应答率仅46%左右,证实治疗前C反应蛋白水平对患者原发性无应答有一定影响。本研究中,继发性失应答与持续应答组治疗前的C反应蛋白水平并无明显差异,第4次注射IFX前的C反应蛋白的差异才出现统计学意义,提示对于继发性失应答患者而言,治疗后C反应蛋白水平的变化才是主要影响因素。刘爱玲的研究认为[18],维持治疗前C反应蛋白较用药前降低60%以上可作为CD混着持续应答的预测指标,警示C反应蛋白治疗前后的变化情况对继发性失应答的影响更大。有研究发现[19],体质量指数对IFX继发性失应答的发生也有一定影响,认为肥胖患者脂肪细胞高表达TNF-α会对IFX应答造成干扰,是继发性失应答的危险因素之一。本研究中,失应答组与持续应答组的体质量指数的差异并无统计学意义,推测与本研究中患者体质量指数较为接近,并未出现体质量指数>30 kg/m2的肥胖患者有关。但临床还是建议CD患者积极控制体质量指数,将其维持在正常范围内或将受益,值得参考[20]。
综上所述,第4次注射IFX前的IFX谷浓度≤3.5 μg/mL及C反应蛋白≥3 mg/L是活动期CD患者IFX发生继发性失应答的危险因素,临床应重视CD患者诱导治疗后、维持治疗前相关指标的检测。
