农药残留分析实时分析新技术研究进展
2018-12-05潘兴鲁董丰收吴小虎刘新刚徐军郑永权
潘兴鲁 董丰收 吴小虎 刘新刚 徐军 郑永权


摘要
敞开式离子化质谱(ambient mass spectrometry, AMS)技术由于实时、原位分析、不需要复杂样品处理过程等特点,已经成为质谱研究领域的一个研究热点。实时直接分析(direct analysis in real time, DART)作为一种典型的敞开式离子化质谱技术,自2005年报道以来,已经被广泛应用到各个领域不同样品的分析过程中。本文主要从DART发展历程、构造及原理以及在农药残留分析领域应用进展进行综述,并对其发展进行了展望。
关键词
实时直接分析; 质谱; 农药残留
中图分类号:
S 481.8
文献标识码: A
DOI: 10.16688/j.zwbh.2018302
Research advances in direct analysis in real time of pesticide residues
PAN Xinglu, DONG Fengshou, WU Xiaohu, LIU Xingang, XU Jun, ZHENG Yongquan
(Institute of Plant Protection, Chinese Academy of Agricultural Sciences,Laboratory of Quality &
Safety Risk Assessment for Agri-products Biohazards (Beijing), Ministry of Agriculture and
Rural Affairs,Key Laboratory of Control of Biological Hazard Factors (Plant Origin) for Agri-products
Quality and Safety, Ministry of Agriculture and Rural Affairs, Beijing 100193, China)
Abstract
Ambient ionization mass spectrometry (AMS) has become a hot area in the field of mass spectrometry due to the advantages of real-time and in situ analysis, and simple sample preparation. Direct analysis in real time (DART) as a typical AMS has been widely applied in the analysis procedure in every field since the first report in 2005. In this paper, the development course, structure and mechanism of the DART, the application of DART-MS in the field of pesticide residue analysis were briefly summarized. Finally, the development tendency of DART-MS was prospected.
Key words
direct analysis in real time; MS; pesticide residue
質谱技术由于其高灵敏度、高准确度以及高通量等特点,已被广泛应用到各个分析领域。作为质谱重要组件之一,离子源正朝着通用性更强、灵敏度更高、耐用性更好的方向不断发展[1]。从最初的电子轰击到现在的喷雾电离,质谱实现了从有机小分子到生物大分子分析的飞跃[2]。但是,复杂的样品前处理过程(提取、浓缩、净化)往往会消耗大量的时间,严重制约着质谱在实时、高通量分析中的应用。
敞开式离子化质谱的出现为实时、原位分析提供了可能。敞开式离子化质谱是一种在大气压环境下,无需样品前处理直接完成样品的离子化的新型质谱技术[3]。目前已经报道了30多种敞开式离子化质谱技术,其中最为广泛应用的就是实时直接分析技术(direct analysis in real time, DART)[4-5]和解吸电喷雾电离技术(desorption electrospray ionization, DESI)。本文主要综述了DART发展历程、构造及原理以及在农药残留分析领域的应用。
1 DART发展历程
2001年初,为了拓展可调谐能量电子单色仪(tunable energy electron monochromator, TEEM)的使用范围[6],Laramee和Cody在美国JEOL公司实验室研究了与TEEM具有类似功能的常压热电子源的潜在应用价值,试图开发出一种安全的放射性材料替代品,用于化学试剂监测和有毒工业化学传感器制造,如:镍-63或镅-241。
几种相应的方案设计和离子光学模型应运而生,在大气压下利用氮气和氦气放电提供电子是最早提出的概念之一。基于这一理念,在2013年实现了常压热电子源与飞行时间质谱的联用。对所产生的离子检验结果显示,电子激发态的氦或振动激发态的氮是产生样品离子化的主要原因。试验发现,这种电子源对远离实验室的痕量级蒸汽具有非常高的灵敏度,例如施工工地打开的胶水产生的气体;对化学试剂如丙酮、乙酸、乙腈、吡啶和硝酸同样具有高灵敏度,例如在一个房间打开化学试剂瓶盖,几百毫秒内就能在另一个房间检测到。由于具有多种样品采集功能,这种大气压电子源能够与质谱或离子迁移光谱联用。随后该成果受到美国军方的重视,主要在佛罗里达州埃奇伍德化学生物中心用于化学战剂的现场测试[7]。
在得到初步的试验结果之后,发明者决定推迟发表结果,并在分别位于马萨诸塞州的JEOL公司实验室和佛罗里达州埃奇伍德化学生物中心两个实验室同时独立开展重复性验证试验。DART成功地对数百种化学物质进行了样品采集测定,包括化学战剂、药物制剂、代谢物、氨基酸、多肽、低聚糖、合成有机物、有机金属化合物、毒品、爆炸物、工业有毒材料。这些化合物来源于不同的物质表面,包括多孔混凝土、沥青、人体皮肤、货币、航空公司登机证、名片、水果、蔬菜、香料、饮料、体液、园艺植物叶片、鸡尾酒杯、普通实验室设备和服装。2005年DART离子化技术文章在Analytical Chemistry杂志发表,同年JEOL公司的DART商品化设备问世。JEOL公司的AccuTOF DART问世以来,被用于各种小分子样品的分析檢测,具有分辨率高、分析速度快、样品损耗低、绿色环保等优点,可以轻松实现高通量检测和样品筛选[7]。
自2005年DART离子化技术发表以来,每年关于DART-MS的出版文章数量快速增加(图1)。在Web of Science上以DART-MS为关键词检索,从2005年到2017年共发表了623篇文章,到2018年7月共发表了660篇文章。
图1 2005-2018年发表的DART-MS研究论文数量
Fig.1 Number of publications per year about
DART-MS from 2005 to 2018
2 DART构造及原理
2.1 DART构造
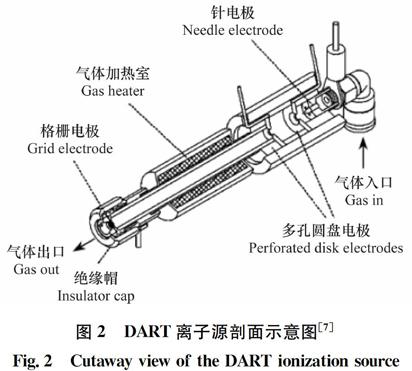
DART源主要包括一个封闭的离子源(初级离子源)和一个开放的反应区[8]。图2是DART离子源的剖面图。
图2 DART离子源剖面示意图[7]
Fig.2 Cutaway view of the DART ionization source
首先,气体由进气口进入放电室,放电室由一个针电极和一个多孔圆盘电极组成,针电极能够提供1~5 kV的高压,高压激发辉光放电,分别使氦气原子和氮气分子变为电子激发态和振动激发态,由此在腔室内形成50~60℃的离子、电子和激发态气体组成的等离子流体,多孔圆盘电极能够除去等离子流体中的电子。低温等离子流体进入第二个气体加热腔室,可以将等离子流体加热到50~100℃[9]。加热后的等离子流体经过格栅电极过滤掉极性相反的离子,防止离子重组造成信号丢失。位于离子源出口的陶瓷绝缘帽能够避免格栅电极对样品和实验人员产生伤害。DART离子源与质谱进样口通过绝缘陶瓷转接口相连,转接口连有一个真空泵,用于抽去大量的中性粒子避免中性物质污染质谱,同时可以减小DART气流对质谱真空度的影响。DART离子源与质谱主要有两种连接模式:一是无角度模式,是指气流朝向质谱接口;二是反射模式,是指通过样品表面反射,将产生的离子进入质谱检测。
2.2 DART工作原理
从DART离子源出来的等离子流体进一步与环境中的介质作用或者与分析物作用,将分析物从基质表面进行解吸附离子化[10]。DART离子源能形成正离子和负离子,形成离子的形式主要取决于分析物的理化性质,包括气相碱度(GB)或气相酸度(GA)、电离能(IE)、电子亲和能(EA)以及与其他化合物形成加和离子的能力[11]。
2.2.1 正离子电离模式
正离子模式下,最有可能发生的反应包括彭宁离子化、质子转移和电荷转移。彭宁离子化是指当一种气体的亚稳态原子同另一种气体的原子和分子碰撞时,只要前者的激发能大于后者的电离能,后者就能被电离,前者返回基态。惰性气体的亚稳态原子具有较大的激发能,且惰性气体的激发能顺序为He*>Ne*>Ar*>Kr*[12]。相对于其他惰性气体,处于电子激发态的氦原子(23S)具有最高的内能(19.8 eV),所以DART离子源一般采用氦气作为离子化气体。绝大多数有机物的离子化能约为10 eV,稍小于激发态的氦原子内能(19.8 eV),所以能够使有机物分子电离而不产生很多碎片离子[13-15]。
He+能量→He*(1)
He*+M→M+·+e-+He(2)
环境中的少量水分子导致了离子化过程中的另一个反应——质子转移。水分子的离子化能约为12.6 eV,所以激发态的氦原子能够高效地将水分子电离,生成水分子阳离子,水分子阳离子进一步与其他水分子作用,形成水分子簇阳离子[(H2O)nH]+。当分析物(M)的质子亲合能大于水分子质子亲合能时,就会发生质子转移,产生[M+H+][12-16]。
He*+H2O→H2O+·+e-+He(3)
H2O+·+H2O→H3O++OH·(4)
H3O++nH2O→[(H2O)n+H]+(5)
M+[(H2O)n+H]+→[M+H]++nH2O(6)
电荷交换是形成分子离子峰的另一种途径。氧分子的电离能约为12.07 eV,所以激发态的氦气使空气中的氧分子电离生成氧正离子自由基,氧正离子自由基夺取分析物的电子,形成分析物阳离子[10, 14]。
He*+O2→O+·2+e-+He(7)
O+·2+M→M+·+O2(8)
正离子模式下,彭宁离子化和电荷交换能生成M+·,而质子转移能够形成[M+H]+,在DART离子源中M+·和[M+H]+可能会同时存在,其比例并非取决于空气中水分含量或He*与样品之间的距离,而主要受化合物的气相酸碱度和电离能影响,较低的电离能容易产生M+·,而高气相碱度容易生成[M+H]+[8]。但是,当这两种离子同时出现在质谱上时,就会对元素的同位素峰产生干扰。针对这一问题,部分研究采用氩气替代氦气作为离子化气体,氩气的激发态内能为11.55 eV(3P2)和11.72 eV(3P0),不能使水分子(IE = 12.65 eV)电离,所以能够避免产生[M+H]+离子干扰,但其灵敏度也随之下降[17-18]。
在中等极性分析物的DART质谱图中,经常能观察到铵离子[M+NH4]+产生。铵离子可能是源于样品中普遍存在的杂质,或者是实验室微量的氨气。试验过程中在电离区准备一瓶10%~25%的氨水能够增加[M+NH4]+的产生。
M+[NH4]+→[M+NH4]+(9)
2.2.2 负离子电离模式
负离子模式下,激发态的氦气能够与大气中氮气发生彭宁离子化,产生热电子。大气中的氧气捕获热电子形成氧负离子,氧负离子与分析物反应生成分析物与氧气的加合负离子;或者形成的加合负离子解离形成分析物负离子。
He*+N2→N+·2+e-+He(10)
O2+e-→O-·2(11)
O-·2+M→[M+O2]-·(12)
[M+O2]-·→M-·+O2(13)
根据分析物的性质,分析物可以直接捕获电子,或者解离后捕获电子形成分析物负离子。同时,也可以通过脱质子作用或者与负离子加合形成分析物负离子[16,19]。
M+e-→M-·(14)
MX+e-→M-+X·(15)
MH→[M-H]-+H+(16)
M+X-→[M+X]-(17)
另外,环境大气中产生的离子包括O-·2、NO-·2、CO-·3以及痕量有机溶剂产生的CN-、Cl-、OH-都有可能与分析物结合形成加合物负离子[20]。
2.3 影响DART离子化的因素
2.3.1 掺杂剂影响DART离子化
试验过程中经常会发现分析物DART质谱信号会随着环境变化产生明显的改变。例如样品表面残留物产生的蒸汽或实验室化学试剂蒸汽都会显著影响DART质谱信号[21]。DART负离子对检测硝酸甘油等爆炸物具有高灵敏度,即使对于蒸气压极低的化合物也有较高的灵敏度[16]。试验发现,当在DART旁边放一瓶敞口的浓度为0.1%的三氟乙酸(H-TFA),就可以检测到爆炸物与三氟乙酸的加合离子[M+TFA]-。同样,二氯甲烷也能使分析物产生[M+Cl]-,以此提高DART对爆炸物检测的灵敏度[22]。另外,氨水能够促进分析物形成加合离子[M+NH4]+。例如含羰基或羟基化合物、羰基酯和有机过氧化物等较容易形成[M+NH4]+,所以在DART离子源旁放置一瓶氨水,能够使信号提高100倍[23-24]。通常,人们会在反应区引入合适的掺杂剂来降低分析物的检测限。但是,残留的溶剂蒸汽和一些无关的气体可能对DART质谱产生信号干扰。
2.3.2 分析物分子量和气体影响离子化
由于DART需要将分析物从样品表面解吸电离,所以DART通常用来检测质荷比在50到1 200范围内的小分子和中型分子。现在商品化的DART工作气体温度可以从50℃升至500℃,要解吸电离高分子量的分析物必须较高的温度,可用于DART检测的分析物分子量上限主要取决于分析物的挥发性和热稳定性。对于挥发性强的化合物,DART可以检测到m/z高达3 500的气体离子。工作气体温度对分析物质谱信号具有决定作用,对于大多数分析物,都有一个起始温度,当小于这个起始温度时,就不会观察到质谱信号;但是,温度过高分析物容易挥发和损失。较低的温度适合检测挥发性有机化合物,较高的温度适合检测高沸点化合物和长链糖类。另外,工作气体流速也影响DART離子化,流速过低会造成激发态的气体数量少,分析物离子化效率低;流速过高会造成样品损失,进入质谱的分析物数量减少。
因此,在实际试验过程中,需要对影响DART离子化效率的参数进行详细的优化,从而获得最优的质谱响应信号。
3 DART在农药残留分析中的研究进展
农药是目前最有效的病虫害防控物质,由于农药长期使用,其在环境介质中释放和扩散势必会造成环境污染和农药残留问题。同时,随着食品安全问题不断曝光,食品和环境中的农药残留已经成为社会关注的焦点。质谱技术由于其高灵敏度、高准确度以及高通量等特点,已经被广泛应用到农药残留分析中。其中液相色谱质谱联用(LC-MS)和气相色谱质谱联用(GC-MS)是该领域最主要的技术手段[25-26]。然而LC-MS和GC-MS均需要专业的仪器操作与仪器维护技术;同时,由于各种复杂的化学试剂以及繁琐的前处理过程,其缺点是耗时长、溶剂消耗大,不适合快速实时高通量检测分析;另外GC-MS分析技术还要求分析物具有良好的挥发性和热稳定性。DART-MS作为一种高性能的敞开式直接离子化质谱技术,能够满足对样品无损、快速、环保、原位分析的高通量需求,DART-MS既可以对原始或者经简单处理的样品直接检测分析,也可以与复杂的前处理过程相结合。目前,DART-MS已经逐渐成为农药残留分析的热点研究技术。
3.1 DART-MS结合无前处理或者简单的样品处理
由于DART能够直接检测样品而几乎不要任何前处理,所以DART-MS被认为是一种理想的高通量检测方法。一些低黏度的液体(如水和饮料)和固体样品(粮食、水果)可以用于直接分析检测。Yong等利用DART-QqQ法建立了红葡萄酒和白葡萄酒中31种农药的快速直接检测方法,无需样品制备和色谱分离,在多反应检测模式下,分析物在10~1 000 ng/mL范围内线性良好;与传统的QuEChERS方法相比,分析效率提高一倍;同时作者还证明了DART-QqQ比DART-Tof具有更高的灵敏度[27]。Marinella等采用直接实时分析-高分辨质谱(DART-Orbitrap)建立柑橘和苹果果皮上的农药实时检测方法,利用镊子夹住1 cm×3 cm果皮直线低速通过DART离子源对果皮上的农药进行直接分析,其精密度良好(RSD<14%);通过此方法测的农药浓度与将样品通过溶剂萃取然后进行UHPLC-Orbitap检测结果一致,该方法在农药快速实时检测和保证食品安全方面具有重要意义[28]。Elizabeth等采用棉签擦拭果蔬表面后引入DART电离源中,建立农药在具有不同表面特征的果蔬(樱桃番茄、橙子、桃、胡萝卜)上的快速残留检测方法,并评估了两种不同材质的棉签对擦拭效果和离子化的影响。结果发现,棉花棒只适合用于擦拭光滑的果实表面,而α-聚酯只能在温度较低的离子源下使用,当温度过高时,α-聚酯离子化产生的质谱信号会对分析物产生强烈的干扰[29]。Sara等同样利用擦拭的方法建立了果蔬上的农药残留分析方法。作者认为由于DART-MS缺乏色谱保留时间信息和碎片离子信息,容易产生假阳性的结果。所以作者建立了一套防止假阳性结果的数据标准,首先必须检测到分子离子,除此之外还必须检测到至少两个碎片离子或两个同位素离子或一个碎片离子和一个同位素离子,并基于此标准建立了一套精确分子离子、碎片离子和同位素离子数据库[30]。其他的简单样品处理方法主要包括简单的溶剂萃取、调整酸性饮料pH值[31]、啤酒脱气[32]、混合物过滤[33]、样品稀释等[23]。
3.2 DART-MS結合常规前处理方法
DART通常被认为是一种不需要样品前处理的电离技术,但是复杂样品干扰、样品浓度过低等因素会对DART的质谱信号造成一定的影响。而样品前处理技术往往能够改善DART的信号强度。目前,极性农药的分析检测存在较多的困难,一个是从极性溶剂中提取极性农药容易产生共流出杂质从而抑制质谱信号;另一个是极性化合物在反相色谱中的保留效果不好。Francisco团队针对这一问题采用快速极性农药提取法(QuPPe)结合DART建立了7种极性农药在莴苣和芹菜中的残留分析方法,方法回收率在71%~115%之间,符合残留分析检测的要求[34]。Tomas等比较了水果中福美双和福美锌直接检测和经QuEChERS前处理后DART-MS检测的信号差异。结果发现基质对DART-MS直接检测信号有明显的抑制作用,而经QuEChERS前处理后DART-MS的信号提高了15倍[35]。通常水体和饮料中的农药残留水平较低,不适合直接检测,Wang等将固相微萃取技术与DART-MS串联,建立了6种三嗪类除草剂在湖水和果汁中的残留分析方法,回收率在85%~106%之间,重现性良好(RSD=3.1%~10.9%)。与常规的DART-MS相比,该方法灵敏度和重现性更好[36]。
DART-MS技术既能用于原始样品原位检测,又能准确定量经复杂处理后的样品。试验过程中需要根据样品的特点和分析物的性质选择合适的检测方法。
4 结论与展望
综上所述,DART-MS在农药残留检测方面发展迅速,已经在直接分析方面展现了巨大的优势,是一种高效的实时无损分析方法。随着DART-MS的逐步发展,它将在农药残留分析领域发挥更重要的作用。尽管DART-MS比传统的LC-MS具有快速、直接、原位等优势,但该分析方法在某些方面还需要进一步提高,例如目前只能实现样品表面的农药残留定量分析,如何实现样品内部化学成分的直接、快速准确定量分析将是未来发展的重要方向。
参考文献
[1] 张佳玲,霍飞凤,周志贵,等.实时直接分析质谱的原理及应用[J].化学进展,2011,24(1):101-109.
[2] 冯鲍盛,白玉,刘虎威.实时直接分析质谱新技术及其应用[J].中国科学:化学,2014(5):19.
[3] TAKATSZ, WISEMAN J M, GOLOGANB, et al. Mass spectrometry sampling under ambient conditions with desorption electrospray ionization [J]. Science, 2004,306: 471-473.
[4] COOKS R G, OUYANG Z, TAKATS Z, et al. Ambient mass spectrometry [J]. Science, 2006,311:1566-1570.
[5] WESTON D J. Ambient ionization mass spectrometry: current understanding of mechanistic theory; analytical performance and application areas [J]. Analyst, 2010,135:661-668.
[6] LARAME J A, CODY R B, DEINZER M L. Discrete energy electron capture negative ion mass spectrometry [M]∥Encyclopedia of Analytical Chemistry: Applications, Theory and Instrumentation, 2006.
[7] CODY R B, LARAME J A, DURST H D. Versatile new ion source for the analysis of materials in open air under ambient conditions [J].Analytical Chemistry, 2005,77:2297-2302.
[8] RUMMEL J L, MCKENNA A M, MARSHALL A G, et al. The coupling of direct analysis in real time ionization to Fourier transform ion cyclotron resonance mass spectrometry for ultrahigh-resolution mass analysis [J]. Rapid Communications in Mass Spectrometry,2010,24(6):784-790.
[9] SHELLEY J T, WILEY J S, CHAN G C, et al. Characterization of direct-current atmospheric-pressure discharges useful for ambient desorption/ionization mass spectrometry [J].Journal of the American Society for Mass Spectrometry,2009, 20: 837-844.
[10] JORABCHI K, HANOLD K,SYAGE J. Ambient analysis by thermal desorption atmospheric pressure photoionization[J].Analytical and Bioanalytical Chemistry,2013,405:7011-7018.
[11] GROSS J H. Direct analysis in real time—a critical review on DART-MS [J].Analytical and Bioanalytical Chemistry,2014,406: 63-80.
[12] HIRAOKA K,NINOMIYA S,CHEN L C, et al. Development of double cylindrical dielectric barrier discharge ion source [J].Analyst, 2011, 136:1210-1215.
[13] ANDRADE F J,SHELLEY J T, WETZEL W C, et al. Atmospheric pressure chemical ionization source. 1. Ionization of compounds in the gas phase [J]. Analytical Chemistry, 2008,80:2646-2653.
[14] CODY R B.Observation of molecular ions and analysis of nonpolar compounds with the direct analysis in real time ion source [J].Analytical Chemistry, 2008,81:1101-1107.
[15] FURUYA H, KAMBARA S, NISHIDATE K, et al. Quantitative aspects of atmospheric-pressure Penning ionization[J]. Journal of the Mass Spectrometry Society of Japan, 2010,58: 211-213.
[16] SONG L, DYKSTRA A B, YAO H, et al. Ionization mechanism of negative ion-direct analysis in real time: a comparative study with negative ion-atmospheric pressure photoionization[J].Journal of the American Society for Mass Spectrometry, 2009,20:42-50.
[17] DANE A J, CODY R B.Selective ionization of melamine in powdered milk by using argon direct analysis in real time (DART) mass spectrometry [J].Analyst,2010,135:696-699.
[18] YANG H, WAN D, SONG F, et al. Argon direct analysis in real time mass spectrometry in conjunction with makeup solvents: a method for analysis of labile compounds [J].Analytical Chemistry, 2013,85:1305-1309.
[19] MCEWEN C N, LARSEN B S. Ionization mechanisms related to negative ion APPI, APCI, and DART [J]. Journal of the American Society for Mass Spectrometry,2009,20:1518-1521.
[20] CODY R B, DANE A J. Soft ionization of saturated hydrocarbons, alcohols and nonpolar compounds by negative-ion direct analysis in real-time mass spectrometry [J].Journal of the American Society for Mass Spectrometry, 2013,24: 329-334.
[21] SONG Liguo, GIBSON S C, BHANDARI D, et al. Ionization mechanism of positive-ion direct analysis in real time: a transient microenvironment concept[J].Analytical Chemistry, 2009,81(24):10080-10088.
[22] CHERNETSOVA E S, MORLOCK G E, REVELSKY I A. DART mass spectrometry and its applications in chemical analysis [J]. Russian Chemical Reviews,2011, 80: 235.
[23] VACLAVIK L, CAJKA T, HRBEK V,et al. Ambient mass spectrometry employing direct analysis in real time (DART) ion source for olive oil quality and authenticity assessment [J].Analytica Chimica Acta,2009, 645: 56-63.
[24] ZHAO Yeping, LAM M, WU Danlin, et al. Quantification of small molecules in plasma with direct analysis in real time tandem mass spectrometry, without sample preparation and liquid chromatographic separation, rapid communications in mass spectrometry: an international journal devoted to the rapid dissemination of up-to-the-minute [J]. Research in Mass Spectrometry, 2008,22: 3217-3224.
[25] ZHU Yulong, LIU Xigang, XU Jun,et al. Simultaneous determination of spirotetramat and its four metabolites in fruits and vegetables using a modified quick, easy, cheap, effective, rugged, and safe method and liquid chromatography/tandem mass spectrometry [J].Journal of Chromatography A,2013,1299:71-77.
[26] DONG F, CHEN X, LIU X, et al. Simultaneous determination of five pyrazole fungicides in cereals, vegetables and fruits using liquid chromatography/tandem mass spectrometry [J].Journal of Chromatography A, 2012,1262: 98-106.
[27] WEI Yong, GUO Tianyang, FANG Pingping, et al. Direct determination of multi-pesticides in wine by ambient mass spectrometry [J].International Journal of Mass Spectrometry, 2017,417:53-57.
[28] FARRE M, PICOO Y, BARCELOO D. Direct peel monitoring of xenobiotics in fruit by direct analysis in real time coupled to a linear quadrupole ion trap-orbitrap mass spectrometer[J].Analytical Chemistry,2013,85:2638-2644.
[29] CRAWFORD E, MUSSELMAN B.Evaluating a direct swabbing method for screening pesticides on fruit and vegetable surfaces using direct analysis in real time (DART) coupled to an Exactive benchtop orbitrap mass spectrometer[J].Analytical and Bioanalytical Chemistry, 2012,403:2807-2812.
[30] EDISON S E, LIN L A,GAMBLE B M, et al. Surface swabbing technique for the rapid screening for pesticides using ambient pressure desorption ionization with high-resolution mass spectrometry [J].Rapid Communications in Mass Spectrometry,2011, 25:127-139.
[31] BENNETT M J, STEINER R R. Detection of gamma-hydroxybutyric acid in various drink matrices via AccuTOF-DART [J].Journal of Forensic Sciences, 2009,54:370-375.
[32] CAJKA T, RIDDELLOVA K, TOMANIOVA M, et al. Recognition of beer brand based on multivariate analysis of volatile fingerprint [J].Journal of Chromatography A,2010,1217:4195-4203.
[33] SHEN Y,VAN BEEK T A, CLAASSEN F W, et al. Rapid control of Chinese star anise fruits and teas for neurotoxic anisatin by direct analysis in real time high resolution mass spectrometry[J].Journal of Chromatography A,2012,1259: 179-186.
[34] LARA F J,CHAN D, DICKINSON M,et al. Evaluation of direct analysis in real time for the determination of highly polar pesticides in lettuce and celery using modified Quick Polar Pesticides Extraction method [J].Journal of Chromatography A,2017,1496: 37-44.
[35] CAJKA T, RIDDELLOVA K,ZOMER P, et al. Direct analysis of dithiocarbamate fungicides in fruit by ambient mass spectrometry [J]. Food Additives & Contaminants: Part A, 2011,28: 1372-1382.
[36] WANG Xin,LI Xianjiang, LI Ze,et al. Online coupling of in-tube solid-phase microextraction with direct analysis in real time mass spectrometry for rapid determination of triazine herbicides in water using carbon-nanotubes-incorporated polymer monolith [J]. Analytical Chemistry,2014,86: 4739-4747.
(責任编辑: 田 喆)
