氯化碘催化的喹啉-2-羧酸乙酯类化合物的合成
2018-11-28张宝华胡永青刘宏果张之奎
张宝华,胡永青,刘宏果,张之奎
(1.石家庄学院 化工学院,河北 石家庄 050035;2.石家庄鹏海制药股份有限公司,河北 石家庄 050600)
0 引言
喹啉类化合物是组成含氮杂环化合物的主要结构单元,广泛存在于药物、天然产物、杀虫剂和除草剂结构中[1-3].除经典的合成方法外,近年来发展起来的喹啉类化合物的合成新方法有:微波合成法[4]、超声波合成法[5]、金属催化合成法[6-8]和非金属I2催化合成法[9-11].这些合成方法大多收率较高,但微波合成法和超声波合成法对设备要求高,给规模化生产带来不便.金属催化合成法对环境不友好,非金属I2催化合成法值得借鉴.笔者报道用氯化碘(ICl)催化苯胺、乙醛酸乙酯和炔制备喹啉-2-羧酸乙酯类化合物的方法.
1 实验部分
1.1 仪器和试剂
1H-NMR 和13C-NMR 用 Brucker Avance DMX400(400 MHz,125 MHz,Bruker公司,德国)测定;HRMS用VG Zabspec高分辨磁质谱仪(Waters公司,美国)测定;试剂均为分析纯.
1.2 喹啉-2-羧酸乙酯类化合物1的一般合成过程
氮气保护下,将苯胺 2(1.1 mmol)、乙醛酸乙酯(1.1 mmol)、炔 3(1.0 mmol)和 N,N-二甲基甲酰胺(DMF)(5 mL)加入到反应瓶中,搅拌,再加入ICl(0.05 mmol),50℃条件下反应36~48 h.TLC监测反应完毕,减压蒸出DMF,残留物加入10 mL二氯甲烷,用饱和食盐水(10 mL×3)洗涤,无水Na2SO4干燥,过滤,浓缩,硅胶柱纯化[V(乙酸乙酯)∶V(石油醚)=1∶20],得到化合物 1(图 1).
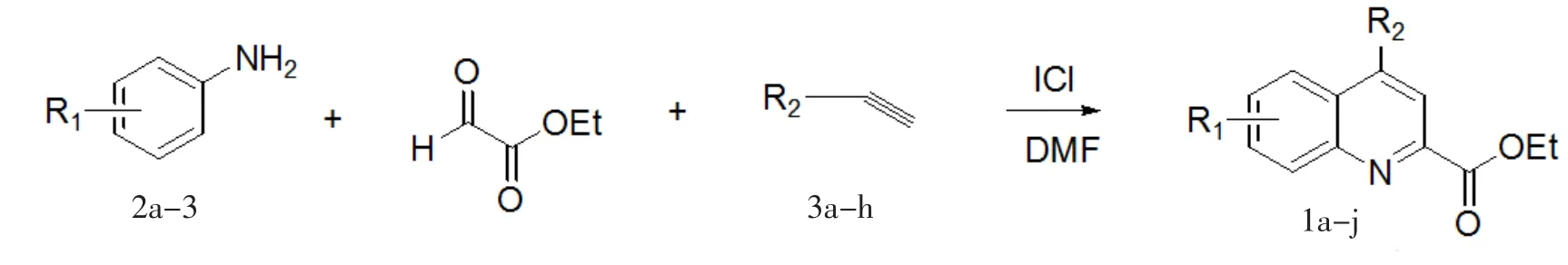
图1 苯胺、乙醛酸乙酯和炔的反应
6-甲氧基-4-苯基喹啉-2-甲酸乙酯(1a):收率 89%;1H NMR(400 MHz,CDCl3),δ:8.27(d,1H,J=9.3 Hz),8.09(s,1H),7.57~7.50(m,5H),7.43(dd,1H,J=1.5 Hz,J=9.3 Hz),7.21(d,1H,J=1.5 Hz),4.55(q,2H,J=7.0 Hz),3.80(s,3H),1.46(t,3H,J=7.0 Hz);13C NMR(125 MHz,CDCl3),δ:165.5,159.4,147.8,145.3,144.1,137.8,132.5,129.2,129.0,128.7,128.6,122.7,121.7,103.0,62.1,55.5,14.3;HRMS (EI):Calcd.for C19H17NO3[M]+:307.120 8;Found:307.1214.
4-(4-甲苯基)-6-甲氧基喹啉-2-甲酸乙酯(1b):收率 94%;1H NMR(400 MHz,CDCl3),δ:8.25(d,1H,J=9.3 Hz),8.07(s,1H),7.56~7.35(m,5H),7.24(d,1H,J=2.7 Hz),4.55(q,2H,J=6.8 Hz),3.80(s,3H),2.47(s,3H),1.46(t,3H,J=6.8 Hz);13CNMR(125 MHz,CDCl3),δ:165.6,159.4,148.0,145.3,144.2,138.5,134.7,132.6,129.4,129.0,122.6,121.7,103.1,62.0,55.4,21.3,14.3;HRMS(EI):Calcd.for C20H19NO3[M]+:321.1365;Found:321.136 9.
6-甲氧基-4-(4-甲氧基苯基)喹啉-2-甲酸酯(1c):收率 92%;1H NMR(400 MHz,CDCl3),δ:8.25(d,1H,J=9.3 Hz),8.06(s,1H),7.49(d,2H,J=8.4 Hz),7.43(dd,1H,J=3.2 Hz,J=9.3 Hz),7.27(d,1H,J=3.2 Hz),7.07(d,2H,J=8.4 Hz),4.55(q,2H,J=7.1 Hz),3.90(s,3H),3.56(s,3H),1.47(t,3H,J=7.1 Hz);13C NMR(125 MHz,CDCl3),δ:165.6,159.8,159.3,147.7,145.2,144.3,132.5,130.7,130.2,129.3,122.7,121.7,114.1,103.2,62.0,55.3,14.3;HRMS(EI):Calcd.for C20H19NO4[M]+:337.131 4;Found:337.131 2.
4-(4-氟苯基)-6-甲氧基喹啉-2-甲酸乙酯(1d):收率 82%;1H NMR(400 MHz,CDCl3),δ:8.26(d,1H,J=9.3 Hz),8.05(s,1H),7.54~7.49(m,2H),7.44(dd,1H,J=2.9 Hz,J=9.3 Hz),7.27~7.21(m,2H),7.14(d,1H,J=2.9Hz),4.55(q,2H,J=7.0 Hz),3.81(s,3H),1.47(t,3H,J=7.0 Hz);13C NMR(125 MHz,CDCl3),δ:165.5,162.9(d,JC—F=247.3 Hz),159.4,146.7,145.3,144.2,133.8,132.7,131.0(d,JC—F=7.7 Hz),129.2,122.8,121.8,115.8(d,JC—F=21.4Hz),103.0,62.1,55.5,14.3;HRMS(EI):Calcd.for C19H16FNO3[M]+:325.111 4;Found:325.111 8.
4-(2-氟苯基)-6-甲氧基喹啉-2-甲酸乙酯(1e):收率 79%;1H NMR(400 MHz,CDCl3),δ:8.27(d,1H,J=9.3 Hz),8.10(s,1H),7.52~7.24(m,5H),6.39(t,1H,J=2.5 Hz),4.54(q,2H,J=7.2 Hz),3.81(s,3H),1.47(t,3H,J=7.2 Hz);13C NMR(125 MHz,CDCl3),δ:165.5,159.5,159.4(d,JC—F=246.8 Hz),145.1,144.0,142.2,132.6,131.5,130.7(d,JC—F=8.2 Hz),129.2,125.0(d,JC—F=15.9 Hz),124.5,123.0,122.5,116.0(d,JC—F=21.8 Hz),103.0,62.1,55.4,14.3;HRMS(EI):Calcd.for C19H16FNO3[M]+:325.111 4;Found:325.111 9.
4-(4-氯苯基)-6-甲氧基喹啉-2-甲酸乙酯(1f):收率 85%;1H NMR(400 MHz,CDCl3),δ:8.27(d,1H,J=9.3 Hz),8.05(s,1H),7.52(d,2H,J=9.0 Hz),7.47(d,1H,J=9.0 Hz),7.44(dd,1H,J=2.5 Hz,J=9.3 Hz),7.12(d,1H,J=9.3 Hz),4.55(q,2H,J=7.20 Hz),3.82(s,3H),1.47(t,3H,J=7.0 Hz);13C NMR(125 MHz,CDCl3),δ:165.4,159.5,146.5,145.1,144.1,136.2,134.6,132.7,130.7,129.0,128.9,123.0,121.5,102.6,62.1,55.4,14.3;HRMS(EI):Calcd.for C19H16ClNO3[M]+:341.081 9;Found:341.081 6.
4-(4-乙酰基苯基)-6-甲氧基喹啉-2-甲酸乙酯(1g):收率 67%;1H NMR(400 MHz,CDCl3),δ:8.28(d,1H,J=9.3 Hz),8.14(d,2H,J=8.3 Hz),8.08(s,1H),7.65(d,2H,J=8.3 Hz),7.45(dd,1H,J=2.9 Hz,J=9.3 Hz),7.11(d,1H,J=2.9 Hz),4.55(q,2H,J=7.0 Hz),3.81(s,3H),2.70(s,3H),1.48(t,3H,J=7.0 Hz);13C NMR(125 MHz,CDCl3),δ:197.6,165.4,159.7,146.5,145.2,144.2,142.6,137.0,132.8,130.0,128.7,123.0,121.6,102.7,62.2,55.5,26.7,14.3;HRMS(EI):Calcd.for C21H19NO4[M]+:349.131 4;Found:349.130 8.
4-苄基-6-甲氧基喹啉-2-甲酸乙酯(1h):收率 57%;1H NMR(400MHz,CDCl3),δ:8.21(d,1H,J=9.3Hz),8.00(s,1H),7.39~7.30(m,4H),7.25~7.18(m,4H),7.53(q,2H,J=7.0 Hz),4.43(s,2H),3.83(s,3H),1.46(t,3H,J=7.0 Hz);13CNMR(125 MHz,CDCl3),δ:165.7,159.2,146.0,145.5,143.8,138.3,132.9,128.8,128.6,126.7,122.5,122.2,101.7,62.0,55.5,38.8,14.3;HRMS(EI):Calcd.for C20H19NO3[M]+:321.136 5;Found:321.1367.
6-甲基-4-苯基喹啉-2-甲酸乙酯(1i):收率 84%;1H NMR(400MHz,CDCl3),δ:8.29(d,1H,J=9.3Hz),8.10(s,1H),7.70(s,1H),7.62(dd,1H,J=1.8 Hz,J=9.3 Hz),7.56~7.51(m,5H),4.56(q,2H,J=6.7 Hz),2.49(s,3H),1.49(t,3H,J=6.7 Hz);13C NMR(125 MHz,CDCl3),δ:165.6,149.0,146.7,146.5,139.0,137.6,132.3,130.8,129.6,128.7,128.5,127.6,124.3,121.4,62.1,22.0,14.3;HRMS(EI):Calcd.for C19H17NO2[M]+:291.1259;Found:291.1256.
6-苄氧基-4-苯基喹啉-2-甲酸乙酯(1j):收率 86%;1H NMR(400MHz,CDCl3),δ:8.30(d,1H,J=9.1 Hz),8.06(s,1H),7.53~7.26(m,12H),5.06(s,2H),4.55(q,2H,J=7.4 Hz),1.48(t,3H,J=7.4 Hz);13C NMR(125 MHz,CDCl3),δ:165.5,158.3,148.0,145.4,144.3,137.7,136.0,132.6,129.8,129.0,128.7,128.6,128.5,128.1,127.4,104.7,70.1,62.0,14.3;HRMS(EI):Calcd.for C25H21NO3[M]+:383.1521;Found:383.151 8.
2 结果与讨论
2.1 催化剂的筛选
以p-甲氧基苯胺2a、乙醛酸乙酯和苯乙炔3a为原料,CH2Cl2为溶剂,40℃下分别加入5 mol%的对四丁基碘化铵(TBAI)、N-碘代丁二酰亚胺(NIS)、碘和 ICl,对催化剂进行筛选(表 1).结果显示,TBAI没有催化活性,NIS催化活性中等,ICl催化活性最好,1a的收率达到74%.

表1 催化剂的筛选

表2 反应条件的优化
2.2 反应条件的优化
以ICl为催化剂,对反应的溶剂、温度和催化剂用量进行了优化(表2).结果显示,相对于非极性溶剂,极性溶剂效果较好.以DMF为溶剂,产物收率最高.升高反应温度,收率增加,当反应温度为50℃时,收率最高,升温至60℃,收率没有提高,优选50℃;催化剂用量增加,收率提高,用量为5 mol%时,1a的收率达89%,用量增至8 mol%,收率反而下降,可能是ICl浓度增大后,ICl会被空气氧化成I2O5,产生氧化副反应,故催化剂用量优选为5 mol%.
2.3 喹啉-2-羧酸乙酯类化合物的合成
在最优反应条件下,考察各种取代的苯胺2、乙醛酸乙酯与炔3合成喹啉-2-羧酸乙酯类化合物1的反应,结果见表3.各种炔均可与苯胺、乙醛酸乙酯反应,获得满意的结果,产物的收率为57%~94%.苯环上具有供电子取代基对反应有利,炔苯环上2位有取代基会降低收率.苯胺的供电子取代基对反应有利,且取代基供电子能力越强,收率越高.苄基炔为底物的反应,收率仅57%,说明脂肪炔反应活性不高.

表3 ICl催化的喹啉-2-羧酸乙酯类化合物的合成
3 结论
以ICl为催化剂,以DMF为溶剂,50℃下,各种取代的炔与苯胺、乙醛酸乙酯反应制备了喹啉-2-羧酸乙酯类化合物,收率为57%~94%.
