一种Off/On型荧光光度法检测鱼肉中氟含量
2018-11-14熊海涛唐志华吴迎春庞海霞1
熊海涛, 唐志华,吴迎春,庞海霞1,
1(陕西省催化基础与应用重点实验室,陕西 汉中,723001) 2(陕西理工大学 化学与环境科学学院,陕西 汉中,723001)
随着现代工业的发展,含氟物质与日俱增,其通常以废气、废水及废渣的形式向大气水体土壤中排放,给生态环境带来巨大危害[1]。因此,对氟含量的准确监测就具有重要意义。
目前,对氟定量分析的方法主要有:离子选择电极法[2-3]、分光光度法(包括催化光度法)[4-6]、离子色谱法[7-9]、极谱法[10]、石墨炉分子吸收光谱法[11-12]及荧光光度法[13-15]等。在这些方法中,离子选择电极与分光光度法尽管仪器简单,操作方便,但是重现性均较差;离子色谱法需要较为苛刻的分离条件,极谱法会带来一定的环境污染,而石墨炉分子吸收光谱法往往需要昂贵的仪器设备。荧光光度法具有灵敏度高、选择性好及线性范围广等优点。近年来该法结合时间分辨技术、偏振技术、同步扫描和三维扫描等实验新技术,在食品检测中得到广泛应用。
聚乙烯吡咯烷酮(PVP)是一种水溶性高分子聚合物,具有良好化学稳定性、成膜性及保护胶体作用等。尤其是近几年,PVP与一些纳米材料相结合而制备出多种功能性复合材料[16-18]并应用于药物分析领域[19-20]。另外,PVP也具有一定的荧光特性[21-22],但是未见其分析应用方面的文献报道。本研究利用强酸性溶液中,F-竞争性结合Fe3+而使PVP-Fe3+体系荧光得到恢复,基于此特性建立了一种Off/On型荧光光度法分析氟离子含量的新方法。该方法灵敏度较高,试剂廉价易得,无二次污染。该方法有望用于生物与环境水样中氟离子含量的批量分析。
1 材料与方法
1.1 仪器与设备
F4600荧光光度计,日本日立公司;HH-6型恒温水浴锅,江苏省金坛市金祥龙电子有限公司;HL-3000型电子天平,日本AND公司;FW135型绞碎机,天津市泰斯特仪器有限公司;SX2-4-13型马弗炉,上海有限微行炉业公司。
1.2 材料与试剂
PVP(美国Sigma-Aldrich公司,wt: 10000):3.0 mmol/L;FeCl3(天津市天力化学试剂有限公司):8.0 mmol/L;KF(天津市天力化学试剂有限公司):0.1 mmol/L;醋酸-醋酸钠缓冲溶液(0.20 mol/L)。
氯乙酸-氢氧化钾缓冲溶液:准确称量13.135 0 g氯乙酸和5.218 0 g KOH,用二次水溶解后移入1 000 mL容量瓶中定容;B-R缓冲液:磷酸(0.04 mol/L)、HCl(0.04 mol/L)及醋酸(0.04 mol/L)各100 mL,混合而成;
草鱼、鲢鱼及鲫鱼:均购自汉中市汉台区汉丰水产市场;
所用试剂均为分析纯,实验用水为超纯水(电阻率18.24 MΩ·cm)。
1.3 实验方法
取2支10 mL比色管依次编号1、2,各加入0.5 mL PVP(3.0 mmol/L)溶液与8.0 mmol/L FeCl3溶液,2号比色管另加标准系列KF或样品溶液,然后均用氯乙酸-氢氧化钾缓冲溶液(pH=2.0)定容至刻度线,每支比色管振荡3 min,再静置30 min之后,用F4600荧光光度计分别扫描荧光光谱(1,2号比色管对应荧光分别记为F1、F2,用荧光恢复(ΔF=F2-F1)对F-浓度做图,通过得到的工作曲线确定样品中F-含量。
2 结果与分析
2.1 PVP、PVP-Fe3+及PVP-Fe3+-F-反应体系的荧光光谱研究
按照1.3实验方法,分别以270 nm激发波长研究了PVP、PVP-Fe3+及PVP-Fe3+-F-三个不同反应体系的荧光发射光谱(如图1所示)。

图1 不同体系荧光发射光谱图Fig.1 Fluorescence emission spectrums of different systems注:C(PVP)=0.01 mmol/L;C(Fe3+)=0.3 mmol/L;C(F-)=0.01 mmol/L;pH=2.0;温度(25℃);时间(25 min)。
结果表明,3种不同体系的荧光发射波长均为544 nm,单独PVP体系的荧光强度为1 860,PVP-Fe3+体系的荧光强度为208,说明Fe3+能在强酸性介质中猝灭PVP的荧光,这与文献相一致[21]。而当PVP-Fe3+体系中加入少量的F-后,反应体系的荧光强度变为836,这可能是基于加入的F-竞争性结合了原有反应体系中的Fe3+而生成[FeF6]3-络合物,致使PVP-Fe3+生成物中的PVP被释放到溶液中,结果使体系荧光强度有所恢复。
2.2 实验条件优化
2.2.1 最佳缓冲溶液确定
按照实验方法,用氯乙酸-氢氧化钾缓冲溶液、醋酸-醋酸钠缓冲溶液及B-R缓冲溶液进行实验且保持其他因素不变的情况下,初步研究表明:在氯乙酸-氢氧化钾缓冲溶液下荧光恢复ΔF值最大。因此,实验选择氯乙酸-氢氧化钾缓冲溶液作为下面研究的最佳缓冲溶液。
2.2.2 最佳pH的选择
固定其他条件不变,取pH=1.5,2.0,2.5,3.0及3.5氯乙酸-氢氧化钾缓冲溶液配制反应体系溶液。由图2可以发现:在pH=2.0时, PVP的荧光恢复最大。这主要是由于强酸性介质中不利于游离的F-存在,而较弱的酸性介质中则不利于Fe3+的稳定存在。因此,在以后的研究中,选择pH=2.0的氯乙酸-氢氧化钾缓冲溶液作为最佳pH值。
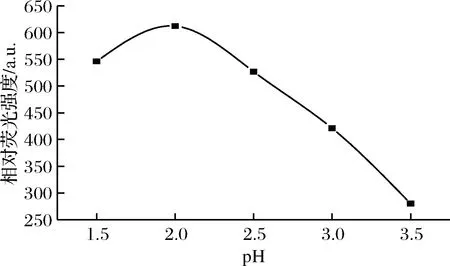
图2 pH对相对荧光强度ΔF的影响Fig.2 Effect of pH on ΔF注:C(PVP)=0.010 mmol/L;C(Fe3+)=0.3 mmol/L;C(F-)=0.01 mmol/L;温度(25℃);时间(25 min)。
2.2.3 最佳PVP浓度的选择
作为研究体系中的荧光探针,PVP浓度会直接影响F-的分析特性。选定加入不同浓度PVP溶液,对PVP-Fe3+及PVP-Fe3+-F-两个体系分别进行荧光光谱扫描。图3表明:随着PVP浓度的增加荧光恢复程度逐渐增大,但是当其浓度超过0.015 mmol/L后体系的荧光恢复又逐渐减弱。这可能是由于太低浓度的PVP会得到较弱的荧光发射峰值,而过高浓度的PVP会致使少量F-存在时,恢复的体系荧光发射不明显。因此,选择0.015 mmol/L PVP浓度作为最佳浓度。

图3 PVP浓度对ΔF的影响Fig.3 Effect of PVP concentration on ΔF注:C(Fe3+)=0.3 mmol/L;C(F-)=0.01 mmol/L;pH=2.0;温度(25℃);时间(25 min)。
2.2.4 最佳Fe3+浓度的选择
在确定pH为2,PVP浓度为0.015 mmol/L,温度与时间保持不变的条件下,改变Fe3+浓度以进行反应体系的荧光光谱扫描。由图4可以观察到:随着Fe3+浓度的增大,荧光恢复程度呈现出先增强后减弱的趋势,仅当Fe3+浓度为0.4 mmol/L时体系荧光恢复最强。可能是由于PVP和F-同时对Fe3+进行竞争反应,较低浓度的Fe3+对PVP的荧光猝灭较弱(背景信号较高),不利于方法灵敏度的提高,而高浓度的Fe3+与一定量PVP反应后,溶液中存在的游离Fe3+浓度仍然较高,会导致因少量的F-引起的荧光恢复较弱。为此,选取Fe3+最佳浓度为0.4 mmol/L。
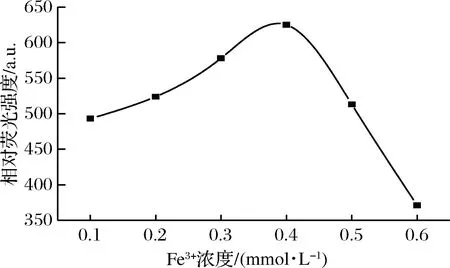
图4 Fe3+浓度对ΔF的影响Fig.4 Effect of Fe3+ concentration on ΔF注:C(PVP)=0.015 mmol/L;C(F-)=0.01 mmol/L;pH=2.0;温度(25 ℃);时间(25 min)。
2.2.5 最佳反应时间的选择
设定PVP-Fe3+及PVP-Fe3+-F-两种体系溶液均反应5、15、25、35、45及55 min后进行荧光光谱扫描(荧光强度恢复研究)。图5说明:在2种体系各自反应35 min后,二者的荧光强度差异(恢复)最大,再延长反应时间,荧光恢复程度基本不变,这说明PVP和F-同时对Fe3+竞争反应可以在35 min之内完成。因此,选定35 min后,对两种体系进行荧光光谱扫描。
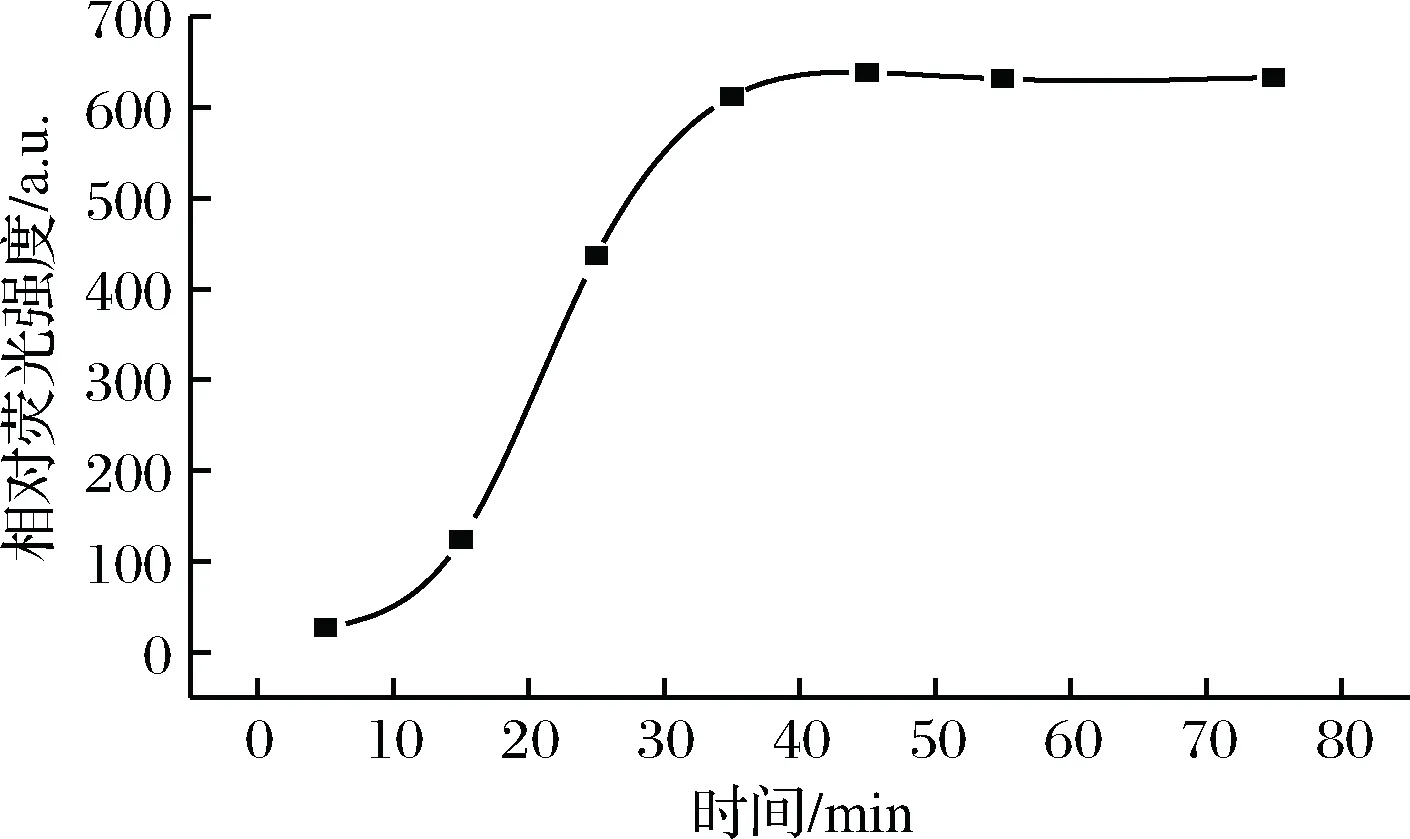
图5 反应时间对ΔF的影响Fig.5 Effect of reaction time on ΔF注:C(PVP)=0.015 mmol/L;C(Fe3+)=0.4 mmol/L;C(F-)=0.01 mmol/L;pH=2.0;温度(25℃)。
2.2.6 最佳反应温度的选择
在其他实验条件不变的情况下,考察反应温度对选定反应体系荧光强度变化的影响。由图6可以看出:随着温度增加,在20~40 ℃,ΔF值基本保持不变;继续升高反应温度,ΔF值逐渐下降,这可能是由于温度过高会使PVP分子结构不稳定。所以,选择在常温下(25 ℃)对不同体系的荧光光谱进行研究。
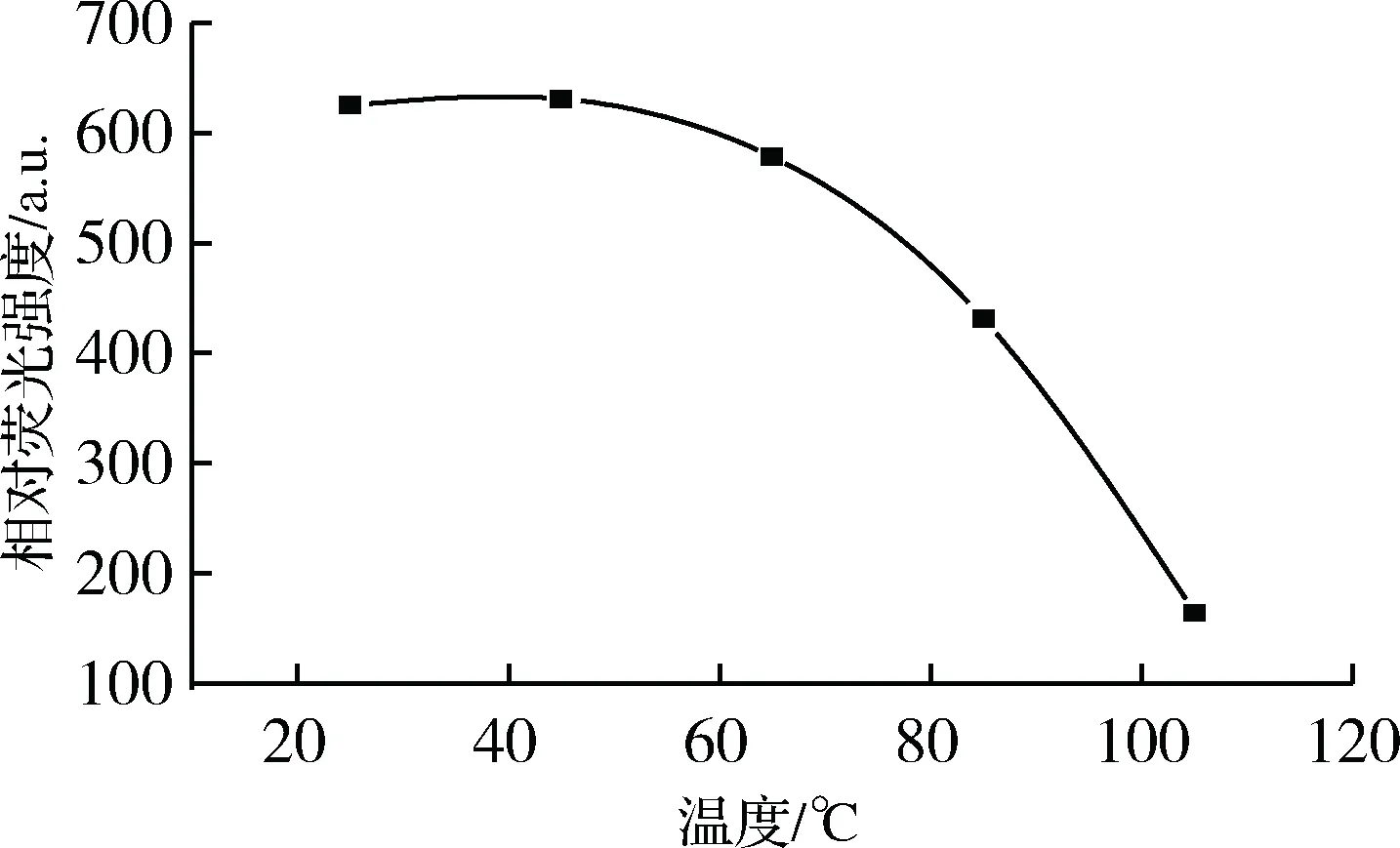
图6 温度对相对荧光强度ΔF的影响Fig.6 Effect of temperature on ΔF注:C(PVP)=0.015 mmol/L;C(Fe3+)=0.4 mmol/L;C(F-)=0.01 mmol/L;pH=2.0;时间(35 min)。
2.3 建议方法的分析特性
在最佳实验条件下,F-浓度在1.5~30.0 μmol/L与体系荧光恢复程度(ΔF)呈良好的线性相关(如图7与图8所示),其回归方程为ΔF=63 334.1C(mmol/L)+7.89, 相关系数r=0.997 5。按照国际纯粹与应用化学联合会(IUPAC)建议,计算方法的检出限为0.6 μmol/L。对含有3.0 μmol/L F-的反应体系进行连续8次荧光光谱扫描,其相对标准偏差为2.8%,说明该方法具有良好的重现性。
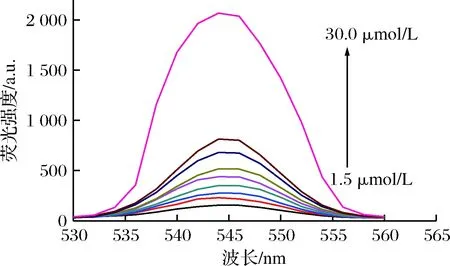
图7 不同F-浓度对体系荧光强度的响应Fig.7 Fluorescence emission spectra of F- withdifferent concentrations
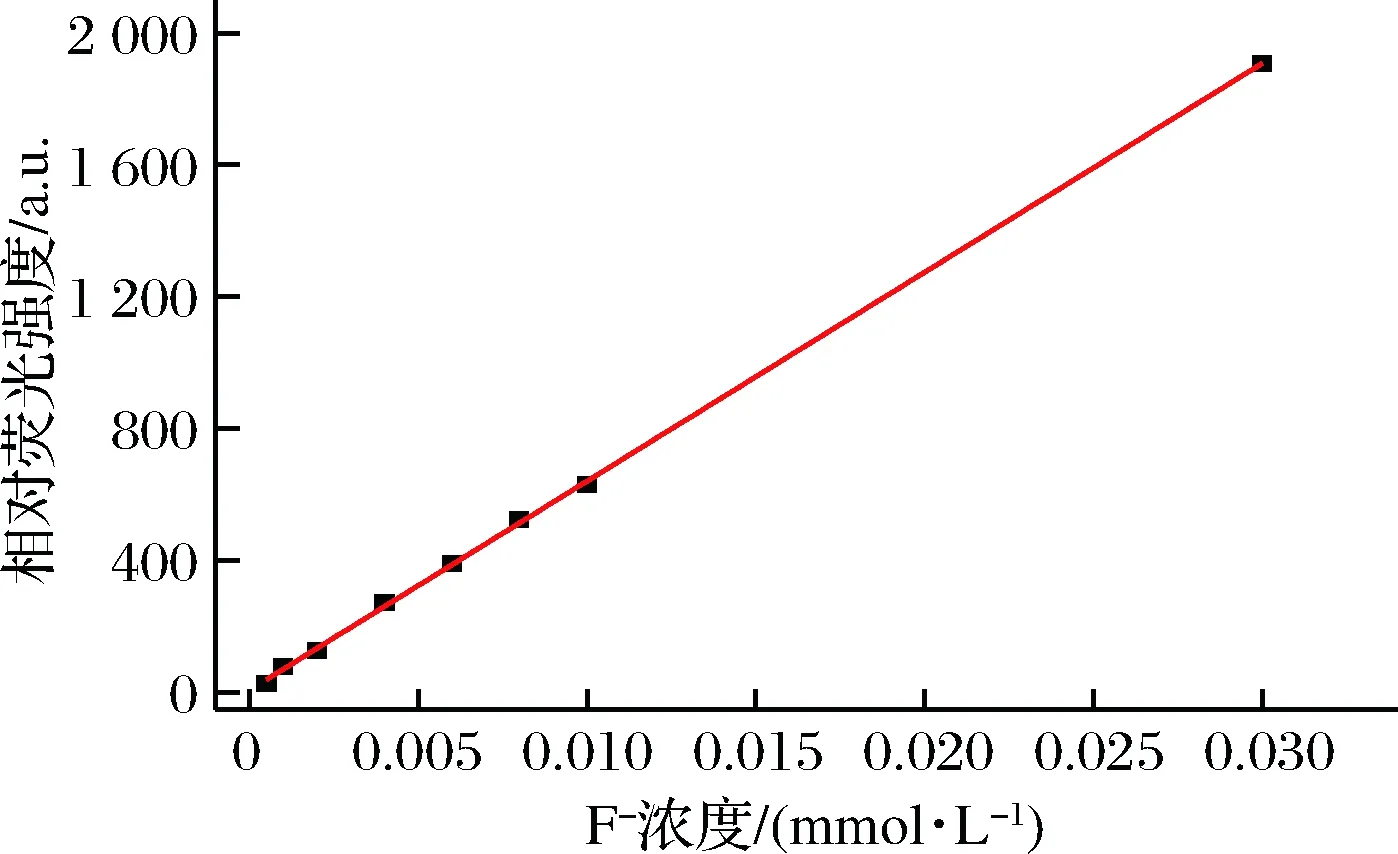
图8 校准曲线Fig.8 Calibration curve
2.4 干扰离子考察
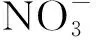
2.5 样品分析
2.5.1 鱼肉样品前处理
取适量鱼(包括草鱼、鲤鱼及鲫鱼)肉并去皮、去骨,再将鱼肉组织清洗干净,然后用绞碎机将其绞碎。接着,准确称取2.000 0 g鱼肉于坩埚中,加4 mL 0.5 mol/L硝酸镁溶液与少量1.0 mol/L氢氧化钠溶液,搅拌混匀后放置30 min(固定样品中的氟)。然后,在水浴上挥干,再用电炉加热炭化至不冒烟,再将其于600 ℃马弗炉内灰化6 h。待灰化完全,取出放冷,将灰分全部转移至洁净烧杯中并加高纯水和少量氢氧化钠溶解,再加入适量活性炭搅拌5 min,静置30 min以后,先用滤纸过滤1次,将滤液经过0.45、0.22 μm水系滤膜过滤,得到透明的所需要样品溶液,并用缓冲溶液定容到10 mL容量瓶中备用。同样的方法,再平行处理2份。
2.5.2 样品测定结果及回收率
在最优的实验条件下,按照1.3实验方法测定样品中F-含量,并分别添加3.0 μmol/L标准样品液进行加标回收实验。分析结果如表1所示:测得草鱼、鲢鱼及鲫鱼样品中F-的含量分别为1.9、3.0及2.6 μg/g,加标回收率在93.33%~100.00%,其相对标准偏差均小于5.3%。这说明本实验所建立起来的方法具有较高的准确度与精密度。

表1 样品测定结果及回收率实验(n=3)Table 1 Determination results of samples and recovery rate (n=3)
3 结论
本文基于强酸性介质中,少量F-能竞争性结合Fe3+-PVP体系中Fe3+而形成[FeF6]3-配离子,导致反应体系的荧光强度发生显著恢复,据此建立了一种Off/On型荧光光度法检测氟的新方法。采用该方法测定3种鱼肉样品中F-的最高含量为3.0 μg/g,远低于国标中氟含量(21.0 μg/g),说明该地区草鱼受到氟污染的程度较低。该方法操作简便、试剂廉价且无污染,有望为食品监督与检测部门分析本地区鱼肉样品中F-含量提供技术参考。
