苦参素对晚期糖基化产物诱导的心力衰竭的治疗作用及其机制
2018-11-09刘仲伟唐治国李晓晴
张 勇,刘仲伟,唐治国,潘 硕,赵 娜,李晓晴
(陕西省人民医院心血管内一科,西安 710068;*通讯作者,E-mail:mufu00404@163.com)
在全球范围内,2型糖尿病(type 2 diabetes mellitus,T2DM)的发病率正在逐年升高[1]。T2DM的心血管并发症已经成为棘手的公共卫生问题,特征性的并发症包括心肌梗死、缺血性心肌病、心源性猝死以及糖尿病心肌病(diabetic cardiomyopathy,DbCM)[2]。DbCM表现为心脏收缩及舒张功能的显著下降,最终进展为心力衰竭[3]。目前认为心肌细胞凋亡造成的心脏泵功能下降是DbCM心力衰竭的重要发病机制之一[4]。
在糖尿病的进展过程中,持续的高血糖水平会导致代谢紊乱的发生。体内的葡萄糖基与其他代谢产物,例如氨基酸以及某些核酸进行非酶糖基化反应,产生一组高分子量的荧光物质,即晚期糖基化产物(AGEs)。糖尿病患者体内AGEs水平显著升高,参与了T2DM心血管并发症的发生与发展[5]。研究表明,血AGEs浓度与糖尿病心力衰竭具有显著的相关性[6]。此外,体外研究显示,AGEs能够直接诱导人类H9c2心肌细胞发生凋亡[7]。因此,能够抑制AGEs诱导的心肌细胞凋亡的药物具有潜在的治疗应用价值。
作为丝裂原活化蛋白激酶(mitogen activated protein kinase,MAPK)蛋白酶家族的成员,p38 MAPK是凋亡通路的关键信号分子。作为p38 MAPK上游的MAPK激酶(MAPK kinase,MKK),MKK3及MKK6可通过磷酸化激活p38 MAPK。而这些MKK的激活又依赖其上游的MKK激酶(MKK kinase,MKKK)[8]。凋亡信号调节激酶1(apoptosis signal regulating kinase 1,ASK1)是具有代表性的MKKK,在静息状态下与其内源性抑制物硫氧还原蛋白(thioredoxin,Trx)结合。既往研究表明,AGEs能够通过促进Trx1-ASK1复合体的解离而诱导ASK1的活化[9]。
苦参素是提取自苦参、苦豆子以及广豆根等多种豆科植物中的一种生物碱,具有抗炎、抗氧化、抗肿瘤、免疫调节、抗纤维化以及抗凋亡等多种药理学活性。研究表明,苦参素对例如腺苷酸活化蛋白激酶(AMP-activated protein kinase,AMPK)蛋白激酶以及Janus蛋白激酶等具有抑制活性[10,11]。本课题组的前期研究表明,苦参素能够通过调控MKKs/p38 MAPK信号通路而产生心脏保护作用[8]。本研究制作AGEs诱导的心力衰竭动物模型,探讨ASK1-Trx复合体介导的MKKs/p38 MAPK信号通路在其中扮演的角色。此外,本研究还将观察苦参素对AGEs诱导的心力衰竭的治疗作用,并探讨ASK1-Trx复合体介导的MKKs/p38 MAPK信号通路是否为苦参素的作用靶点。相信本研究结果不仅能够深化对DbCM发病机制的认识,且为苦参素在DbCM的临床治疗应用方面提供理论依据。
1 材料与方法
1.1 主要试剂
甘油醛(Sigma-Aldrich公司),胎牛血清(BSA,Hyclone公司),PD-10脱盐柱(GE Healthcare公司),MKK3抗体、磷酸化MKK3抗体(Phosphor-MKK3)、MKK6抗体、磷酸化MKK6抗体(Phosphor-MKK6)均购自Abcam公司,p38抗体、磷酸化p38抗体(Phosphor-p38)购自Cell Signaling Tech公司,活化caspase3、GAPDH抗体均购自Abcam公司。
1.2 AGEs的制备
本研究中AGEs的制备参照了本课题组的方案及既往文献报道[8,12]。无菌条件下,0.1 mmol/L的甘油醛与BSA在磷酸钠缓冲液(0.2 mmol/L,pH=7.4)中孵育7 d。以层析法使用PD-10脱盐柱(GE Healthcare)去除未成基团的糖类。
1.3 实验动物与分组
9周龄SD大鼠50只,SPF级,体质量180-220 g,购自西安交通大学动物实验中心(生产许可证号:SCXK陕2012-003)。将上述动物随机分为5组,每组10只,对照组(Ctrl)、AGEs暴露组(AGEs)、低剂量苦参素治疗组(AGEs+L-Mat)、中剂量苦参素治疗组(AGEs+M-Mat)和高剂量苦参素治疗组(AGEs+H-Mat)。Ctrl组接受生理盐水连续腹腔注射20 d;AGEs组接受剂量为1 mg/d的AGEs连续腹腔注射20 d;AGEs+L-Mat组、AGEs+M-Mat组及AGEs+H-Mat组接受剂量为1 mg/d的AGEs及剂量为50 mg/(kg·d)、100 mg/(kg·d)以及200 mg/(kg·d)的苦参素溶液连续腹腔注射20 d。末次注射后20 d,使用二氧化碳窒息法处死动物并获得标本。
1.4 血流动力学检测
采用颈外动脉左心室插管法对大鼠心脏血流动力学指标进行评估。采用异氟烷吸入麻醉动物。暴露右侧颈外动脉,将2F Mikro Tip导管插入血管并连接压力换能器采集压力信号,出现心室压力波形后确认导管位于左心室。以生物信息采集系统(AD Instrument)生物压力检测模块记录压力信号,计算左室收缩压(LVSP)、左室舒张末期压力(LVEDP)、左室内压最大增加速率(+LVdP/dtmax)以及左室内压最大衰减速率(-LVdP/dtmax)。
1.5 免疫荧光检测大鼠心肌细胞凋亡
收集并修剪大鼠心室肌细胞,OCT包埋剂包埋,冰冻切片(5 μm)。4%多聚甲醛溶液固定,用20 μmol/L蛋白酶K溶液处理切片。TUNEL染色试剂盒按照试剂盒说明书对上述切片进行处理。在倒置荧光显微镜下观察并使用Image J软件(版本号1.38)分析。
1.6 蛋白免疫印迹法检测p38 MAPK凋亡信号通路活化情况
处死大鼠,收集心室肌组织并经过RIPA裂解液处理及低温离心,获得总细胞提取物,用总蛋白提取试剂盒获得总蛋白。采用BCA法检测蛋白浓度,SDS-PAGE法将蛋白分离并电转印至PVDF膜。以15%脱脂牛奶封闭,分别用MKK3抗体(1 ∶500)、磷酸化MKK3抗体(Phosphor-MKK3,1 ∶500)、MKK6抗体(1 ∶500)、磷酸化MKK6抗体(Phosphor-MKK6,1 ∶500)、p38抗体(1 ∶250)、磷酸化p38抗体(Phosphor-p38,1 ∶250)、活化caspase3(1 ∶1 000)或GAPDH(1 ∶500),4 ℃孵育10 h。TBST洗涤后,室温下与相应二抗孵育30 min,ECL显色法显色并捕捉图像,Image J软件分析条带。
1.7 免疫共沉淀法评估ASK1-Trx复合体解离情况
将400 μg总细胞提取物于5 μg正常兔血清以及蛋白A/G琼脂糖凝胶亲和层析介质,4 ℃摇床孵育10 h。加入5 μg第一蛋白(即Trx)抗血清与提取物及50 μl蛋白A/G琼脂糖凝胶亲和层析介质,孵育2 h。RIPA裂解液洗涤,以14 000g离心10 min,收集免疫沉淀。SDS-PAGE法分离蛋白、电转印,用第二蛋白抗体(即ASK1抗体)对分离的蛋白行蛋白免疫印迹法检测。TBST洗涤,室温下与相应二抗孵育30 min,ECL显色法显色并捕捉图像,Image J软件分析条带。
1.8 统计学分析
本研究所得数据表示为均数±标准差,使用SPSS 16.0软件进行统计学分析。数据组间差异比较使用单因素方差分析(ANOVA)或Student-t检验。P<0.05为差异具有统计学意义。
2 结果
2.1 苦参素处理对大鼠心功能的影响
与Ctrl组相比,AGEs组大鼠LVEDP显著升高(P<0.05,见图1A),LVSP、+dP/dtmax、-dP/dtmax均显著降低(P<0.05,见图1B-D)。与AGEs组相比,苦参素处理的AGEs+L-Mat,AGEs+M-Mat及AGEs+H-Mat的LVEDP均显著下降(P<0.05),LVSP、+dP/dtmax、-dP/dtmax均显著升高(P<0.05),且具有显著的浓度依赖性(P<0.05,见图1)。
2.2 苦参素处理对大鼠心肌细胞凋亡的影响
心脏组织TUNEL荧光染色显示,与Ctrl组相比,AGEs组心脏组织内心肌细胞凋亡明显增多(见图2);与AGEs组相比,苦参素处理的AGEs+L-Mat、AGEs+M-Mat、AGEs+H-Mat组心肌细胞凋亡明显减少,且具有显著的浓度依赖性(P<0.05,见图3)。
2.3 苦参素处理对MKKs/p38 MAPK凋亡信号通路活化的影响
各组大鼠心脏组织内MKKs/p38 MAPK凋亡信号通路活化结果表明,与Ctrl组相比,AGEs组心脏组织内MKK3、MKK6以及p38 MAPK的磷酸化水平,活化caspase3的表达水平均显著增加(P<0.05,见图4);与AGEs组相比,AGEs+L-Mat、AGEs+M-Mat、AGEs+H-Mat组的心脏组织MKK3、MKK6、p38 MAPK磷酸化水平及活化caspase3水平均显著降低,且具有显著的浓度依赖性(P<0.05,见图4)。

与Ctrl组相比,*P<0.05;与AGEs组相比,#P<0.05;与AGEs+L-Mat组相比,△P<0.05;与AGEs+M-Mat组相比,○P<0.05

图2 各组大鼠心肌细胞凋亡TUNEL染色、DAPI复染及其融合图像Figure 2 The TUNEL, DAPI and merge staining of apoptosis in myocardial tissue
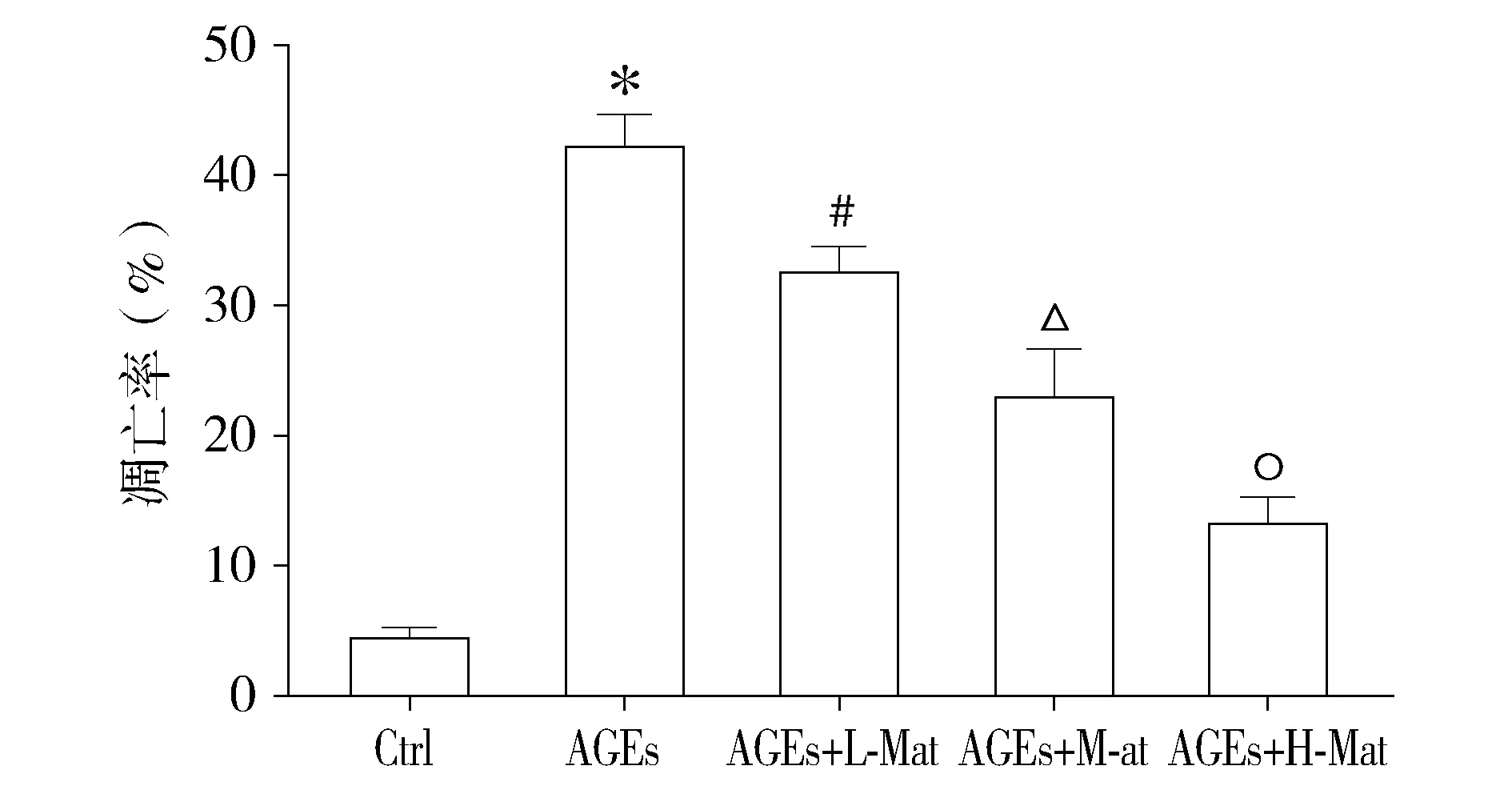
与Ctrl组相比,*P<0.05;与AGEs组相比,#P<0.05;与AGEs+L-Mat组相比,△P<0.05;与AGEs+M-Mat组相比,○P<0.05
2.4 苦参素处理对ASK1-Trx复合体解离的影响
各组大鼠心脏组织内免疫共沉淀结果表明,与Ctrl组相比,AGEs组心脏组织内ASK1-Trx复合体解离水平明显增加(P<0.05,见图5);与AGEs组相比,AGEs+L-Mat,AGEs+M-Mat及AGEs+H-Mat组心脏组织ASK1-Trx复合体解离水平明显降低,且具有显著的浓度依赖性(P<0.05,见图5)。
3 讨论
DbCM是在糖尿病患者中发生的一种特异性的心肌疾病,心力衰竭是其重要临床表现之一[3]。糖尿病造成的多种代谢紊乱可导致心肌细胞的多种病理改变,包括肥大、水肿以及凋亡等[13]。本课题组及其他既往研究表明,心肌细胞凋亡不仅是DbCM的特征性病理改变,也是导致DbCM出现心力衰竭的主要原因之一[8,14,15]。AGEs在糖尿病患者体内大量产生,近期的一些研究表明,AGEs水平升高与心功能下降显著相关且AGEs能够作为充血性心力衰竭进展的一项生物标志物[16]。本研究以AGEs处理大鼠,结果提示大鼠表现出明显的心脏收缩与舒张功能下降,同时伴有心肌组织内出现心肌细胞凋亡,提示AGEs通过诱导大鼠心肌细胞凋亡,导致有效收缩单位丧失而参与心功能受损的病理生理过程。
细胞凋亡及其调控机制非常复杂,目前认为p38 MAPK凋亡信号通路参与了该过程[17]。在正常生理状态下,p38 MAPK与其抑制因子Keap1结合而处于静息状态[18]。当受到有害因子刺激时,p38 MAPK被磷酸化而与Keap1解离从而诱导caspase3的活化进而激活整个caspase凋亡瀑布[18]。目前认为MKK3及MKK6是诱导p38 MAPK磷酸化的重要上游分子[19]。本研究的结果显示,AGEs可使大鼠心脏组织内MKK3、MKK6和p38 MAPK的磷酸化水平以及活化的caspase3水平明显升高,证实AGEs能够诱导心脏组织MKKs/p38 MAPK/caspase凋亡通路显著活化而诱发凋亡。

与Ctrl组相比,*P<0.05;与AGEs组相比,#P<0.05;与AGEs+L-Mat组相比,P<0.05;与AGEs+M-Mat组相比,○P<0.05

A.各组大鼠心肌组织免疫共沉淀结果 (第一蛋白Trx;第二蛋白ASK1)与Ctrl组相比,*P<0.05;与AGEs组相比,#P<0.05;与AGEs+L-Mat组相比,P<0.05;与AGEs+M-Mat组相比,○P<0.05 B.各组大鼠心肌组织与Trx结合的ASK1相对水平比较
值得注意的是,MKKs的磷酸化也受其上游的蛋白激酶调控,这类蛋白激酶被称作MKKK,ASK1是MKKK的典型代表之一[20]。在正常生理状态下,ASK1与其内源性抑制因子Trx结合形成复合体[21]。在有害病理因子的作用下,该复合体解离而释放出具有活性的ASK1,其能诱导MKK3及MKK6发生磷酸化[20]。本研究中通过免疫共沉淀的方法对ASK1-Trx复合体的解离程度进行评估,结果显示AGEs处理显著提高了ASK1-Trx复合体的解离程度,释放的ASK1诱导其下游的MKK3和MKK6发生磷酸化,最终导致p38 MAPK凋亡通路的激活。
近年来相关的药理学研究显示,苦参素具有多种药理学活性,包括抗炎、抗肿瘤、抗氧化以及抗纤维化等[22]。本课题组前期多项研究表明苦参素在DbCM中具有心脏保护的治疗作用,且其抗心肌细胞凋亡的活性也已得到了证实[8,14,23]。本研究以不同剂量的苦参素治疗AGEs暴露的大鼠,结果提示苦参素对大鼠心脏组织内ASK1-Trx复合体的解离具有显著的抑制作用,进而降低了MKK3和MKK6的磷酸化水平,从而进一步抑制p38 MAPK凋亡通路的活化,结果使心脏细胞凋亡水平显著降低,最终改善了AGEs诱导的心脏收缩及舒张功能不全。
总之,作为T2DM的一种标志性代谢产物,AGEs参与了DbCM心力衰竭的发生与发展过程。本研究结果提示,AGEs促进ASK1-Trx复合体解离,激活其下游MKKs/p38 MAPK信号通路,诱导心肌细胞凋亡从而诱发心力衰竭。苦参素抑制ASK1-Trx复合体解离,减少AGEs诱导的心肌细胞凋亡,减轻心力衰竭。苦参素能够通过抑制AGEs诱导的心肌细胞凋亡改善心脏收缩及舒张功能,ASK1-Trx复合体是其作用的分子靶点。
