UPLC-MS/MS法测定人血浆中金刚烷胺的含量
2018-11-02江峰
江峰
帕金森病(Parkinson disease,PD),是中老年常见的运动障碍疾病,目前以药物治疗最为有效[1]。中国帕金森指南将金刚烷胺作为首选治疗以震颤为主及年龄〈65岁的早期PD患者[2]。结合国情,金刚烷胺作为治疗PD基药[3]纳入国家医保甲类目录[4]。然其治疗窗窄,过量致昏迷、死亡[5],肾功能障碍者易蓄积中毒[6],故应开展临床用药监测。有文献报道采用LC-MS法,但存在局限性,如检测时间长(≥6.5 min)、灵敏度低、样本处理过程复杂、血浆用量较大等[7-10]。本实验建立一种快速、灵敏、操作简便的UPLC-MS/MS法,旨在为临床开展治疗药物监测和药动学探究提供方法学基础。
1 仪器与试药
1.1 仪器
Waters Acquity H-Class超高效液相色谱仪、Xevo TQD三重四级杆质谱仪、MassLynx数据处理系统(美国Waters公司);Vortex-Genie 3多功能旋涡混合器(美国Scientific Industries公司);HSC-12A恒温槽(天津恒奥科技发展有限公司);Herens Pico 21离心机(美国赛默飞世尔科技公司);AE-240电子天平(梅特勒-托利多仪器有限公司);pHS-3C型pH计(上海雷磁仪器厂);Milli-Q5 超纯水机(德国默克密理博公司)。
1.2 药品和试剂
金刚烷胺(纯度:97%,批号:MKBF8627V)购自美国Sigma公司;盐酸伪麻黄碱(内标纯度:100%,批号:171237-200304)由中国药品生物制品检定所提供;甲醇、甲酸、乙腈为色谱纯(德国默克公司),二氯甲烷(分析纯,国药集团化学试剂有限公司);超纯水(德国默克密理博公司)。
2 实验方法
2.1 对照品溶液和内标溶液的配制
精密称取金刚烷胺对照品2.33 mg,置于100 ml量瓶,用超纯水溶解并稀释至刻度,摇匀,配成浓度为23.3 μg·ml-1的金刚烷胺储备液。将金刚烷胺储备液稀释200倍配成116.5 ng·ml-1金刚烷胺工作液,备用;精密称取内标盐酸伪麻黄碱对照品1.24 mg,置于100 ml量瓶,用超纯水溶解并稀释至刻度,摇匀,配成浓度为12.4 μl·ml-1的盐酸伪麻黄碱储备液。用超纯水稀释盐酸伪麻黄碱储备液,配制成2.5 μg·ml-1的内标溶液。
2.2 色谱条件
采用Acquity UPLC BEH C18色谱柱(2.1 mm×50 mm,1.7μm);流动相为0.01%甲酸水(A)—甲醇(B)。流速:0.25 ml·min-1;进样体积:5μl;柱温为30 ℃。采用梯度洗脱,即0 min时,A:B=(80:20,v/v),1.5min 时,A:B=(10:90,v/v)2 min 时,A:B=(10:90,v/v),4 min 时,A:B=(80:20,v/v)。
2.3 质谱条件
离子源:电喷雾离子源(ESI源),多反应离子监测(MRM)正离子模式;金刚烷胺离子反应为:m/z152.2→135.48;毛细管电压3.7 kV,锥孔电压35 V,碰撞能量16 eV;内标伪麻黄碱离子反应:m/z166.29→148.29;毛细管电压3.7 kV,锥孔电压20 V,碰撞能量10 eV。
2.4 血浆样品处理
取血浆样品500 μl置10 ml玻璃离心管中,加入20 μl内标溶液(2.5 μg·ml-1),混合后加入2 ml二氯甲烷,涡旋混匀2 min,4 000 r·min-1离心5 min,取上清液1.5 ml,40℃水浴中以氮气流吹干,残渣加1 ml流动相复溶,涡旋3 min,0.22 μm微孔滤膜过滤,1 μl进样。
2.5 方法学考察
2.5.1 基质效应考察 分别取5种不同来源的空白血浆500 μl,经液液萃取N吹干后,加入流动相配置的金刚烷胺和内标伪麻黄碱混合溶液(金刚烷胺浓度依次是1、150、600 ng·ml-1每个浓度各5 管),通过UPLC-MS/MS法分析,获得峰面积,与相应浓度混合对照品溶液峰面积之比评价基质效应,结果均在88%~100%之间,结果表明,本方法金刚烷胺及其内标的测定均不受基质效应干扰。
2.5.2 标准曲线制备 取金刚烷胺工作液加入空白血浆中,配制成浓度为 0.7,2.8,7,28,70,140,280,700 ng·ml-1的含药标准血浆样品,按”2.4”处理后,再按“2.2”“2.3”条件进样测定,记录色谱图;以金刚烷胺浓度(x)为自变量,峰面积和内标峰面积比(y)为应变量,用加权(W=1/χ2)最小二乘法进行线性回归分析,得回归方程:y=0.01261x+0.01737(r=0.997 3),结果表明,金刚烷胺在0.7~700 ng·ml-1范围内(r=0.997 3)有良好线性关系,定量下限为0.7 ng·ml-1。
2.5.3 专属性试验 空白血浆、含药血浆样品(含内标)和患者血浆样品(含内标)分别按“2.2”“2.3”“2.4”方法考察血浆中内源性物质及常规合并用药是否干扰测定。所得色谱图见图1。金刚烷胺与内标的出峰时间分别为2.14 min、1.00 min;二者能很好地分离,峰形良好,无杂质峰干扰。结果表明,空白血浆中内源性物质不干扰金刚烷胺及内标的测定。

图1 金刚烷胺色谱图
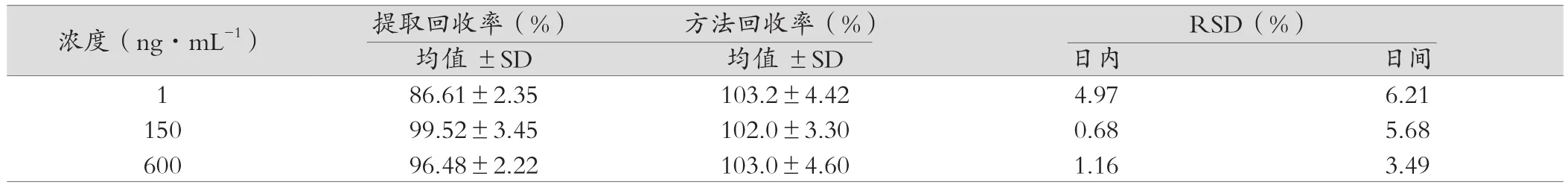
表1 回收率和精密度试验结果 (n=5)

表2 金刚烷胺稳定性试验结果(n=5)
2.5.4 回收率和精密度实验 取空白血浆,配制金刚烷胺浓度分别为1、150、600 ng·ml-1的对照品血浆各5份,按“2.4”操作并进行UPLC-MS分析,将结果与相应浓度对照品水溶液结果比较,求算提取回收率及随行的标准曲线计算方法回收率。同时,每种浓度样品在一日内平行操作测定5次,考察日内精密度。同法每日操作测定1 次,连续5日,考察日间精密度。数据见表1。
2.5.5 稳定性实验 取空白血浆配制成1、150、600 ng·ml-1的含药标准血浆样品各5份,考察样品在不同保存条件下的稳定性。结果表明金刚烷胺经过-20 ℃放置30 d,3次反复冻融,以及室温放置3 d均稳定。
3 讨论
3.1 色谱条件的选择
考察了水、0.01%甲酸和0.1%甲酸,发现流动相中加入甲酸可明显增强待测物响应,且0.01%甲酸效果优于0.1%甲酸;恒速洗脱易使金刚烷胺峰形变宽,梯度洗脱可使峰形良好。
3.2 内标的选择
通过考察伪麻黄碱对血浆中金刚烷胺测定的影响,结果表明用伪麻黄碱作内标其保留时间为1.0 min,而金刚烷胺保留时间为2.14 min,二者分离度达5.5,不会被其它杂质干扰。
3.3 生物样品处理方法的选择
比较了乙酸乙酯、二氯甲烷、乙醚、乙醚-二氯甲烷(4:1)(v/v)[11]、环己烷、正戊烷对金刚烷胺的萃取效果,以二氯甲烷效果最好,可显著减少杂质干扰,且萃取回收率最高,故选其为萃取剂。血浆样品处理参考了文献[11-12]萃取剂、涡旋时间以及流动相等并做改进,分离效果良好。
3.4 标曲范围的选择
本研究是为建立测定人血浆金刚烷胺血药浓度方法学,通过前期预实验,得金刚烷胺谷浓度范围(529.73±86.49)ng·ml-1。故选取的标准曲线范围足以用于临床对金刚烷胺的监测。
3.5 实验方法的选择
金刚烷胺临床给药剂量较低,浓度测定灵敏度要求较高,故本实验采用UPLC-MS/MS法,在3 min内完成金刚烷胺的定量分析,提高工作效率。采用MRM模式,屏蔽其他成分的影响,并用内标法定量,极大地提高准确性。
4 小结
本文建立了测定人血浆金刚烷胺血药浓度UPLC-MS/MS 法,该法快速、灵敏、准确、操作简便,可用于血药浓度监测以及药动学相关性研究。
