玉米雄穗分枝数分化发育基因研究进展
2018-11-01代资举王新涛张富才李保全
代资举,王新涛,杨 青,张富才,李保全
(1河南省农业科学院作物设计中心,郑州450002;2宝丰县农业科学研究所,河南宝丰467400)
0 引言
玉米(Zea maysL.)是一种来自中美洲高度分枝的大刍草(Zea maysssp.Parviglumis)经过长期驯化形成的[1]。在选择和驯化过程中,玉米雄穗作为产量性状重要因子是主要选择目标之一。在正常发育的玉米中,雄穗处于植株顶端,具有顶端优势,有分枝,先于雌穗发育,在养分供给上优于雌穗,因此二者间在发育中存在着竞争,同时雌雄穗的发育进程部分重叠,确保花期吻合,使得正常授粉结实[2]。玉米雄穗性状主要包含雄穗分枝数、分枝长度、分枝夹角、雄穗重、雄穗长、主轴长、小穗密度等。玉米雄穗分枝数(tassel branch number,TBN)作为衡量雄穗大小的重要指标,是玉米育种与杂交种种子生产中与产量形成有关的重要农艺性状之一[3]。Geraldi等[4]的研究表明雄穗分枝数与玉米产量呈现负相关性。然而在玉米杂交种种子生产过程中,作父本的亲本植株需要较为发达的雄穗,以利于提高制种产量[5]。同时较小适中的雄穗又是理想株型的构成要素之一,过度发达的雄穗影响株型的冠层结构,影响植株整体光能利用率[6]。因此在育种实践中选育具有适度减少雄穗分枝数的杂交种是目前玉米育种的一个趋势。前期利用‘郑单958’骨干亲本‘郑58’和‘昌7-2’构建的188个RIL家系群体,结合288个多态性分子标记构建的连锁图谱和2年玉米雄穗分枝数表型数据,共检测到5个控制玉米雄穗分枝数的一致性主效QTL,分别位于玉米5条染色体上,然后通过连续回交及分子标记辅助选择构建了位于bin5.05的控制雄穗分枝数主效QTL-qTBN5近等基因系(near isogenic line,NIL),对基因遗传效应进行了验证,并将qTBN5进一步定位在13.2 Mb区间之内[7]。由于玉米雄穗分枝数是典型数量性状,其分化发育过程受多基因控制,而且基于突变体的遗传分析方法已鉴定分离出多个控制玉米雄穗分枝数的基因,然而如何将这些基因资源应用于育种实践是关键。本文对玉米雄穗分枝分化发育过程相关基因的生物学基础进行了综述,重点描绘了控制玉米雄穗分枝数关键基因及其调控网络,为克隆玉米雄穗分枝数主效基因、挖掘玉米雄穗分枝数优异基因资源,进而为玉米产量和株型相关性状的遗传改良提供理论参考。
1 玉米雄穗分枝分化发育过程
玉米是雌雄同株,异花授粉作物,雄穗长在顶端,其发育有其独特之处。曹明秋等[8]根据雄穗分化过程将雄穗分化发育分为以下时期:生长锥未伸长期、生长锥伸长期、小穗分化期、小花分化期、性器官形成期。不同的分化历期,其生长锥变化和幼穗形态都有其特征(表1)。其中在雄穗生长锥伸长期向雄穗小穗分化期过渡期间启动了雄穗分枝的分化发育。由于玉米茎顶端分生组织(shoot apical meristem,SAM)的发育方向是不确定的,在不同生长阶段发育成不同组织。在营养生长阶段,SAM发育成叶片,在腋芽处形成新的原基。而在玉米营养生长向生殖生长转换时期,SAM转变发育成花序分生组织(inflorescence meristem,IM),IM可产生3类分生组织,分别是分枝分生组织(branch meristem,BM)、小穗成对分生组织(spikelet pair meristem,SPM)和小花分生组织(floret meristem,FM),即IM首先在主轴底部启动一些分枝分生组织(branch meristem,BM)发育成长分枝,之后产生成对小穗分生组织SPM,SPM发育成对小穗(spikelet meristem,SM),最后产生小花分生组织FM,FM最终形成小花,同时BM发育和IM相似,会产生新的分枝和SPM,随后产生SM和FM[9-12]。雄穗分枝分化发育涉及诸多基因,某些关键基因功能的变化,就可能使其不会产生分枝或者分枝过多。
2 玉米雄穗分枝数性状的QTL定位
玉米雄穗分枝数的遗传表现为主效基因+微效多基因模式,且存在小的加性和上位性效应[13-14]。随着现代分子生物技术的发展,一些控制玉米雄穗分枝数QTL被不同研究者利用不同群体、标记类型和定位方法鉴定出来。Berke和Rocheford[15]利用F2群体鉴定到3个控制雄穗分枝数QTL,分布于第2、4、7染色体上,其中第7染色体上QTL贡献率最大。Mickolson等[16]利用重组自交系(recombinant inbred line,RIL)群体,在第1、2、3、4染色体上共定位到6个雄穗分枝数QTL,其中第2染色体QTL贡献率最大。汤华等[17]利用‘N87-1’ב综3’构建F2:3群体,定位到9个雄穗分枝数QTL,分别位于第1、3、4、5、9、10染色体上,贡献率介于6.11%~12.01%之间。Upadyayula等[5]利用BC1S1家系群体,定位到2个雄穗分枝数QTL,分别位于第4、7染色体,贡献率分别为7.9%和11.7%。高世斌等[18]利用‘N87-1’ב9526’构建F2:3群体,定位到6个雄穗分枝数QTL,分布于第2、4、7、10染色体上,贡献率为5.6%~28.4%。Briggs等[19]利用玉米和类蜀黍(teosinte)构建的BC作图群体鉴定到31个雄穗分枝数QTL,玉米10条染色体上均有分布。王迪等[20]利用‘齐319’ב黄早四’和‘披478’ב黄早四’分别构建了两套F2:3群体,10条染色体上定位到40个雄穗分枝数QTL,贡献率为2.93%~23.78%。Brown等[21]利用5000份RIL组成的(nested association mapping,NAM)群体,共检测到39个雄穗分枝数QTL。杨钊钊等[22]利用以‘黄早四’为共同亲本,构建了11个不同组合的RIL群体,共定位到11个雄穗分枝数QTL,分别位于第2、3、4、5、7、8染色体上,贡献率为9.7%~20.9%。Chen等[23]利用F2群体和高密度遗传图谱检测到7个控制雄穗分枝数QTL,分布于第1、3、4、5、7、8、9染色体上。Yang等[24]利用368个自交系鉴定到30个控制雄穗分枝数QTL。Wu等[25]利用NAM群体和全基因组关联分析检测到50个控制雄穗分枝数QTL。Chen等[26]利用BC1S1和RIL家系群体定位到4个控制雄穗分枝数QTL,分别位于第2、3、5、7染色体上。而Xu等[27]利用栽培玉米和类蜀黍(teosinte)发展作图群体,利用SNP标记全基因组扫描检测到14个控制玉米雄穗分枝数QTL。代资举等[7]利用RIL家系群体,定位到5个控制玉米雄穗分枝数主效QTL,分别位于玉米5条染色体上,贡献率为5.81%~19.92%。以上研究表明玉米雄穗分枝数是多基因控制数量性状,控制该性状基因在多数染色体上都是存在的(图1),且存在主效QTL。这些定位结果不仅加深了对玉米雄穗分枝数遗传规律的理解,而且为玉米雄穗分枝数相关基因的克隆、功能分析及分子标记辅助育种奠定了基础。

表1 玉米雄穗分化时期特征
3 玉米雄穗分枝分化发育的遗传调控
玉米雄穗分枝发育涉及众多关键基因,基于突变体的遗传分析方法,已鉴定分离出多个调控玉米雄穗分枝数发育基因,如ramosa突变体,其基因突变体ramosa1(ra1)、ramosa2(ra2)和ramosa3(ra3)等,由于分生组织抑制作用解除,可以自由长出分枝,主要表现为雄穗基部分枝数和混合分枝数增多,这些混合分枝产生单个或者成对小穗,混合分枝产生的行为更像是SPM抑制丧失而非BM[28]。Ramosa突变体表型表明ramosa基因在调控玉米花序分枝分生组织中扮演着重要角色,这些基因已经克隆,其中ra1和ra3基因分别位于第7染色体的2个不同区域,ra1编码植物特有的含有一个Cys2-His2锌指结构域的类EPF蛋白转录因子,在雄穗短分枝中的小穗对分生组织的原基中表达,而ra3基因编码6-磷酸海藻糖酶(trehalose-6-phosphate phosphatase,TPP),通过合成海藻糖用以修饰进入花序分生组织的糖信号,进而调控ra1的转录活性,ra2基因位于第3染色体,是一个含有LATERAL ORGAN BOUNDARY(LOB)结构域的转录因子,在茎顶端分生组织和分枝分生组织原基中表达较高,ra2促进ra1表达以限制分生组织生长[29-30]。玉米ramosa1 enhancer locus2(rel2)基因,编码一个TOPLESS-like转录共抑制因子,其蛋白C-端的2个EAR-like模体能与RA1互作,参与生长素相关的花序发育,rel2突变体显著增强了ra1和ra2的表型,rel2:ra1和rel2:ra2双突变体表现出雄穗直立向上且分枝数多,表明REL2通过形成转录复合体来调控ra1的功能[31-33]。参与ramosa途径调控玉米花序分枝的另一个基因是sessile spikelets1(Sos1),Sos1为一个半显性突变基因,Sos1突变体雄穗不形成成对的小穗,只有少数的雄穗分枝,而Sos1和ra1相互作用后分枝数比ra1突变体少,说明Sos1对ra1存在较强的上位性,能有效抑制ra1增加雄穗分枝数的功能,在Sos1突变体中ra1表达量下降,说明SOS1通过负调节RA1参与ramosa途径,而Sos1对ra2具有增效作用,同时与ra3存在加性互作[34]。
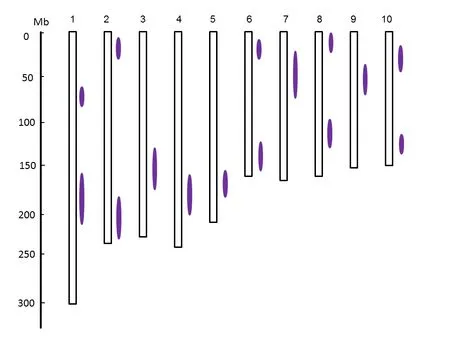
图1 玉米雄穗分枝数QTL在基因组染色体上的分布
另外一些调控玉米雄穗分枝数分化途径,如thicktassel dwarf1(td1)和fascinated ear2(fea2)分别编码拟南芥基因CLAVATA1(CLV1)和CLV2同系物,影响SAM到IM的顺利转换,其突变体表现为雄穗分枝数增加和大量小穗[35-36]。liguleless2(lg2)基因位于第3染色体上,编码一个bZIP结构蛋白,主要控制玉米叶舌和叶耳的发育,同时参与花序建成的调控,其突变体雄穗下部长分枝分化不能启始,在ra1:lg2和ra2:lg2双突变体中,雄穗虽然基部长分枝不能启始,类似lg2表型,但是上部分枝数增加,表现为ramosa表型,由此可见lg2是雄花序基部分枝发生所需要的,而且调控途径与ramosa不同[37-38]。barren stalk1(ba1)突变体雄穗只有一个主轴而没有分枝、小穗和小花,导致突变的原因是位于第3染色体ba1基因编码起始位点上游存在Helitron转座子插入,该基因编码一个碱性螺旋-环-螺旋(helix-loophelix)结构蛋白,是一个植物特有的bHLH转录因子家族成员[39]。barren inflorescence2(bif2)基因是位于第1染色体上的一个编码丝氨酸/苏氨酸激酶,参与生长素极性运输途径,影响SPM和BM的形成,bif2突变体表现为雄穗分枝难以分化、小穗和小花数减少[40]。而tasselsheath4(tsh4)、unbranched2(ub2)和unbranched2(ub3)基因是一类SQUAMOSA PROMOTER BINDING(SBP)-box转录因子家族成员,研究表明SBP转录因子与花发育等植物生长发育、形态建成、光反应及逆境协迫等相关,其单、双和三突变体表现出雄穗分枝数的显著减少,而增强基因表达可以增加玉米雄穗分枝数和花药数,提高玉米产量[41-43]。而GRF互作引子GRF-interacting factor1(gif1)在茎顶端分生组织和花序分生组织活跃分裂的细胞中表达,与ra2和ub3表达的组织区域重叠,通过直接结合花序发育关键基因ub3启动区,进而调控ub3的表达而影响玉米花序分枝数目的形成[44]。以上这些利用玉米花序突变体进行遗传分析,分离到了一批重要的控制玉米雄穗分枝数功能基因,丰富和提升了对玉米雄穗分枝数分化发育及花序建成遗传调控的认识(图2),为玉米雄穗的分子设计及产量相关性状的遗传改良提供理论指导和基因资源。
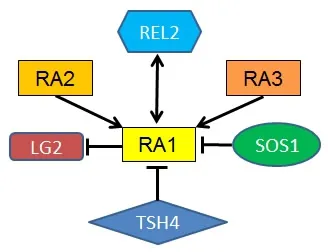
图2 玉米雄穗花序分枝调控途径
4 展望
玉米雄穗分枝数作为衡量雄穗大小的重要指标,是复杂的数量性状,其QTL定位易受到材料类型及标记密度等因素影响[45]。尽管不同的研究者在玉米10条染色体上都定位到控制玉米雄穗分枝数的QTL[14-27],但由于玉米基因组的高度复杂性、遗传背景及繁杂的遗传互作关系,使得通过传统的定位方法和有限的群体及标记很难鉴定出一致性的主效QTL,而且没有经过近等基因系、导入系、染色体片段代换系等进行基因遗传效应验证,效应大小差异较大,因此很难分离雄穗分枝发育相关基因。因此在传统定位基础上,通过发展玉米雄穗分枝数主效QTL近等基因系[7],结合QTL-seq[46]、RAR-seq[47]和 GBS[48]等新一代测序技术和基因定位分析方法,可以有效鉴定玉米雄穗分枝数主效QTL,加快雄穗分枝发育相关基因研究进程。
雄穗分枝分化发育涉及诸多基因,发育进程中某些关键基因功能的改变,就可能使其不会产生分枝或者分枝过多。尽管一些调控玉米雄穗分枝数发育重要基因,基于突变体遗传分析法结合图位克隆的策略被分离出来,这些基因功能的缺失或者改变都使得玉米雄穗分枝数发生了改变,对阐释分枝分化基因调控起到重要作用,但这些突变体材料通常呈现出极端表型,不仅雄穗分枝数改变,同时表现出其他一些农艺性状的改变,如雌穗、株高等重要性状[28-44],不能直接应用于玉米育种实践,因此需要通过广泛的表型变异寻找单一精确的表型类型。为此,一方面可以通过基因编辑技术改造玉米雄穗分枝分化关键基因结构创造新的变异,另一方面根据这些基因特征通过自然群体去寻找新的等位变异,如通过自然变异分离出的弱突变等位基因FEA2和FEA3[38,49],然后经过这些优良等位变异的评估、组装分析,找出最优组合,不仅可以加深对雄穗分枝数发育调控网络的理解,而且拓宽携带优异等位基因种质资源的利用空间,为适宜大小的玉米雄穗分子设计奠定基础。
