光催化降解水体有机污染物的研究进展
2018-10-18任向红刘建友
周 锋,任向红,刘建友,刘 嫔
(火箭军工程大学 装备管理工程系,西安 710025)
近年来,水体环境和水资源污染问题日益严峻,全球化趋势日益明显[1]。光催化技术作为一种低成本、高效、安全的环境友好型环境净化技术,被认为是全球面临严峻的能源危机和环境污染问题最好的解决方式之一。光催化材料是该技术发展的重中之重,光催化以半导体材料TiO2的研究最多,但其本身具有只对紫外光有响应且量子效率不高的局限性。
太阳辐射能主要集中在可见光区(400~760nm) 约占50%和红外区(>760nm)约占43%,而紫外区(<400nm)很少,约占7%。为了提高太阳能利用率,研究者趋向于对TiO2进行改性或发展新型光催化材料来拓展光催化材料的光响应范围,以及提高材料的量子产率和稳定性。本文以可见光响应范围为主,对近年来国内外光催化技术的发展现状、光催化材料、光催化材料发展存在的问题及发展趋势等方面进行了综述。
1 光催化发展现状
通过对常用的Elsever,Wiley,ACS,RSC等数据统计光催化领域的发文趋势,1998年至今,近20年来与之相关的发文量逐年递增,反映了人们在光催化领域的研究和关注热度持续升高,其中,中国在光催化领域的科研热度远远高于其他国家和地区。目前光催化的应用研究非常广泛,有光催化降解有机污染物、光电解水制备氢气、抗菌材料、自清洁材料、太阳能电池、医学应用等方面,而诸多的应用研究主要依赖于材料体系的研发。本文讲述的材料体系以光催化降解有机污染物方面的应用为主。
2 光催化材料
光催化材料是指一类在光照作用下可以引发或诱发其他物质的氧化-还原反应的材料,以半导体光催化材料为主。目前,光催化材料的报道非常多,有TiO2、非TiO2氧化物、Ag@AgX、CdS、铋酸盐、钴酸盐、磷酸盐以及石墨相氮化碳(g-C3N4)等,但各种光催化材料的光响应程度、制备工艺、光稳定性、经济成本等优缺点各不相同,因此,当前的研究倾向于修饰改性的复合型光催化材料体系。
2.1 光催化的基本原理
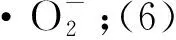
有机物+·OH → CO2+H2O+其他产物
由此看出,光催化剂主要是通过光生载流子进行氧化还原反应的,影响光催化活性的因素主要有:(1)光响应范围;(2)产生光生载流子的效率,即量子产率;
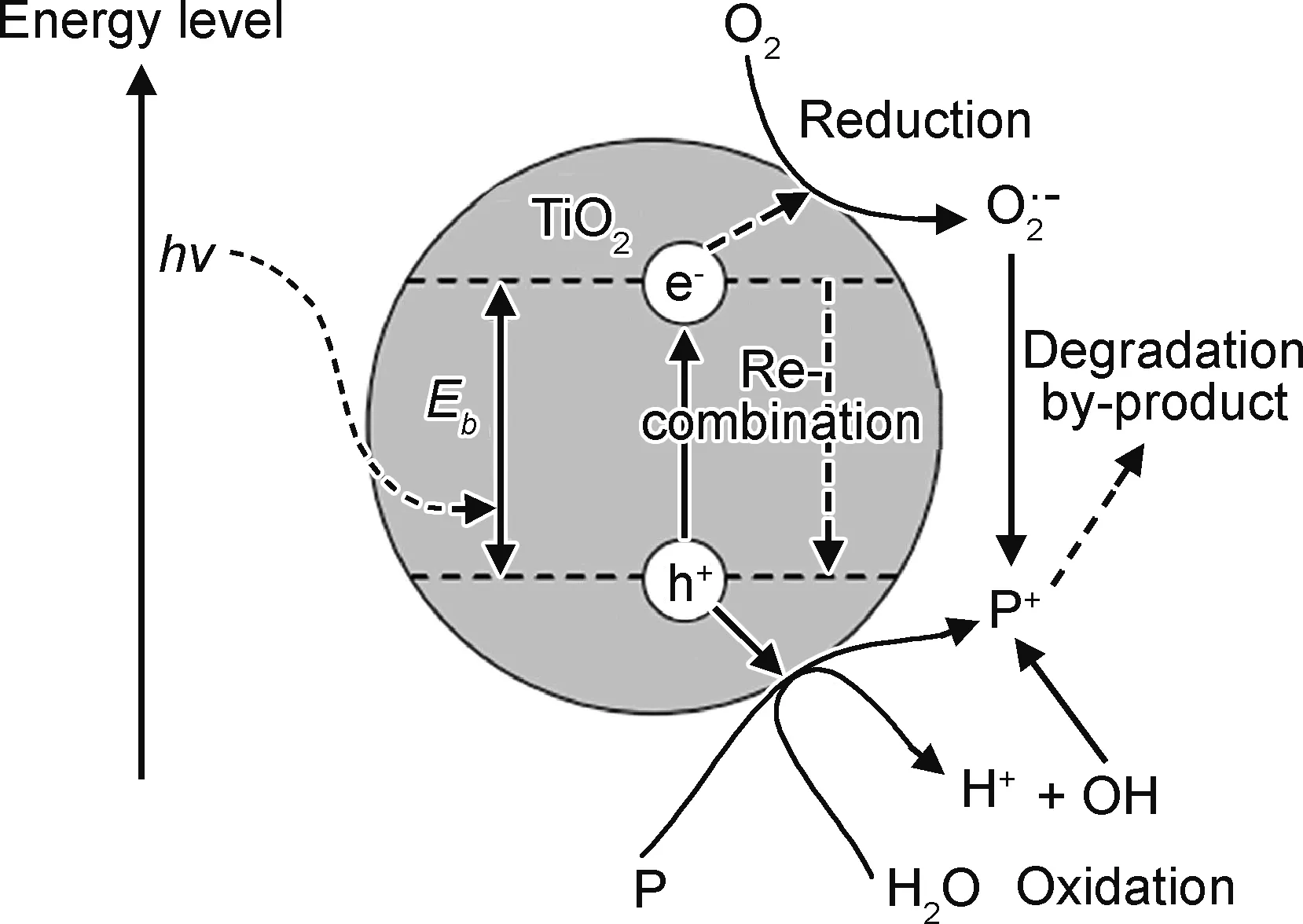
图1 光生电子-空穴的作用机理[3]Fig.1 The mechanism of photoelectric-cavitation[3]
(3)光生电子-空穴对的复合速率,即光生载流子的寿命;(4)需要克服光腐蚀作用,即稳定性。
2.2 光催化材料的分类
本研究根据材料的物质成分对其进行分类,可分为二氧化钛(TiO2)、非TiO2氧化物、硫化物、卤化物、铋基材料、杂多酸、石墨相氮化碳以及金属-有机骨架材料等。
2.2.1 二氧化钛(TiO2)
2.2.1.1 传统TiO2
TiO2是最为常见、研究最多的光催化材料,具有经济、绿色、耐腐蚀、光催化活性强等特点,有锐钛矿、板钛矿和金红石3种晶型,均是由TiO6八面体基本结构单元组成,其中,锐钛矿TiO2光催化活性最好,如Zhao等[4]制备了TiO2/CA (海藻酸钙)薄膜,在紫外光下120min对甲基橙(MO)的降解率达到82.25%,具有很好的热稳定性,且重复回收效果较好;另外,该课题组用分子印迹技术制备了在TiO2/CA表面印迹MO分子的复合膜[5],发现在紫外光下对MO的选择性吸附降解(98.12%)优于甲基红(MR),且具有较好的稳定性。但锐钛矿TiO2的带隙较宽 (3.2eV),只对紫外光响应且量子产率较低,所以,近年来对TiO2的研究多集中在对其进行修饰改性以提高量子产率和拓展其光响应范围。
2.2.1.2 黑色TiO2
氢化是通常被用来引入Ti3+或者其他还原位点,以及改变材料的物化性质,即一定温度下在含有氢气或者氢等离子体环境中对材料进行处理。2011年陈晓波教授等[6]通过氢化处理制备出黑色TiO2,发现氢化处理后形成了晶型无序的核壳纳米粒子,显著地改变了TiO2的结构、化学、电子以及光学性质,其光吸收范围延伸到了可见和红外光区域,同时具有结构和化学缺陷、更强的导电性。这一发现为TiO2材料的发展带来了新的希望,并引起了全世界广泛的科学研究兴趣。另外,还可以通过还原、氧化等方法处理得到黑色TiO2。Liu等[7]在氩气氛围下通过化学还原法成功合成了一种3D介孔结构的黑色TiO2复合型材料(TiO2/MoS2/TiO2),发现在可见光范围内其对MO的光催化降解率可达89.86%。
2.2.2 非TiO2氧化物
非TiO2氧化物光催化剂有ZnO,Cu2O,Ag2O,Fe2O3,SiO2,SnO2,WO3等,其中,ZnO是典型的单组分非TiO2氧化物半导体,其与TiO2禁带宽度以及能带位置最为相近,且具有更为丰富的形貌结构可调性,但依然存在光响应范围窄的缺点。
为了拓宽光催化材料光响应范围,研究人员采用掺杂、表面修饰或复合等方法制备了一系列的光催化材料,如ZnO-GaN异质结纳米薄膜、ZnO-Ag-GO薄膜、CuO-TiO2-ZnO三元纳米复合材料、α-Fe2O3@SnO2@Cu2O三元异质结材料、Y2O3@TNSs纳米片等。SnO2,WO3,Y2O3等光电活性系列氧化物半导体材料均可通过复合或掺杂等方法提高其催化活性。
2.2.3 硫化物
改变阴离子提升价带位置可以实现带隙减小以拓展光响应范围成为提高光催化效率,硫属化合物即为经典代表。CdS,ZnS即为硫化物光催化剂的典型代表,CdS 的禁带宽度为2.5eV,能带比ZnS(3.6eV)窄,对可见光响应,但容易发生阳极光腐蚀。研究者发现通过掺杂、负载或复合等方法可以提高硫化物的稳定性,如Qin等[8]将硫化物负载在氧化石墨烯上对硫化物的活性进行改进,制备了ZnS/RGO复合材料,有效提高了对降解MO的光催化活性。这是因为氧化石墨烯为空间网状结构,可以为半导体光催化剂分散的附着位点,使底物与催化剂的接触面积更大;且石墨烯的良好导电性可以加速载流子的运输,可以有效阻碍光腐蚀的发展从而提高光催化剂的稳定性。Yan等[9]用水热法制备得到CdS/CoWO4异质结构,其对亚甲基蓝(MB)的降解率达到了83%;Anjum等[10]制备了ZnO-ZnS/Ag2O-Ag2S纳米复合材料并发现其对邻氯苯酚的降解率最高可达96%。
2.2.4 卤化物
一些金属颗粒在特定频率的光辐射下,会发生表面等离基元共振效应,如Pt,Au及Ag的纳米粒子,其价电子抵抗正电荷回复力形成耦合作用而出现附加光吸收峰。以AgX为例,在光照下能够原位生成与母体紧密接触的金属Ag形成Ag@AgX材料体系,由于AgX光化学活性很强,而存在稳定性不够的问题。但是从纳米结构的设计调控以及负载非贵金属及非金属等方面形成的复合材料可以有效地提高其光催化活性及稳定性,如Dong等[11]通过N掺杂石墨烯复合AgX@Ag (X=Br,Cl),有效提高了AgX@Ag光催化体系的稳定性和可见光催化活性,对罗丹明B(RhB)的降解率可达86%和89%。
2.2.5 石墨相氮化碳(g-C3N4)
2009年,Wang 等[12]发现石墨相氮化碳(g-C3N4)的光催化性能,该体系就引起了人们极大的研究兴趣。g-C3N4是一种非金属半导体光催化材料,其带隙约为2.7eV,故对可见光有响应,对酸、碱、光具有很好的耐腐蚀性,且结构和性能易于调控,但依然存在量子效率低的问题。目前,提高g-C3N4量子效率的途径主要有金属元素掺杂、碳材料复合、半导体材料复合、导电聚合物复合、形貌控制、结构控制及制备方法改进等。如,左士祥等[13]以凹凸棒石为骨架制备了Ag@AgBr/g-C3N4—凹凸棒石复合脱硫光催化剂(Ag@AgBr/FCN-ATP),在可见光下对二苯并噻吩(DBT)光催化氧化脱除,结果表明其脱硫率可达85.2%;他们认为这是由于Ag 与 DBT 中的S 形成σ配位键吸附作用,Ag@AgBr和 FCN-ATP 之间的异质结构具有良好的光学吸收特性,而内电场和匹配的能带结构的协同作用提高了光生电子和空穴的分离效率。
另外,Wang等[14]认为Z型g-C3N4/WO3的复合半导体可以加速电荷分离,相对单一的g-C3N4和WO3降低了电荷复合率,从而提高光催化活性,故g-C3N4的Z型半导体材料成为最近的研究热点。
2.2.6 铋基材料
铋基材料具有储量丰富、无毒、耐光腐蚀等优点而受到人们的广泛关注。由于Bi3+具有充满的6s2电子构型,可与O的2p轨道发生部分重叠而使半导体中的价带顶端向上移动,使Bi(Ⅲ)化合物的禁带宽度降低,而表现出良好的可见光响应光催化活性;此外,Bi5+具有空的6s轨道,也会影响能带位置使响应范围向可见光区红移。目前,铋基光催化剂主要包括铋的氧化物(Bi-O)和硫化物(Bi-S)、含铋的多元金属化合物(Bi-X-O,X=Ti,W,V,Nb,Mo,Fe,Y)以及铋的卤氧化物(Bi-O -Y,Y=F,Cl,Br,I)。由于各种晶相的Bi2O3存在光量子效率不高、结构不稳定的问题,故当前的研究多集中于含Bi多元金属化合物,Zhao等[15]制备的Z型 Bi12GeO20/g-C3N4异质结构复合材料在降解RhB及还原Cr(Ⅵ)表现出很好的光催化活性,除此之外,还有钛酸铋、钼酸铋、钨酸铋、钒酸铋、碱式碳酸铋及含铋卤氧化物等。目前,为了拓展铋基光催化材料的光催化性能,利用复合的方法将含铋化合物半导体与导带位置较负的半导体复合构成Z型光催化剂是拓展铋基材料的有效方法之一。
除了铋基材料外,过渡元素钴基光催化材料的研究也较多,如钴的磷酸盐、甲基磷酸盐及硼酸盐等,主要应用于光解水方面,而对有机污染物降解方面的研究还比较少。
2.2.7 Ag3PO4材料
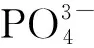
但是,Ag3PO4晶体存在物化稳定性不够、可见光辐照下易被腐蚀的缺点,故当前的研究多集中在对其修饰改性上,主要有形貌控制,纳米金属颗粒沉积,与其他半导体材料复合如石墨烯,TiO2,ZnO,Fe3O4,AgX,BiPO4等,以提高对可见光响应范围并改变其与周围环境之间的电荷转移特性,从而改善其光催化活性。
2.2.8 杂多酸材料
多酸又称多金属氧酸盐(polyoxometalate,POM),可以分为同多酸和杂多酸,其中光催化材料以杂多酸为主。杂多酸是由杂原子(P,Si等约70种)为中心和配原子(如Mo,Fe,W等)按照一定的结构,通过氧原子配位桥联组成的一类含氧多酸,其中配原子主要有V,Nb,Ta,Mo,W等元素,杂原子有很多种,几乎囊括第一、二、三过渡元素以及部分金属、非金属元素,且杂原子可以以不同的价态存在同一体系中。POM具有明显的结构特点:一般杂原子与配原子的比值是一定的,且配原子一般呈现八面体配位形成边角相连的金属-氧簇八面体MO6,每3个八面体共边相连组成三金属簇(M3O13),三金属簇之间共角相连,与杂原子组成中心多面体,主要有四面体,如Keggin结构和Dawson结构;八面体,如Anderson结构和Waugh结构;二十面体,如Dexter-Silverton结构;此外,还有Strandberg结构和Yamase 结构等。杂多酸的结构通常为纳米级,具有类似半导体金属氧化物结构,存在能带和导带之间的禁带,受特定波长光照POM中的M-O-M桥键上的O2p的电子向过渡金属M5d空轨道跃迁,即由充满电子的高分子轨道(HOMO)跃迁到空的低分子轨道(LUMO),而形成电子-空穴对,如图2所示,可以看出杂多酸光催化降解有机物的机理与二氧化钛是一致的。
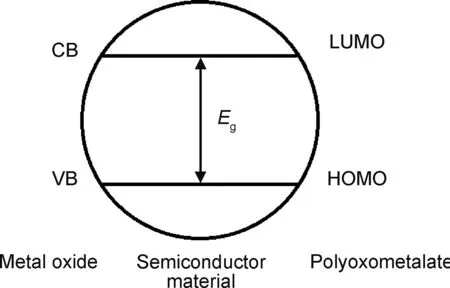
图2 半导体与多酸价带结构对比图Fig.2 Comparison of band structure of semiconductor and POM
杂多酸具有强酸性质、强氧化性、较好的化学稳定性和光催化活性,以及材料制备反应条件温和,不腐蚀设备等优点,使其成为一种新型的绿色多相高效催化剂,在光催化降解农药、有机染料、有机卤化物以及气态有机物等方面具有良好的应用前景。常见的杂多酸光催化材料有H3PW12O40,H4SiW12O40,K4W10O32,K6[MnSiW11O39], NdPW12O40-TiO2复合催化剂等。胡美琴[20]制备了铁取代杂多酸盐(PW11Fe)替代传统Fenton反应中的Fe3+,与H2O2构成一个新颖的光催化体系,发现在可见光(λ≥400nm)下可以有效降解染料X3B和MO,由于可见光吸收较弱,则以碘作为可见光敏化剂,构建NaI/H2O2/PW复合体系有效地实现了2,4,6-三氯苯酚的可见光(λ≥450nm)降解。另外,POM可以与传统光催化剂复合,如Tan等[21]制备了复合型POM/TiO2光催化剂,通过降解甲苯的实验,发现在紫外光照射下,其光催化活性远远高于单独的TiO2。但杂多酸材料体系仍然存在其本身可见光活性不强和固定负载的问题。
2.2.9 金属-有机骨架材料
金属-有机骨架材料(metal-organic frameworks, MOF)是以金属阳离子为节点、有机配体为连接体的多孔配位聚合物的总称。其具有超高的比表面积、丰富的拓扑结构,且兼具有机化合物的可剪裁修饰、易调变的特性和无机化合物的稳定性。作用机理以Bi2MoO6/UiO-66(Zr)的MOF型材料体系[22]为例,如图3所示。
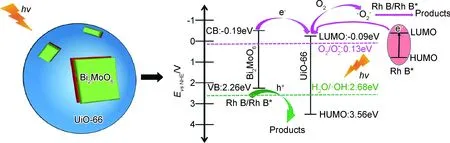
图3 Bi2MoO6/UiO-66(Zr)降解RhB的机理 [22]Fig.3 Mechanism of degradation of rhodamine B by Bi2MoO6/UiO-66(Zr)[22]
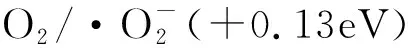
其可能的反应过程如下:
RhB+hv→RhB*→RhB+·+e-
(1)
Bi2MoO6+hv→Bi2MoO6(h++e-)
(2)
UiO-66(Zr)+e-→UiO-66(Zr)(e-)
(3)
O2+UiO-66(Zr) (e-)→·O2-+UiO-66(Zr)
(4)
·O2-+Rh B/Rh B+·→CO2+H2O+其他产物
(5)
Bi2MoO6(h+)+Rh B/Rh B+·→CO2+H2O+其他产物
(6)
美国化学会(ACS)公布当前化学领域十大热门研究课题中涉及“MOF”材料的就有两个,“筑网化学”与“金属有机骨架(MOF)和共价有机骨架(COF)应用”。筑网化学即利用分子键的强大功能将分子链接起来,构建成块状晶体开放框架,其代表产物MOF和COF多孔材料成为当下最受欢迎的新型材料。绝大多数金属离子都可以被选作合成MOF的节点金属离子;常见的有机配体主要有芳香类多羟酸化合物和含氮杂环类(吡啶、咪唑、三氮唑、四氮唑、嘧啶、吡嗪)化合物等。应用于水体有机污染物降解的常见MOF材料有ZIF系列、MIL系列和UiO系列等,如表1所示[23-32]。

表1 一些可见光响应降解水体有机污染物的MOF材料Table 1 Some visible-light-driven MOF materials for the degradation of water organic pollutants
与传统半导体光催化材料相比,MOF材料具有可以在分子水平进行灵活调控的优点,其结构上的确定性将有利于催化剂界面电荷迁移和光催化机理的研究。
2.3 光催化材料的修饰改性
光催化材料的修饰改性方法有元素掺杂、贵金属沉积、染料敏化、形貌结构调控以及与其他半导体复合等途径来拓宽光响应范围和抑制载流子复合以提高光催化活性。
2.3.1 元素掺杂
通过能带结构调控以降低半导体带隙是拓展光响应范围的有效途径之一,而掺杂其他元素即引入杂质能级是最为常见的方法,元素掺杂具有简单易行、操作简便、适于产业化推广应用等优点。按掺杂元素类别可以分为金属掺杂、非金属掺杂和联合掺杂。
金属掺杂,以过渡金属元素较多,如Cr,Mn,Fe,Co,Zr,Mo,Ru,In,Cu,Mg,V等,多价态的过渡金属掺杂改性可以使光催化剂存在晶格缺陷或产生不同的结晶度,能够有效抑制光生电子空穴的复合;有研究[33]证明过渡金属离子同时还能扩展光吸收范围。另外,还有稀土元素掺杂和贵金属掺杂。稀土元素如Ta,Pr,Ce,Eu,La等,也能有效抑制光电子空穴的复合,这是由于稀土元素的4f轨道未充满,可接收和传输光生电子,导带成为电子的捕获陷阱,稀土离子的价带顶成为捕获空穴的陷阱,促使载流子有效分离迁移至表面参与反应;贵金属如Ag,Au,Pt,Pd,因其负载半导体表面容易形成电子集体震荡而产生等离子共振,进而提升光生电子-空穴对的分离效率,Pan等[34]通过计算证明了金属原子Pt,Pd等镶嵌到g-C3N4的三角孔隙中能够降低带隙能而增加光吸收范围,并提高了载流子迁移率。
非金属掺杂,主要有C,N,S,P,B,F等,以此引入杂质能级,通过更低能带的形成而降低半导体带隙,一般以降低导带顶带为主,并为光生电子提供供体和受体,进而增强半导体材料对可见光的吸收;其中,C元素主要依靠其较好的导电能力和价电子存储能力而吸收电子,进而提升光生电子和空穴分离效率。
由于单一元素掺杂容易受到其自身属性的局限,如金属元素掺杂容易形成潜在的载流子复合中心,因此,掺杂浓度必须控制在较小范围内,如果浓度过高会产生金属簇,阻塞半导体的表面,进而减少光的吸收和降低光催化效率。为了获得更优的光电性能,于是出现了多种元素联合掺杂,其中,以金属/非金属联合掺杂的研究较多,这是由于金属和非金属元素分别具有不同的导带和价带能带属性,两者之间可以形成协同作用,而获得更好的可见光响应或促进光生载流子的有效分离。常见的掺杂型催化剂及降解水体有机污染物效果,如表2所示[11,35-60]。

表2 常见掺杂型可见光催化剂及降解水体有机污染物的效果Table 2 Common visible-light-driven doped photocatalyst and the effect of degrading organic pollutants in water
2.3.2 贵金属沉积
贵金属沉积是以单质纳米颗粒形态沉积在半导体材料表面对光催化材料进行修饰改性的。当贵金属粒子(Ag/Au/Pt)受到光照时,在入射光子的频率与金属内的等离子体(电子云)振荡频率一致时会产生共振耦合,而表现出对入射光具有很强吸收作用,即局域表面等离子体共振(SPR)效应,与半导体复合则形成表面等离子体光催化材料,如Ag@AgX(X=Cl,Br,I)就是典型的等离子体光催化材料,还有Ag/TiO2,Au/TiO2,Pt/Bi2WO6, Au@ZnO等。
贵金属沉积的光催化反应机理一般认为是:贵金属在可见光作用下发生表面等离子体共振效应,可以促进光生电子从金属脱离,在费米能级的作用下直接迁移到半导体的导带,相应地在金属表面留下空位。Dai 等[61]利用第一性原理的理论计算对贵金属-载体界面的电子迁移过程进行了比较系统的研究,验证了这一机理,同时还发现表面等离子体光催化材料的光催化机理与载体本质属性、贵金属/载体的界面均存在很大的关联。目前,为了能更好地研究体系反应机理,研究者倾向于能够设计和精确控制等离子体材料体系结构的原子层沉积(ALD)方法进行贵金属沉积的修饰改性。
2.3.3 染料敏化
染料敏化,也称表面光敏化,即将光活性化合物化学吸附或物理吸附在光催化剂的表面,可以拓宽激发波长范围,实现可见光响应,从而提高光催化氧化的效率。其作用机理是染料分子被激发后向半导体的导带注入电子实现电荷分离,同时能够活化空气中氧分子,进而氧化分解有机染料污染物,如图4所示[62]。其降解机理与传统光催化的本质区别:不涉及半导体的带-带吸收以及空穴的生成和反应,而是染料分子吸收可见光诱发活性自由基和分子氧的共同作用降解污染物,常见的敏化染料有赤藓红、硫堇、曙红 Y等。

图4 染料敏化半导体光催化机理[62]Fig.4 Mechanism of dye sensitized semiconductor photocatalysis[62]
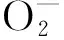
2.3.4 形貌结构调控
非均相光催化反应主要发生在界面,使反应物在催化剂表面充分吸附是提高催化速率的关键因素,而通过对催化剂的尺寸及结构进行调控增加催化剂颗粒的比表面积是提高光催化效率的有效途径之一。一般而言,催化剂的粒径越小,越有利于吸收光子,也越有利于光生电子与空穴的分离;其比表面积越大,则越有利于有机污染物分子的吸附,能够提供更多的光催化反应中心。
研究发现当半导体材的颗粒尺寸降低到纳米范围,特别是小于或等于盖茨阿里的激子波尔半径时,会产生量子尺寸效应。张光友等[64]采用溶胶-凝胶法制备了纯纳米TiO2进行光催化降解偏二甲肼污水,实验证明该技术对偏二甲肼污水具有良好的降解效果。这是由于纳米级半导体粒子具有量子尺寸效应,可将纳米颗粒形象称为量子点,一方面使材料体系的导带和价带能级变为分立的能级,带隙变宽,导带与价带电位差变大,进而提高氧化还原能力;另外,会伴随出现较强的激子共振,光生电子-空穴能够高效分离,进而提高量子产率。
由于粒径小容易导致催化剂团聚,影响光催化材料对光的有效吸收及与反应物的充分接触,于是出现了纳米线、纳米管、纳米棒,但是这些材料体系的后续分离和回收比较困难,而纳米负载型材料和纳米管阵列材料则很好地解决了这一问题。Mehdi等[65]制备的MWCNT/TiO2的纳米复合材料,通过实验获在最佳条件下对浓度在10mg/L以下的四环素能100%降解,且对0.5, 0.8mg/L的降解能在10min内完成,而对20, 30mg/L的四环素在100min内的降解率分别为98.2%, 92.8%。另外,该光催化材料体系对现实制药废水表现出了很好的降解效果,在240min内废水的COD从2267mg/L降到了342mg/L,TOC从1295mg/L降到了228mg/L。Mariusz等[54]利用电化学氧化法制得系列N, I, B掺杂的TiO2纳米管阵列,通过实验发现掺杂型TiO2纳米管阵列较纯TiO2纳米管阵列的带隙能都降低了,其中以B-TiO2材料体系的光催化性能最好,在MB溶液体积与光催化剂的几何面积比为30mL/2.5cm2时,150min内对 MB降解效率在90%以上。
此外,近年来多级孔催化复合材料体系的研究也很多,这是由于其兼具微孔、介孔、大孔,对小分子、大分子的催化作用是全方位的,且孔道分布更加优化,催化性能往往优于常规的催化剂。
2.3.5 复合半导体
半导体复合,即与其他半导体形成异质结构,是一种灵活可控的光催化材料修饰改性方法,基本原理是当两种成分不同半导体材料接触后,其费米能级将会相向移动,最终稳定在同一位置,从而改变其体系的带隙;另外,在两相界面处会出现电子和空穴的交换,形成空间电荷区,半导体材料受到入射光激发产生的电子和空穴在空间电场的协助下,能够发生高效快速的分离。
2.3.5.1 一般半导体复合
半导体可以区分宽带隙半导体和窄带隙半导体,从而可以根据需要进行相互修饰,可以宽带隙半导体有效抑制电子和空穴的复合,提高光催化效率;窄带隙半导体修饰,其不仅可以抑制电子和空穴的复合,还可以拓展光催化材料对光的响应范围,提高光能的利用效率。CdS /TiO2复合光催化剂体系即为经典的二元半导体复合异质结构,可见光照射激发CdS使e-从其价带跃迁到导带,对应产生的h+则留在CdS的价带,e-迁移到TiO2的导带上。这种迁移有利于电荷的分离,从而提高光催化的效率,由于此类材料的能带分布存在势差,会造成氧化还原能力分布不均或者相互抵消而降低体系的光催化活性。此外,复合半导体有很多,比如ZnO-ZnS/Ag2O-Ag2S[10]等。
近年来,随着石墨烯等碳材料的蓬勃发展,其在光催化领域的研究也越来越多。这是因为碳材料通常具有大比表面积,吸附能力强,将碳材料吸附和半导体光催化结合,可以提高光催化剂吸附容量和可见光降解效率,而如碳纳米管,石墨烯,C60,g-C3N4等。这种微纳复合材料可以同时完成污染物的吸附和降解,完全降解水中的污染物,并且不需要后期处理即可以重复利用。张平等[66]制备了一种磁响应TiO2/石墨烯纳米复合材料,对20mg/L亚甲基蓝溶液的降解率可达92%以上,且通过磁性回收利用降解率依然可以达到90%。
2.3.5.2 Z型复合半导体
Z 型光催化体系(也称Z型异质结),它包括两个光系统(光系统Ⅰ,Ⅱ)的光激发过程和一系列氧化还原中间体的转换。其既能保证宽的光响应范围,又能提高材料体系的氧化还原能力,相对于单一半导体材料光催化性能得到了明显提升。该体系使为光催化材料的选择性和设计空间更大了,因为Ⅰ,Ⅱ部分只需分别满足各自响应的光激发过程和对应的半反应,在不同光催化剂上分别完成还原和氧化过程,可以有效抑制逆反应的发生,且光生电子与空穴能够有效地分离与传输,使光催化体系的稳定性随之增强。
目前,具有良好导电性的Au,Ag,Cd,W 等金属和层状石墨烯RGO可作为全固态Z 型光催化材料光生载流子的传输介质,如图5所示。如Hua等[67]通过Ag2MoO4和Ag3PO4的溶液相反应法合成了Z型Ag3PO4/Ag/Ag2MoO4复合光催化剂对RhB,MO和MB表现出优越的光催化降解性能,可见光照射5min其降解效率分别达到了95%,97%和90%,并表现出较高的稳定性。目前,用于光催化降解有机污染物的固态Z型光催化材料体系已经有一些[68],但材料体系作用机理和材料体系的拓展有待进一步探索研究。

图5 全固态Z模型体系(a)PSI-PSII;(b)PSI-Au-PSII; (c)PSI-RGO-PSII[68]Fig.5 All-solid Z model system (a)PSI-PSII;(b)the PSI-Au-PSII;(c)the PSI-RGO-PSII[68]
3 结束语
近年来,光催化技术作为解决全球范围日益严峻的能源危机和环境污染问题的有效途径,人们的研究热情逐年高涨,也取得了很多的研究成果,但在光催化降解有机污染物方面,依然存在太阳能利用率低、量子产率低、光生电子-空穴的有效分离以及光化学稳定性的问题。
(1)二氧化钛及其他氧化物、卤化物等材料体系的研究多集中在通过掺杂、敏化、复合以及形貌调控手段来拓展其光响应范围,如二氧化钛经“黑化”处理的光响应范围向红外区拓展,而硫化物能对可见光响应但容易发生光腐蚀,稳定性不够。
(2)近年来,一些新兴光催化材料体系越来越受研究者关注,如铋基材料、石墨相氮化碳、Ag3PO4系列、杂多酸(POM)、金属-有机骨架材料(MOF)以及石墨烯等。其中,g-C3N4材料和铋基光催化材料体系能够对可见光响应,但存在量子产率低的问题;杂多酸(POM) 材料体系对可见光吸收相对较弱;金属-有机骨架材料体系由于其结构上的确定性有利于催化剂界面电荷迁移和光催化机理的研究而成为科学家的“新宠”,但这些新型材料光催化降解有机物污染物的机理还有待进一步探索研究。
(3)所有材料体系的修饰改性方法基本上是一致的,但各种方法都存在一定的局限性:元素掺杂和贵金属沉积需要精确控制用量范围;染料敏化则存在材料本身的稳定性不够的问题;形貌结构调控以纳米级为主,但纳米颗粒不利于回收,而负载型纳米光催化剂难以保持较高的光催化活性等问题;且修饰手段的改性机理还没有达到共识,比如N掺杂型材料的有机污染物降解机理等。但Z型复合半导体因其结构的特殊性为材料体系的改性提供了很大的设计空间。
(4)目前,大多数材料体系多为实验室环境研究,研究成果向工程化应用转化还缺乏一定的实践经验。本文介绍的9类所有的光催化材料中,通过研究比较可知,单一组分材料性能都存在缺陷,所以,多元复合材料体系将是今后的一个发展趋势,如金属-有机骨架材料体系、微纳米介孔材料体系、多级孔复合材料体系和Z型半导体等。另外,实际上水体环境是复杂多变的,光催化剂对同时处理大量存在的重金属和多样的有机污染物以及反应过程中的各种物质、环境条件等相互之间协同机理还需要进一步探索研究。
