煤对CO2的解吸实验及热力学参数研究
2018-10-18任立峰吴明明翟小伟
邓 军,任立峰,吴明明,马 砺,翟小伟
(1.西安科技大学 安全科学与工程学院,陕西 西安 710054;2.西安科技大学 陕西省煤火灾害防治重点实验室,陕西 西安 710054;3.鄂尔多斯市营盘壕煤炭有限公司,内蒙古 鄂尔多斯 017300)
0 引 言
燃烧化石燃料排放大量温室气体CO2,已造成严重的温室效应[1]。为了减少CO2等温室气体的大量排放,有学者提出了利用深部煤层储存CO2进而增产煤层气的方法[2],不仅减少了温室气体CO2排放量,而且促进煤层气开采[3]。CO2被用于各种煤自燃火灾的治理中并取得了良好的效果[4]。因此,研究CO2与煤的吸附解吸机理就显得尤为重要。Busch A等研究发现CO2和CH4在解吸等温曲线位于吸附等温线的上方[5]。张子戌等研究得到CH4和CO2混合气体的解吸曲线都滞后于吸附曲线,解吸过程中游离相中的CO2浓度低于原始混合气体[6]。Wang等发现80%CH4+20%CO2二元解吸试验表明解吸过程中气体组成的变化是非线性的[7]。马东明等研究得到煤对CO2解吸的吸附热为115.03 kJ/mol[8]。祝捷等研究得到Langmuir方程可以反映煤样吸附/解吸变形随气体压力的变化规律[9]。邢万丽等得到CO2解吸过程中受煤基质膨胀的影响粉煤中CO2的有效扩散系数随压力增大而减小[10]。李全中等得到在超临界条件下,煤对CO2的吸附/解吸数据符合Gibbs吸附理论,吸附量随吸附压力的增大符合先增大后减小的趋势[11]。高莎莎等研究得到在低温低压条件下CO2和CH4置换吸附/解吸过程主要向解吸需要热量低的方向、吸附释放热量高的方向进行[12]。煤的含水量,粒度变质程度等会对煤吸附气体的特性产生影响[13]。Xia等采用密度泛函理论(DFT-D)研究得到含氧官能团与CO2分子之间形成的氢键抑制CO2解吸作用[14]。Liu等研究得到含氧官能团抑制煤中微孔对CO2解吸[15-16]。现在研究煤对CO2吸附/解吸过程中研究主要采用在一定条件下,煤对CO2等气体的吸附量,基于Langmuir吸附模型根据吸附等温线计算煤对CO2吸附热力学参数揭示煤对CO2的吸附机理[17]。由于Langmuir模型的假设条件过于理想,在研究结果有一定的局限性。同时针对煤对CO2解吸过程及热力学参数研究相对较少。因此,文中通过等温解吸试验探讨适合解释煤对CO2解吸过程的数学模型,基于热力学理论计算得到煤对CO2解吸过程中的热力学数据,揭示煤对CO2的解吸热力学规律,对煤层气增产及煤自燃火灾防治方面的应用提供一定的参考。
1 实验系统及过程
1.1 实验样品
实验样品是分别采自新疆硫磺沟矿(LHG)的长焰煤,陕西王凹矿(WW)的弱粘煤,山东龙固矿(LG)的气煤和山西王家岭(WJL)的瘦煤,4种样品的工业分析见表1.将煤样粉碎成粒度0.25~0.177 mm,采用DZF-6050型真空干燥箱,在60 ℃条件下干燥5 h,干燥完成之后立即进行解吸实验。

表1 煤样的工业分析
1.2 实验系统及过程
实验系统如图1,解吸罐空体积为V1,采用高精度CS502B型恒温槽,实现煤解吸温度高精度控制。系统抽真空采用罗茨真空泵机组:型号ZJZX30-4型,实验系统的压力采用ZDO-5(0~12 MPa)热偶压力传感器进行测量。在进行煤解吸CO2实验时,首先用真空泵将装好煤的解吸罐,抽至真空状态(真空度小于4 Pa),之后将解吸罐置于333 K水浴中连续脱气4 h.在脱气完成之后,调整水浴温度至实验温度Tm;缓慢向充气罐中充入一定量的CO2气体,体系的压力在5 MPa左右时停止记录气体压力Pi,之后关闭解吸罐阀门等待压力平衡之后记录解吸罐内压力Pj,打开解吸罐阀门向外释放ΔP的CO2气体;之后关闭解吸罐阀门等待压力平衡之后记录解吸罐内压力Pj+1,重复上述放气和解吸步骤,得到一系列的Pi和Pj,直到Pj小于0.1 MPa压力之后结束实验,将整个解吸过程中每个平衡压力点的解吸量由解吸平衡压力从小到大顺序进行累加得到每个解吸平衡压力煤吸附CO2量,绘制得到一条煤解吸CO2的等温曲线。分别通过实验得到煤样在303,313,323,333和343 K等5种温度时,压力为0.1~5 MPa范围内4种煤对CO2的解吸等温线。

图1 实验系统Fig.1 Experimental system
2 实验结果及分析
2.1 CO2在煤表面等温解吸曲线
2.1.1 吸附模型
1)Langmuir吸附模型是单分子吸附理论广泛用于描述气体在固体表面单层物理吸附的研究中,所代表是吸附热不随吸附而变化,每一个吸附点的能量不变,这是一种理想的吸其方程如下式[18-19]
N=abP/(1+bP)
(1)
2)Freundlich吸附模型所代表的是吸附热随吸附量呈对数形式降低物理或化学吸附过程,其表达式如下式[19]
N=k1ln(k2P)
(2)
3)Tempkin吸附模型适用于描述中等覆盖度(0.3~0.7)化学吸附解吸过程,且吸附热随吸附量呈线性降低,其表达式如下式[19]
N=k1ln(k2P)
(3)
式中N为吸附量,mmol/g;P为解吸平衡压力,MPa;a和b为Langmuir方程的拟合参数;K和n为Freundlich方程的拟合参数;k1和k2为Tempkin方程的拟合参数;R2为拟合相关性系数。
2.1.2 吸附等温线
实验测得样品对CO2的解吸等温线及3种吸附模型拟合的曲线如图2~5所示。3种经典吸附模型的拟合参数见表2.采用相关系数R2作为判定不同吸附模型对4种煤解吸CO2等温曲线的拟合的优劣程度指标。

图2 LHG样品的解吸实验曲线Fig.2 Test curves of desorption of LHG sample

图3 WW样品的解吸实验曲线Fig.3 Test curves of desorption of WW Sample
由图2到5可得,Tempkin模型拟合曲线拟合系数R2较低,不适合解释煤对CO2的解吸过程。对比Langmuir和Freundlich模型的拟合结果,解吸温度为303,313和323 K时,Freundlich方程的拟合曲线拟合参数R2可达0.992以上,可准确的表示煤对CO2的解吸规律;当解吸温度为333和343 K时,Langmuir方程拟合参数R2最低可达0.997以上,能准确表示煤对CO2的解吸规律。Langmuir模型反映气体吸附解吸过程吸附热稳定不变与吸附量不存在对应关系,是经典的物理吸附模型[18]。Freundlich模型基础是吸附势理论,主要描述吸附热随吸附量增加呈对数降低趋势的吸附过程[19]。Tempkin模型适用于中等覆盖度(0.3~0.7)化学吸附解吸过程,且吸附热随吸附量呈线性降低[19]。CO2与煤表面吸附活性位置(如碱性酸性结构对CO2具有较强的吸附力)的作用较强,煤表面活性吸附位不均匀程度会对CO2解吸产生显著影响,在解吸过程中CO2会优先在易解吸的位置上发生。在解吸温度较低时,CO2对煤表面不均匀程度敏感性较强,Freundlich模型能更好的解释CO2的解吸规律。在333和343 K温度时解吸等温曲线符合Langmuir模型的变化规律,随解吸体系温度升高,CO2分子与煤表面之间的作用力显著减小,导致CO2对煤表面不均匀程度的敏感性显著降低造成的。在温度较低时,煤表面对CO2吸附解吸属于较强的物理吸附解吸过程,CO2对煤表面吸附位有一定的选择性,随温度的升高,吸附解吸的选择性降低,逐渐符合经典的物理吸附解吸模型。煤对CO2的吸附量随变质程度的变化而变化,煤的比表面积呈现先减小后增加的U型趋势,其中长焰煤的弱粘煤变质程度较低,含有较多的官能团和侧链,煤的芳香也较少,比表面积也大于变质程度中等的气煤和贫瘦煤[20]。因此长焰煤的弱粘煤对CO2的吸附量显著的大于气煤和贫瘦煤。
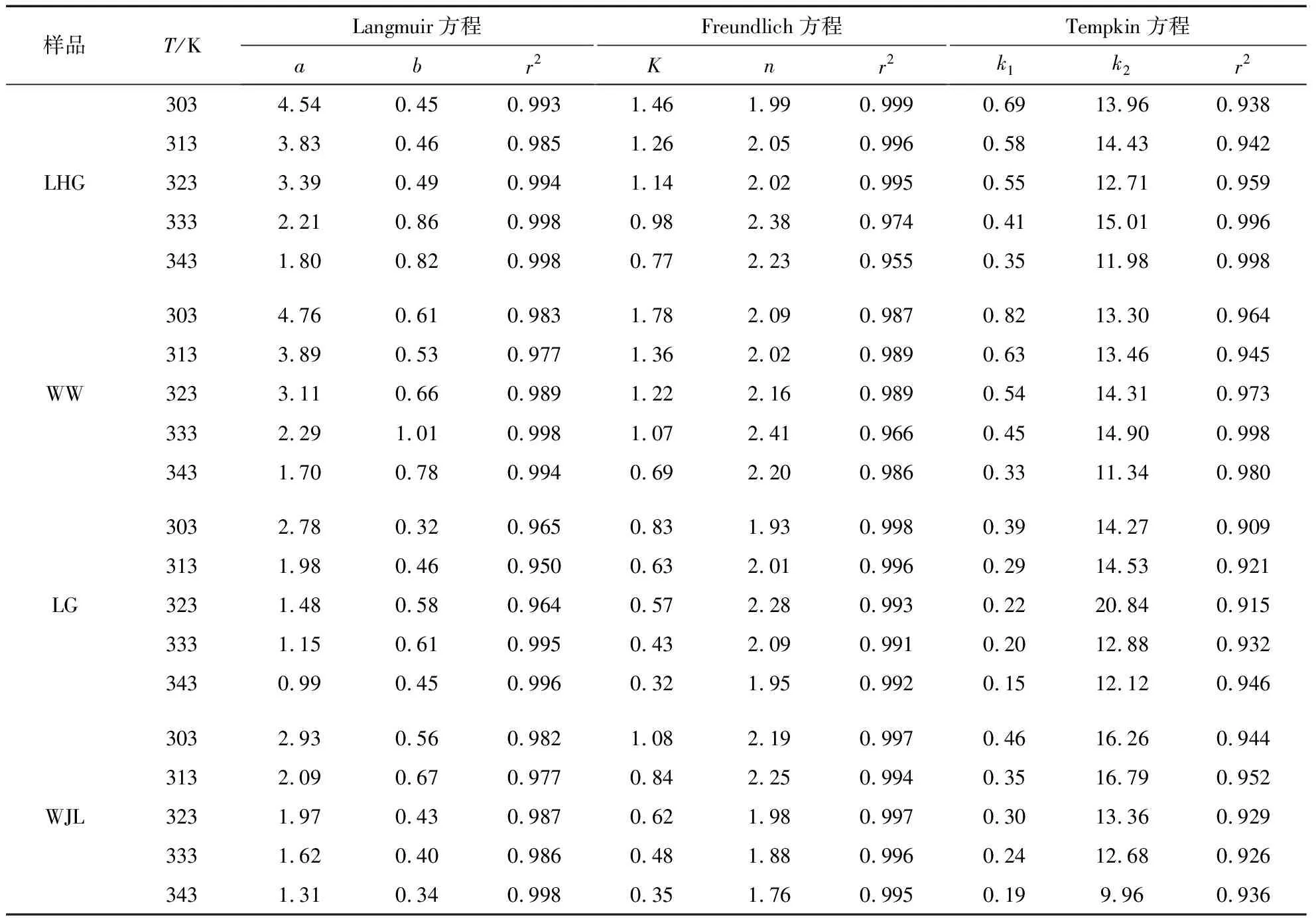
表2 煤样解吸实验拟合结果
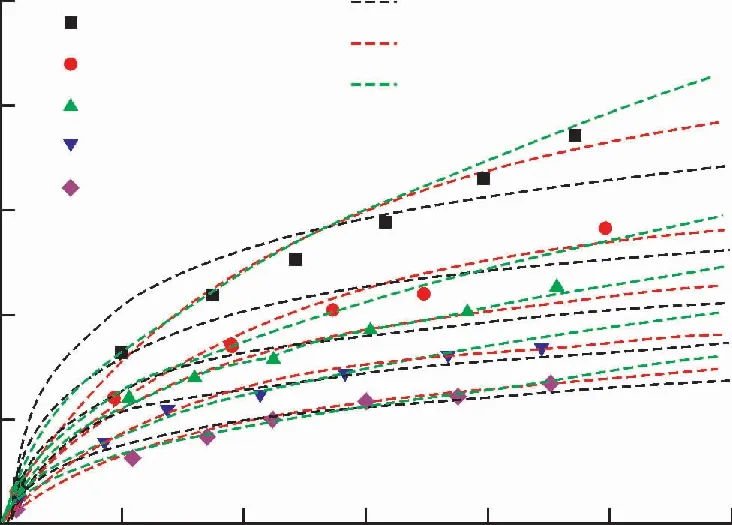
图4 LG样品的解吸实验曲线Fig.4 Test curves of desorption of LG sample
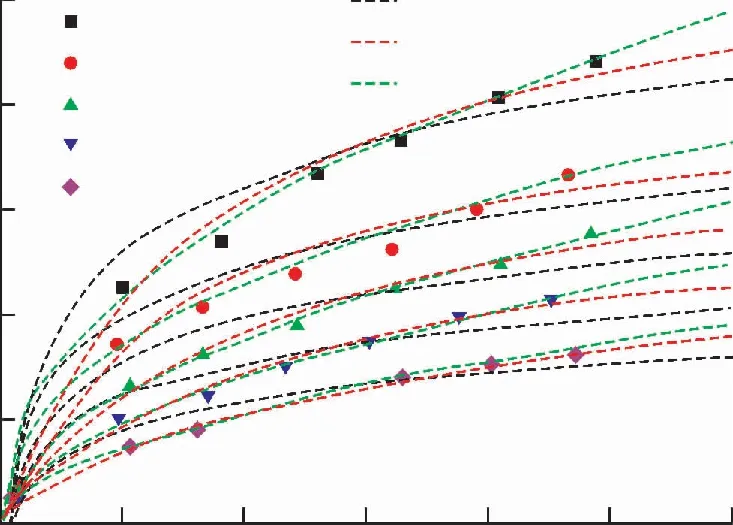
图5 WJL样品的解吸实验曲线Fig.5 Test curves of desorption of WJL sample
2.2 CO2在煤表面的等量吸附线
根据煤在303,313,333 K温度时解吸等温曲线,采用Freundlich方程将解吸等温线转换成等量解吸线,分别选择吸附量为0.1,0.2,0.3,0.4 mmol /g,求得等吸附量条件下CO2的解吸平衡压力P与温度T关系,得到等量解吸线如图6到9所示。4种煤对CO2等量解吸线为4条直线,在吸附量不变时,CO2气体解吸压力与解吸温度之间呈正相关关系,解吸平衡压力升高时解吸温度也相应的升高,这证明4种煤样对CO2的吸附和解吸作用属于物理吸附[20]。将CO2在煤表面的等量解吸线向坐标轴延长,将会在较小的温度范围内相交,对应特定解吸温度范围,有学者在进行煤对CH4的吸附过程研究中也发现了这一现象[21]。LHG样品对CO2解吸对应的特征温度平均为270 K(-3.15 ℃),WW样品对CO2解吸对应的特征温度平均为277 K(3.75 ℃),LG样品对CO2解吸对应的特征温度平均为278 K(4.85 ℃),WJL样品对CO2解吸对应的特征温度平均为298 K(24.85 ℃),这是由于随着煤的变质程度的增加,芳香核排列有序化缩合程度高,煤表面的官能团和侧链逐渐减少,煤表面具有更强的各向异性造成。

图6 LHG样品的等量解吸线Fig.6 Equivalent desorption curves of LHG sample

图7 WW样品的等量解吸线Fig.7 Equivalent desorption curves of WW sample

图8 LG样品的等量解吸线Fig.8 Equivalent desorption curves of LG sample

图9 WJL样品的等量解吸线Fig.9 Equivalent desorption curves of WJL sample
2.3 煤解吸CO2的等量吸附热
由Clapeyon-Clausius方程可推出吸附解吸平衡压力、温度和等量吸附热(Qst)的关系式(4)[22-23]。
(4)
式中Qst为等量吸附热,kJ/mol;P为解吸平衡压力,MPa;R为气体常数,8.314 J/(mol·K);T为解吸实验温度,K;C为常数。式(1)表明1/T和lnP的关系是线性的,通过线性拟合的斜率可以得到等量吸附热Qst,使用吸附方程表示吸附压力和吸附量之间的关系,之后针对相同的吸附量值,计算不同吸附解吸温度下的平衡压力。最后采用1/T和lnP的拟合直线的斜率求出Qst.

表3 吸热曲线拟合结果
计算得到4种煤解吸过程的等量吸附热如图10所示。不同煤样的等量吸附热曲线的拟合其拟合系数见表3.4种煤对CO2解吸过程的等量吸附热随吸附量的增加符合Qst=cln(N)+d对数降低的关系;这是由于煤体表面的非均一性和解吸过程中CO2气体分子间的相互作用引起的[24-25]。煤本身是非均质的吸附剂,煤表面含有大量的基团,矿物质,特别是含氧基团对CO2的作用力较大,对CO2在煤表面的解吸有阻碍作用[26]。解吸的CO2气体分子间作用力会随着随CO2吸附量不断增加而逐渐增强,这会导致CO2在煤表面解吸过程中等量吸附热随CO2吸附量增加而不断减小。CO2在煤表面解吸的等量吸附热随吸附量的增加呈现对数趋势不断减小,在吸附温度较低时,煤表面非均质性对CO2的吸附产生的影响远大于CO2气体分子之间的相互作用。不同变质程度煤对CO2解吸过程中的等量吸附热均随着吸附量的增加而减小,但是变化的幅度却不一样,长焰煤和气煤的最小,弱粘煤次之,瘦煤最大。这是由于解吸过程中等量吸附热主要受煤样表面被吸附CO2分子间的作用力和煤表面不均匀各向异性的影响共同作用的影响的结果。随着变质程度的增加,芳香核排列有序化缩合程度高,煤表面的官能团和侧链逐渐减少[20]。因此变质程度煤的表面具有更强的各向异性,煤表面对CO2吸附性较强的吸附位点种类和数量发生变化,这造成不同变质程度煤的解吸的等量吸附热不同。

图10 煤样对CO2吸附热Fig.10 Adsorption heat of CO2 on coal samples
3 结 论
1)随解吸体系温度升高,CO2对煤表面不均匀程度的敏感性逐渐降低;Freundlich模型在温度为323 K以下可准确描述吸附过程,Langmuir模型对于温度为333和343 K时拟合度较好。样品对CO2解吸的特征温度分别为:270 K(LHG)、277 K(WW)、278 K(LG)和298 K(WJL),解吸特征温度随煤变质程度的升高而升高;
2)煤表面会形成一个非均匀的吸附力场,对煤表面附近的CO2发生作用而发生吸附,煤体的表面呈各相异性对CO2解吸影响大于CO2气体分子之间作用的影响;这会使得CO2气体在煤表面解吸过程中的等量吸附热随吸附量的增加呈Qst=cln(N)+d的对数的降低规律;
3)煤对CO2气体的等量吸附热是煤表面CO2吸附(解吸)作用能力大小的间接反映,4种煤对CO2的等量吸附热在吸附量为0.1 mmol时在-60到-90 kJ/mol之间变化;等量吸附热随吸附量增加呈对数降低规律,反应出煤对CO2的解吸能力随吸附量的增加而逐渐增强。
