聚硅酸铝铁混凝剂的制备、性能与混凝机理研究
2018-10-10劳德平丁书强许成文满伟慧
劳德平 丁书强 倪 文 许成文 王 雪 满伟慧
(1.北京科技大学土木与资源工程学院,北京100083;2.北京低碳清洁能源研究院,北京102211;3.山东省济宁市环境保护科学研究所,山东济宁272025)
聚硅酸铝铁(PSAF)混凝剂是通过将金属阳离子Al3+和Fe3+引入到活化硅酸网链状结构中,使之与聚硅酸的羟基端发生取代和络合吸附反应,防止了硅酸凝胶化,进而形成稳定的胶体溶液[1-2]。使用过程中,通过金属阳离子的水解及聚硅酸长链高分子结构与带电胶体颗粒和污染物分子相互作用而达到净化废水的目的。此类混凝剂综合了聚硅酸网链结构吸附架桥、铝盐絮体大而脱色效果好、铁盐絮体密实又沉降迅速的多重优点,且制备工艺简单、环保高效而又价格低廉[3-4]。当前,很多学者[5-7]致力于以固体废弃物为原料制备无机高分子混凝剂,且在验证产品混凝性能和混凝机理方面也作了深入研究。
本研究以高铝粉煤灰和氧化铁皮为原料,浸取、聚合制备无机高分子混凝剂PSAF,考察混凝条件对模拟废水净化效果的影响,对其与市售混凝剂PAC的混凝效果进行比较,并通过分析、测定自制混凝剂混凝过程中絮体粒度和动电位的变化来揭示混凝过程的机理。
1 试验原料、试剂、仪器及模拟废水的配制
(1)试验原料。粉煤灰取自神华集团国华电力公司,平均粒度为17.66µm,主要化学成分为Al2O3、SiO2、Fe2O3,含量分别为52.85%、37.61%和2.12%。氧化铁皮取自山东莱芜钢铁公司下属轧钢车间,有效元素Fe含量为83.80%。
(2)化学试剂。碳酸钠、盐酸、氢氧化钠为分析纯试剂,甲基橙、高岭土为化学纯试剂,均为国药化学试剂有限公司产品。市售聚合氯化铝混凝剂(PAC)由河南某化工制品公司生产,有效成分Al2O3含量为46%。试验各阶段用水均为自制去离子水。
(3)试验仪器。KSL-1200X型台式箱式炉(1200 ℃),HH-4型数显控温水浴锅,MYP2011-250型电动搅拌器,SHB-ⅢS型台式循环水式多用真空泵(压力范围为1×105~2×105Pa),101型数显电热鼓风干燥箱(室温~300℃),雷磁pHS-2F型pH计,MYP11-2A型恒温磁力搅拌器。
(4)混合模拟废水的配制。称取12.5 mg甲基橙和25 mg高岭土溶于250 mL去离子水中,置于磁力搅拌器上搅拌均匀,得到一定浓度的稳定的混合模拟废水,静置0.5 h后取液面以下2 cm处浑浊液,测得原始混合模拟废水的浊度为71 NTU,TOC为232 mg/L。
2 试验方法
2.1 混凝剂PSAF的制备及其特征分析
(1)元素的浸出。取10 g粉煤灰与碳酸钠的混合物(Na2CO3与SiO2的物质的量之比为0.8),在900 ℃下焙烧3 h,取出自然冷却后用研钵碾压以恢复烧前粒度,取5 g置于120 mL浓度为3 mol/L的HCl溶液中,在40℃下浸出0.5 h后过滤,滤液经收集后定容到250 mL;取5 g氧化铁皮置于40 mL浓度为6 mol/L的HCl溶液中,在40℃下浸出1 h后过滤,滤液经收集后定容到150 mL。分别测定上述定容液的铝、铁、硅浓度。
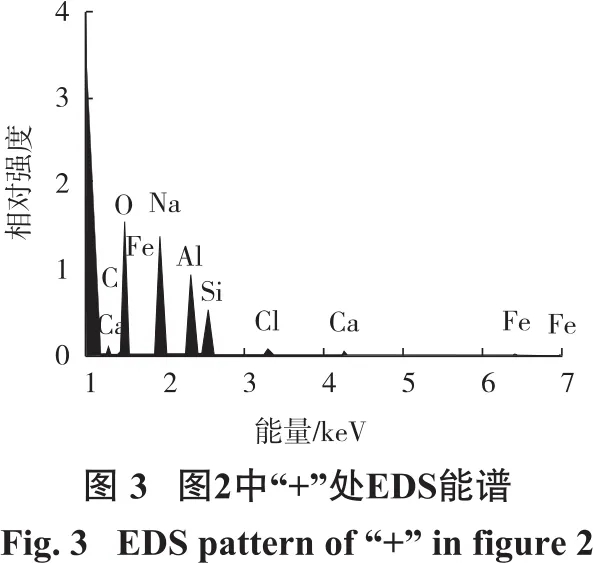
(2)PSAF合成过程。用上述定容液,按Al与Fe物质的量之比1.4配制混合液共251 mL,置于500 mL烧杯中,在磁力搅拌(300 r/min)作用下缓慢滴加0.1 mol/L的NaOH溶液,控制碱化度B为0.5(pH=3),聚合温度为40℃,时间为1.4 h。反应结束后,将制得的混凝剂陈化12 h,所得黄色半凝胶状液体即为混凝剂PSAF,将其置于电热鼓风干燥箱中低温干燥后得到PSAF固体,测得其密度为1.51 g/cm3,粒度为207 nm,黏度为38.10 mPa·s。PSAF的XRD图谱见图1,SEM图片见图2,图2中“+”处EDS能谱图见图3。
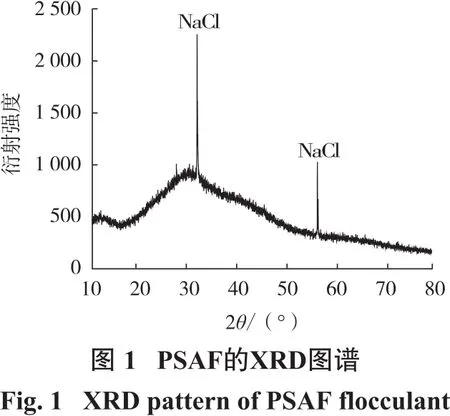

由图1可见,图中除有较强的氯化钠结晶峰外,其他均为无定形衍射峰[8-9]。
由图2可见,产品微观呈现丰富多枝的网状聚集,比表面积较大[10]。
由图3可见,混凝剂的主要组成元素为Na、Si、Al、Fe、Cl,以及混入的Ca等元素。
2.2 模拟废水的处理
取250 mL配置好的混合模拟废水置于400 mL烧杯中,用0.1 mol/L的HCl溶液和0.1 mol/L的NaOH溶液调节废水pH值,在磁力搅拌作用下加入一定量的自制PSAF或市售混凝剂PAC,加药混凝过程先在300 r/min转速下快搅2 min,再在60 r/min转速下慢搅一定时间后测其Zeta电位,混凝废水静置0.5 h后取液面下2 cm处的上清液,测试其浊度、TOC;排出全部上清液后,用吸管吸取杯底相对粗实的混凝絮体,保存以测试其粒度。
2.3 分析测试
采用X射线荧光光谱仪(ZSX Primus II,Rigaku,Japan)测定粉煤灰和氧化铁皮的化学成分,X射线衍射 仪(D8 ADVANCE,Bruker,Germany)表 征 自 制PSAF的结构,扫描电子显微镜(Nova NanoSEM 450,FEI Company,Czech)观察PSAF的微观表面形貌,全自动密度测定仪(METTLER TOLEDO,DM40,Switzerland)测定混凝剂的密度,旋转黏度计(Brookfield DVP+USA)测定液体混凝剂的黏度,散射式光电浊度仪(WGZ-100,0~100 NTU)测定混凝模拟废水的浊度,总有机碳分析仪测定上清液的TOC值,马尔文激光粒度分析仪(Mastersizer 2000E,Malvern,UK,粒度测试范围为0.02~2 000µm)测试混凝絮体的粒度,Zeta电位仪(Malvern,Zetasizer Nano ZS90,UK)测定絮体的Zeta电位。
3 废水混凝影响因素试验结果与分析
3.1 混凝剂投加量的影响
混凝剂投加量影响试验固定混凝温度为室温、pH=7、慢搅(混凝)时间为10 min,试验结果见图4。

由图4可看出,随着混凝剂投加量的增加,废水浊度降幅先显著增大后趋于稳定,总有机物去除率先显著增大后趋于稳定;PSAF的混凝效果优于PAC,这主要是因为PSAF较PAC多引入了聚硅酸和元素铁,混凝过程水解作用后形成的絮体大且密实[11-12]。另外,无机高分子混凝剂主要是通过双电层压缩、吸附电中和、絮凝架桥及网捕卷扫等4种方式与废水中污染物发生作用。当投加量较小时,废水中混凝剂浓度相对偏低,有效电荷量和活性吸附点位较少,混凝过程以吸附电中和作用为主,混凝后絮体小且沉降速度慢;随着混凝剂投加量的增大,混凝剂水解后产生了大量的有效电荷和较长分子链,且PSAF分子量比PAC分子量要大许多,混凝过程以絮凝架桥和网捕卷扫为主,辅以吸附电中和作用,混凝后形成的絮体大,沉降速度也快[13-14]。试验确定PSAF和PAC的适宜投加量分别为20 mL/L和24 mL/L。
3.2 模拟废水初始pH的影响
模拟废水初始pH对混凝效果影响试验固定PSAF和PAC的投加量分别为20 mL/L和24 mL/L,慢搅时间为10 min,试验结果见图5。

由图5可看出,PSAF的混凝效果优于PAC。模拟废水的初始pH从5增大至8,以PSAF为混凝剂情况下混凝废水的浊度降幅和总有机物去除率大幅度上升;pH继续增大至10,混凝废水的浊度降幅和总有机物去除率小幅下降。模拟废水的初始pH从5增大至9,以PAC为混凝剂情况下混凝废水的浊度降幅和总有机物去除率大幅度上升;pH继续增大至10,混凝废水的浊度降幅和总有机物去除率小幅下降。这是由于pH变化改变了水中污染物胶体的带电性质及电荷量,同时也影响了混凝剂的水解形态,进而影响到絮凝效果[11-12,15]。废水中污染物呈现出带负电荷的胶体状态,而PSAF和PAC中含有大量的金属阳离子及其水解后形成的羟基络离子,在合适的混凝条件下会发生双电层吸附及电中和作用,另外,聚硅酸大分子结构也会起到较强的絮凝架桥及网捕卷扫作用,增强了混凝废水的处理效果[13,16]。当废水酸性较强时,混凝剂不易发生水解,混凝体系吸附电中和作用较弱,颗粒难以脱稳凝聚且絮体微小,另外,酸性条件下,聚硅酸不稳定,所以混凝效果较差[11,13];随着废水初始pH值的增大,废水溶液中OH-增多,混凝剂容易发生水解,金属阳离子水解形成单核和多核羟基络离子,在pH=8~9时达到最大,这些络离子和溶液中胶体颗粒间发生双电层吸附及电中和作用使胶体颗粒脱稳,另外,聚硅酸大分子链增强了体系絮凝架桥作用,所以最终形成的絮体大且密实,混凝效果大大增强[11,17];当pH过大时,大量的OH-与混凝剂中的金属阳离子生成沉淀,使混凝剂吸附电中和性能大大减弱,导致混凝效果变差[11,13]。因此,模拟废水适宜的pH=8.5。
3.3 混凝时间的影响
混凝时间对混凝效果影响试验固定PSAF和PAC的适宜投加量分别为20 mL/L和24 mL/L,为了便于比较,2种混凝剂情况下模拟废水的初始pH均为8.5,试验结果见图6。

由图6可看出,PSAF的处理效果优于PAC。混凝时间从2 min延长至14 min,混凝废水浊度的降幅均显著增大;继续延长混凝时间,混凝废水浊度的降幅均下降。混凝时间从2 min延长至18 min,混凝废水总有机物去除率均显著增大;继续延长混凝时间,混凝废水总有机物去除率微幅下降。这是由于混凝剂金属阳离子水解形成的羟基络合物及大分子链聚硅酸在一定时间内较稳定,能够较好地与胶体颗粒产生吸附电中和及絮凝架桥作用[17-18]。搅拌时间太短,混凝剂与废水混合不够充分,混凝效果较差;延长混凝时间,混凝剂充分溶解于废水中,能够综合发挥双电层压缩、吸附电中和、絮凝架桥及网捕卷扫作用,使混凝效果逐渐变好;混凝时间太长,已经形成的絮体可能会在搅拌剪切作用下被破坏,絮体变得小而松散,沉降速度降低,混凝效果变差[13,18]。因此,适宜的混凝土慢搅时间为14 min。
4 混凝过程机理研究
4.1 混凝剂投加量的影响机理
混凝剂投加量对最终絮体粒度及体系Zeta电位影响试验固定混凝温度为室温、pH=7、慢搅时间为10 min,试验结果见图7。
由图7可看出,混凝剂投加量增大,絮体的Zeta电位上升、粒度增大;在混凝剂投加量相同的情况下,以PSAF为混凝剂的絮体粒度更大,但絮体的Zeta电位更低。PSAF和PAC分别在18 mL/L及15 mL/L左右时达到零电点[19-20]。
由于PSAF、PAC水解后带正电荷,且随着投加量的增加正电荷数量不断增加,混凝过程中双电层吸附及电中和作用增强,污染物颗粒表面的Zeta电位降低,当达到零电点时,颗粒凝聚进而脱稳下沉;污染物颗粒表面的Zeta电位超过零电点后,继续增大混凝剂的投药量,造成污染物颗粒表面的Zeta电位增大,结合图4可知,混凝废水的浊度及总有机物去除率呈现稳定态势,这是由于此时主要以大分子量聚硅酸架桥粘结作用为主[1]。

4.2 模拟废水初始pH的影响机理
模拟废水初始pH对最终混凝体系Zeta电位影响试验的PSAF和PAC投加量分别为20 mL/L和24 mL/L,慢搅时间为10 min,试验结果见图8。

由图8可看出,随着模拟废水初始pH值的升高,Zeta电位降低,这是因为混凝剂不断水解,使带负电的胶体颗粒体系电位下降,凝聚下沉;pH在8附近时,体系达到零电点,结合图5可知,此时混凝效果最佳,这是吸附电中和及絮凝架桥等多方面共同作用的结果;超过零电点后,体系Zeta电位变号,绝对值增大,出现反稳现象,此时主要依靠混凝剂中聚硅酸大分子架桥絮凝作用维持混凝效果[1,17,21-23]。
4.3 混凝时间的影响机理
混凝时间对最终絮体粒度影响试验固定PSAF和PAC的投加量分别为20 mL/L和24 mL/L,模拟废水的初始pH=8.5,试验结果见图9。

由图9可看出,无论以PSAF还是PAC为混凝剂,混凝废水絮体的粒度均随混凝时间的延长先增大后变小。相同混凝时间情况下,PSAF对应的絮体粒度更大[14],这与混凝剂产品的聚集度有关:PSAF引入了聚硅酸,其聚集度较PAC大,故吸附架桥能力更强,最终宏观表现为絮体粒度更大[24];达到最佳混凝时间后,继续延长混凝时间,絮体粒度变小,是由于已经形成的大粒度絮体被搅拌剪切作用所破坏[3]。
最佳混凝条件下(PSAF和PAC的投加量分别为20 mL/L和24 mL/L、pH=8.5、混凝慢搅时间为14 min)絮体粒度的分布见图10。

由图10可看出,原始模拟废水中絮体的粒度主要集中区为0.5~10 μm,经PSAF处理的混凝废水中絮体的粒度主要集中区为150~500 μm,经PAC处理的混凝废水中絮体的粒度主要集中区为30~1 000 μm;经统计分析的D50分别为2.18、162.92、137.64µm,验证了PSAF混凝废水的效果优于市售PAC[1]。
5 结论
(1)自制混凝剂PSAF的XRD分析表明,产品主要呈现氯化钠的结晶相,其他均为无定形物质;SEM显示产品呈现空间网状结构,呈丰富多枝的网状聚集,结合EDS能谱图可知混凝剂产品主要元素为Si、Al和Fe,另外还含有部分Ca。
(2)混凝试验结果表明:污染物去除率随混凝剂投加量的增加而增大,最终均趋于稳定,PSAF效果总体较市售PAC好,且2种混凝剂处理废水后絮体粒度也呈现相同变化规律。Zeta—投加量关系表明,PSAF及PAC投加量分别在18 mL/L、15 mL/L左右时,废水体系达到零电点,继续增大投加量,电位变号,混凝体系以絮凝架桥作用为主;当pH在8~9时,混凝去除率较高,此时混凝废水体系达到零电点附近,pH太高,溶液中会形成氢氧化物沉淀,使混凝剂性能降低,影响污染物的去除;混凝慢搅时间在14 min左右时浊度降幅和有机物去除率最大,过长的搅拌时间,会使已经形成的大絮体在搅拌剪切作用下被破坏,这与絮体粒度—混凝时间关系结果对应,同样PSAF较PAC形成的絮体粒度要大,混凝效果要好。
(3)在PSAF和PAC的投加量分别为20 mL/L和24 mL/L、pH=8.5、混凝慢搅时间为14 min条件下,PAC混凝废水絮体的D50为137.64µm,PSAF混凝废水絮体的D50为162.92µm。
