干湿交替和外源氮对农田土壤CO2和N2O释放的影响
2018-09-27张传更王广帅
张传更,高 阳,王广帅,李 双
(中国农业科学院农田灌溉研究所,河南 新乡 453003)
在全球气候变化背景下,干旱、极端降雨事件和人类活动会导致土壤频繁的经历干旱和再湿润过程[1]。干湿交替能够改变土壤生态系统的水分、养分状况和土壤物理性质,进而影响土壤的碳氮循环过程和土壤温室气体的排放[2-3]。人类活动造成的温室气体排放中14%来源于农田生态系统,农田生态系统排放的温室气体就全球升温潜势(GWP)标准下的贡献率达到22%[4]。农业生产中的温室气体减排已成为当前国内外全球变化领域关注的热点,是减缓气候变化的重要途径之一[5-6]。近年来,水肥一体化节水灌溉作为一种重要的农业生产措施得到了广泛的推广和应用,而如何通过科学的水肥灌溉措施来降低农田温室气体排放是一个研究热点。
水肥一体化会使农田土壤经历更为频繁的干湿交替循环,尤其是在干旱/半干旱地区。而诸多研究表明,干湿交替能加速土壤碳氮的释放,主要表现为以温室气体(如CO2和N2O)排放和以矿化形态(如和)从土壤中淋失[7-8]。贺云龙等[9]和Huygens等[2]认为干旱土壤湿润后,土壤CO2和N2O释放量会激增,而随着湿润土壤再干旱,释放速率急速下降[2,9]。欧阳扬等发现干旱土壤再湿润对CO2的释放有相似的激发效应[10]。Fraser等在研究干湿交替对农田土壤的影响试验中,也发现了干旱土壤再湿润可以激发CO2的释放[11]。近几年,国内外对土壤遭受干湿交替的研究逐步深入,涉及到中度、轻度和重度干旱等因素,不同类型土壤酶活性对干湿交替的响应机制等研究[12-13];然而,土壤中氮矿化机制对干湿交替的响应机制仍不清晰[14],更少涉及到农田土壤氮循环的研究。此外,已有的干湿交替研究更多地关注单一因素的作用,而非多因子交互作用[15]。土壤中的碳氮并不是孤立存在的,在各种外界环境改变的状态下,干湿交替条件下碳的响应往往是伴随着其他元素的变化而一起变化。因此,深入探讨干湿交替与其他因子耦合对碳氮转化的影响是十分必要的。本文以潮土为研究对象,通过进行干湿交替与外加氮源下农田土壤的碳氮动态变化和温室气体(CO2和N2O)排放的研究,为制定科学的水氮管理措施和农业生产温室气体减排措施提供理论依据与数据支撑。
1 材料与方法
1.1 试验材料
试验所用土样分别取自中国农业科学院七里营综合试验基地(35°08′N,113°45′E,海拔81 m)和河南省沁阳市广利灌区(35°40′N,112°55′E,海拔150 m),两地都位于半干旱、半湿润的暖温带大陆性季风气候区。七里营试验区的潮土起源于黄河冲积沉积物,属于典型的碱性砂壤土;广利灌区的潮土属于典型的碱性黏壤土,质地黏重,耕性差,通气透水性差。使用直径4 cm的土钻采集上层0~40 cm深度的土样,随机取60钻后混合。一部分土样(约3 kg)装入自封袋,然后立即放入装有冰块的保温箱中,带回实验室在4℃下保存;剩余的土壤装入布袋带回实验室,剔除植物残体和石块,用静电吸附去除细小的植物须根,风干后过4 mm筛备用。另一部分用于培养试验和测定土壤基本理化性质。供试土壤的基本理化性质见表1。
1.2 试验设计
培养试验在中国农业科学院七里营试验基地的人工气候室内进行。称取相当于100 g烘干质量的风干土分别按密度1.51、1.48 g·cm-3填装于500 mL塑料瓶中,盖子上钻有一个小孔,利于注射器采集气体样品;用去离子水调节土壤含水量至土壤持水量的70%,置于25℃下培养7 d(平衡培养)以恢复土壤生化性质,之后开始干湿交替培养试验。本试验设置氮浓度和干湿循环两个因素,其中干湿循环频率设4个水平,分别为0(即恒湿,作为对照)、2、6、12。干旱是指使土壤干燥到35%土壤持水量(WHC),湿润期指的是土壤湿度维持在70%WHC,培养过程中丧失的水分通过称量来补充。干湿循环和试验流程详见图1。
同一干湿频率中,一个处理不加氮,另一个处理加氮(采用含氮量为46.67%的尿素)。砂壤土中对应干湿频率添加的外源氮浓度分别为4、15、5、2.5 g·L-1(N);黏壤土中对应干湿频率添加的外源氮浓度分别为5、12、4、2 g·L-1(N)。同一土壤培养试验共有8个处理,每个处理3次重复。外加氮频率和溶液浓度见表2。
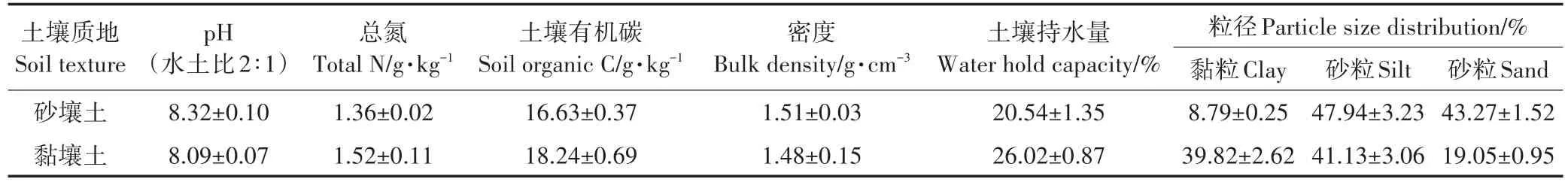
表1 土壤基本理化性质Table 1 Soil physical and chemical properties
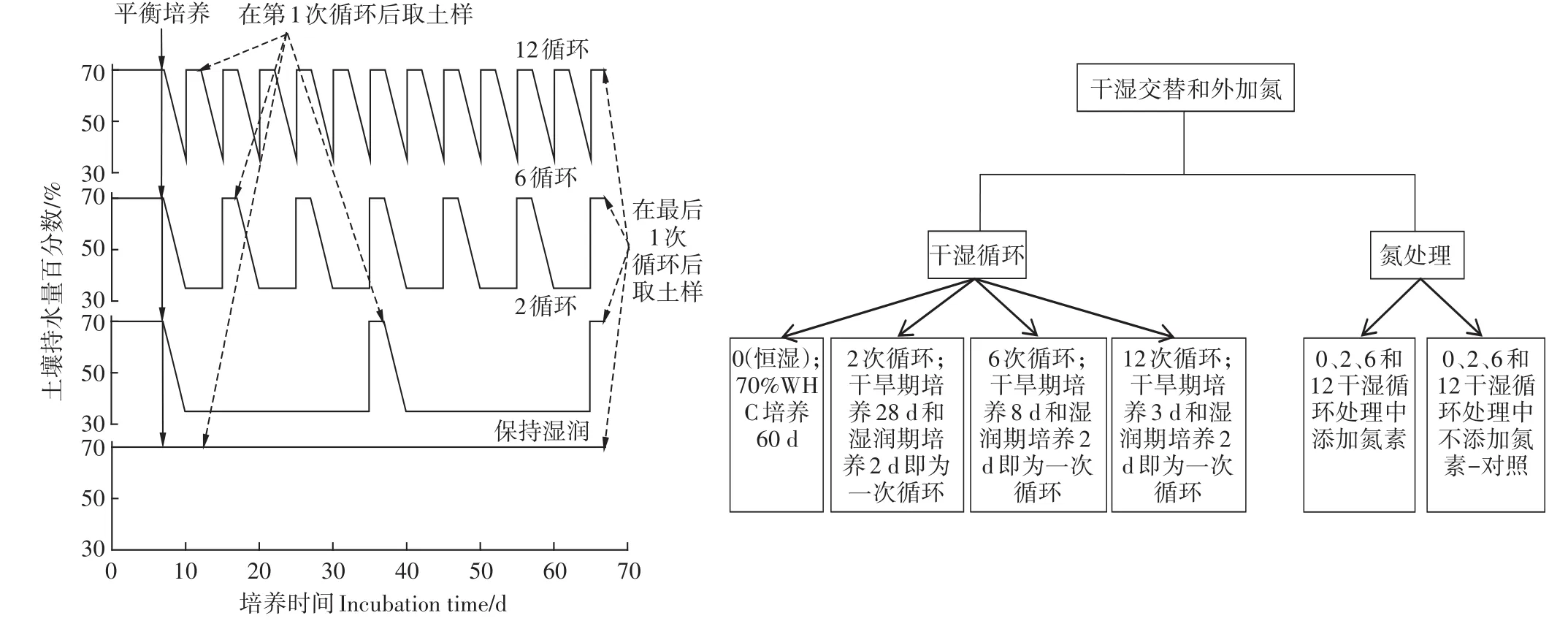
图1 土壤干湿循环、取样时间和试验流程示意图Figure 1 Schematic of the drying-rewetting cycles and sampling times and testing flow
1.3 测定项目与方法
1.3.1 土壤理化性质测定
土壤pH值用酸度计测定,土壤全氮含量用凯氏定氮法测定,土壤质量含水量采用烘干法测定,土壤粒径分布采用激光粒度仪(Mastersizer 2000)测定[16];土壤有机碳采用重铬酸钾外加热法[17]测定;土壤持水量(WHC)和土壤容重采用Fierer和Schimel的方法测定[7]。
第一次和最后一次循环湿润期结束时,采集土壤样品,一部分用于测定和(新鲜土样置于4℃冰箱保存),一部分测定土壤可溶性有机碳。取10 g新鲜土壤样品放入50 ml三角瓶中,加入50 mL的浓度为2 mol·L-1的KCl溶液(优级纯GR),室温下将混合液振荡15 min(200 r·min-1),提取上清液用于和含量分析,使用AA3-HR连续流动分析仪(德国,Seal Analgtical)测定土壤中和含量。称取10 g(干土质量)新鲜土样,放入150 mL的离心管中,加入50 mL去离子水,常温下以250 r·min-1振荡60 min,之后,在3000 r·min-1下离心10 min,取上部悬浮液过0.45 μm微孔滤膜,用Vario TOC-CUBE有机C分析仪(德国,Elementar)测定浸提的上清液中的可溶性有机碳含量,即为可溶性有机碳含量[18]。
1.3.3 CO2和N2O排放量测定
在每一次湿润开始和结束(湿润阶段培养瓶完全密封)使用注射器(30 mL)抽取培养装置内的气体样品,采用气相色谱仪器(GC-2010 plus,日本岛津)测定土壤CO2和N2O的排放量,并参照Lang等的CO2和N2O排放的数学模型[19],通过公式(1)计算:

式中:F为温室气体排放速率:CO2(mg CO2-C·g-1·d-1)和N2O(μg N2O-N·kg-1·d-1);V是培养瓶上部空间体积,L;C1和C2分别代表土样和空白培养瓶中温室气体浓度,mg·kg-1;T是培养温度(25℃);M代表温室气体分子量(CO2-C为12,N2O-N为28);W代表土样质量(干),g;t代表培养瓶密封时间,d。

表2 氮溶液浓度和添加频率Table 2 Concentration and frequency of nitrogen addition
1.4 数据分析
采用Excel 2007及Origin 8.5做图;利用DPS12.50软件不同处理间的差异进行方差分析,差异显著性水平(P<0.05)通过最小显著差数法(LSD)进行检验。
2 结果与分析
2.1 CO2释放规律
2.1.1 每个再湿润阶段CO2释放速率的动态变化
砂壤土和黏壤土干湿循环各处理的CO2释放速率都高于与之对应的恒湿组(图2)。在砂壤土和黏壤土处理中,12循环处理的CO2释放速率的变化趋势与恒湿处理相似,都是在培养的前30 d有明显的下降趋势,然后趋于平稳。而在砂壤土加氮处理中,12循环-N与恒湿-N处理的CO2释放速率在整个培养周期呈现逐渐下降的趋势;在砂壤土加氮处理中,12循环-N与恒湿-N处理的CO2释放速率在整个培养末期趋于平稳。
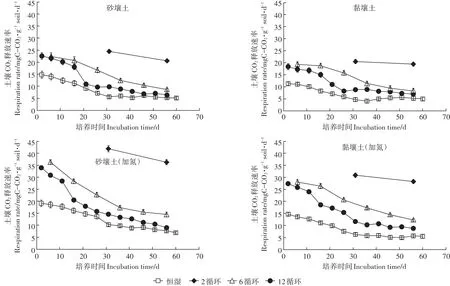
图2 干湿交替下每个再湿润阶段CO2释放速率变化Figure 2 Dynamics of soil CO2release rate during each re-wetting phrase of drying-wetting cycles
从总体分析,干湿循环中干旱期越长,再湿润阶段CO2的释放速率越大。通过对同一种土壤第一次和最后一次CO2的释放速率进行差异性分析(表3),外源N的恒湿和干湿组处理的CO2释放速率都高于与之对应未加氮的恒湿和干湿组处理(图2)。相同处理下,第一次循环砂壤土和黏壤土的CO2释放速率之间差异显著,并且第一次循环砂壤土的CO2释放速率显著高于黏壤土(表3);最后一次砂壤土的CO2释放速率同样高于黏壤土。两种农田土壤中砂壤土的CO2释放速率显著高于黏壤土,说明砂壤土CO2释放变化对干湿交替的响应更为强烈(图2)。总之,2种不同农田土壤CO2释放速率的变化模式一致。
两种农田土壤,虽然添加氮都促进了CO2的释放,但添加氮对砂壤土CO2的释放激发效应要比黏壤土强烈。在黏壤土中,12循环-N、6循环-N、2循环-N和恒湿-N的CO2平均释放速率分别比未加氮源处理的CO2平均释放速率提高了37.14%、41.12%、48.33%和23.29%;在砂壤土中,12循环-N、6循环-N、2循环-N和恒湿-N的CO2平均释放速率分别比未加氮源处理的CO2的平均释放速率提高了45.62%、47.66%、73.36%和49.30%。在两种农田土壤处理中,干燥期越长(2循环组),外加N源对土壤CO2释放速率的激发效应越强。
2.1.2 干湿交替对土壤可溶性有机碳(DOC)的影响
本试验条件下,砂壤土和黏壤土各处理在最后一次循环时的DOC含量相比于初始和第一次循环显著增加,并且从表4看出,砂壤土各处理的DOC含量在整体上都略高于黏壤土,表明砂壤土中难溶性有机质转化为DOC速率更高些,砂壤土对干湿交替响应的更为强烈。砂壤土和黏壤土中的各12循环-N、6循环-N、2循环-N和恒湿-N等处理DOC含量都低于对应的12循环、6循环、2循环和恒湿等处理,说明外加N源能加速DOC的消耗。在最后一次循环时,砂壤土和黏壤土的2循环处理的DOC含量最高,2循环-N处理的DOC含量次之;最后一次循环时,砂壤土6循环处理和恒湿处理之间差异不显著,砂壤土6循环-N处理和恒湿-N处理之间同样差异不显著,两处理组中的DOC含量非常接近;最后一次循环时,黏壤土6循环处理与恒湿处理之间差异不显著,6循环-N处理DOC含量显著高于恒湿-N处理。
2.2 N2O的释放
2.2.1 每个再湿润阶段N2O释放速率的动态变化
砂壤土和黏壤土在首次和最后一次循环时各处理的N2O释放速率之间的差异显著,并且加氮各处理的N2O释放速率显著高于未加氮处理(图3,表5);在砂壤土和黏壤土中,外加N源提高了恒湿和干湿组处理的N2O释放速率。砂壤土和黏壤土的干湿交替处理N2O释放速率都高于与之对应的恒湿组(图3)。在砂壤土和黏壤土中,对比各恒湿组和干湿组处理,发现除了2循环-N和2循环处理外,其他处理的N2O释放速率均呈现逐渐较少的趋势。在砂壤土和黏壤土中,12循环处理的N2O释放速率在培养的前30 d有明显的下降趋势,然后趋于平稳,并在培养后期,12循环处理的N2O释放速率的变化趋势与恒湿处理一致。在砂壤土和黏壤土中,12循环-N处理的N2O释放速率则与6循环处理的变化趋势较相似。

表3 各处理土壤CO2释放速率的变化(mg C-CO2·g-1soil·d-1)Table 3 Variations of CO2release rate from the two soils in different treatments(mg C-CO2·g-1soil·d-1)
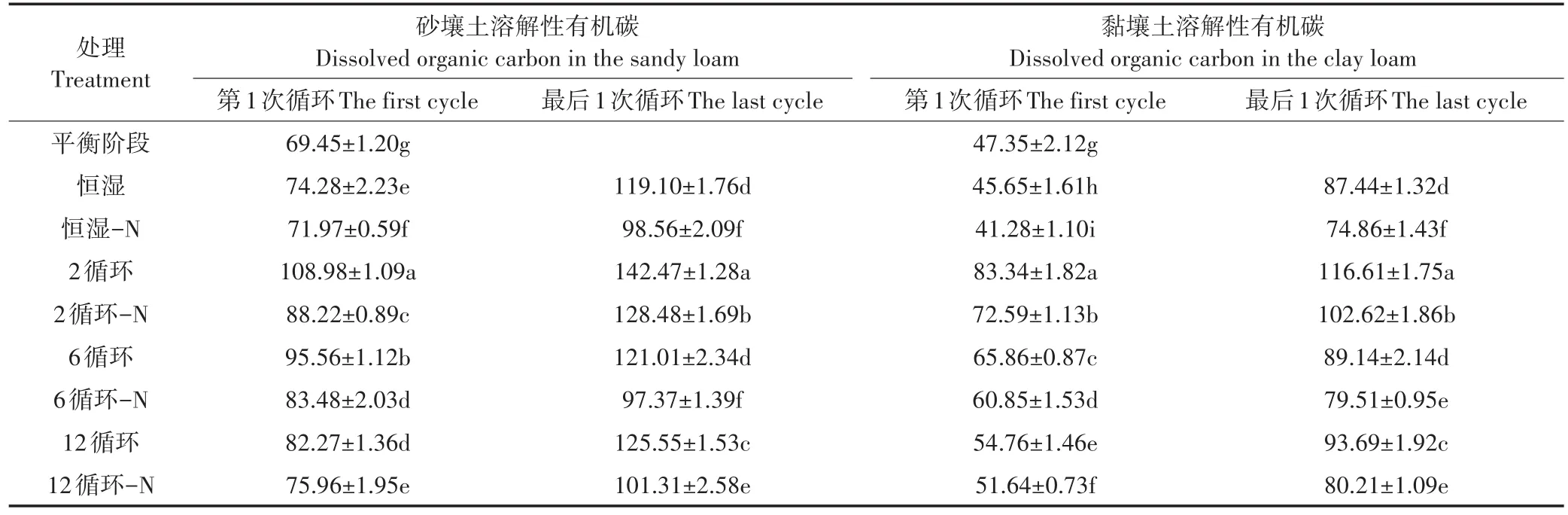
表4 各处理土壤可溶性有机碳的变化(mg·kg-1)Table 4 Variations of dissolved organic carbon in the two soils in different treatments(mg·kg-1)
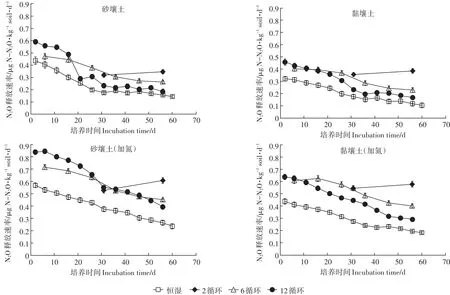
图3 干湿交替下每个湿润阶段N2O释放速率Figure 3 Dynamics of soil N2O release rate during each re-wetting phrase of drying-wetting cycles
在培养前期,砂壤土和黏壤土中干湿循环中干旱期越短,再湿润阶段N2O的释放速率越大;在培养后期,砂壤土和黏壤土中各处理的N2O释放速率变化与对应各处理的CO2释放规律一致,释放速率都是随着干旱期增长而增加。相同处理下,第一次循环时砂壤土和黏壤土中除了2循环-N外各处理的N2O释放速率之间差异显著(表3),最后一次循环时砂壤土和黏壤土中除了12循环外各处理的N2O释放速率之间的差异显著(表3)。总体来看,黏壤土的N2O释放速率低于与之相同处理的砂壤土N2O释放速率。
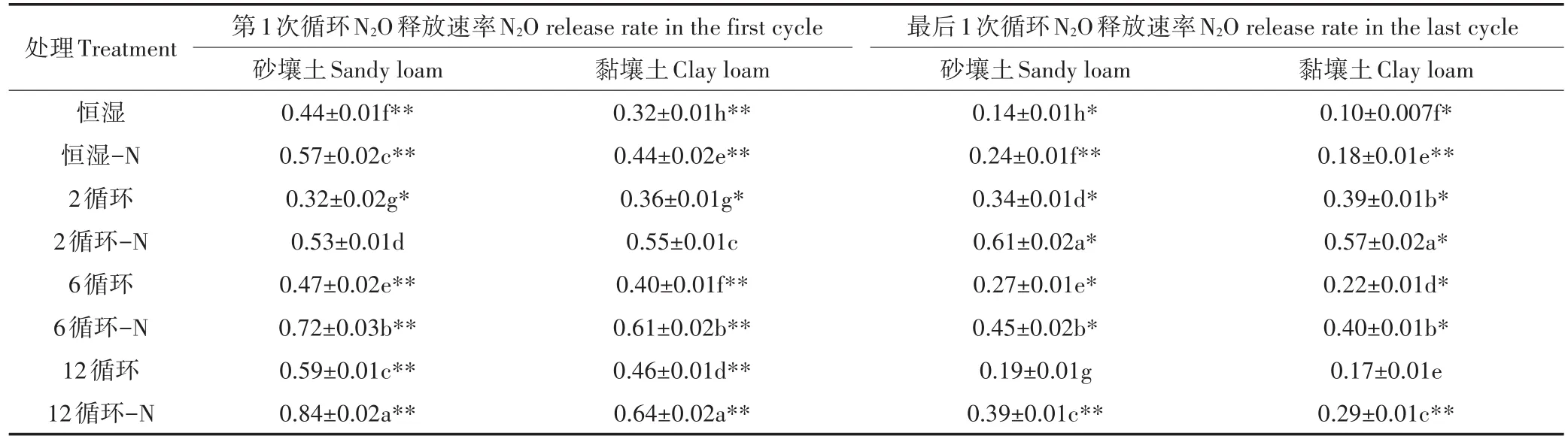
表5 各处理土壤N2O释放速率的变化(mg N-N2O·kg-1soil·d-1)Table 5 Variations of N2O release rate from the two soils in different treatments(mg N-N2O·kg-1soil·d-1)
两种农田土壤中,相比于黏壤土,在砂壤土中添加氮源更能促进N2O的释放。在黏壤土壤中,12循环-N、6循环-N、2循环-N和恒湿-N的N2O平均释放速率分别比未加氮源处理的N2O平均释放速率提高了46.96%、51.48%、60.42% 和58.07%;在砂壤土壤中,12循环-N、6循环-N、2循环-N和恒湿-N的N2O平均释放速率分别比未加氮源处理的N2O平均释放速率提高了61.87%、68.27%、70.11%和85.44%。由此可以看出,在两种农田土壤处理中,干燥频率越高,外加N源对土壤N2O释放速率的激发效应越强。
如图4所示,砂壤土和黏壤土各处理第一次循环和最后一次循环再湿润阶段土壤无机氮(和)含量变化。总体来看,砂壤土各处理的第一次循环和最后一次循环无机氮(和)含量高于黏壤土,说明干湿交替更能加速砂壤土有机氮的矿化速率,添加的有机氮在砂壤土中更易被转化;砂壤土和黏壤土中的各12循环-N、6循环-N、2循环-N和恒湿-N等处理无机氮(和)含量都高于对应的12循环、6循环、2循环和恒湿等处理。对比第一次循环和最后一次循环再湿润阶段土壤的和含量,可以发现通过持续的恒湿处理和多次的干湿循环处理后,土壤的无机氮含量都有所增加,12循环组处理无机氮含量(和)增加最为显著。在12循环、6循环和2循环等处理中,砂壤土和黏壤土的无机氮(和)含量随着干湿频率的递增而增加,表明干湿循环能显著增加土壤中氮的矿化速率,并且干湿频率越高效应越显著;而在12循环-N、6循环-N和2-循环-N处理中,砂壤土和黏壤土的无机氮(和)含量高于与之对应的未加氮处理,表明外加氮源显著增加了各处理土壤中无机氮的含量。
2.3 土壤可溶性有机碳、无机氮(和)及 CO2、N2O释放速率的相关关系
选取砂壤土和黏壤土整个试验周期内每次复水后各处理的土壤可溶性有机碳、无机氮(和)及CO2、N2O释放速率进行相关性分析,结果见表6。砂壤土的CO2释放速率与N2O释放速率、呈极显著正相关,而与可溶性有机碳和呈显著相关性;黏壤土的CO2释放速率与N2O释放速率、呈极显著正相关,与可溶性有机碳呈显著相关性。砂壤土和黏壤土的N2O释放速率都与、显著正相关。
2.4 CO2和N2O释放积累总量

图4干湿交替对土壤无机氮(NO-3和NH+4)的影响Figure 4 Effects of drying-wetting treatments on soil inorganic nitrogen(NO-3and NH+4)content
图5 为干湿循环和恒湿对照处理在整个试验培养周期内的土壤CO2和N2O释放的积累量。砂壤土和黏壤土的加氮各处理的CO2和N2O释放的积累量都高于未加氮处理,总体呈现恒湿-N处理>12循环-N>恒湿>6循环-N>12循环>6循环>2循环-N>2循环,而且砂壤土的CO2和N2O释放积累量增加最为显著。在砂壤土中,恒湿对照的土壤CO2释放的积累量492.54 μg C-CO2·g-1土与之对应的12-循环的积累量为376.10 μg C-CO2·g-1土,增加了30.96%;恒湿-N对照的土壤CO2释放的积累量为706.56 μg C-CO2·g-1土与之对应的12循环-N的积累量为532.23 μg C-CO2·g土,增加了32.75%。砂壤土中,恒湿-N的土壤CO2释放的积累量比与之对应的恒湿处理的积累量增加了43.45%;12循环-N的土壤CO2释放的积累量比与之对应的12循环的积累量增加了41.51%。在黏壤土中,恒湿对照的土壤CO2释放的积累量410.36 μg CCO2·g-1土与之对应的12-循环的积累量为320.84 μg C-CO2·g-1土,增加了27.90%;恒湿-N对照的土壤CO2释放的积累量为 508.39 μg C-CO2·g-1土,与之对应的12循环-N的积累量为444.24 μg C-CO2·g-1土,增加了14.45%;黏壤土中,恒湿-N的土壤CO2释放的积累量比与之对应的恒湿处理的积累量410.36 μg C-CO2·g-1土,增加了23.89%;12循环-N的土壤CO2释放的积累量比与之对应的12循环的积累量增加了38.46%。由图5可以看出,外加氮处理能够增加土壤中N2O的释放总量,其中砂壤土表现得最为显著,如恒湿-N的土壤N2O释放的积累量为23.33 μg N-N2O·g-1土,与之对应的恒湿处理的积累量为14.13 μg NNO2·g-1土,增加了65.51%;12循环-N的土壤N2O释放的积累量为17.50 μg N-N2O·g-1土,与之对应的12循环的积累量为 9.95 μg N-NO2·g-1土,增加了75.84%。在黏壤土中,恒湿-N的土壤N2O释放的积累量 18.36 μg N-NO2·g-1土,与之对应的恒湿处理的积累量为12.81 μg N-NO2·g-1土,增加了 43.33%;12循环-N的土壤N2O释放的积累量为15.10 μg N-NO2·g-1土,与之对应的12循环的积累量为10.09 μg NNO2·g-1土,增加了49.53%。在砂壤土中,恒湿对照的土壤N2O释放的积累量比与之对应的12-循环的积累量增加了42.01%;恒湿-N对照的土壤N2O释放的积累量比与之对应的12循环-N的积累量增加了33.31%。在黏壤土中,恒湿对照的土壤N2O释放的积累量比与之对应的12-循环的积累量增加了26.96%;恒湿-N对照的土壤N2O释放的积累量比与之对应的12循环-N的积累量增加了21.59%。图中还可以看出,在黏壤土和砂壤土中,6循环-N的N2O释放的积累量与12循环的释放积累量非常接近。
表6 土壤可溶性有机碳、无机氮(和)及CO2、N2O释放速率的相关关系Table 6 Correlation of soil dissolved organic carbon and inorganic nitrogen(/)and soil CO2and N2O release rate
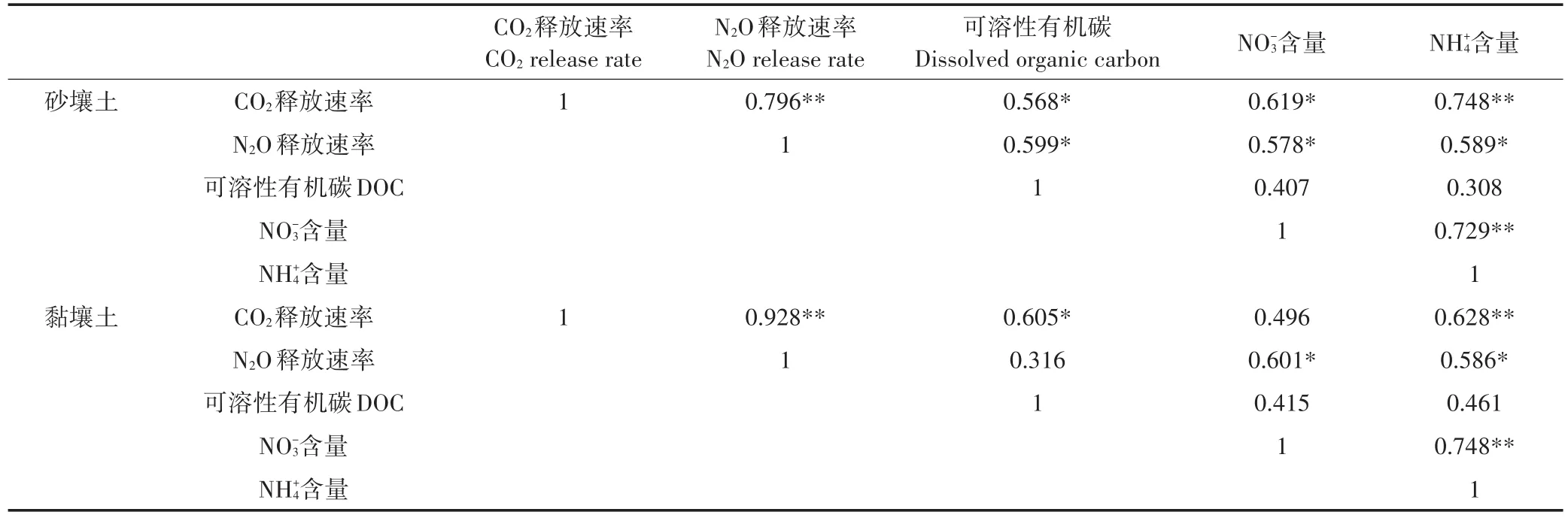
表6 土壤可溶性有机碳、无机氮(和)及CO2、N2O释放速率的相关关系Table 6 Correlation of soil dissolved organic carbon and inorganic nitrogen(/)and soil CO2and N2O release rate
注:*表示在P<0.05水平上显著相关,**表示在P<0.01水平上显著相关。Note:*represent significant correlation among treatments at 0.05 level,**represent significant correlation among treatments at 0.01 level.
NO-3含量NH+4含量砂壤土N2O释放速率N2O release rate 0.796**1 CO2释放速率N2O释放速率可溶性有机碳DOC NO-3含量NH+4含量CO2释放速率N2O释放速率可溶性有机碳DOC NO-3含量NH+4含量0.748**0.589*0.308 0.729**1 0.628**0.586*0.461 0.748**1 CO2释放速率CO2release rate 1可溶性有机碳Dissolved organic carbon 0.568*0.599*1 0.619*0.578*0.407 1黏壤土10.928**1 0.605*0.316 1 0.496 0.601*0.415 1

图5 土壤CO2/N2O释放在整个培养阶段的积累量Figure 5 Cumulative CO2and N2O emissions from the two soils in the different drying-wetting treatments
3 讨论
3.1 干湿交替对土壤CO2释放和有机碳矿化的影响
干湿交替能够显著激发土壤CO2释放(图2)。有研究表明,干旱土壤再湿润后,土壤CO2释放量能够激增至原来的2~10倍[20];随着湿润土壤再干旱,土壤CO2释放速率急速降低[21]。本研究中,砂壤土和黏壤土等农田土壤中CO2的释放对干湿交替的响应都表现出类似的激发现象,并且砂壤土CO2的释放变化对干湿交替的响应更为强烈。
砂壤土CO2的释放速率高于黏壤土,可能是由于砂壤土性质则介于砂土与黏土之间,土粒之间孔隙较大,通气透水性好。有研究表明,当黏土颗粒间水分的排出,颗粒之间相互靠拢以及颗粒间距缩短而引起的体积收缩,黏土颗粒集聚[22],这种结果增加了难溶性有机质转化被微生物直接利用的难度。干燥土壤再次复水时,添加的水会导致土块的快速崩溃,把以前形成的干燥裂缝快速闭合[23],最终导致在土壤湿润阶段土壤孔隙封闭,抑制了温室气体的排放。因此,本试验条件下同一处理下的砂壤土CO2和N2O释放积累量增加得最为显著。但是在整个培养周期内,本研究中砂壤土和黏壤土的CO2和N2O的释放累积量呈现恒湿-N>12循环-N>恒湿>6循环-N>12循环>6循环>2循环-N>2循环(图5)。水分是影响土壤CO2和N2O释放速率的主要因素之一,随着湿润土壤再干旱,土壤CO2释放速率急速降低[24],因而在整个试验培养周期内,恒湿处理的CO2和N2O释放速率维持在一个稳定且较高的水平。在本文中,砂壤土恒湿-N的土壤CO2释放的积累量比对应的恒湿处理的积累量增加了43.45%,12循环-N的CO2积累量比对应的12循环增加了41.51%;黏壤土恒湿-N的CO2积累量比对应的恒湿处理增加了23.89%,12循环-N的积累量比对应的12循环的积累量增加了38.46%。这些研究结果均说明外加氮源促进了土壤CO2的释放。
可溶性有机碳(DOC)虽仅占土壤有机碳库的一小部分,但作为微生物的重要能量来源,其含量直接影响微生物数量及其活性,并且与温室气体排放密切相关[25-26]。砂壤土和黏壤土的CO2释放速率都与DOC呈显著相关(表3),即DOC含量越高,CO2释放速率越高。有研究表明,干旱后土壤再湿润会使得微生物调节渗透压以排出含碳化合物,同时土壤再湿润后土壤颗粒裂解,裸露出更多的有机质被微生物得以利用,最终导致DOC浓度在短期内迅速升高[27]。本试验研究中,砂壤土和黏壤土的12循环-N、6循环-N和2循环-N等处理在第一次循环和最后一次循环时的DOC含量整体上高于恒湿对照的,表明12循环-N、6循环-N和2循环-N等处理土壤中难溶性有机质转化为DOC速率更高些,说明干湿交替提高了土壤中碳的矿化速率,并且砂壤土中碳的矿化速率对干湿交替响应的更为显著。本试验条件下,外加氮源促进了CO2的释放,并且在两种农田土壤处理中,干燥期越长,外加N源对土壤CO2释放速率的激发效应越强。有研究表明,在实际的生产中,施用化肥氮也可以促进农田土壤CO2的排放,如李晓密等研究不同施肥下冬小麦-夏玉米轮作农田温室气体排放时发现施氮增加CO2的排放,并且尿素区>硝态氮肥区[28];王永生等研究发现施氮能显著增加宁夏引黄灌区稻田CO2的排放[29]。添加氮源能够促进土壤CO2排放的原因在于:N源的添加降低了外源性物质的C/N,增加了可矿化态碳的潜力,加快了微生物量的周转速度,促进了有机质的矿化过程[30]。从本试验的结果来看,干湿交替能够显著激发砂壤土和黏壤土中CO2释放,并且是干湿频率越高,土壤有机碳矿化率越高。Borken和王苑等的研究也得出了相似的规律[31-32]。在两种农田土壤处理中,干燥期越长,外加N源对土壤CO2释放速率的激发效应越强。
3.2 干湿交替对土壤N2O的释放和有机氮矿化的影响
干湿交替使得土壤频繁的经历干旱和湿润过程,也使得硝化作用和反硝化作用交替进行,从而促进了N2O的产生和氮的矿化[33-34]。在本试验条件下,干湿交替能够显著激发土壤N2O的释放。这与刘学华和Beare等的研究结果相似[34-35]。研究表明干湿交替增加了微生物的死亡量并破坏了土壤环境和有机物间的相互作用,使得土壤中氮的矿化量增加,而且土壤的硝化和反硝化量显著高于长期湿润的土壤[7];也有研究表明,稻田土壤落干阶段的N2O的排放远大于田间淹水时期的N2O排放量。其原因可能是稻田中土壤含水量较高时(淹水)N2O的排放主要来自于反硝化作用,在落干阶段N2O的排放要来自于硝化和反硝化,同时落干阶段微生物更活跃[36]。本文中砂壤土和黏壤土2种农田土壤的N2O释放变化对干湿交替的响应都表现出类似的激发现象,并且砂壤土中N2O的释放对干湿交替的响应更为强烈。培养前期,砂壤土和黏壤土处理的干湿频率越高其土壤N2O的释放速率也越高,与欧阳扬在农田生态系统进行的的试验结果相似[10]。有研究表明,氮肥的施用对农田土壤N2O的排放有明显的促进作用[37-38]。在本试验条件下,砂壤土和黏壤土中的12循环-N、6循环-N、2循环-N和恒湿-N处理N2O的释放速率都高于对应的12循环、6循环、2循环和恒湿处理。在砂壤土中,恒湿-N的N2O释放的积累比对应的恒湿处理增加了65.51%,12循环-N的N2O积累量比对应的12循环增加了75.84%;在黏壤土中,恒湿-N的N2O释放积累量比对应的恒湿处理增加了43.33%。这12循环-N的积累量比对应的12循环增加了49.53%。这说明外加N源能提高N2O的释放速率,并且砂壤土增加的最为显著;并且是干燥期越短、外加N源对土壤N2O释放速率的激增效应越显著,分析其原因认为:(1)是因为经过多次的干湿交替后土壤团粒结构遭到破坏,暴露给微生物的有机质会进一步增加,从而增加了土壤养分的生物可利用性[31,39];(2)是12循环处理的干旱期最短并不会导致微生物的大量死亡也不会抑制微生物的活性[40-41],也可能和本试验条件下设置的干燥程度较弱,使得微生物能保持活性且能高效利用土壤中裸露出的有机质和复水时所加的N源有关。
4 结论
(1)干湿交替激发了砂壤土和黏壤土的CO2和N2O的释放速率;两种农田土壤中CO2和N2O的释放速率对干湿交替频率的响应模式相类似;在相同处理下,砂壤土的碳氮矿化速率对干湿频率的响应更为强烈。
(2)外加氮源都促进了2种农田土壤的CO2和N2O释放量:干燥期越长,外加N源对土壤CO2释放速率的激发效应越强;干燥期越短,外加N源对土壤N2O释放速率的激发效应越强。
(3)干湿交替增加了砂壤土和黏壤土中可溶性有机碳和无机氮(和的含量。在农田实际生产中,高频干湿循环导致土壤中可溶性有机碳和无机氮(和)的含量增多,增大了无机氮和)淋失和温室气体(CO2和N2O)排放的可能性。
