拉米夫定对乙肝合并肺结核患者免疫功能及肝功能的影响
2018-09-26韩美玉
韩美玉
肺结核(pulmonary tuberculosis)是结核分枝杆菌引发的慢性传染病,以肺部感染最为常见。我国肺结核发病率和死亡率均很高,是22个高发国家其中之一[1]。慢性乙型肝炎简称乙肝,是乙型肝炎病毒(hepatitis B virus,HBV)引发的慢性传染病,一般有3个月左右的潜伏期,也是我国常见传染病之一[2]。目前,乙肝合并肺结核在临床上较为多见,发病率约达39%,此类患者本身肝脏功能就有可能存在一定损伤,而常规抗结核治疗药物又对患者肝脏有一定损害,难以避免,副作用严重者甚至导致肝脏衰竭致死[3-5]。因此,寻找既能起到抗结核作用,又能起到保护肝脏的理想化治疗方法势在必行。本文在常规抗结核治疗的基础上加用拉米夫定进行治疗,旨在分析探究其对乙肝合并肺结核患者免疫功能及肝功能的影响,现具体报道如下。
1 资料和方法
1.1 一般资料
患者纳入标准:①符合乙肝及肺结核防治指南中的诊断标准[6];②肺结核涂片结果阳性;③肺结核首次治疗;④HBV血清标志物结果阳性;⑤无原发性心、肾功能异常。患者排除标准:①患自身免疫性肝病、酒精性肝病等其他肝脏疾病患者;②近期内使用过会引起肝损伤的药物者,如5-氟尿嘧啶、甲氨蝶呤等;③有饮酒史患者;④有吸烟史者。
选取2015年5月至2016年12月于本院接受治疗且符合纳入标准的患者146例,采用随机数字法分为研究组和对照组各73例。2组患者的各项基本资料比较,差异无统计学意义(P>0.05),具有可比性,详细数据请见表1。本次研究经医院医学伦理委员会批准,所有患者均已告知并签署知情同意书,同意自愿配合此次研究。
1.2 仪器与试剂
AU5800全自动生化分析仪(美国贝克曼库尔特公司);荧光定量PCR分析仪(南京庚辰科学仪器有限公司);CytoFLEX流式细胞仪(美国贝克曼库尔特公司);甘草酸二胺胶囊(正大天晴药业集团股份有限公司;规格50 mg;批号H10940191);拉米夫定片(湖南千金湘江药业股份有限公司;规格0.1 g;批号H20103481);异烟肼片(安徽华辰制药有限公司;规格0.1 g;批号H34020110);利福平胶囊(重庆药友制药有限责任公司;规格0.3 g;批号H50020505);盐酸乙胺丁醇片(广州白云山明兴制药有限公司;规格0.25 g;批号H44020250);ALT、TBiL、AST酶联免疫吸附法试剂盒(上海酶联生物科技有限公司,规格96人份,批号:S10910113)。
1.3 治疗方法
对照组:采用常规抗结核及护肝治疗,护肝治疗采用甘草酸二胺;抗结核治疗采用异烟肼-利福平-乙胺丁醇治疗方案,其中异烟肼口服,0.4 g/次,一日一次;利福平口服,0.6 g/次,一日一次;乙胺丁醇口服,1.0 g/次,一日一次。
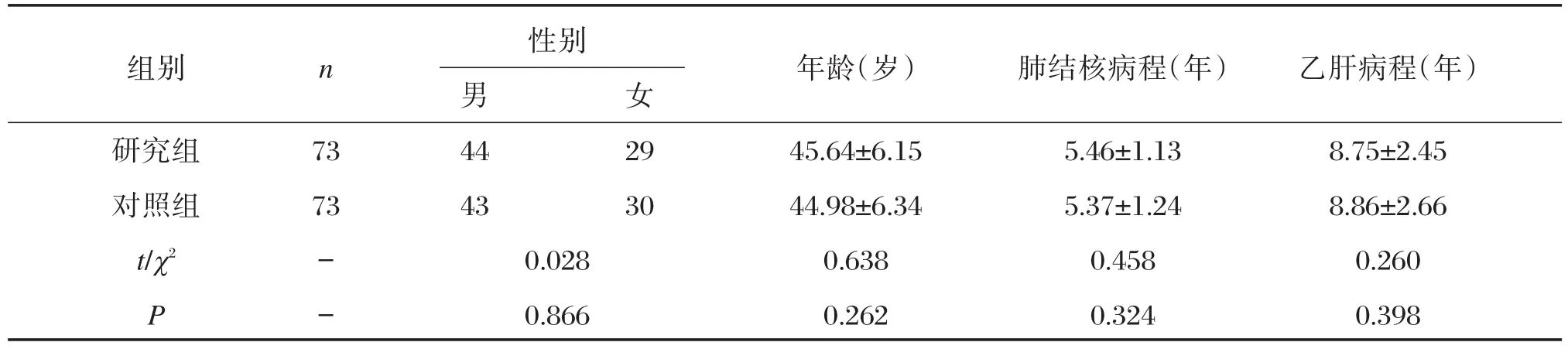
表1 2组患者临床基础资料比较Table 1 Comparison of basic clinical data of 2 groups
研究组:在对照组治疗基础上加用拉米夫定治疗,口服,100 mg/次,一日一次,自治疗开始时使用,于3个月治疗结束时终止。
2组患者均进行3个月治疗后进行评价。
1.4 疗效评价指标
采用AU5800全自动生化分析仪分别于治疗前、治疗1个月及治疗3个月后测定谷丙转氨酶(alanine aminotransferase,ALT)、总胆红素(total bilirubin,TBiL)、谷草转氨酶(aspartate aminotransferase,AST)等肝功能指标水平。采用荧光定量PCR分析仪测定治疗前后所有患者HBV-DNA含量。采用CytoFLEX流式细胞仪测定两组患者治疗前后CD4+、CD8+、CD4+/CD8+免疫功能指标水平。并统计两组治疗时不良反应发生情况以作比较。
1.5 统计学方法
采用SPSS 19.0统计学软件对所得所有数据进行统计分析。连续变量使用()表示。研究组与对照组比较计量资料采用独立样本t检验,计数资料以率(%)表示,采用卡方(χ2)检验。P<0.05表示差异具有统计学意义。
2 结果
2.1 2组患者治疗前后肝功能指标情况
分别于治疗前、治疗1个月及治疗3个月后测定所有患者ALT、TBiL、AST等肝功能指标水平,具体结果如表2所示。研究发现,治疗前,2组各项指标差异无统计学意义(P均>0.05)。治疗后,2组各项肝功能指标水平均有所增加,且对照组增加幅度更大。治疗3个月后,研究组的各项指标值明显低于对照组,差异具有统计学意义(P均<0.05)。
2.2 2组患者治疗前后免疫功能指标情况
治疗前后分别测定2组患者CD4+、CD8+、CD4+/CD8+等免疫功能指标水平,具体结果如表3所示。研究结果提示,治疗前,2组各项指标相比较,差异无统计学意义(P>0.05);治疗后,2组CD4+和CD4+/CD8+水平均有所上升,CD8+水平均有所下降,但研究组是变化明显,而对照组较治疗前无明显变化。2组治疗后数据相比较,差异具有统计学意义(P<0.05)。
2.3 2组患者治疗前后血清HBV-DNA含量情况
分别于治疗前后测定患者血清HBV-DNA含量,具体数据如表4所示,研究发现,治疗后研究组患者HBV-DNA水平呈下降趋势,对照组HBVDNA水平呈上升趋势,最终研究组HBV-DNA含量低于对照组,2组治疗后数据相比较,差异具有统计学意义(P<0.05)。
表2 2组患者治疗前后肝功能指标情况比较(±s)Table 2 Comparison of liver function indexes before and after treatment in the 2 groups of patients(±s)

表2 2组患者治疗前后肝功能指标情况比较(±s)Table 2 Comparison of liver function indexes before and after treatment in the 2 groups of patients(±s)
与研究组相比,bP<0.05;同组与治疗前相比,aP<0.05。
研究组对照组AST(U/L)TBiL(μmol/L)ALT(U/L)治疗前18.27±6.18 9.41±5.78 20.96±5.37治疗1个月后78.59±12.3a 45.34±6.48a 75.67±9.44a治疗3个月后89.51±16.42a 65.25±9.58a 91.87±13.65a治疗前19.04±6.24 9.66±5.37 20.58±5.22治疗1个月后97.15±12.34a/b 66.18±6.34a/b 105.19±9.83a/b治疗3个月后108.63±16.18a/b 78.16±9.78a/b 119.31±13.54a/b
表3 2组患者治疗前后肝功能指标情况比较(±s)Table 3 Comparison of immune function indexes before and after treatment in the 2 groups of patients±s)
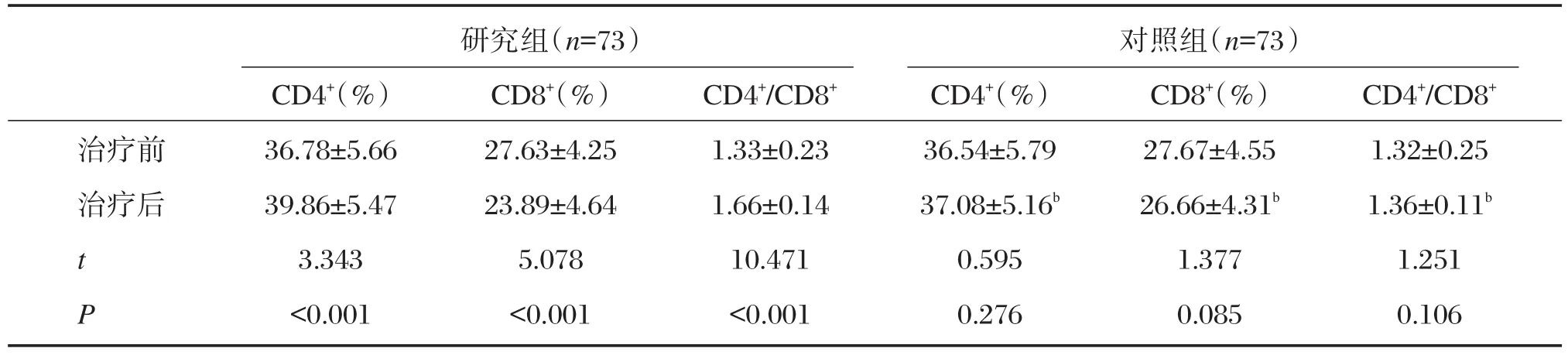
表3 2组患者治疗前后肝功能指标情况比较(±s)Table 3 Comparison of immune function indexes before and after treatment in the 2 groups of patients±s)
与研究组相比,bP<0.05。
研究组(n=73) 对照组(n=73)治疗前治疗后t P CD4+(%)36.78±5.66 39.86±5.47 3.343<0.001 CD8+(%)27.63±4.25 23.89±4.64 5.078<0.001 CD4+/CD8+1.33±0.23 1.66±0.14 10.471<0.001 CD4+(%)36.54±5.79 37.08±5.16b 0.595 0.276 CD8+(%)27.67±4.55 26.66±4.31b 1.377 0.085 CD4+/CD8+1.32±0.25 1.36±0.11b 1.251 0.106
表4 2组患者治疗前后血清HBV-DNA含量比较(copies/mL±s)Table 4 Comparison of serum HBV-DNA levels before and after treatment in the 2 groups of patients(copies/mL±s)

表4 2组患者治疗前后血清HBV-DNA含量比较(copies/mL±s)Table 4 Comparison of serum HBV-DNA levels before and after treatment in the 2 groups of patients(copies/mL±s)
与研究组相比,bP<0.05。
对照组(n=73)6.44±1.13 8.56±1.23b 11.384<0.001治疗前治疗后t P研究组(n=73)6.39±1.04 3.14±1.25 17.077<0.001
2.4 2组患者不良反应情况
2组均出现不良反应情况,主要表现为恶心呕吐、消化不良、皮疹、腹泻、乏力等。其中研究组不良反应共15例,不良反应发生率为20.55%;对照组不良反应共17例,不良反应发生率为23.29%。2组不良反应无显著差异(P=0.160,χ2=0.689)。
3 讨论
近年来,我国肺结核发病率逐渐增高,至今已有大于450万肺结核患者,常规抗结核治疗即会对患者肝脏造成一定的损伤,而合并乙肝患者在抗结核治疗中相比于单一肺结核患者更易造成肝损伤[7-8]。因此,寻找既能达到治疗目的,又能起到肝保护作用的药物十分重要。拉米夫定是一种抗病毒药物,对病毒DNA的合成和延长有竞争性抑制的作用,但不干扰正常细胞脱氧核苷的代谢,长期运用可有效改善肝脏炎症及坏死情况[9-10]。本文旨在探究其对乙肝合并肺结核患者肝功能的影响,并从免疫功能及HBV-DNA复制等多方面进行辅助说明。
本研究发现,治疗前,所有患者ALT、TBiL、AST等肝功能指标水平差异无统计学意义。通过治疗,2组各项指标均呈上升趋势,由以上数据可知,肝功能的各项指标亦呈现高表达状态,不使用拉米夫定治疗的对照组各项指标呈持续增高趋势,而加用拉米夫定抗病毒治疗的研究组各项指标虽也升高,但相比于对照组上升幅度得到有效控制,最终研究组各项肝功能指标值远低于对照组,其数据差异具有统计学意义(P<0.05)。说明拉米夫定可有效减轻患者肝脏损伤,减缓患者肝功能指标水平上升趋势,改善患者肝功能状态,这与李多云等人[11]的研究相符。有研究提示,CD4+、CD8+作为机体重要的免疫细胞,其比例失衡可能与肝细胞损伤相关,其比值的变化与HBV感染患者免疫功能的变化相关[12]。本研究结果显示,通过治疗,2组患者CD4+和CD4+/CD8+水平均有所上升,CD8+水平均有所下降,且研究组变化明显,2组治疗后数据相比较,差异具有统计学意义(P<0.05)。说明研究组的治疗方法对于患者免疫功能的改善具有更好的效果,其指标变化与厉景南等人[13]报道相一致。除此以外本研究对2组治疗时的不良反应进行了统计,研究组不良反应发生率为20.55%,低于对照组不良反应发生率23.29%,2组不良反应发生率均较低,且无明显差异(P>0.05)。说明拉米夫定抗病毒治疗具有较好的使用安全性。血清HBV-DNA作为乙肝病毒复制的可靠指标,其含量降低表示患者病情减轻,因此,测定其含量能了解患者乙肝病情[14]。研究发现,通过治疗,研究组患者HBV-DNA含量有所降低,对照组HBV-DNA含量有所增加,治疗后研究组HBV-DNA水平低于对照组,2组数据差异具有统计学意义(P<0.05)。说明联用拉米夫定进行抗病毒治疗,对于乙肝病毒的控制具有良好的效果,这与大多数拉米夫定抗病毒治疗报道相符。
综上,拉米夫定抗病毒治疗对于乙肝合并肺结核患者来说,能有效提高患者免疫功能,减轻患者肝损伤从而改善其肝功能状态,提高治疗有效率,在临床实践中具有实用和推广价值。当然,慢性病除了积极配合治疗以外,良好的生活习惯和心理建设也是十分重要,患者应当保持良好的休息,培养良好的生活习惯,调整好心理状态,积极对待疾病和生活[15]。