基于网络药理学的人参二醇对阿尔茨海默病细胞保护作用的研究
2018-09-10梁喜才姚璎珈王玉莹李秀丽王雅萌杨静娴
梁喜才,姚璎珈,王玉莹,李秀丽,王雅萌,蔺 莹,时 悦,杨静娴
(辽宁中医药大学药学院,辽宁 大连 116600)
阿尔茨海默病(Alzheimer’s disease,AD)是一种常见的中枢神经系统退行性疾病,现代研究发现,AD的发病机制复杂且尚不明确,以β淀粉样蛋白(β-amyloid,Aβ)级联反应假说最为公认。淀粉样前体蛋白(amyloid precursor protein,APP)的水解异常,导致了Aβ42的形成,Aβ42聚集激活AD患者和小鼠脑中非受体酪氨酸激酶(non-receptor tyrosine kinase,FYN)的活性,而FYN的表达增加,加重Aβ诱导的突触损伤和过早死亡[1]。在海马区域,FYN是突触后致密物质的组成成分之一,能够通过磷酸化N-甲基-D-天冬氨酸受体(N-methyl-D-aspartate receptors,NMDAR),使NMDAR2B磷酸化增加,导致Ca2+内流增加,引起细胞内Ca2+超载,造成突触损伤、神经元凋亡,从而引起和加重AD的发生和发展[2-3]。
人参二醇(panaxadiol,PD)是从人参中提取出的有效成分。目前,国内外研究表明,PD对受损的神经细胞具有一定的保护作用,而且对APP/PS1双转基因小鼠的学习记忆能力也有改善作用[4-6]。本实验利用APP转染小鼠神经母瘤细胞(mouse neuroblastoma N2a cells,Neuro-2a),构建AD的细胞模型作为体外实验,以探索PD对AD的治疗作用,为将人参进一步开发成为治疗AD新药提供实验依据。
1 材料
1.1细胞株N2a细胞、293T细胞,均购于首都医科大学。
1.2药物与试剂PD购于成都普菲德公司(纯度98.36%,批号19666-76-3)。DMEM高糖培养基、胎牛血清(fetal bovine serum,FBS)、胰蛋白酶消化液、青霉素/链霉素(penicillin and streptomycin,P/S),均购于Gibco公司;APP595/596质粒、GFP质粒DNA,以及慢病毒辅助质粒pLP1、pLP2、pLP/VSV-G,均为实验室前期构建;Lipofectamine TM 2000购于Invitrogen公司;MTT细胞增殖与活性检测试剂盒购于Dojindo公司;乳酸脱氢酶(lactate dehydrogenase,LDH)试剂盒购于南京建成生物技术有限公司;凋亡试剂盒购于天津三箭生物技术股份有限公司;钙离子荧光探针购于AAT Bioquest;FYN-Y416抗体购于ABclone。
1.3仪器Ti-S型荧光显微镜(日本尼康);CO2培养箱(美国UNAIRE公司);流式细胞仪(美国BD公司);ZHJH-C1112B双人超净工作台(美国Agilent公司)。
2 方法
2.1网络分析
2.1.1处方来源 进入CNKI(http://kns.cnki.net/kns/brief/default_result.aspx)检索页面,选择高级检索,主题词为“老年痴呆”,匹配词选“模糊”,排序时间选2000-2017年,其余设为默认。检索出与“老年痴呆”相关文献共9871条。并筛选《中医方剂大辞典》中,方剂主治或功效中含有与“记”、“忘”、“智”、“痴”、“呆”等关键字的所有方剂[7],共筛选出107个方剂,将方剂中的药材按出现频次进行排序。
2.1.2人参小分子数据库的建立 通过TCMSP (http://ibts.hkbu.edu.hk/LSP/tcmsp.php)数据库,将所有的人参小分子的数据及AD靶点进行收集和下载,人参共有380个化学小分子成分,通过对这些药物分子的药理学和分子特性(ADME/T OB≥30%;DL≥0.11;BBB≥-0.3)预测和评价,获得人参潜在药效成分,最终共有18个活性成分被收集。并通过TCMSP 检索出29个AD相关靶点,并通过Pubmed数据库检索出与Ca2+相关靶点。
2.2分子模拟对接根据Protein Data Bank数据库(http://www.rcsb.org)下载FYN结构。将靶标和中药中化学成分的三维结构导入PyMOL中,对蛋白结构进行清除配体,删除靶蛋白分子结构中的水分子,在将人参成分及分开的受体与配体导入AutoDockTools-1.5.6,加上极性氢原子,赋予电荷。以原配体分子所在的位置作为结合位点,活性口袋部分进行分子定位,再将定位后的值输入Vina软件,进行分子对接评分。分子对接后,以原配体分子与靶蛋白受体的对接分数为域值,选取人参成分中的中药化学成分与相关靶蛋白对接分数高于阈值的靶蛋白,即认为该靶蛋白与人参中药中的化学成分具有较好的相互作用。并使用Cyto Scape_v3.5.0构建药物-靶点-疾病网络(C-T-D 网络)。
2.3建立AD细胞模型N2a细胞、293T细胞均培养于高糖DMEM完全培养基 (10% FBS、1% P/S)中,于37℃、5% CO2培养箱中培养,3 d换液1次。将目的质粒用Lipofectamine 2000介导转染293T细胞。用浓缩病毒上清感染N2a细胞,感染3 d后,在倒置荧光显微镜下观察荧光。
2.4MTT法检测细胞活力将细胞以5×103/孔的密度接种于96孔板中, 分为GFP-N2a、APP-N2a、APP-N2a+PD 3组。24 h后,每孔加入10 μL MTT溶液,继续培养4 h后取出,弃培养基,加入100 μL DMSO,室温静置10 min,用酶标仪在450 nm处检测吸光度(A)值。
2.5LDH释放量的检测细胞以5×103每孔接种96孔板,每组设3个复孔,培养24 h后取上清液,根据试剂盒说明书操作,用紫外-可见光分光光度计于510 nm下测定吸光度值。
2.6流式细胞术检测细胞凋亡及细胞内Ca2+浓度细胞接种于6孔板,分两组分别处理:第1组用不含EDTA的胰酶消化,PBS清洗2遍后,加入5 μL Annexin V-Light 650混匀后,加入5 μL PI混匀,室温避光反应15 min;另一组分为GFP-N2a、APP-N2a、APP-N2a+PD、APP-N2a+PP2、APP-N2a+PP2+PD 5组,分别加Cal-630AM 10 μmol·L-1,于37℃、5% CO2培养箱中孵育1.5 h,室温0.5 h,用流式细胞仪检测细胞凋亡及细胞内Ca2+浓度。
2.7Westernblot检测FYN-Y416的蛋白表达水平在PD及FYN抑制剂PP2作用24 h后,根据全蛋白提取试剂盒说明书提取N2a蛋白,将蛋白(20 μg)等量上样到10% SDS-PAGE电泳,转移到PVDF膜上,膜封闭1 h,一抗FYN-Y416(1 ∶2 000)孵育过夜,室温下用HRP标记的二抗(1 ∶5 000)孵育1 h,凝胶成像系统拍照保存,并用Image J定量测定信号强度。

3 结果
3.1用药频次分析对治疗AD的107个方剂进行频次分析,可得到188种药材,从高到低频次排序,统计出频次前20的药材见Tab 1。
3.2人参活性成分的筛选根据TCMSP数据库评分标准分析,在人参中有18种化合物具有良好的口服生物利用度(OB≥30%)、类药性(DL≥0.18)和血脑屏障渗透性(BBB≥-0.30)。人参筛选的活性化合物的化学信息和网络信息见Tab 2。

Tab 1 Top 20 frequency of Chinese medicinein formulas of AD treatment
3.3AD相关靶点的筛选通过TCMSP数据库进行AD检索,检索到AD相关靶点29个(Fig 1),将下载的靶点输入到Uniprot数据库,并通过Pubmed数据库确定FYN可磷酸化GluN2B受体,使Ca2+浓度增加。
3.4人参成分与FYN分子对接结果将人参成分与FYN进行分子对接,为使假阳性率降低,本研究组将人参成分采用AutoDockTools-1.5.6和Vina两种方法与FYN进行对接。结果显示,有7个成分与FYN具有较好的相互作用,其中PD与FYN作用最好(Tab 3)。
3.5成功建立APP-N2a细胞模型将APP595/596及GFP质粒转染293T细胞包装病毒液,感染N2a细胞,3 d后可观察到绿色荧光(Fig 2),表明模型建立成功。
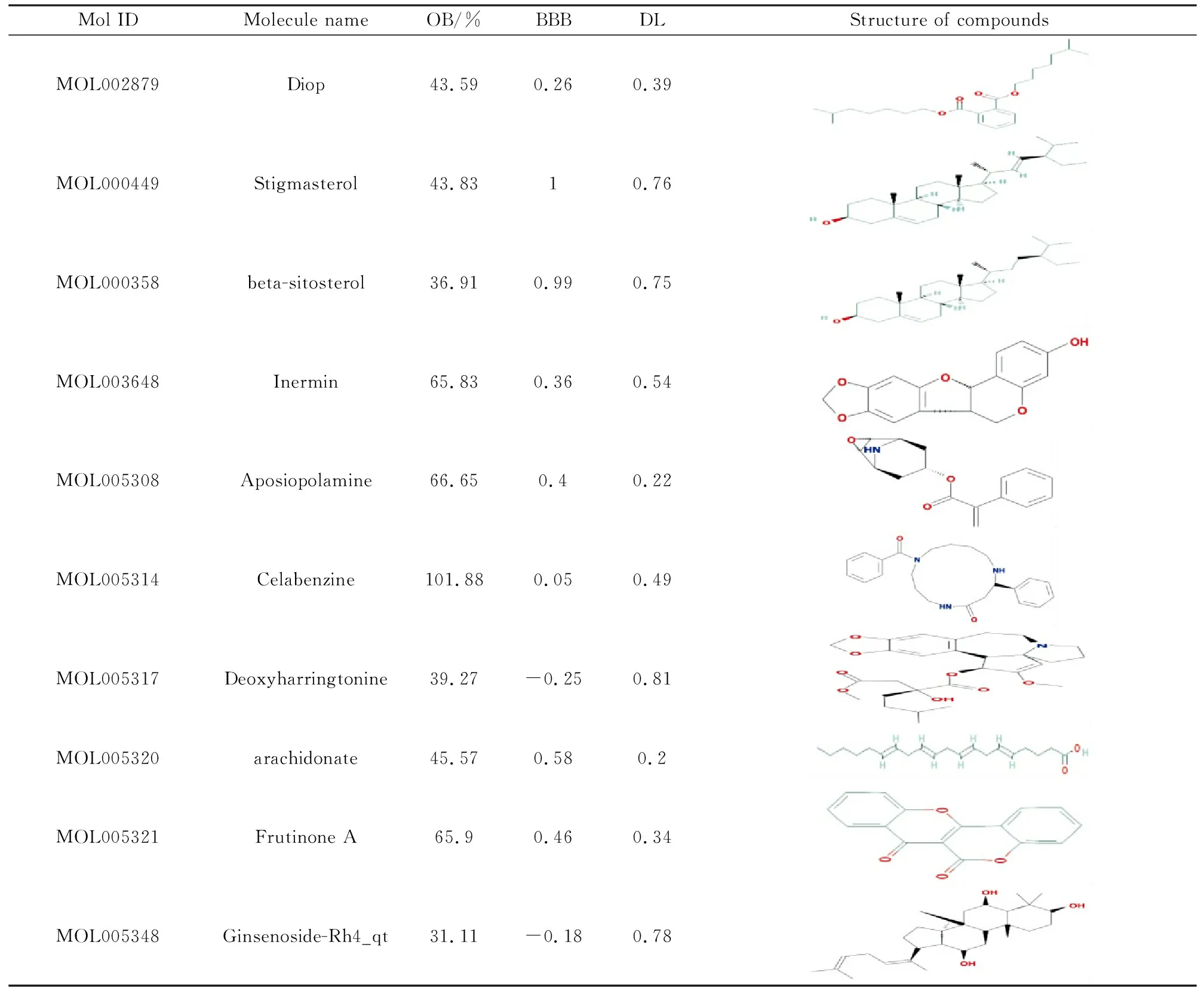
Tab 2 Active compounds of ginseng
续表2
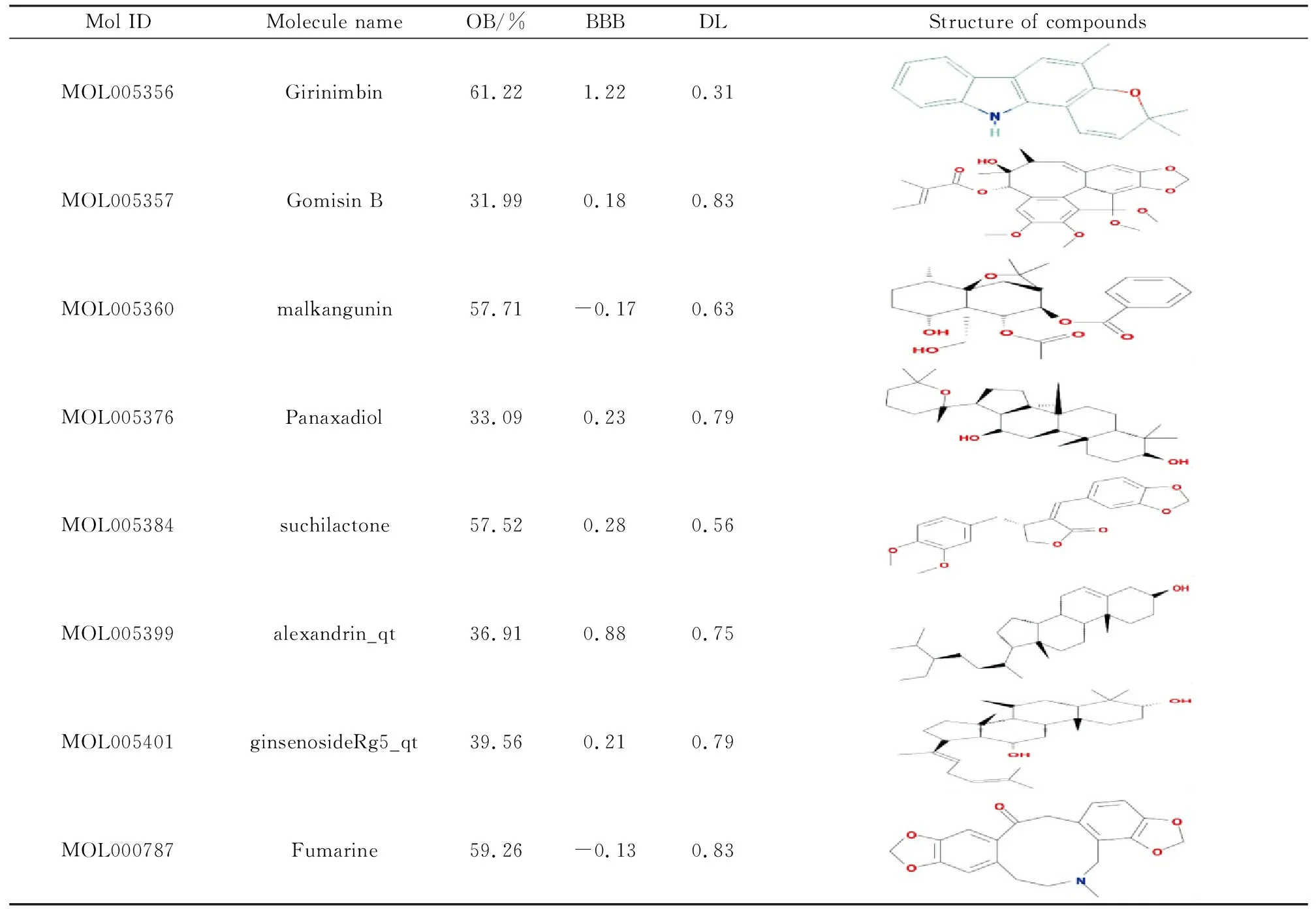
Mol IDMolecule nameOB/%BBBDLStructure of compoundsMOL005356Girinimbin61.221.220.31MOL005357Gomisin B31.990.180.83MOL005360malkangunin57.71-0.170.63MOL005376Panaxadiol33.090.230.79MOL005384suchilactone57.520.280.56MOL005399alexandrin_qt36.910.880.75MOL005401ginsenosideRg5_qt39.560.210.79MOL000787Fumarine59.26-0.130.83

Fig 1 AD-related targets-disease network diagram

Fig 2 Expression of APP in N2a cells(×20)
TG:Transgenic; NTG:No Ttransgenic.

Tab 3 Docking scores of Gginseng compounds and FYN protein
3.6PD能明显提高APP-Na2细胞的活力Fig 3的MTT检测结果显示,与对照组相比,转染APP595/596基因的模型组细胞存活率明显下降(P<0.01),而不同浓度的PD可使细胞活力上升,其中经75 mg·L-1PD处理的细胞活力最高。上述结果显示,75 mg·L-1PD为保护APP-N2a细胞的最佳浓度。
3.7PD减少APP-N2a细胞的LDH释放量Fig 4的LDH检测结果显示,模型组LDH的释放量为对照组的1.5倍,差异具有统计学意义(P<0.01);PD给药组与模型组相比,能明显降低LDH的释放量(P<0.01)。
3.8PD抑制APP-N2a细胞的凋亡Fig 5流式细胞技术结果显示,模型组凋亡细胞的百分比80.9%,与对照组的16.4%相比,差异有统计学意义;PD给药组的凋亡细胞百分比为71.6%,明显低于模型组,说明人参二醇能有效抑制APP-N2a细胞的凋亡。
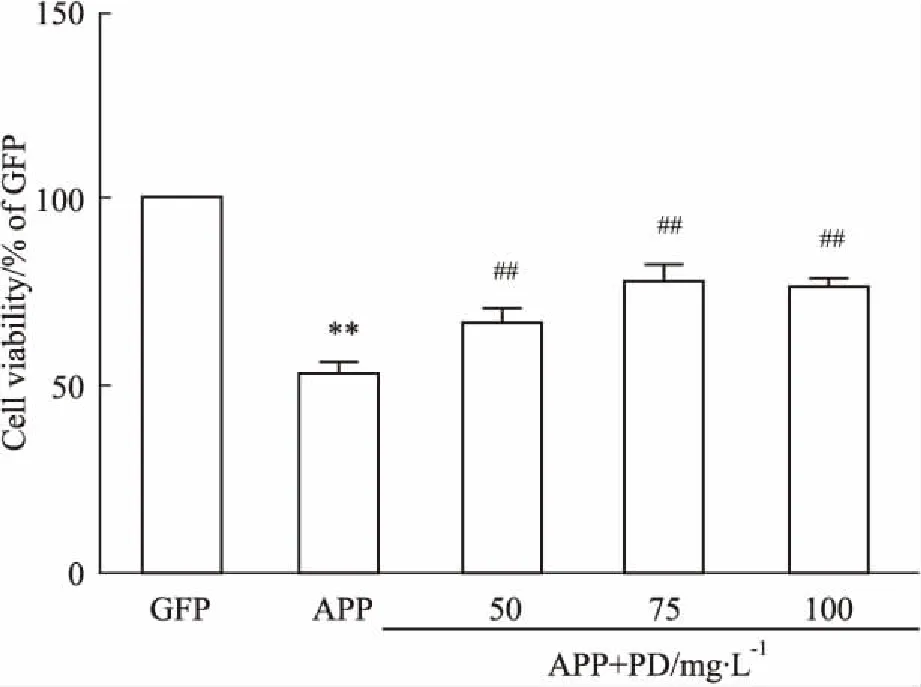
Fig 3 The cell viability was detected by MTT
**P<0.01vsGFP group;##P<0.01vsAPP group
3.9PD降低AD细胞内FYN-Y416蛋白表达Fig 6的Western blot结果显示,与对照组相比,模型组FYN-Y416蛋白的表达量明显增多(P<0.01);与模型组比较,PD给药组和FYN抑制剂组FYN-Y416表达明显降低(P<0.01)。
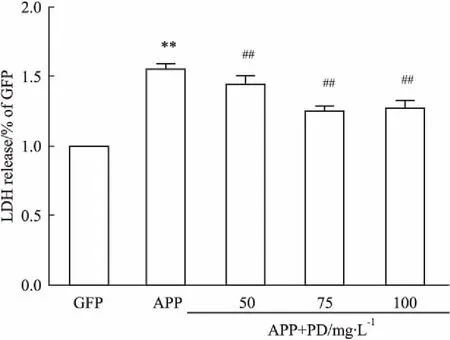
Fig 4 The release of lactate dehydrogenasewas determined by LDH )
**P<0.01vsGFP group;##P<0.01vsAPP group
3.10PD减轻APP-N2a细胞内Ca2+超载如Fig 7所示,与模型组细胞数相比,对照组的细胞数的百分比为50%,差异有统计学意义(P<0.01);而给药组和抑制剂组细胞数的百分比分别为62.5%、68.75%,明显高于模型组(P<0.01),说明PD能减轻APP-N2a细胞的Ca2+超载。
4 讨论
网络药理学是从生物网络的角度,研究疾病发生和发展过程,认识药物与机体的相互作用,并指导新药发现的新学科。应用高通量组学数据、分子网络数据,对药物-靶点网络整体的分析,有助于理解药物的多靶点、多途径网络调控模式,研究药物的作用机制和促进药物创新。但网络药理学存在一定的局限性,若要将研究的结果用于临床,尚需要药理实验验证。
AD多起病于老年期,病程缓慢且不可逆,以进行性认知功能障碍、记忆力衰退、语言以及社会适应程度的改变为主要临床表现。国际阿尔茨海默病协会指出,每6 s就会确诊1位AD患者,估计2015年全世界有4 680万人患有痴呆症,到2050年,这个数字将达到1.135亿[9]。AD患者脑内,Aβ与细胞性朊蛋白(PrPc)结合,激活了FYN,从而使NMDAR2B磷酸化增加[8]。FYN能够磷酸化NMDAR2B的1472位点,该位点的磷酸化会阻碍NMDAR2B和接头蛋白AP2的结合,进而抑制其内化,导致含有NMDAR2B的NMDA受体在细胞膜上表达增多,引起Ca2+大量内流,导致Ca2+超载[10-13],从而引起神经元机能亢进,介导记忆和认知障碍。抑制AD神经元过度活动,恢复突触前Ca2+储存,可作为控制AD相关神经元活动过度的关键因素,并作为改善治疗疾病的目标[14]。

Fig 5 The anti-apoptosis cellstic effect of PD(75 mg·L-1) on the N2a cells transfected with APP595/596
A:Effects of PD on the APP-N2a apoptotic cells were measured by flow cytometry; B:Quantitative analysis of apoptosis in APP-N2a cells.**P<0.01vsGFP group;##P<0.01vsAPP group.
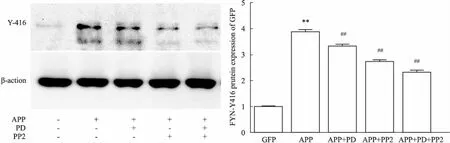
Fig 6 The expression of p-FYN protein was detected by Western
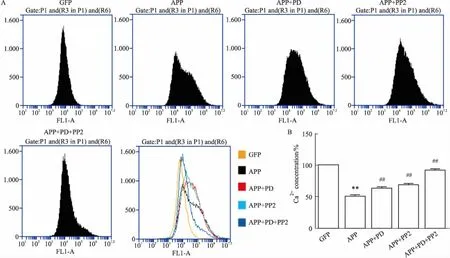
Fig 7 PD reduced intracellular Ca2+ overload in APP-N2a
A:The Ca2+levels of cells in all groups were measured by flow cytometry; B:Quantitative analysis of Ca2+levels in cells.**P<0.01vsGFP group;##P<0.01vsAPP group.
从CNKI中的9871检索结果和《中医方剂大辞典》中方剂主治或功效中含有与“记”、“忘”、“智”、“痴”、“呆”等关键字的所有方剂中,综合整理出107个方剂,并对这107个方剂中的药材进行统计,得到出现频率最多的前20味中药材,其中人参共出现68次,并根据TCMSP数据库的评分准则(OB≥30%;BBB≥-0.3;DL≥0.18)对人参成分进行筛选,得出18个人参成分。再根据TCMSP数据库及Pubemd数据库预测出有关AD的相关靶点,从29个AD靶点中,筛选出FYN靶向参与了AD脑内Ca2+的调控。并利用分子对接技术,对人参的18个成与FYN模拟对接,并筛选出评分最高的药物为PD(9.5)。在体外成功构建AD模型,进一步研究了PD对APP-N2a细胞的保护作用,通过MTT法和LDH法发现,75 mg·L-1的PD对APP-N2a细胞具有促进存活能力、减少损伤的保护作用。为了进一步研究PD对神经细胞保护作用,本实验室对FYN-Y416蛋白表达量及细胞内Ca2+浓度进行检测,结果表明,PD可以明显降低APP-N2a细胞FYN-Y416蛋白表达,并减轻其Ca2+超载现象。
综上所述,PD具有神经保护作用,能通过抑制FYN的磷酸化,减轻AD细胞Ca2+超载现象,提高细胞的存活率,降低损伤程度,并且可减少细胞凋亡,为治疗AD相关新药研发提供重要的实验依据。
