Fenton试剂深度处理脱墨浆废水的反应动力学研究
2018-09-10罗清谢飞张安龙
罗清 谢飞 张安龙
摘 要:研究了以Fenton试剂为氧化剂,以聚丙烯酰胺(PAM)为絮凝剂对脱墨浆造纸废水氧化絮凝的深度处理方法,并对其氧化机理及动力学进行了分析。通过一系列单因素实验研究结果表明,Fenton氧化过程中各个影响因素对CODCr去除率均有不同的影响,综合比较各个实验结果发现,当体系中FeSO4投加量为0.5 g/L、n(H2O2)∶n(Fe2+)=1.5∶1、初始pH值=3.0、反应时间35 min时,氧化絮凝后CODCr去除率达到55.1%。以一级反应动力学方程为模型,对研究中氧化过程进行了多因素的动力学分析。通过多元回归分析模拟得到反应速率常数k的表达式为k=0.273[H2O2]-0.067[Fe2+]0.594。
关键词:Fenton;造纸废水;CODCr去除;深度处理;动力学
中图分类号:TS75
文献标识码:A
DOI:10.11980/j.issn.0254-508X.2018.04.004
Abstract:Advanced treatment wastewater from papermaking using deinked pulp as raw material was studied with the oxidationflocculation method by Fenton′s reagent as oxidant and PAM as flocculant, and the oxidation mechanism and kinetics were analyzed. According to the results from a series of singlefactor experiments, it was found that the various influence factors in the oxidation process had different effects on CODCr removal efficiency. From the experimental results, a desirable CODCr removal rate of 55.1% was obtained after oxidationflocculation at FeSO4 dosage 0.5 g/L, molar ratio n(H2O2)∶n(Fe2+)=1.5∶1, initial pH=3.0 and reaction time t=35 min. A multifactor kinetic of oxidation process analysis was carried out by using firstorder model reaction rate constant k was expressed as k=0.273[H2O2]-0.067[Fe2+]0.594 through multiple regression analysis.
Key words:Fenton; papermaking wastewater; CODCr removal; advanced treatment; kinetics
造纸废水的回收利用过程中会产生大量的难降解物质,其中脱墨浆废水对水体污染问题最为严重,近年来脱墨浆废水的深度处理倍受关注[1-3]。脱墨浆废水因其水质复杂、水中有机物含量高、难降解物质多等特点 [4-5],普通的氧化处理方法难以满足造纸废水国家标准GB3544—2008规定的排放要求,需要研究一种较好的深度氧化处理方法,来处理脱墨浆废水。
Fenton试剂是近几年来研究的热点[6-8],Fenton试剂可以氧化降解绝大部分有机物,用于去除制浆造纸废水中具有生物毒性或生物难降解的有机污染物具有明显优势,正日益受到国内外的关注。Fenton试剂在水处理中的作用主要包括对有机物的氧化和混凝两种[9-12]。对有机物的氧化作用是指Fe2+与H2O2作用生成具有极强氧化能力的羟基自由基HO·,可以破坏有机物结构,并将有机物矿化为CO2和H2O[13-15];另一方面,反应中生成的Fe(OH)3胶体具有絮凝、吸附功能,也可去除水中部分有机物[16-17]。Fenton作用下的氧化过程影响因素很多,如FeSO4投加量、n(H2O2)∶n(Fe2+)、初始pH值、反应时间等均会对氧化效果产生不同程度的影响。
本实验是以Fenton 试剂深度处理脱墨浆废水的研究对象,探讨各影响因素对氧化降解反应的影响并测定氧化降解后的CODCr值,从而获得Fenton氧化的最佳工艺条件,并通过多元回归分析模拟得到Fenton 氧化体系的反应动力学速率常数。为更好地将Fenton试剂应用于的脱墨浆废水深度处理提供科学依据。
1 实 验
1.1 实验废水
实验中所用的废水采集于某造纸厂脱墨浆废水二级生物处理单元出水口,主要指标:CODCr 93.43 mg/L,色度4倍,pH值7.5, SS 13 mg/L。
1.2 仪器与药品
仪器:JJ-1型精密电动搅拌器;PB-10型pH计;5B-6C (V8)型多参数水质测定仪等。
药品:二氯甲烷:色谱纯,天津市康科德科技有限公司;氯化钠(NaCl)、无水硫酸钠(Na2SO4):优级纯,国药集团;过氧化氢(H2O2):分析纯(质量分数30%),天津市大茂化学試剂厂;七水合硫酸亚铁(FeSO4·7H2O)、亚铁(Fe2+):分析纯,天津市大茂化学试剂厂;氢氧化钠(NaOH)、聚丙烯酰胺(PAM): 分析纯,相对分子质量为1000万,天津市康科德科技有限公司。
1.3 实验方法
1.3.1 Fenton反应方法
(a)取100 mL的废水置于烧杯,放在电动搅拌器上,并用预先制备好的H2SO4溶液调节废水pH值至设定条件。
(b)根据实验设计,每次实验根据FeSO4·7H2O的投加量和摩尔比,依次确定并加入实验所需Fe2+和H2O2的用量,并在適宜的转速下先投加FeSO4·7H2O,再边搅拌边加入适量的H2O2(质量分数30%)。
(c)维持废水温度在室温下进行Fenton氧化过程。
1.3.2 pH值调节方法
Fenton反应至设定时间时,用预先准备好的NaOH溶液和H2SO4溶液调节其pH值至7.0~7.5,终止反应。
1.3.3 絮凝方法
Fenton反应以及pH值调节后的废水中加入一定量的PAM,慢速搅拌30 s,静置沉淀20 min,取上清液进行分析。
2 结果与讨论
Fenton试剂在水处理中的作用,主要包括对有机物的氧化和混凝两种。对有机物的氧化作用是指Fe2+与H2O2作用生成具有极强氧化能力的羟基自由基HO·,可以破坏有机物结构,并将有机物矿化为CO2和H2O[18-19];另一方面,反应中生成的Fe(OH)3 胶体具有絮凝、吸附功能,也可去除水中部分有机物。其主要反应机理如下:
Fe2++H2O2Fe3++OH-+HO·(1)
Fe3++H2O2Fe2++HOO·+H+(2)
由于反应体系生成的Fe(OH)3胶体絮凝效果不是很好,故加一定量的PAM絮凝剂以增强体系的絮凝效果。
2.1 FeSO4投加量的影响
在Fenton反应体系中, FeSO4起着催化作用,通过控制Fe2+的浓度可有效提高降解效果。将实验条件设计为:pH值=3.0,n(H2O2)∶n(Fe2+)=1∶1,反应时间为5、10、15、20、25、30、30 min,PAM投加量2 mg/L,研究不同反应时间下Fe2+浓度对CODCr去除率的情况,实验结果见图1。
由图1可以看出,随着FeSO4投加量的增加,废水的CODCr去除率均有所增加,当FeSO4投加量为0.5、0.6、0.8 g/L,且Fenton氧化反应30 min时的废水中CODCr去除率几乎相同,均达到了45%以上。这是由于Fenton反应过程中,Fe2+起着催化剂作用,当催化剂Fe2+浓度较小时,不利于催化反应的充分进行,H2O2产生HO·的量较少并且产生的速度较慢[20-22]。当Fe2+浓度较高时,Fe2+可以催化Fenton氧化反应进行,从而使得水中的较多的污染物质被氧化,导致水中的CODCr值逐渐下降。
随着FeSO4投加量的增加,Fenton氧化反应30 min时,反应停止,加入NaOH溶液调节废水pH值至中性,再用PAM 絮凝20 min后,废水中CODCr的去除率呈现先增加后下降的变化趋势,见图2。当FeSO4投加量为0.5 g/L,氧化絮凝后,废水的CODCr去除率最大,达到了56.8%。根据式(1)可知,当Fe2+浓度过高时,产生的Fe3+不仅反应后的出水色度增大,而且过量的Fe2+有部分存在于水体系中,被氧化成Fe3+,一定程度上抑制了HO·的生成,使得CODCr 的去除率随着FeSO4投加量的增加,呈现先增加后降低的趋势。
综合经济因素和处理效果,选择FeSO4投加量在0.5 g/L为去除CODCr的最佳条件。
2.2 摩尔比的影响
在Fenton反应体系中,H2O2作为反应体系的主要反应物,在pH值=3.0,FeSO4投加量为0.5 g/L,反应时间为5、10、15、20、25、30 min,PAM加量2 mg/L的条件下,研究H2O2与Fe2+不同摩尔比n(H2O2)∶n(Fe2+),即H2O2用量对CODCr去除率的影响,结果如图3所示。
从图3可以看出,随着n(H2O2)∶n(Fe2+)的逐渐增加,氧化反应的速率逐渐提高,CODCr 的去除率也随之增加。这是因为n(H2O2)∶n(Fe2+)的增加,也就意味着Fenton氧化体系中H2O2的用量在逐渐增加,而Fenton氧化体系主要依靠H2O2在Fe2+的催化作用下产生HO·来去除有机物[20],所以H2O2用量直接影响着CODCr 的去除率。H2O2用量增加,氧化体系产生更多的HO·,CODCr氧化效果提高且CODCr去除率增大。
随着n(H2O2)∶n(Fe2+)的增加,Fenton反应30 min时,反应停止,加入NaOH溶液调节废水pH值至中性,再用PAM 絮凝20 min后,废水中CODCr 的去除率呈现先增加后下降的变化趋势,如图4所示。当n(H2O2)∶n(Fe2+)=1.5∶1时,氧化絮凝后,脱墨浆废水的CODCr去除率最大,达到了68.1%。随着H2O2的量增加,H2O2产生的HO·也随之增多,使得CODCr的去除率也随之增加,但当H2O2的量继续增加时,CODCr 的去除率有所下降,一方面是因为H2O2是HO·的捕捉剂[23],当体系中H2O2超过一定量以后,随着H2O2浓度的增加,对羟基自由基的捕捉作用也随之增加,生成的一部分HO·被消耗掉,如式(3)所示。而反应产生HOO·的氧化能力没HO·强,造成了H2O2的无效分解,从而导致CODCr去除率随之下降,且H2O2具有一定的还原性,在测定CODCr时,会消耗掉一部分氧化性物质,导致CODCr测定发生偏差;另一方面可能是由于过量的H2O2没有产生更多的羟基自由基,反而在反应一开始就将Fe2+迅速氧化成Fe3+[23],根据式(1)可知,Fe3+抑制了HO·的生成,不能生成大量的HO·,使得水中的污染物质不能被有效降解,从而导致CODCr的去除率不升反降。
综合经济因素和处理效果,选择n(H2O2)∶n(Fe2+)=1.5∶1为去除CODCr 的最佳条件。
2.3 初始pH值的影响
在Fenton反应体系中,初始pH值作为反应体系的主要条件,在n(H2O2)∶n(Fe2+)=1.5∶1,FeSO4投加量为0.5 g/L,反应时间30 min,PAM投加量2 mg/L的条件下,通过调节初始pH值,研究不同初始pH值对CODCr去除率的影响,结果如图5所示。
从图5可以看出,当初始pH值等于3.0或5.0时,Fenton反应过程是正常进行的,CODCr的去除率在逐渐增加。当初始pH值大于7.0或者小于1.0时,Fenton反应过程中CODCr去除率呈现了负增长,这是因为如前所述,初始pH值增加,形成的Fe(OH)3会无效分解H2O2且使得水中的色度较高,Fe(OH)3具有一定的还原性,会消耗测定CODCr的氧化剂,从而Fenton处理后,初始pH值大于7.0和pH值小于1.0的废水的CODCr值比未经处理的废水的CODCr值更大,CODCr去除率呈现负增长。
随着初始pH值的增加,氧化絮凝后,废水中CODCr的去除率呈现先增加后下降的再增加的变化趋势,如图6所示。当初始pH值=3.0时,废水的CODCr去除率最大,达到了53.4%。
Fenton氧化反应是在酸性条件下发生氧化作用的,在中碱性条件下,Fe2+不能催化H2O2使其产生HO·,从而不能发生氧化反应[24]。从式(1)和式(2)可以看出,當pH值较低,即当H+浓度过高时,对Fenton氧化反应有抑制作用,抑制Fe2+的再生以及HO·的产生,分析当pH值低于2.0时,Fe2+与H2O2的反应会产生具有还原性的[Fe (H2O )6]2+,其会被CODCr测定试剂氧化,导致CODCr值升高,且同时H2O2会形成一种较为稳定的过氧化形式[H3O2]+,从而降低了H2O2与Fe2+反应的可能性[24];当pH值较高时,Fe3+会生成络合物Fe(OH)3,其也具有一定的还原性,导致CODCr值升高,且Fe(OH)3的生成阻断了Fe2+的再生,同时Fe(OH)3络合物也会催化H2O2无效分解为H2O和O2,导致Fenton氧化无法进行。
综合经济因素和处理效果,选择初始pH值=3.0时为去除CODCr的最佳pH值条件。
2.4 反应时间的影响
在Fenton反应体系中,反应时间影响反应体系的经济效益,在n(H2O2)∶n(Fe2+)=1.5∶1,FeSO4投加量为0.5 g/L,初始值pH值=3.0,PAM投加量2 mg/L的条件下,研究不同反应时间对CODCr去除率的影响,结果如图7所示。
从图7可以看出,在前35 min内,CODCr去除率随着反应时间的增加而增加,当反应时间35 min时,CODCr的去除率达到了55.1%;继续增加反应时间,CODCr的去除率有所下降;反应60 min时,氧化反应停止,加入NaOH溶液调节废水pH值至中性,再加PAM絮凝20 min后,CODCr的去除率达到了51.7%。
这是由于反应前35 min内,产生的HO·较多并且占主导地位,随着HO·的逐渐增多,分解破坏废水中一些难降解有机物占据了主导地位[20];反应进行到35 min后,废水中难降解的有机物逐渐减少,而且反应过程中pH值在逐渐降低,降低到一定程度时,生成较多的H+抑制了Fe2+的生成,从而使得链式反应无法继续进行,CODCr的去除率逐渐降低。反应后期CODCr稍有升高,可能是因为水中难降解的大分子物质被分解成了小分子物质[25],影响了CODCr值的测定。
综合经济因素和处理效果,选择35 min为CODCr 去除的最佳反应时间。
2.5 反应动力学模型研究
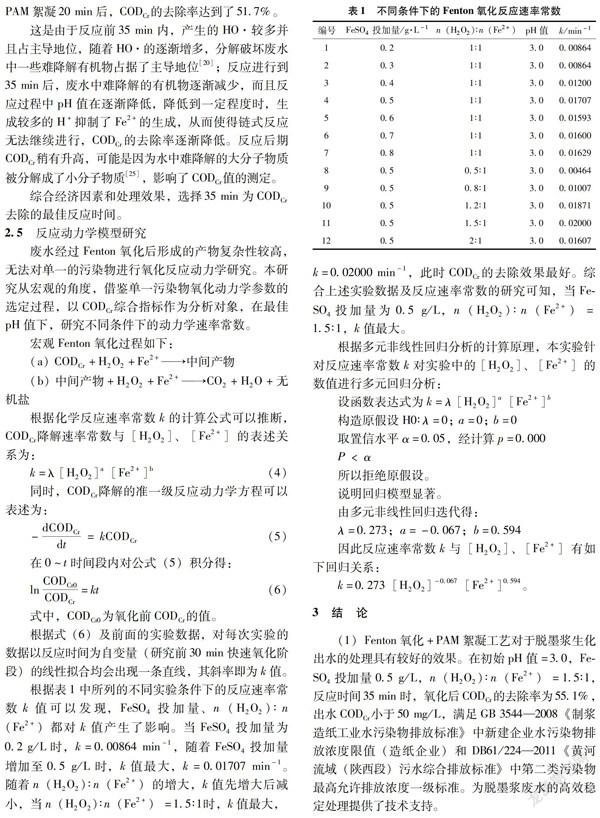
废水经过Fenton氧化后形成的产物复杂性较高,无法对单一的污染物进行氧化反应动力学研究。本研究从宏观的角度,借鉴单一污染物氧化动力学参数的选定过程,以CODCr综合指标作为分析对象,在最佳pH值下,研究不同条件下的动力学速率常数。
3 结 论
(1)Fenton氧化+PAM絮凝工艺对于脱墨浆生化出水的处理具有较好的效果。在初始pH值=3.0,FeSO4投加量0.5 g/L,n(H2O2)∶n(Fe2+)=1.5∶1,反应时间35 min时,氧化后CODCr的去除率为55.1%,出水CODCr小于50 mg/L,满足GB 3544—2008《制浆造纸工业水污染物排放标准》中新建企业水污染物排放浓度限值(造纸企业)和 DB61/224—2011《黄河流域(陕西段)污水综合排放标准》中第二类污染物最高允许排放浓度一级标准。为脱墨浆废水的高效稳定处理提供了技术支持。
(2)实验以CODCr综合指标作为分析对象,研究了不同条件下氧化过程的动力学速率常数k值,并通过多元非线性回归模拟得到最佳pH值=3.0时的反应速率常数k的表达式为:k=0.273[H2O2]-0.067[Fe2+]0.594。
参 考 文 献
[1] Simstich B, Beimfohr C, Horn H. Lab scale experiments using a submerged MBR under thermophilic aerobic conditions for the treatment of paper mill deinking wastewater.[J]. Bioresource Technology, 2012, 122(5): 11.
[2] Lu X G, Li F, Yan P P, et al. The Removal of Deinking Wastewater Using Neutralization, Activated Carbon, and Hydrogen Peroxide Oxidation[J]. Advanced Materials Research, 2013, 779/780: 1547.
[3] Balea A, Monte M C, De l F E, et al. Application of cellulose nanofibers to remove waterbased flexographic inks from wastewaters[J]. Environmental Science & Pollution Research, 2017, 24(5): 1.
[4] SHI Changwei. Treatment of Deinking Wastewater with Coagulation Process[J]. China Pulp & Paper, 2012, 31(2): 40.
史長伟. 混凝沉淀法处理脱墨废水的研究[J]. 中国造纸, 2012, 31(2): 40.
[5] HUANG Xin, FENG Wenying. Research Progress of Natural Biological Degradability of Wastewater[J]. Paper and Paper Making, 2016, 35(5): 29.
黄 馨, 冯文英. 造纸废水自然生化降解性的研究进展[J]. 纸和造纸, 2016, 35(5): 29.
[6] MO Lihuan, ZHOU Zhiming, WANG Yufeng. Advanced Treatment of Pulping Effluent by Ultrasonic Strengthened Fenton Process[J]. China Pulp & Paper, 2012, 31(1): 23.
莫立焕, 周志明, 王玉峰. 超声波强化Fenton试剂深度处理制浆中段废水[J]. 中国造纸, 2012, 31(1): 23.
[7] Ribeiro M C M, Starling M C V M, Leo M M D, et al. Textile wastewater reuse after additional treatment by Fenton′s reagent[J]. Environmental Science & Pollution Research International, 2016, 24(7): 1.
[8] Begum A, Agnihotri P, Mahindrakar A B, et al. Degradation of endosulfan and lindane using Fenton′s reagent[J]. Applied Water Science, 2017, 7(1): 207.
[9] WU Yanyu, ZHOU Shaoqi, QIN Fanghui, et al. Oxidation and coagulat ion of humic subs tances from landfi ll leachate by Fenton′ s reagent[J]. Journal of the Chemical Industry and Engineering Society of China, 2009, 60(10): 2609.
吴彦瑜, 周少奇, 覃芳慧, 等. Fenton试剂对垃圾渗滤液中腐殖质的氧化/混凝作用[J]. 化工学报, 2009, 60(10): 2609.
[10] Yoon J, Cho S, Cho Y, et al. The characteristics of coagulation of fenton reaction in the removal of landfill leachate organics[J]. Water Science & Technology, 1998, 38(2): 209.
[11] Yun W K, Hwang K Y. Effects of reaction conditions on the oxidation efficiency in the Fenton process[J]. Water Research, 2000, 34(10): 2786.
[12] Deng Y. Physical and oxidative removal of organics during Fenton treatment of mature municipal landfill leachate.[J]. Journal of Hazardous Materials, 2007, 146(1/2): 334.
[13] Fajerwerg K, Debellefontaine H. Wet oxidation of phenol by hydrogen peroxide using heterogeneous catalysis FeZSM-5: a promising catalyst[J]. Applied Catalysis B Environmental, 1996, 10(4): L229.
[14] Centi G, Perathoner S, Torre T, et al. Catalytic wet oxidation with H2O2 of carboxylic acids on homogeneous and heterogeneous Fentontype catalysts[J]. Catalysis Today, 2000, 55(1): 61.
[15] Shen Tong. Research on Degradation of Refractory Organics in Heterogeneous Fenton system With AuFe[D]. Harbin: Harbin Institute of Technology, 2013.
沈 彤. AuFe3O4构建的非均相Fenton体系处理难降解有机物的研究[D]. 哈尔滨: 哈尔滨工业大学, 2013.
[16] WANG Juan, YANG Zaifu. Application of Fenton Oxidation Technology in Wastewater Treatment[J]. Environmental Science & Technology, 2011, 34(11): 104.
王 娟, 杨再福. Fenton氧化在废水处理中的应用[J]. 环境科学与技术, 2011, 34(11): 104.
[17] LI Shaofeng, HUANG Junli, TAO Huchun. Treatment of some reactive dyes by Fenton reagent[J]. Journal of Harbin University of Civil Engineering and Architecture, 2001, 34(5): 76.
李绍峰, 黄君礼, 陶虎春. Fenton试剂降解水中活性染料的研究[J]. 哈尔滨建筑大学学报, 2001, 34(5): 76.
[18] Neyens E, Baeyens J. A review of classic Fenton′s peroxidation as an advanced oxidation technique.[J]. Journal of Hazardous Materials, 2003, 98(1/3): 33.
[19] Bautista P, Mohedano A F, Gilarranz M A, et al. Application of Fenton oxidation to cosmetic wastewaters treatment.[J]. Journal of Hazardous Materials, 2007, 143(1): 128.
[20] ZHAO Deng, ZHANG Anlong, LUO Qing, et al. Deep Treatment of Papermaking Wastewater by FentonFlocculation Process[J]. Paper & Paper Making, 2013(3): 58.
赵 登, 张安龙, 罗 清, 等. Fenton絮凝工艺深度处理造纸废水[J]. 纸和造纸, 2013(3): 58.
[21] TANG Youmin, GUAN Baohong, WU Zhongbiao. Mechanism and kinetic of methyldopa removal by Fenton′s reagent[J]. Environmental Science, 2008, 29(5): 1271.
汤优敏, 官宝红, 吴忠标. Fenton去除废水中甲基多巴的机制及动力学[J]. 环境科学, 2008, 29(5): 1271.
[22] Guedes A M, Madeira L M, Boaventura R A, et al. Fenton oxidation of cork cooking wastewater—overall kinetic analysis[J]. Water Research, 2003, 37(13): 3061.
[23] ZHA Fugeng, ZHANG Mingxu, XU Meijuan. Optimization and kinetic study of Fenton process for treatment of landfill leachate[J]. Chinese Journal of Environmental Engineering, 2014(7): 2837.
查甫更, 张明旭, 徐美娟. Fenton法处理垃圾渗滤液的参数优化及反应动力学模型[J]. 环境工程学报, 2014(7): 2837.
[24] QI Peishi, ZHAO Junjie, LIU Yunzhi, et al. Kinetics of advanced treatment of highviscosity petrochemical wastewater with oxidation by Fenton′s reagent[J]. Ciesc Journal, 2011(2): 490.
祁佩时, 赵俊杰, 刘云芝, 等. Fenton试剂深度处理稠油石化废水的反应动力学[J]. 化工学报, 2011(2): 490.
[25] He Li. Study on the Treatment of Landfill Leachate By Fenton+ Enhanced SBR Method[D]. Xi′an: Chang′an University, 2013.
何 丽. Fenton+強化SBR法处理城市垃圾渗滤液的研究[D]. 西安: 长安大学, 2013. CPP
(责任编辑:马 忻)
