甘薯叶绿原酸的微波协同双水相提取及其抗氧化活性
2018-09-03蒋益花蒋新龙
蒋益花 蒋新龙
(浙江树人大学生物与环境工程学院,杭州 310015)
甘薯叶作为甘薯的副产品之一,少部分用作饲料外,加工利用度低,而其中富含绿原酸类化合物[1-2]。
绿原酸是含有羧基和邻二苯酚羟基的苯丙素类有机酸。现代医学与天然产物研究发现,绿原酸在人体中具有显著的抗氧化、抗衰老、抗肿瘤、抑菌消炎、预防心血管疾病、防晒以及改善认知等功能[3-5]。
目前,绿原酸的提取方法主要有:浸提法[1-2]、微波法[6]、超声波法[7]、酶解法[8]、超临界流体萃取法[9]、半仿生提取法[10]、液膜法[11]、索氏提取法[12]等方法。浸提法得率较低,操作时间长,有机溶剂对环境污染大;索氏提取法易出现费时和溶剂用量过大问题;酶解法工艺操作控制较严格,因需调节酸碱度易造成部分酚类物质氧化而被破坏;超临界二氧化碳萃取法绿原酸氧化损失少、提取的产品质量较好、提取效率较高,但设备投资高不适合大规模生产;液膜法产品纯度低,膜价格高,过滤速度慢;超声波辅助提取法简便快捷、提取温度低、时间短、得率高,但获得产品纯度不高;半仿生提取法产品纯度低。双水相萃取是根据组分在两相间的选择性分配而达到目标成分分离的目的[13],因其操作条件较温和、分离过程可控、操作简单等优点,所以易于工业放大;尤其适用于具有生物活性的生物物质的分离和提纯[13]。目前,双水相体系用于绿原酸分离纯化的研究报道较多[14-15],但直接用于提取绿原酸的极少。本研究排除成本高、体系黏度大、回收难的高聚物双水相体系,直接用有机溶剂水溶液和一定量的无机盐配成双水相体系作为提取剂进行微波协同提取绿原酸,并考察了所提取甘薯叶绿原酸的抗氧化活性,为甘薯叶资源化开发利用提供借鉴。
1 材料与方法
1.1 材料与仪器
红心番薯叶[red.fleshIpomoeabatatas(L.)Lam.leaves]于2016年4月上旬采自浙江省诸暨市次坞镇种植地。将采摘的新鲜甘薯叶除去泥沙、黄叶等,再用清水漂洗干净,50 ℃鼓风干燥72 h,粉碎过60目筛,放入自封袋中,置于干燥器中备用。绿原酸标准品购于中国药品生物制品检定所;所用其他试剂均为国产分析纯;所用水为蒸馏水。
D8017Tl-2H型格兰仕微波炉;7220型分光光度计;GZX-91400MBE电热恒温鼓风干燥箱。
1.2 方法
1.2.1 绿原酸含量的测定
采用紫外分光光度法测定绿原酸含量[16]。以20 μg/mL的绿原酸为标准溶液制作标准曲线。精密量取1.00、2.50、3.75、5.00、6.25 mL绿原酸标准溶液,放置于10 mL容量瓶中,用75%乙醇定容,将绿原酸标准对照品配制成2.0、5.0、7.5、10.0、12.5 μg/mL 5个质量浓度的溶液,在329 nm波长下测定其吸光度A。以绿原酸质量浓度C(μg/mL)作横轴,吸光度A为纵坐标绘制标准曲线,得到绿原酸质量浓度C(μg/mL) 与吸光度A之间的回归方程为:A=0.053 1C+0.013 02,线性范围0~12.5 μg/mL,相关系数R2=0.999 9。吸取甘薯叶粗提液适量,同法测定其吸光值,根据回归方程计算绿原酸含量。
式中:C为回归方程计算所得值;V为粗提液总体积。
1.2.2 微波协同双水相体系提取工艺实验
提取方法:称取0.500 0 g甘薯叶粉末样品于500 mL烧杯中,加入一定体积的有机溶剂溶液和一定质量的无机盐,在一定微波功率条件下微波处理一定时间,趁热抽滤得滤液。静置5 min,待其分层,收集上清液,得到甘薯叶绿原酸粗提液(Sweet Potato Leaf Chlorogenic acid extract,SCE),测定绿原酸含量。
单因素实验:称取0.500 0 g红薯叶粉末样品,按照1.2.2方法对绿原酸提取过程中的乙醇体积分数、磷酸氢二钾用量、提取时间、液料比和微波功率五因素分别进行水平筛选及优化。设置液料比100∶1(V/m),50%的乙醇溶液,微波功率320 W提取时间30 s,考察析相盐磷酸氢二钾用量(3.0、4.0、5.0、6.0、7.0 g)对绿原酸得率的影响;设置液料比100∶1(V/m),磷酸氢二钾5.0 g,微波功率320 W提取时间30 s,考察有机相乙醇体积分数(30%、40%、50%、60%、70%)对绿原酸得率的影响;设置50%的乙醇溶液,磷酸氢二钾5.0 g,微波功率320 W提取时间30 s,考察液料比(40∶1、60∶1、80∶1、100∶1、120∶1V/m)对绿原酸得率的影响;设置液料比100∶1(V/m),50%的乙醇溶液,磷酸氢二钾5.0 g,微波功率320 W,考察提取时间(15、30、45、60、75、90、100 s)对绿原酸得率的影响;设置液料比100∶1(V/m),50%的乙醇溶液,磷酸氢二钾5.0 g,提取时间75 s,考察微波功率(160、320、480、640、800 W)对绿原酸得率的影响。
正交优化实验:在单因素实验的基础上,以无机盐用量为固定值,选取有机溶剂体积分数、液料比、提取时间和微波功率4个因素为自变量,以绿原酸得率为评价指标,利用正交实验 L9(34)对提取条件进行优化。
1.2.3 抗氧化活性实验
DPPH·法是用以评价天然抗氧化剂抗氧化活性的一种简便快速、灵敏可行的方法[17-18]。根据文献[19]并加以改进,用无水乙醇配制2×10-4mol/L的DPPH·溶液。在10 mL具塞试管中加入2 mL所需浓度(2、4、8、10、16、20 μg/mL)的测定液和2 mL DPPH·溶液,总体积4 mL。混合均匀,室温避光反应30 min,以溶剂调零点,测定DPPH·混合溶液在517 nm处的的吸光值A。结果以清除率K表示。
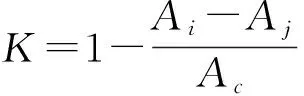
式中:Ai为2 mL DPPH·溶液加入2 mL测定液的吸光度;Aj为2 mL测定液加入2 mL溶剂的吸光度;Ac为2 mL DPPH·溶液添加2 mL溶剂的吸光度。
1.3 统计方法及分析软件
指标均重复测定3次并取平均值,利用Origin8软件作图;应用SPSS20.0软件进行数据统计,并用Duncan多重比较(SSR法)检验各处理平均数之间的差异显著性(P<0.05)。
2 结果与分析
2.1 双水相体系的确定
有机溶剂的确定:在离心管中分别加入相同体积的乙醇、丙酮、异丙醇三种有机溶剂,再分别加入定量的磷酸盐和硫酸铵比较分相情况。结果表明,丙酮、乙醇的分相效果较好。考虑丙酮的毒性较大,所以选择乙醇作为有机相。
分相盐的确定:加入相同体积的乙醇溶液,再分别逐量0.5 g递增地加入等量不同的盐:硫酸铵、磷酸二氢钾、无水硫酸钠、碳酸钠、碳酸氢钠、氯化铵等。置于离心管中比较分相情况。结果表明,在乙醇/水双水相萃取体系中,磷酸氢二钾的分相能力强。与其他盐不分层或难于分层。所以选取磷酸氢二钾作为分相盐。
2.2 单因素实验
2.2.1 磷酸氢二钾用量的影响
实验结果见图1。由于甘薯叶绿原酸属于苯丙素类有机酸,易溶于弱碱性溶液,磷酸氢二钾与乙醇形成的双水相提取剂为弱碱性,有利于甘薯叶绿原酸的溶出。在乙醇-磷酸氢二钾双水相中,下相由溶解有磷酸氢二钾的水及少量乙醇构成,上相则由混有少量水的乙醇构成,易溶于乙醇相的绿原酸提取出后进入上相。双水相的形成是磷酸氢二钾与乙醇争夺水分子的过程。随着磷酸氢二钾用量的增加,盐对水的束缚能力增强,使上相中乙醇的相对体积分数增加[20]。因此,盐的用量改变可影响到上相的极性,最终影响到绿原酸的得率。由图1可知,磷酸氢二钾用量为5.0 g时,绿原酸的得率达到最高值。后续固定磷酸氢二钾质量浓度100 mg/mL,通过优化调节乙醇体积分数和用量获得高选择性双水相体系。

图1 甘薯叶绿原酸提取条件单因素实验结果
2.2.2 乙醇体积分数对绿原酸得率的影响
由图1可知,在50%时绿原酸的得率达到最高值。这是因为乙醇体积分数直接影响双水相萃取效果。水量过多无法形成双水相体系,过少则盐不能完全溶解;乙醇量太少也无法形成双水相,太多则会导致盐的析出。因此,初步确定乙醇最佳体积分数为50%。
2.2.3 液料比对绿原酸得率的影响
由图1可知,液料比在40~100∶1(V/m)范围内,绿原酸得率随着液料比的增加而提高,当液料比高于100∶1(V/m)时,绿原酸得率反而下降,可能是因为当液料比过大时,液体中间部分较难受到微波辐射,只能通过传统方式受热,使得传热速率下降,导致绿原酸得率下降[21]。因此,控制好一个适当的液料比,会使体系达到一个较好的提取效果,故初步选取最佳液料比为100∶1(V/m)。
2.2.4 提取时间对绿原酸得率的影响
由图1可知,在75 s时间内,绿原酸得率随提取时间增加而提高,但提取时间超过75 s时,绿原酸得率不增反降,这主要由于绿原酸中的酚羟基容易被氧化,长时间的微波提取并不能达到很好的提取效果,故初步选取最佳提取时间为75 s。
2.2.5 微波功率对绿原酸得率的影响
由图1可知,在微波功率为160~800 W范围内,随着微波功率的增加,绿原酸得率先增加后减少,在480 W时达到最大值。其主要原因可能是微波功率过高,体系升温过快,加速了绿原酸的氧化与降解,使粗提液中绿原酸有效浓度下降。考虑到得率最高,初步选取最佳微波功率为480 W。
2.3 正交设计优化绿原酸提取工艺
以单因素实验结果为基础,采用4因素3水平的正交实验方法,对绿原酸提取工艺参数进行优化,实验设计和结果见表1,方差分析结果见表2。
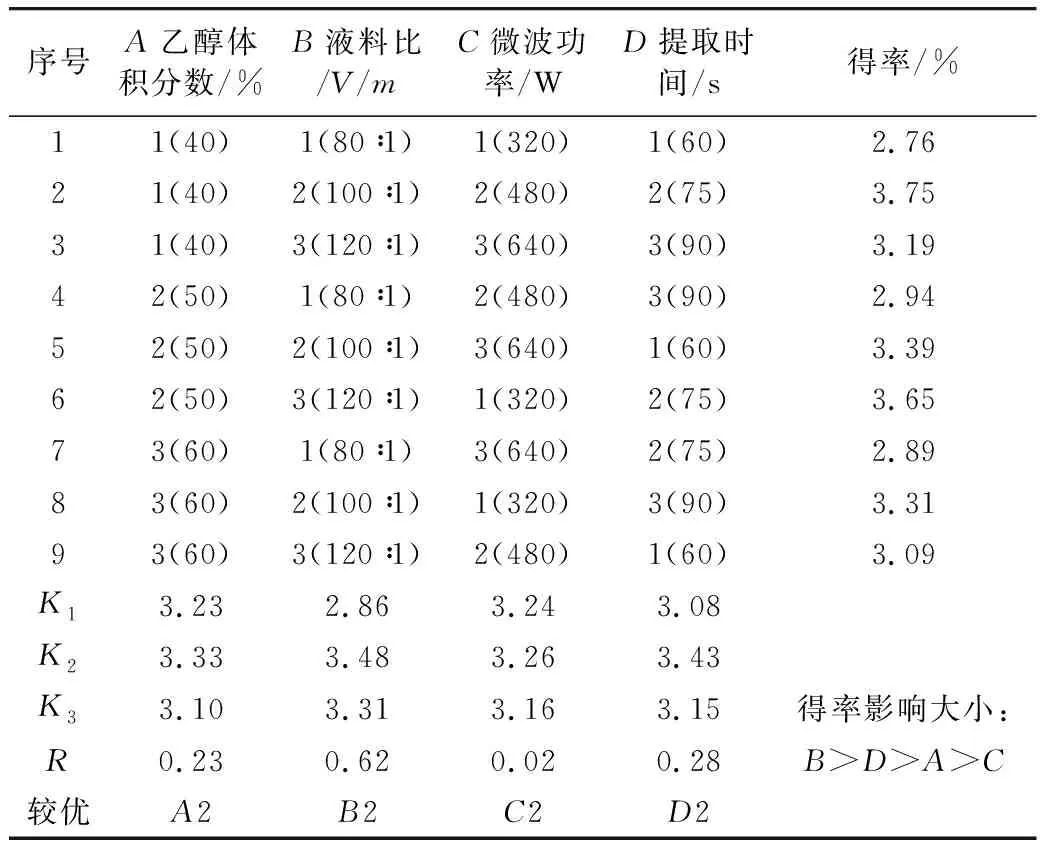
表1 正交实验设计及结果
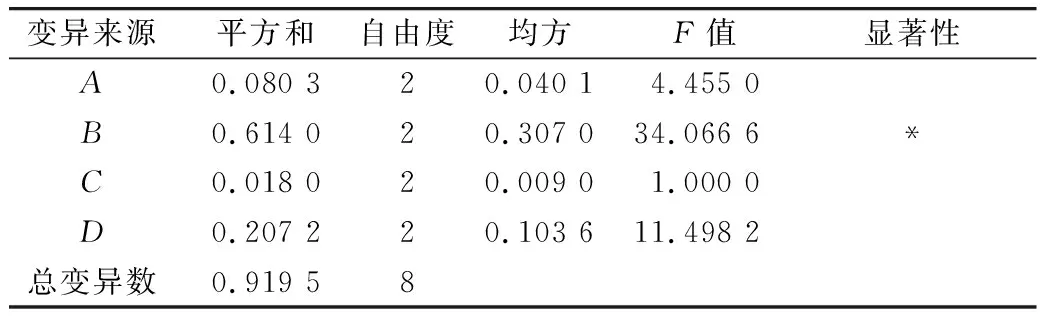
表2 方差分析表
注:因素C影响小,故作为方差分析的误差处理;F0.05(2、2)=19.00,*表示因素影响显著。
表1中K1、K2、K3表示每个因素所进行3次实验所得的绿原酸得率的平均值。R为平均数的极差,R越大表明变化幅度大,说明该因素的水平变化对绿原酸得率的影响越大,该因素即是最大影响因素。由表1可以看出影响绿原酸得率的因素主次依次排列为:液料比(B)>提取时间(D)>乙醇浓度(A)>微波功率(C)。由表2可以看出,对绿原酸得率的影响液料比(B)显著,其他都不显著。直观分析,实验的最优水平组合为A1B2C2D2;根据每个因素K1、K2、K3实验的最优水平组合为A2B2C2D2。Duncan法分析结果表明,乙醇浓度、微波功率三水平之间均无显著差异。综合分析提取成本和得率,确定最佳工艺条件A1B2C1D2,即乙醇体积分数40%,液料比100∶1(V/m),提取时间75 s,微波功率为320 W。

表3 对比实验结果
注:同列不同字母表示差异显著P<0.05,下同。
2.4 工艺验证性实验
为考察优选微波协同双水相提取(简称:微波双水相提取,下同)甘薯叶绿原酸工艺的稳定性,称取甘薯叶0.5000 g,按优化的提取工艺条件进行实验,即磷酸氢二钾质量浓度100 mg/mL,40%乙醇溶液,微波功率320 W,微波时间75 s,液料比100∶1(V/m)。重复实验3次,计算绿原酸得率。同时吸取上层醇溶液,挥干溶剂,制成干浸膏,测定干浸膏中绿原酸的含量。分别精密称取3份醇提浸膏,配制成一定质量浓度的供试液,测定绿原酸含量。验证实验结果,甘薯叶绿原酸得率分别为3.75%、3.73%、3.68%,平均为(3.72±0.036)%。干浸膏中绿原酸的质量分数分别为9.31%、9.40、9.42%,平均为(9.38±0.059)%。实验结果表明经过正交实验优选的提取工艺条件稳定,适合规模化生产。
2.5 对比实验
为了进一步研究双水相提取在得率和纯度上的优势,进行微波提取和微波双水相提取的对比实验,实验条件和结果见表3。实验结果表明,微波双水相提取所得得率略小但差异不显著(P>0.05),但提取干浸膏中绿原酸的含量提高了2.2倍,说明双水相提取的纯度明显提高。
2.6 抗氧化性实验
将甘薯叶绿原酸粗提液(SCE)分别配制成质量浓度为2、4、8、12、16、20 μg/mL的供试品溶液,按照1.2.3方法测定对DPPH·的清除率,并以相同质量浓度的绿原酸、VC作为阳性对照,实验结果见图2。根据图2的量效关系构建实验浓度和清除率的线性方程,并求出清除率为50%时所需的浓度(IC50),见表4。表4表明,甘薯叶绿原酸粗提液、绿原酸和VC在实验浓度范围内与清除DPPH·自由基呈现出良好的量效关系。SCE清除DPPH·的能力(IC50=(12.29±0.33) μg/mL)强于对照物VC(IC50=(14.64±0.38)μg/mL)和绿原酸(IC50=(16.78±0.55)μg/mL),SCE比绿原酸和VC对DPPH·的清除效果明显(P<0.05)。

表4 甘薯叶绿原酸粗提液清除DPPH·自由基的能力

图2 甘薯叶绿原酸粗提液清除DPPH·自由基的能力
3 讨论
本研究使用乙醇、磷酸氢二钾和水三种绿色材料,组成新型稳定的乙醇-磷酸氢二钾双水相萃取体系。研究发现,分相盐磷酸氢二钾质量分数过高或有机相乙醇体积分数过高都不利于甘薯叶绿原酸的提取。磷酸氢二钾质量分数过高,可使上相中乙醇的相对体积分数增加;乙醇体积分数过高,会导致磷酸氢二钾的析出。双水相的形成是磷酸氢二钾与乙醇争夺水分子的过程[20]。通过优化调整物质组成,可获得高选择性萃取体系。实验结果表明,乙醇-磷酸氢二钾双水相萃取体系中,以40%乙醇溶液、磷酸氢二钾质量浓度100 mg/mL组合为最佳。
本研究根据微波辅助萃取选择性高、萃取效率高等特点,将双水相萃取和微波辅助萃取相结合研究微波协同双水相体系提取甘薯叶绿原酸工艺。在单因素基础上,通过正交实验优化了甘薯叶绿原酸工艺。结果表明,液料比对绿原酸得率的影响显著,液料比是影响绿原酸得率的最主要因素。影响绿原酸得率的因素主次依次排列为:液料比>提取时间>乙醇浓度>微波功率。固定条件磷酸氢二钾质量浓度100 mg/mL下最佳提取工艺条件为乙醇浓度40%,液料比100∶1(V/m),提取时间75 s,微波功率为320 W。该工艺条件下得率为(3.72±0.036)%,其干浸膏的绿原酸质量分数为(9.38±0.059)%,而在不加入分相盐的微波提取条件下得到的甘薯叶绿原酸的得率为(3.86±0.035)%,其干浸膏绿原酸质量分数为(4.23±0.025)%。对比实验结果表明,加入分相盐磷酸氢二钾形成了水相体系,所得得率略小但差异不显著(P>0.05),主要是目标物绿原酸进入双水相体系,表面性质、电荷作用和氢键、离子键、疏水键以及环境等都会对绿原酸的分配造成影响[22],使得其在上、下两相中的浓度不同,绿原酸主要集中在本研究萃取的上相,损失了下相绿原酸,所以得率略低于单独微波提取。对比实验结果也表明,微波双水相提取干浸膏中绿原酸的含量明显提高,纯度提高了2.2倍。主要原因是由于分相盐磷酸氢二钾的加入,形成了乙醇-磷酸氢二钾双水相体系,甘薯叶粉恰好悬浮于两相之间,易溶于乙醇相的绿原酸提取出后进入上相,易溶于水相的多糖等物质溶于下相。这样,提取和分离过程同时进行,对甘薯叶粗提液中的绿原酸成分起到了一定的纯化、富集作用,这与王晓林等[23]研究结果一致。本研究对比实验发现,虽然微波双水相提取所得干浸膏纯度有所提高,但与于华忠等[24]纯化方法研究结果比较总纯度不高,原因是双水相不具有特异性和专一性[25],甘薯叶中含有其他的一些易溶于乙醇的物质进入有机相,而导致绿原酸的纯度降低,如何进一步纯化甘薯叶绿原酸还有待深入研究。本研究的绿原酸得率与其他参考文献有差异[24],可能是不同时期采摘、不同品种甘薯的差异所致[26]。
本研究经过新型微波双水相提取获得的绿原酸粗提液清除DPPH·的能力强于对照物绿原酸和VC,与李文娜等[27]研究结果一致,甘薯叶粗提液的抗氧化活性与绿原酸含量密切相关。绿原酸粗提液清除DPPH·的能力强于绿原酸,可能是甘薯叶粗提液中黄酮类、酚类等抗氧化物质的存在,强化了其清除DPPH·的能力[28]。
4 结论
对影响甘薯叶绿原酸得率的多个单因素进行分析,并结合正交优化分析,得到微波协同双水相提取甘薯叶绿原酸的最佳工艺条件为:分相盐磷酸氢二钾与有机相乙醇形成乙醇-磷酸氢二钾双水相体系,40%乙醇溶液,磷酸氢二钾质量浓度100 mg/mL,液料比100∶1(V/m),微波功率320 W,微波时间75 s,此提取条件下甘薯叶绿原酸得率为(3.72±0.036)%。对照微波法提取,微波协同双水相提取得率略小,所得干浸膏绿原酸的纯度明显提高,双水相体系起到了一定的纯化、富集作用,但总纯度仍然不高,如何进一步提高总纯度还有待深入研究。甘薯叶绿原酸粗提液清除DPPH·的能力强于对照物绿原酸和VC。微波协同双水相提取工艺,粗提物纯度高,安全便捷,且提取得到的绿原酸粗提物具有较强的抗氧化能力,为甘薯叶的进一步资源化开发利用提供了一定的技术支撑。
