黄芩素促进骨髓间充质干细胞归巢参与溃疡性结肠炎治疗的研究
2018-08-31陈敬根
陈敬根,周 凌,汪 渝,张 奎
0 引言
溃疡性结肠炎(Ulcerative colitis,UC)是一类由包括遗传、环境等多种因素参与的自身免疫疾病,属于炎症性肠病的一种,但病因尚不明确[1]。UC主要累及乙状结肠,病理表现为浅表结肠组织发生弥漫、连续性溃疡糜烂[2]。目前,临床上主要采用激素或免疫抑制剂类药物对该病进行治疗[3]。但此类治疗方法均无法根治,近年来,以间充质干细胞(Mesenchymal stem cells,MSCs)移植治疗为主的细胞疗法在包括UC在内自身免疫疾病的治疗中逐渐得到重视[4]。间充质干细胞是一种具备自我更新能力的多潜能干细胞,研究表明,其可通过影响固有免疫细胞及免疫调节细胞,进而发挥免疫调节作用[5]。因此,该细胞类型已被研究用于治疗系统性红斑狼疮(Systemic lupus erythematosus,SLE)和类风湿关节炎(Rheumatoid arthritis,RA)等多种自身免疫疾病,并取得较好的治疗效果[6-7]。最近研究表明,某些中药成分具有促进间充质干细胞归巢作用,可发挥增强间充质干细胞移植治疗的效果[8]。因此,本课题通过研究黄芩素对间充质干细胞向大鼠溃疡性结肠炎病损部位归巢作用的影响,为该药物作为辅助间充质干细胞移植治疗溃疡性结肠炎的可行性奠定前期研究基础。
1 材料与方法
1.1 实验动物及试剂 6周龄的雌性SD大鼠,购自南京模式动物研究中心;黄芩素(20 mg,FY12960708)购自南京飞宇生物科技有限公司。抗Musashi-1抗体购自Abcam,美国(ab129819);抗Lgr5抗体购自Santa,德国(sc-68580);抗Ephrin B3抗体购自Abcam,美国(ab101699)。
1.2 间充质干细胞提取、鉴定及体外黄芩素预处理 腹腔注射戊巴比妥钠(100 mg/kg)麻醉后处死大鼠,分离股骨及胫骨并置于75%乙醇5 min。无菌条件下,使用M199培养基反复冲洗骨髓腔,收集洗涤液并重悬为单细胞悬液。1 500 r/min 5 min离心单细胞悬液后弃去上清。随后用含10%FBS及1%双抗的M199培养基重悬细胞沉淀后,进行接种培养。间隔3~4 d换液1次,当细胞长至90%培养瓶底面积时行细胞传代。
取第3代细胞,利用0.25%胰蛋白酶消化80%融合的细胞,1 000 r/min离心5 min,用PBS洗涤细胞沉淀2次,并重悬为1×106/L的细胞悬液。吸取100 μl上述细胞悬液于两个EP管中,并分别加入PE标记的抗CD45及CD59抗体。室温孵育30 min后行流式细胞术检测。上述细胞重悬1×106/L的细胞悬液后分为2组:空白组及黄芩素处理组。在细胞增殖至50%密度时,黄芩素处理组加入1 ml含黄芩素的完全培养基至药物终浓度为100 ng/ml,空白组加入1 ml完全培养基。随后共培养24 h。
1.3 溃疡性结肠炎模型构建及分组 利用TNBS灌肠法制作大鼠溃疡性结肠炎模型。大鼠造模前禁食1 d,水合氯醛麻醉后大鼠直肠注入造模液(100 mg/kg TNBS+50%乙醇0.25 ml),诱导溃疡性结肠炎模型。造模成功后,将40只大鼠随机分为4组(空白组、模型组、MSCs组及黄芩素干预MSCs组),其中空白组不造UC模型。模型组及空白组分别经尾静脉注射1 ml PBS,MSCs组经尾静脉注射1 ml细胞悬液(1.0×106个),黄芩素干预MSCs组经尾静脉注射1 ml黄芩素处理后的细胞悬液(1.0×106个)。
1.4 间充质干细胞归巢效果评估
1.4.1 免疫组化法检测干细胞标志物Musashi-1的表达 大鼠尾行静脉注射后每隔5 d处死3只大鼠,收集结肠组织进行石蜡切片。常规利用二甲苯脱蜡及梯度乙醇脱水,加入0.01 mol/L柠檬酸盐缓冲液(pH=6.0),并于微波炉内微波辐射10 min进行抗原修复。PBS洗5次后,山羊血清进行室温封闭10 min,随后加入一抗(抗Musashi-1) 4 ℃过夜;PBS洗涤后,加入生物素标记二抗,37 ℃孵育30 min后加入显色剂(DAB),流水冲洗后封片观察。采用半定量积分法计算染色积分,即分别对阳性细胞数及其着色程度进行分级计分,结果以2项之积表示。阳性细胞率:每张切片随机检测5个视野(400×),所见的阳性细胞分为0~4级(共5级):0级为阴性,记0分;1级阳性细胞占1%~25%,记1分;2级阳性细胞占26%~50%,记2分;3级阳性细胞占51%~75%,记3分;4级阳性细胞占76%~100%,记4分。
1.4.2 Western blot法检测Lgr5和Ephrin-B3在结肠的表达水平 随机抽取不同部位的肠黏膜组织20 mg,裂解并提取结肠组织中的总蛋白,使用BCA法测定蛋白浓度。将蛋白上清与蛋白上样缓冲液构成40 μl体系,在变性条件下进行12%聚丙烯酰胺凝胶中电泳,将目的蛋白转移到PVDF膜上。5%脱脂奶粉室温封闭2 h;PBST洗3次,5 min/次;加入抗Lgr5抗体、抗Ephrin B3抗体,室温孵育1 h;PBST洗3次,5 min/次;加入相应的HRP标记的二抗,室温孵育1 h;洗膜后ECL显色。结果采用Image J进行半定量分析。

2 结果
2.1 间充质干细胞鉴定 骨髓提取的间充质单细胞传代培养3次后,利用流式细胞术检测干细胞表面标志物的表达情况。流式结果表明,经过提取及传代培养后,91.6%的细胞表面有CD90的表达,而CD45的表达量仅为3.98%,表明本实验所用细胞属于CD90+/CD45-的干细胞。见图1。
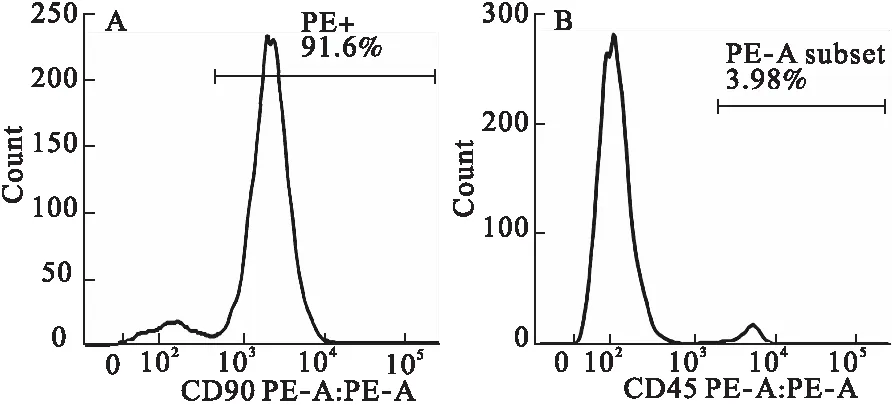
图1 间充质干细胞流式细胞术鉴定结果
2.2 免疫组化分析肠道干细胞标志物Musashi-1的表达情况 对结肠切片进行免疫组化染色,Musashi-1染色积分值及免疫组织化学染色结果如表1、图2所示。t检验结果显示,在尾静脉注射后第5天,模型组的Musashi-1积分值低于黄芩素干预MSCs组,差异有统计学意义(t=2.402,P=0.043);但黄芩素干预MSCs组的Musashi-1积分值与MSCs组比较,差异无统计学意义(t=1.271,P=0.240)。给药后第10天,黄芩素干预MSCs组的Musashi-1积分值高于第10天模型组及MSCs组的积分值,差异有统计学意义(t=6.854,P<0.001;t=3.348,P=0.010)。
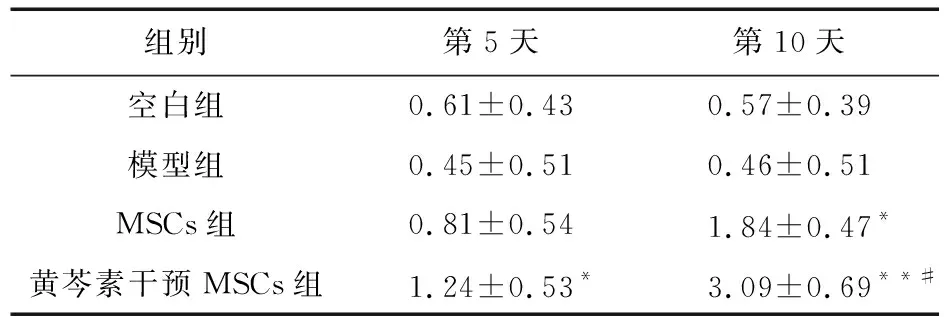
表1 各组间Musashi-1的表达情况分析(n=5)
注:与模型组比较,*P<0.05,**P<0.01;与MSCs组比较,#P<0.05
2.3 Western blot检测Lgr5和Ephrin-B3在结肠的表达水平 见图3、图4。应用Western blot检测各组大鼠结肠组织在不同时间点Lgr5和Ephrin-B3表达水平差异。结果显示,黄芩素干预MSCs组结肠组织的Lgr5和Ephrin-B3表达量高于空白组、模型组、MSCs组。

图2 各组大鼠肠道Musashi-1免疫组化染色结果
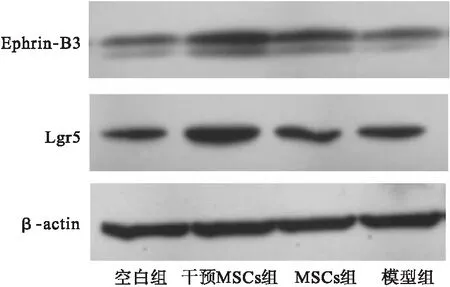
图3 各组结肠组织Lgr5和Ephrin-B3表达水平

图4 各组结肠组织Lgr5和Ephrin-B3相对表达水平
3 讨论
溃疡性结肠炎患者肠道处于反复炎症状态,因此被认为是一种难治性癌前病变。此类患者的结肠黏膜组织受到反复破坏的同时,也伴随着机体免疫调节功能失衡,因此,纠正失调的免疫功能并修复受损肠黏膜屏障是治疗溃疡性结肠炎的关键[9-13]。中医理论认为,溃疡性结肠炎属于“痢疾”、“久痢”和“肠澼”等范畴[14],包括黄芩汤在内的多种方剂均可治疗该病,并取得了良好效果[15]。但黄芩汤治疗溃疡性结肠炎的药理机制不明,因此,本研究选择黄芩汤的主要药理成分黄芩素作为研究对象,从间充质干细胞归巢角度,初步分析黄芩素在治疗溃疡性结肠炎中的可能机制,为今后深入研究其药理作用奠定前期研究基础。
间充质干细胞属于多潜能干细胞,存在于包括脐带血及骨髓等多种组织器官内,在适当环境下可分化为多种三胚层细胞,参与机体组织修复过程[4]。本研究经由骨髓中提取间充质干细胞,并利用其贴壁生长的特点选用经3次传代培养后的细胞进行实验。经过传代培养后,骨髓来源MSCs呈现贴壁生长的特性。公认的观点认为,间充质干细胞表面存在多种分子标志,包括CD90、CD105、CD166等抗原阳性,以及CD45、CD14、CD34等抗原阴性。本研究选取CD90+及CD45-作为表面特异分子标志[16]。流式结果表明,经3代传代培养后的细胞表面CD90、CD45的阳性率分别为91.6%、3.98%,呈现间充质干细胞特点(CD90+/CD45-),可用于后期尾静脉回输实验。
成体干细胞是治疗溃疡性结肠炎的首选细胞,主要存在于结肠隐窝基底部,但该细胞难以获得及体外扩增困难的特点导致其无法用于临床治疗。因此,目前研究主要集中在造血干细胞(Hematopoietic stem cells,HSCT)及MSCs移植的研究上。MSCs具有向病损部位归巢的特性,在病灶部位聚集后可参与靶组织的修复过程。但MSCs向肠道的归巢效率较低,有研究表明,静脉注射人干细胞到裸鼠体内后,仅0.13%的干细胞可在小鼠肠道组织中被检测到[17]。本研究发现,在尾静脉注射未处理的MSCs后的第5天及第10天,肠道干细胞标志物Musashi-1与空白组及模型组无显著性差异,表明未经处理的间充质干细胞归巢至受损肠道组织并分化为肠道干细胞的数量较少,与既往研究相符。但黄芩素干预MSCs组的大鼠结肠组织的Musashi-1在不同时间点(第5、10天)均高于MSCs组,初步提示黄芩素可促进MSCs归巢及向肠干细胞分化,发挥治疗溃疡性结肠炎的作用。
Lgr5和Ephrin-B3是未成熟的肠黏膜细胞标志物,其中Lgr5表达在肠分泌细胞的前体,肠分泌细胞可通过分泌黏液对肠道起润滑作用,对肠黏膜屏障的构成具有重要意义。而Ephrin-B3则是一种表达结肠隐窝底部的标记物,在溃疡性结肠炎患者的结肠组织中隐窝被严重破坏,抑制原有肠干细胞对受损结肠组织的修复[18]。Western blot结果显示,黄芩素干预MSCs组的Lgr5和Ephrin-B3表达水平均明显高于其他各组,提示尾静脉输注黄芩素干预MSCs,可促进肠分泌细胞的分化,并且对结肠隐窝的重建亦有促进作用。
同时,本研究也存在一些不足。黄芩素对于MSCs增殖、分化能力的影响也可能是其发挥促进MSCs归巢的潜在基础,因此,应针对黄芩素对MSCs的直接影响开展研究;并且本研究尚缺乏大鼠溃疡性结肠炎症状改善程度的评估,也需后期进一步实验进行补充。
综上所述,黄芩素可通过促进MSCs向结肠组织归巢来参与肠道黏膜屏障的重建,并发挥治疗溃疡性结肠炎的作用。
