用组织窗代替传统时间窗指导急性脑梗死的再灌注治疗
2018-08-29吴川杰马青峰陈健耿晓坤宋海庆吉训明
吴川杰,马青峰,陈健,耿晓坤,宋海庆,吉训明
卒中目前仍是世界各国的主要致死性和致残性疾病之一,2016年全球疾病负担研究显示,卒中是我国的第一位死亡原因[1]。超过40%的缺血性卒中由颅内大血管急性闭塞引起,大血管闭塞所致的急性卒中使患者6个月的死亡率增加3.5倍,良好预后的比例下降67%[2]。早期的静脉溶栓和血管内治疗可以使闭塞的血管再通,血流再灌注,从而减小梗死体积,降低残疾的发生率,有效改善了患者的整体预后[3-7]。因此,如何使急性脑梗死患者安全有效地接受再灌注治疗就成为了一个亟待解决的问题。
1 传统时间窗存在的问题
目前临床中急性脑梗死的再灌注治疗有着固定的时间窗,国内外指南推荐阿替普酶静脉溶栓的时间窗均为4.5 h[8],前循环大血管闭塞患者机械取栓治疗的时间窗为6 h[9-11]。固定的时间窗使多数患者不能接受再灌注治疗,美国的一项研究显示,按照指南推荐的标准,所有到急诊就诊的急性卒中患者,仅有6.4%的患者能够接受静脉溶栓治疗[12]。澳大利亚一项纳入148 027人的研究显示,按照指南推荐的标准,仅有13%的患者能够接受机械取栓治疗[13]。此外,目前临床中均依据最后正常的时间来计算时间窗,而约20%的患者为醒后卒中[14],按照时间窗的标准这些患者也多数不能进行再灌注治疗。
在一项单中心的研究中,对大脑中动脉M1段闭塞的患者6 h内进行氙增强计算机断层扫描灌注成像(computed tomography perfusion,CTP)检查,发现25%(9/36)的患者梗死核心超过大脑中动脉50%供血区,27%(10/36)的患者梗死体积小于大脑中动脉20%供血区[15]。另外一项研究通过弥散加权成像(diffusion weighted imaging,DWI)显示,20%的患者在动脉闭塞8 h内已经出现梗死体积>70 ml[16]。这也与临床中观察到的结果相符。按照目前的指南推荐,在接受取栓治疗的患者中,66%~94%的患者可以通过机械取栓治疗达到闭塞血管的再通,然而仅有46%的患者最终预后良好[17]。这说明了按照目前的治疗策略20%以上的患者可能是无效再通。我国一项大型登记性研究表明,机械取栓后16%的患者发生了症状性脑出血,症状性脑出血使患者90 d内死亡率增加了46.5%(65.3%vs18.8%)[18]。这从另一方面说明了按照目前的治疗策略,16%的患者可能是有害再通。
因此,虽然按照传统的固定时间窗指导再灌注治疗操作简单,但是限制了可以接受治疗患者的比例,且相当一部分时间窗内的患者再灌注治疗后并不能达到预期的效果。
2 组织窗的优势
众所周知,再灌注治疗的目的是尽快使血流恢复,挽救缺血半暗带(生理功能丧失但是没有死亡的脑组织),梗死核心(已经发生死亡的脑组织)则不能从再灌注中获益。组织窗不再刻板的依据固定的时间来决定患者是否适合接受再灌注治疗,而是通过一系列影像学检查结合临床症状来评估患者是否存在足够的缺血半暗带[19],以此指导再灌注治疗理论上更为合理。与时间窗相比,组织窗有着诸多优势。
首先,组织窗显著扩大了再灌注治疗的适宜人群。日本一项纳入816例卒中患者的研究发现,通过磁共振成像(magnetic resonance imaging,MRI)评估后,用组织窗代替时间窗,可以使30%的醒后卒中患者接受静脉溶栓治疗[14]。在传统时间窗的指导下,发病4.5 h后的急性卒中患者不能接受静脉溶栓治疗。一项研究纳入了172例4.5 h内(平均时间142.6 min)常规静脉溶栓和43例超过4.5 h(平均时间508.8 min)后在多模影像评估组织窗的指导下进行静脉溶栓患者,结果表明这两组患者的良好预后比例相似(64.5%vs60.5%,P=0.62),症状性脑出血发生率差异无统计学意义(2.9%vs2.3%,P=1.0)[20]。应用DWI或CTP联合临床不匹配治疗醒后卒中和晚就诊卒中患者用Trevo装置行神经介入治疗(DWI or CTP Assessment with Clinical Mismatch in the Triage of Wake-Up and Late Presenting Strokes Undergoing Neurointervention with Trevo,DAWN)研究旨在评价机械取栓对前循环大血管闭塞6~24 h内的临床疗效,该研究通过临床症状与梗死核心不匹配的方法来筛选存在缺血半暗带的合适患者,结果显示在组织窗的指导下,发病6~24 h的患者进行机械取栓治疗可获得和发病6 h内患者相似的治疗效果[21]。据此推算,约30%超过6 h取栓时间窗的患者能够在组织窗的指导下接受机械取栓治疗[22]。另外有3项正在进行中的研究(NCT01852201、NCT02142283、NCT02586415)采用多模影像学指导超时间窗患者的血管再通治疗,这些研究有望在不久的将来为临床提供更充分的循证证据。
其次,组织窗指导再灌注治疗显著提高了急性脑梗死患者的治疗效果。DAWN研究中,在组织窗的指导治疗下(超过时间窗后仍进行取栓治疗)49%的患者获得了良好预后,而按照传统时间窗指导治疗(超过时间窗仅进行保守药物治疗)仅13%的患者获得了良好预后[21]。荷兰急性缺血性卒中血管内治疗多中心随机对照临床试验(Multicenter Randomized CLinical trial of Endovascular treatment for Acute ischemic stroke in the Netherlands,MR CLEAN)仅以6 h的时间窗来指导急性大血管闭塞的脑梗死患者进行机械取栓治疗,结果表明机械取栓治疗组的患者3个月后良好预后的比例仅为32.6%[3]。急性神经功能缺损患者扩展时间窗溶栓后联合动脉治疗(Extending the Time for Thrombolysis in Emergency Neurological Deficits-Intra-Arterial,EXTEND-IA)在时间窗的基础上,经过多模影像学评估将不匹配比例>1.2或不匹配体积>10 ml及梗死核心体积<70 ml的患者纳入研究,机械取栓治疗组的患者3个月后良好预后的比例为71%[4]。血管内治疗小梗死灶和前循环近端闭塞并强调CT至再通时间最短化研究(Endovascular Treatment for Small Core and Anterior Circulation Proximal Occlusion with Emphasis on Minimizing CT to Recanalization Times,ESCAPE)纳入了发病12 h内的急性大动脉闭塞所致脑梗死患者,同时用梗死核心体积和侧支循环等组织窗标准来筛选患者,结果表明即使在这些发病12 h的人群中,3个月良好预后的比例仍高达53.0%[5]。这表明了应用组织窗指导机械取栓治疗可以筛选出更适合机械取栓治疗的患者,提高了机械取栓治疗的临床疗效。
3 组织窗的病理生理基础
急性脑梗死的病理生理机制是缺血发生后缺血半暗带向梗死核心的动态演变。动脉血管闭塞后,在梗死核心的周围由于血流量降低会存在一个生理功能丧失但组织尚未发生梗死的区域,这个区域称为缺血半暗带,随着血流的恢复,其生理功能可能完全恢复[23-24]。但是如果没有及时再灌注,随着缺血时间的延长,侧支循环逐渐衰竭,缺血半暗带演变为梗死核心,梗死核心体积逐渐扩大,缺血半暗带体积逐渐减少[25]。因此,再灌注治疗是否有效的关键在于能否在缺血半暗带演变为梗死之前完成。
急性动脉闭塞后脑缺血半暗带的大小由缺血时间和梗死速度决定[26]。传统的时间窗仅关注缺血时间,忽视了梗死速度对缺血半暗带的影响。梗死速度快的患者,在标准再灌注治疗时间窗内,患者大部分缺血半暗带已经发生梗死,如图1患者B,此时再灌注治疗已经没有足够的可以挽救的缺血半暗带,且较大的梗死核心增加了再灌注治疗后症状性脑出血、恶性脑水肿的发生风险,导致并发症风险增加[27]。梗死速度慢的患者,在超过标准再灌注治疗时间窗后仍有大量缺血半暗带的存在,如图1患者C,此时再通治疗仍然能够使患者获益,但是如果仍按照传统时间窗的概念,该患者可能不能接受再灌注治疗。综上可知,以单纯固定时间窗来指导急性脑梗死再灌注治疗有着很大的盲目性,只有如图1患者A所示的梗死速度有望获得良好的治疗效果。
急性血管闭塞后,梗死速度取决于侧支循环的代偿和组织细胞对缺血缺氧的耐受能力两方面[26]。根据经典的缺血半暗带理论,当脑血流降低至10~20 ml/(100 g·min)时,缺血组织的细胞电活动终止,但跨膜离子电位仍保存;当脑血流低于10 ml/(100 g·min)时,缺血组织的细胞将发生不可逆的坏死[28-29]。不同个体的侧支循环不同,当侧支循环足够使脑血流量能够维持时在一定水平时,缺血半暗带可以长时间存在,而当侧支循环衰竭后,梗死很快就会发生。不同患者的侧支循环代偿差异很大,基因型可能是侧支循环的重要决定因素,小鼠研究发现,80%的侧支循环数量和直径差异与Rabep2的基因多态性密切相关[30]。一项研究正在人体中验证这一关联性。另外,不同个体组织细胞对缺血缺氧耐受能力也有差异。例如,有FHM1基因突变的小鼠,其脑组织细胞对缺血缺氧的耐受性较野生型小鼠差,导致其在发生缺血后梗死速度快,梗死体积大,预后差[31]。
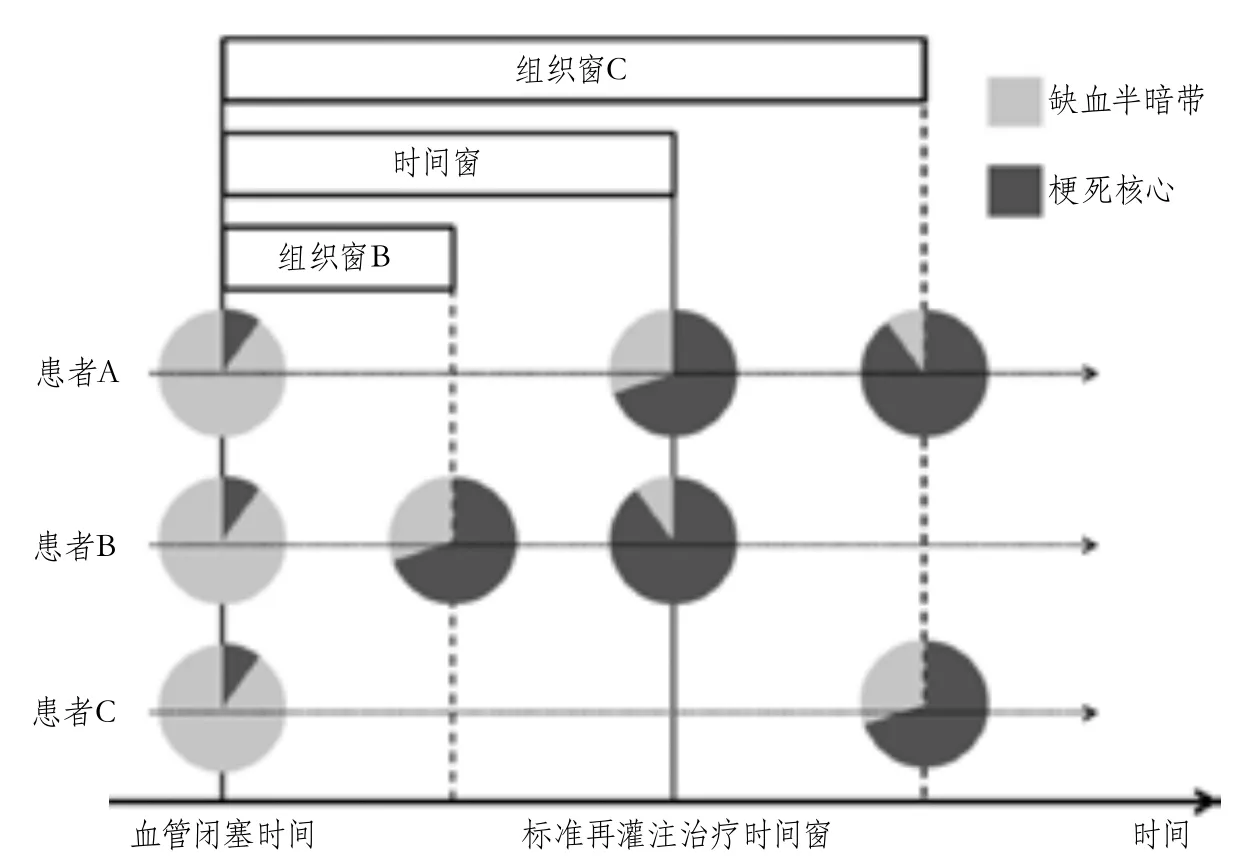
图1 时间窗和组织窗指导下的再灌注治疗对不同患者的影响
与固定时间窗不同,组织窗通过影像学和临床症状评价患者是否有足够的缺血半暗带,绕开了评价梗死速度的困难,直接关注缺血时间和梗死速度造成的最终结果,对每个患者进行个体化的评估和诊治,考虑到了患者个体间的差异,也更加符合脑梗死后的病理生理演变过程。因此,理论上讲,以组织窗来指导急性脑梗死的再灌注治疗可以提高治疗效果,降低治疗的不良反应[19]。
4 组织窗的评价方法
组织窗的评价主要包括梗死核心和缺血半暗带两方面。组织窗是一种基于病理结构的标准,临床中难以直接进行评价。其间接评价仍缺乏统一的标准,目前常用影像学检查和临床症状检查来间接反映梗死核心区和缺血半暗带的大小,梗死核心区域的大小反映了患者进行再灌注治疗的风险,而缺血半暗带的大小反映了患者的获益,梗死核心小且缺血半暗带大的急性脑梗死患者进行再灌注治疗的出血风险更小而获益更多[19]。
梗死核心指脑缺血发生后已经发生不可逆损伤的脑组织,目前常用的评价方法有平扫计算机断层扫描(computed tomography,CT)、MRI-DWI和CTP-脑血流量(cerebral blood flow,CBF)等。梗死核心的定量评价有Alberta卒中项目早期CT评分(Alberta program early CT score,ASPECTS)和梗死核心体积(ml)两种。有研究显示,ASPECTS评分≥7分对应于梗死体积<70 ml,ASPECTS评分≤3分对应于梗死体积>100 ml[32],两种评价方法有着相似准确性[33]。五项大型研究的荟萃分析表明,ASPECTS评分≥6分患者进行机械取栓治疗能够显著获益[17]。虽然有研究提示部分ASPECTS评分<6分的患者再灌注治疗也能够获益[34-35],但这些结果仍需要进一步的随机对照研究来证实。缺血半暗带的体积可能是这部分患者能否获益的关键因素。
缺血半暗带是再灌注治疗后功能可能恢复的脑组织,对治疗的预后至关重要。侧支循环的分级评价[36-37]、CTP成像CBF和达峰时间的不匹配[4]、MRI中DWI与灌注加权成像的不匹配、DWI与液体衰减反转恢复的不匹配[38-39]、梗死核心与临床症状不匹配等都被常被用来间接反映缺血半暗带的体积[21]。但是合适阈值的界定仍需要进一步研究。
总之,组织窗的评价相对复杂,并非所有的医院都具备所需的急诊影像学检查能力,且如何评价组织窗尚无统一的标准。时间窗的判断虽然简单易行,但是目前临床上常规应用固定时间窗指导急性脑梗死再灌注治疗存在诸多的问题。随着诊断技术的进步,使用组织窗指导临床治疗更有优势的证据越来越多。今后临床中应该逐渐推广组织窗的理念和临床应用,将组织窗与时间窗结合起来或逐步用组织窗代替时间窗,同时在这方面也应该进行更多的临床和机制研究,从而更好地指导临床工作,最终使更多的患者获益。
【点睛】越来越多的证据显示用组织窗代替传统的时间窗指导急性脑梗死的血管再通治疗更有优势。
