氧化镁测定中火焰原子吸收光谱法的应用
2018-08-23唐晓玲
唐晓玲
(贵州省地质矿产勘查开发局一O六地质大队,贵州 遵义 563000)
原子吸收光谱法(Atomic Absorption Spectroscopy,AAS)又称为原子分光光度法,通过利用气态原子而吸收一定波长的光辐射,已经成为无机元素定量分析及其应用最为广泛的分析方法,适用于样品中微量及痕量组分分析。该方法有着较高的灵敏度,较快的分析速度,较小的干扰性,被广泛应用于食品、农业及其冶金中某些元素含量的测定。下面采用该方法测定冶金中氧化镁的含量。
1 试验仪器及试剂
原子吸收分光光度计(日本日立公司),硝酸、盐酸为分析纯,氯化锶溶液为100g/L,0.1mol/L EDTA溶液。测定条件:波长约为283.21nm,燃烧器的高度约为20mm,灯电流约为3.12mA,其单色器的通带约为0.12mm,乙炔流量为1L·min-1。试验水为二次去离子水。
氧化镁标准溶液的制定:称取0.12g的高纯氧化镁,置入到250mL的烧杯中,将其加入到10mL的盐酸中,使用低温加热,直至完全溶解,待自然冷却后,用水定容到1L,浓度为50mg/mL。
2 试验方法
移取0、1、2、4、6mL的氧化镁标准溶液,分别将其置入到100mL的容量瓶中,分别加入5.5、5.4、5.3、5.2、5.1mL的盐酸及10mL的氯化锶溶液中,采用水稀释至刻度,充分摇匀。
称取0.12g钛精矿试样,将其置入到聚四氟乙烯坩埚中,采用少量的去离子水将坩埚达到湿润状态,加入15mL的纯盐酸到坩埚中,保证坩埚中的溶液出现浑浊状态。将坩埚置入到电热板上进行加热,适当给予摇动,避免底部结底。待大部分试验在溶解后,加入5mL的氢氟酸,进行加热,直至没有黑色的矿样。再向其中加入3mL的高氯酸,直至冒浓厚的白烟。取下坩埚,待其冷却,使用离子水对坩埚壁进行冲洗,再加热,直至冒出白烟。取下坩埚,待其冷却,最后加入6mL的盐酸进行温热溶解并冷却,将其全部倒入到100mL的容量瓶中,控制溶液酸度,测定氧化镁的含量。若含量偏高时,可采用定量的分液给予稀释,重新测定。均设空白组,将其作为参比,测定标准溶液的吸光度。
3 试验结果
3.1 盐酸用量对测定结果的影响
选取0.1g的标样中,加入不同用量的盐酸,定容在100mL的容量瓶中,其溶液酸度进行控制,溶液中含有5mg/L的氯化锶,分别对氧化镁含量给予测定,并设置空白对照组,每一次盐酸用量进行3次测定,取平均值。其结果如表1所示。由表中可得到:盐酸用量适宜选择6mL,其测试的溶液盐酸浓度为0.012mol/L。

表1 盐酸用量对测定结果的影响
3.2 氯化锶用量对测定结果的影响
取0.1g的标样,加入6mL盐酸,定容在100mL,分别抽取10mL溶液到5个相同的容量瓶中,加入不同量的氯化锶溶液中,定容后测定氯化镁的含量,设置空白对照组,详见表2所示,加入10mL的氯化锶溶液时,测定结果相对较稳定。
3.3 干扰试验
1mg·L-1氯化镁溶液,其允许误差值小于5%,其共存的离子允许量为:SIO2(2)、Ca2+、AL(1)、As3+(1)、Cd2+(1)、Cu2+(1),其杂质加入量已远远超过了铅精矿中的杂质含量。
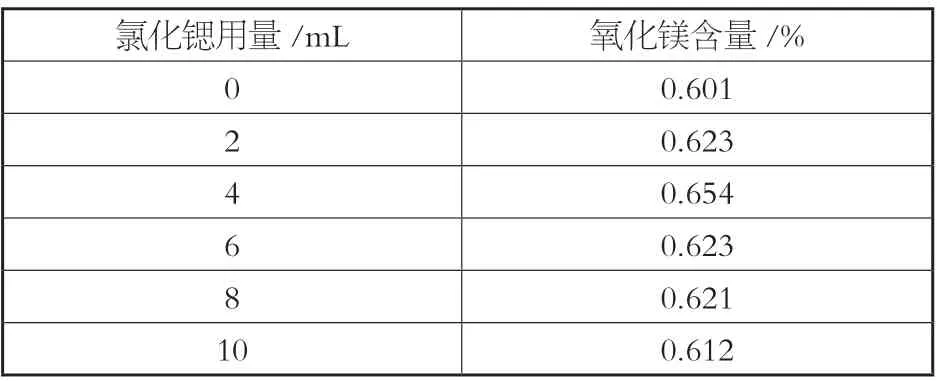
表2 氯化锶用量对测定结果的影响
3.4 样品处理
抽取0.2g的矿样本,将其置入到烧杯之中,并加入少许的水湿润,从中加入10mL的浓盐酸,将其放置在电热板上进行加热,直到硫化氢消失,然后加入5mL的盐酸,并再次蒸干,将器皿中的水吹干,待水煮沸后取下,自然冷却,将全部溶液移入到100mL的容量瓶中,采用水稀释,混合摇匀。同时设置空白对照组。测定结果如表3所示。
3.5 加标回收试验
称取0.1g的矿样,加入到6mL的盐酸溶液中,定容于100mL的容量瓶中,分别移取10mL溶置入到4个50mL的容量瓶中。由于氧化镁含量较高,待标样定容后,可稀释50倍,进行回收试验,详见表4所示。由表中数据可得到:氯化镁的加标回收率较好,可满足回收要求。

表3 样品处理结果 (%)

表4 氯化镁加标回收试验分析
3.6 精密度试验
随机抽取4份样本进行氯化镁精密度试验,同时设置空白对照组,其结果如表5所示。由表5可得到:火焰原子吸收光谱法有着较好的精密度。
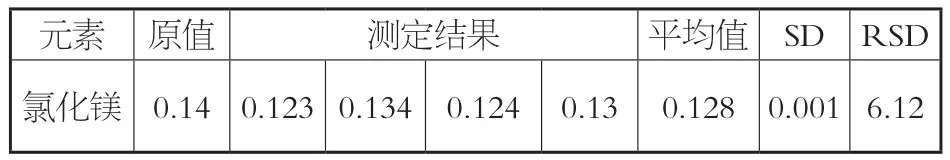
表5 精密度试验分析(%)
4 结语
采用火焰原子吸收光谱法测定钛精矿中的氧化镁元素,操作过程简单且方便,所需要的操作时间较短,且有着较高的准确度、精密度、回收率,能够快速测定氧化镁的含量。同时,在本次研究中增加了空白对照组,增加了测定结果的可靠性。通过以上的试验研究表明:氧化镁测定中火焰原子吸收光谱法有着较高的应用价值,能够作为冶金中氧化镁含量的测定方法。
