清肺平喘口服液对大鼠长期毒性试验研究
2018-08-07董惠峰朱国霞李源王立红张凤洪刘鼎阔
董惠峰 ,朱国霞 ,李源 ,王立红 ,张凤洪 ,刘鼎阔 ,4,
清肺平喘口服液对大鼠长期毒性试验研究
董惠峰1,2,朱国霞3,李源1,2,王立红1,2,张凤洪1,2,刘鼎阔1,2,4,通信作者
(1. 鼎正动物药业(天津)有限公司,天津 300383;2. 天津市饲用微生物制剂企业重点实验室,天津 300383;3. 天津农学院 天津市水产生态及养殖重点实验室,天津 300384;4. 中国农业大学 动物医学院,北京 100094)
为了解清肺平喘口服液长期用药的安全性,本试验研究清肺平喘口服液连续灌服情况下对SD 大鼠的长期毒性情况。将雌雄各半的120只SD大鼠,随机分为对照组和清肺平喘口服液2.52 g/kg、5.04 g/kg和10.08 g/kg剂量组,每组30只,连续给药90 d,以SD大鼠的体重、摄食量、血液生化指数及脏器系数检查作为检查指标,全面评价连续灌服对大鼠的毒性作用。试验结果显示,各组大鼠灌胃给药直至90 d均无死亡,各给药组大鼠毛发光润,摄食、粪便均正常。给药观察期间,3个试验组大鼠的体重、摄食量、血液生化指标、脏器系数与对照组相比均无显著差异(>0.05)。结果提示,清肺平喘口服液在2.52 g/kg、5.04 g/kg和10.08 g/kg剂量下连续灌服对SD大鼠无不良影响。
清肺平喘口服液;大鼠;长期毒性
呼吸系统疾病是动物养殖过程中最为常见、危害极为严重的疾病之一。引发呼吸系统疾病的原因多种多样,既包括细菌、病毒、免疫性抑制等常见因素,又包括混合感染、非典型病原等复杂因素[1-2]。因此,疾病控制难度也逐渐增大,一些传统的抗生素药物由于动物体内产生具有耐药性甚至多重耐药性的病原微生物而难以奏效。有研究显示,多数病原菌可耐受15~20 种抗生素[3]。而中草药具有毒副作用小、不易产生耐药性、药物残留低等优点[4]。因此,越来越多用于治疗呼吸系统疾病的新型中兽药被研发出来。清肺平喘口服液是一种用于治疗呼吸系统疾病的中兽药制剂。桂枝、麻黄、苦杏仁、桔梗及黄芪为该药的主要组成成分。本试验通过观察清肺平喘口服液连续灌胃对大鼠的长期毒性,评价清肺平喘口服液长期用药的安全性,为临床提供无毒性反应剂量提供参考。
1 材料与方法
1.1 试验药物
清肺平喘口服液(生药1 g/mL),批号:20170521,由鼎正动物药业(天津)有限公司提供。
实验前将清肺平喘口服液用蒸馏水配制成不同浓度的混悬液备用。实验时按1 mL/100g体重的灌服量,每天灌服给药一次。
1.2 实验动物
4周清洁级SD大鼠120只,体重在120~150 g之间,平均分为4组,每组动物30只,雌雄各半。组内动物个体体重相差不超过平均体重的10%,组间平均体重相差不超过5%。
1.3 染毒剂量的选择及分组
试验设3个染毒剂量组,根据《中药、天然药物长期毒性研究技术指导原则》的要求,低剂量组原则上应高于同种动物药效学试验的有效剂量。小鼠药效学试验的有效剂量为2.4 g生药/kg体重、高剂量为4.8 g生药/kg体重,取其中间剂量值3.6 g生药/kg体重作为长期毒性的低剂量组,折算成大鼠(200 g)的剂量为2.52 g生药/kg体重。因此设置清肺平喘口服液大鼠长期毒性试验的低剂量组剂量为2.52 g生药/kg体重、中剂量组为5.04 g生药/kg体重、高剂量组为10.08 g生药/kg体重。另设一组生理盐水对照组。
1.4 染毒方法及时间
采用经口染毒,连续染毒90 d。
1.5 试验期间临床观察
每天观察健康状况、采食及饮水变化、体重变化等。分别于第2、4、6、8、10、12、13、15周称量体重,并于给药结束后及停药2周后计算平均摄食量和饲料利用率(动物每食入100 g饲料所增长的体重克数)。将染毒剂量组与对照组加以比较和统计学处理。及时记录和分析大鼠的中毒症状及出现各症状的先后次序、时间。
1.6 血液生化检测
染毒90天结束后和停药2周后,各组各扑杀一半大鼠(雌雄各半)。采血进行血项和肝、肾功能的检测:血项检测包括红细胞计数、白细胞计数和分类、血红蛋白定量等,肝、肾功能常规指标包括谷草转氨酶(AST或SGOT)、谷丙转氨酶(ALT或SGPT)、总蛋白(TP)、血清白蛋白(Alb)、血糖(Glu)、肌酐(Cr)、尿素氮(BUN)、总胆固醇(TCH)和甘油三脂(TG)等。
1.7 大鼠剖检及脏器称重
90 d喂养试验结束,各组取20只大鼠进行剖检,停药2周后对剩余大鼠(雌、雄各半)进行剖检(可结合采血进行),及时做好记录。
剖检试验大鼠的同时,称取大鼠体重及各主要脏器(包括心、肝、脾、肺、肾、胸腺、睾丸及卵巢等)重量,做好记录。计算各脏器的相对重量(脏器重与体重的比值),即脏器系数。
1.8 数据处理
2 结果
2.1 临床表现
大鼠灌胃给药直至90 d各组均无死亡,低、中、高剂量组大鼠毛发光润,摄食、饮水、粪便均正常。给药观察期间,3个试验组大鼠的体重、摄食量及饲料利用率与对照组相比均无显著差异(>0.05)(见表1和表2)。

表1 清肺平喘口服液对大鼠体重的影响
续表1
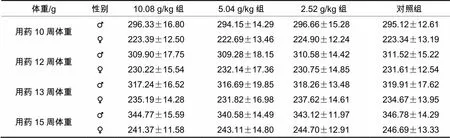
体重/g性别10.08 g/kg组5.04 g/kg组2.52 g/kg组对照组 用药10周体重♂♀296.33±16.80223.39±12.50294.15±14.29222.69±13.46296.66±15.28224.90±12.24295.12±12.61223.34±13.19 用药12周体重♂♀309.90±17.75230.22±15.54309.28±18.15232.14±17.36310.58±14.42230.75±14.85311.52±15.22231.61±12.54 用药13周体重♂♀317.24±16.52235.19±14.28316.69±19.85231.82±16.98318.26±13.48237.62±14.61319.91±17.62234.67±13.95 用药15周体重♂♀344.77±15.59241.37±11.58340.58±14.49243.11±14.80343.12±11.97244.70±12.91346.78±14.29246.69±13.33

表2 清肺平喘口服液对大鼠摄食量及饲料利用率的影响
2.2 血液生化参数
大鼠连续染毒90 d及停药2周后的血液学和血液生化参数测定结果分别见表3和表4。统计学分析显示,与对照组相比清肺平喘口服液各剂量组的血液生化参数之间差异均不显著(>0.05)。

表3 清肺平喘口服液连续染毒90 d时大鼠的血液生化参数
续表3

检测指标性别10.08 g/kg组5.04 g/kg组2.52 g/kg组对照组 血尿素氮/mmol · L-1♂♀7.04±0.246.86±0.857.14±0.256.79±1.087.15±0.398.71±0.387.34±0.718.51±0.89 白蛋白/g · L-1♂♀27.66±1.2428.00±1.1127.57±1.0128.77±0.6028.28±0.8328.23±1.6628.58±0.5028.15±0.55 总蛋白/g · L-1♂♀62.56±2.6560.70±3.2261.38±2.0961.47±1.5962.40±1.8262.70±2.7162.07±2.6959.95±1.68 白蛋白/球蛋白♂♀0.82±0.160.87±0.580.83±0.190.90±0.000.83±0.820.80±0.080.87±0.080.88±0.05 CHOL/mmol · L-1♂♀1.53±0.361.75±0.111.73±0.161.80±0.401.69±0.091.68±0.201.53±0.281.67±0.12 TG/mmol · L-1♂♀0.80±0.360.65±0.360.80±0.360.70±0.321.13±0.180.69±0.100.95±0.190.86±1.00 CRE/μmol · L-1♂♀29.88±1.4829.83±1.5229.10±1.8827.20±1.1528.47±2.0828.18±1.9531.31±3.6631.75±5.93

表4 清肺平喘口服液停药2周时大鼠的血液生化参数
续表4

检测指标性别10.08 g/kg组5.04 g/kg组2.52 g/kg组对照组 CHO/mmol· L-1♂♀1.55±0.131.88±0.081.85±0.442.15±0.091.58±0.122.01±0.171.52±0.162.08±0.28 TG/mmol· L-1♂♀0.92±0.140.81±0.201.16±0.351.20±0.411.17±0.140.87±0.290.90±0.221.53±0.91 CRE/mmol· L-1♂♀28.10±3.2430.55±0.8230.23±2.4029.23±1.5329.88±2.5926.89±1.7129.80±0.6029.40±3.07
2.3 脏器系数
对经口染毒至90 d和停药后2周宰杀的大鼠剖检后,均未发现任何异常和可疑病变。分别将90 d和停药后2周宰杀的对照组、清肺平喘口服液高剂量组中所有大鼠的心、肝、脾、肺、肾、胸腺、睾丸(♂)及卵巢(♀)组织脏器系数进行检测,结果见表5和表6,均未发现异常。

表5 清肺平喘口服液连续染毒90 d时对大鼠脏器系数的影响

表6 清肺平喘口服液停药2周时对大鼠脏器系数的影响
3 讨论
清肺平喘口服液主要成分包括桂枝、麻黄、苦杏仁、桔梗及黄芪。桂枝、麻黄辛温轻散,小汗解表,具有抑制动物气道炎症和改善哮喘的作用[5];苦杏仁—桔梗是临床上用于止咳、平喘、祛痰的经典药对,苦杏仁辛散苦降,以降为主,桔梗既升且降,以升为主,二药伍用,一升一降,升降调和,二者在镇咳作用上具有配伍增效的作用[6]。黄芪培土生金,实卫固表,止咳平喘效果较好[7]。研究表明,桂枝与黄芪属无毒中草药[8-9],但麻黄、苦杏仁、桔梗使用不合理则会对机体产生毒性。麻黄的毒性对中枢神经、肝脏、心脏、心血管等组织器官均易造成损伤[10],苦杏仁主要毒性表现为恶心呕吐、腹痛腹泻、头痛头晕、心悸、血压升高等[11]。研究表明,麻黄-杏仁配伍应用会增加苦杏仁的毒性作用[12]。桔梗的主要成分桔梗皂苷有很强的溶血作用,故不宜注射给药,口服后桔梗皂苷在胃肠道分解,即无溶血作用。但口服大剂量桔梗皂苷,反射性兴奋呕吐中枢,可引起恶心呕吐[13]。本试验通过研究灌服清肺平喘口服液后大鼠的临床表现、血液生化参数变化,评价清肺平喘口服液的长期毒性。
试验结果显示,低、中、高剂量组与对照组大鼠在90 d给药期间,活动正常、毛发光润,未发现中毒症状,动物无一死亡。试验动物的体重变化是反映动物机体中毒效应与毒物毒性的基本指标[14]。实验结果显示,不同剂量给药组大鼠的体重、摄食量及饲料利用率与对照组均无显著差异,但上述指标雄鼠普遍高于雌鼠,可解释为性别差异所造成。脏器系数是毒性试验中检测受试物对靶器官作用情况的重要参数。与未使用受试物的动物相比,脏器相对质量下降表明该器官可能发生萎缩、退行性病变或功能减弱,脏器相对质量上升则可能是由器官水肿、充血、增生性肥大或功能增强所引起[4,15]。本试验中,各给药组与对照组比较,各脏器指数值均无显著性差异,且均在正常值范围内。清肺平喘口服液连续染毒90 d时及停药2周时各给药组雌、雄大鼠与对照组相比,血液生化参数测定结果差异不显著,均在正常值范围内。
4 结论
综上所述,在试验条件下,未发现清肺平喘口服液对大鼠的生长发育产生影响,长期重复应用无长期毒性;停药 2 周未见由蓄积毒性引起的后遗效应。表明清肺平喘口服液对靶动物的临床安全性在可接受范围内。
[1] 任锋. 鸡呼吸困难性疫病的鉴别与防治[J]. 草业与畜牧,2009(7):60-62.
[2] 苑耀辉. 鸡常见呼吸系统疾病及防治策略[J]. 中国畜牧兽医文摘,2016,32(10):10-12.
[3] 沈建忠,王战辉. 兽药残留和细菌耐药性问题在畜产品安全中日益突出[J]. 兽医导刊,2013(5):55-57.
[4] 王玲,郭志廷,林春全,等. 抗球虫中药常山口服液的亚急性毒性试验[J]. 中国兽医学报,2017,37(7):1334-1342.
[5] 张保国,刘庆芳. 桂枝麻黄各半汤药理研究与临床应用[J].中成药,2012,34(3):539-541.
[6] 张金艳,何萍,李贻奎. 苦杏仁、桔梗及二者配伍止咳、祛痰作用的研究[J]. 中国实验方剂学杂志,2010,16(18):173-175.
[7] 王洪军. 自拟黄芪平喘止咳汤治疗支气管哮喘的疗效观察[J]. 临床医学,2011,31(7):122.
[8] 赵国玺,宋莉. 桂枝急性毒性及30天喂养试验研究[J]. 湖北中医杂志,2014,36(2):23-24.
[9] 刘阳,张云鹏,孙影,等. 中药黄芪长期毒性试验研究[J].现代中西医结合杂志,2009,18(29):3545-3546.
[10] 姜雪,孙森凤,王悦. 麻黄的毒性作用研究概况[J]. 山东化工,2017,46(14):49-50.
[11] 杜虹韦,张爱华,赵欣蕾. 苦杏仁毒性及其解毒方法研究进展[J]. 黑龙江中医药,2013,43(4):58-59.
[12] 谭镇岳. 麻黄、杏仁配伍对苦杏仁毒性影响及最佳比例研究[J]. 社区医学杂志,2011,9(24):77-78.
[13] 泰阳,侯建平,孟建国,等. 桔梗的药理学研究进展[J].中国医药科学,2012,2(19):74-75.
[14] 倪莉. 基于机体状态的中药毒性理论研究[J]. 中华中医药杂志,2009,5(2):187.
[15] 马秀兰,宋淑云,叶建新,等. 对成年大鼠脏器系统与体重相关性的探讨[J]. 山西医药杂志,2005,34(8):661-662.
责任编辑:张爱婷
Long-term toxicity of clear away lung-heat to relieve asthma oral liquid in rats
DONG Hui-feng1,2, ZHU Guo-xia3, LI Yuan1,2, WAGN Li-hong1,2, ZHANG Feng-hong1,2, LIU Ding-kuo1,2,4Corresponding Author
(1. S&E Animal Pharmaceutical(Tianjin)Co, Ltd. , Tianjin 300383, China; 2. Enterprise Key Laboratory of Feed Microbial Preparation, Tianjin 300383, China; 3. Tianjin Key Lab of Aqua-Ecology and Aquaculture, Tianjin Agricultural University, Tianjin 300384 , China; 4. College of Veterinary Medicine, China Agricultural University, Beijing 100094, China)
The long-term toxicity of clear away lung-heat to relieve asthma oral liquid in SD rats was researched by continuous perfusion in order to expose its clinical innocuity. 120 SD rats (males and females) were randomly divvied into control group and clear away lung-heat to relieve asthma oral liquid in 3 different dosage groups (2.52 g/kg, 5.04 g/kg and 10.08 g/kg, 30 in each group). The SD rats were administered with clear away lung-heat to relieve asthma oral liquid by continuous perfusion for 90 days. The body weight, food intake, hematology, blood biochemistry and organ coefficient were measured for the overall toxicity assessment to rats. Results: After 90 days, no death occurred in 120 rats. The appetite and excretion of clear away lung-heat to relieve asthma oral liquid rats were normal and their feathers were sleek. During the administration period, the weight, food intake, hematology, blood biochemistry and organ coefficientof the test group rats had no significant differencefrom the control group(>0.05). It was concluded that with the dose of 2.52 g/kg, 5.04 g/kg and 10.08 g/kg clear away lung-heat to relieve asthma oral liquid continuous perfusing, there is no harmful effect for SD rats.
clear away lung-heat to relieve asthma oral liquid; rat; long-term toxicity
S859.79
A
2017-12-08
天津市科技支撑计划项目(13ZCZDNC00700)
董惠峰(1968-),男,工程师,学士,主要从事兽药研发生产工作。E-mail:1247797695@qq.com。
刘鼎阔(1981-),男,高级兽医师,硕士,主要从事中兽药新制剂开发工作。E-mail:liudingkuo1981@163.com。
1008-5394(2018)02-0030-06
10.19640/j.cnki.jtau.2018.02.008
