多层螺旋CT评价冠状动脉周围脂肪与冠心病的相关性
2018-08-07王治愚李念云
王治愚 李念云 王 政
心外膜脂肪组织(epicardial adipose tissue,EAT)是内脏脂肪在心脏表面的堆积,研究表明其与冠状动脉狭窄有显著的相关性,起源于棕色脂肪组织,是一个代谢活跃、功能复杂的内分泌器官[1]。EAT又可分为冠状动脉外膜周围的脂肪组织(pericoronary adipose tissue,PCAT)及心肌表面脂肪组织。PCAT可能通过旁分泌作用及滋养血管分泌机制促进冠状动脉粥样硬化进程[2],可能较EAT体积更好地评价冠心病进展,但目前关于PCAT的研究还很少。多层螺旋CT(multislice spiral computed tomography,MSCT)冠状动脉成像具有良好的各向同性,对脂肪成分识别率较高,其后处理软件的裁剪、CT阈值设定及自动体积测量可较精确地分段测量PCAT体积。本文利用MSCT冠状动脉造影及后处理软件测量PCAT,并分析其与冠心病的相关性。
方 法
1. 临床资料
选取2016年6月~2017年3月我院行冠状动脉CT检查的疑似冠心病患者138例为研究对象,其中,男78例,女60例,平均年龄52.6±6.9岁,给予心脏CTA扫描,对诊断不明确或有中度及以上狭窄患者进一步行冠状动脉造影检查及治疗。研究排除标准:肝脏疾病、肾功能不全、患有甲状腺疾病者,对碘对比剂过敏者。将冠状动脉造影诊断狭窄≥50%定为冠心病诊断标准。临床资料由门诊及住院资料获得,包括基线资料、病史、身高、体重、体质指数(BMI)、吸烟史等。临床指标包括总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)和血糖等生化指标通过我院中心实验室检测。
2. 检查方法
采用Siemens第二代炫速双源CT(Flash CT)心电门控技术,扫描范围自气管隆突下方及至膈顶下方1cm。扫描参数:准直器2mm×128mm×0.6mm,层厚 0.6mm,旋转时间0.28s,管电压80~120kV,管电流290~560 mAs/r,螺距为0.17~042。采用Bolus tracking技术,经右肘正中静脉注入碘普罗胺(370mgI/ml)50~90 ml,速度4.5~5.0ml/s,然后以相同速度注射生理盐水50ml。应用对比剂示踪法,在主动脉根部层面选择感兴趣区检测CT值。当感兴趣区内CT值达到100HU时,延迟5s自动触发扫描。采用螺旋模式,全剂量曝光的范围为30%~80% R-R间期。
3. EAT容积及厚度测定
利用GE AW4.5后处理工作站(由Siemens Flash CT主机直接传输图像至工作站)测定EAT容积及厚度。EAT定义为心包脏层至心肌之间的脂肪组织,测量范围为肺动脉分叉处至心尖部位。利用阈值测定法,将EAT脂肪设定为-200~-30HU区域内的成分,软件自动去除心腔内造影剂、血管壁、心肌等CT值不在所设范围内的成分,最后利用容积测量功能自动计算EAT容积。EAT厚度定义为右室游离壁脂肪厚度,在右心室中部短轴面图像上,分别以25%、50%、75%右室游离壁水平为界,测定EAT前、中、后段厚度,测量时与心室壁切线垂直,并计算三者平均值用于统计分析。
4. PCAT 测定
利用GE AW4.5后处理工作站Coronary Analysis软件分别对左主干-左前降支(LMLAD)、左旋支(LAD)、右冠状动脉(RCA)行行曲面重建,手动将该三支主干自开口处始连续每10mm为一段(图1~4),分段测量三支主要血管周围脂肪组织体积,手动裁剪包含每段血管和冠状动脉周围脂肪的感兴趣区,利用上述阈值测定法(阈值设定为-200~-30HU)和体积自动测量软件测出每段PCAT(冠状动脉周围脂肪组织)体积(图1a~4a),计算每支冠状动脉各段PCAT体积之和作为该血管PCAT体积。以上所有操作均由同一人完成。
5. 冠状动脉病变程度定量评价
冠状动脉狭窄程度的评价根据美国心脏协会(American Heart Association,AHA)评价标准和Gensini积分系统[3]对每支血管病变程度进行定量评定:1分)管腔狭窄程度<25%;2分) 狭窄25%~50%;4分)51%~75%;8分)76%~90%;16分)91%~99%;32分)100%(闭塞)。对不同节段冠状动脉进行评分:左主干病变得分×5;左前降支近段×2.5,中段×1.5,远段×1;对角支的第一对角支×1,第二对角支×0.5;左回旋支近段2.5,远段及后降支均×1,后侧支×0.5;右冠状动脉病变近、中、远和后降支均×1,后侧支×0.5;每例患者冠状动脉病变程度的最终积分为各分支积分之和。冠状动脉狭窄程度分为4级:管腔轻度狭窄(51%~75%)、中度狭窄(76%~90%)、重度狭窄91~99%及完全闭塞(100%)。
6. 统计学方法
应用统计学软件SPSS13.0完成统计分析。计量资料用均数±标准差表示,组间比较:符合正态分布的计量资料采用t检验,非正态分布的计量资料组间比较采用秩和检验。正态分布资料的相关性分析采用Pearson相关分析,非正态分布资料的相关性采用Spearman相关分析。以P<0.05为差异有统计学意义。
结 果
1. 患者基线资料分析
138例研究对象,共检出冠脉狭窄病变者114例,病变259处,其中轻度狭窄32例,中度及以上狭窄116例,经冠状动脉造影确诊冠心病患者82例,排除冠心病诊断56例(CT冠状动脉造影明确排除狭窄,处于临界病变者进一步行冠状动脉造影检查诊断)。冠心病组82例,平均年龄55.4±6.3岁,男47例,女35例,平均BMI为30.7±4.9kg/m2,CAD家族史53例(38%);非冠心病组56例,平均年龄50.5±7.1岁,男31例,女25例,平均BMI为 26.3±5.1kg/m2,CAD 家 族 史 40例(49%)。两组年龄、性别、HDL-C、LDL-C差异无统计学意义(P>0.05);CAD危险因素(包括高脂血症、高血压、糖尿病)、BMI、吸烟、CAD家族史、TC、TG差异均有统计学意义(P<0.05),见表1。
2. 冠心病组与非冠心病组PCAT及EAT厚度的比较
冠心病组与非冠心病组EAT容积、LM-LAD、RCA冠周脂肪、三支血管冠周脂肪之和(Total PCAT)、Gensini积分、钙化积分差异均有统计学意义(P<0.05),以三支血管冠周脂肪之和(Total PCAT)、Gensini积分、钙化积分差异相对显著(P<0.01)。冠心病组平均PCAT体积、Gensini积分、钙化积分分别为 25.1±4.12cm3、38.2±7.51、116.4±23.56, 非 冠 心 病 组 平 均 PCAT 体 积、Gensini积分、钙化积分分别为 17.2±3.32cm3、10.1±6.54、43.2±14.75,冠心病组与非冠心病组EAT 容积分别为 227.1±32.5cm3、181±37.1cm3,冠心病组与非冠心病组PCAT差异较EAT显著。冠心病组与非冠心病组EAT厚度分别为3.51±0.88mm、3.12±0.47mm,LCX 冠周脂肪体积分别为 4.66±0.53cm3、4.39±1.01cm3,差异均无统计学意义(表2)。
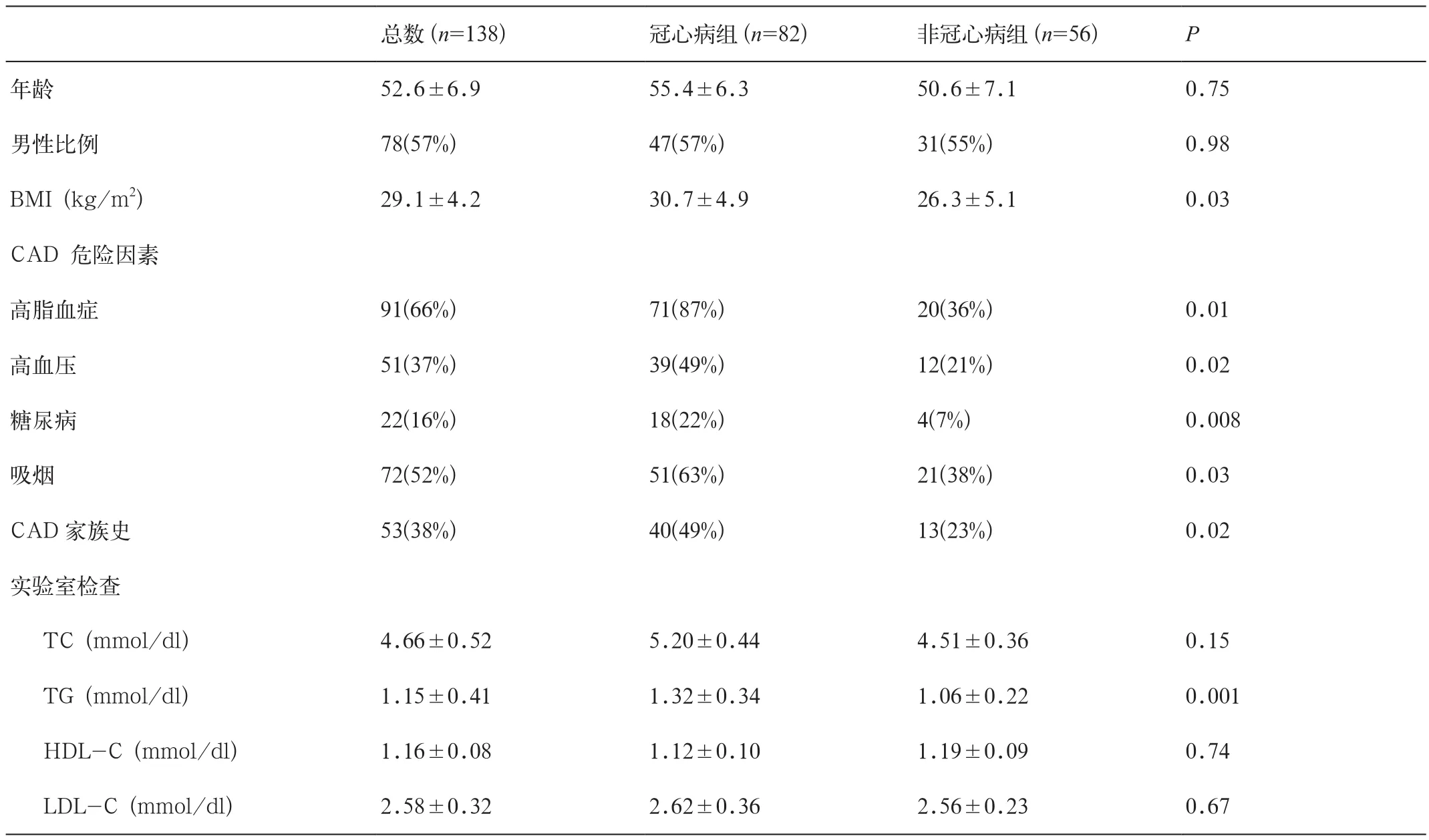
表1 冠心病组与非冠心病组临床资料比较
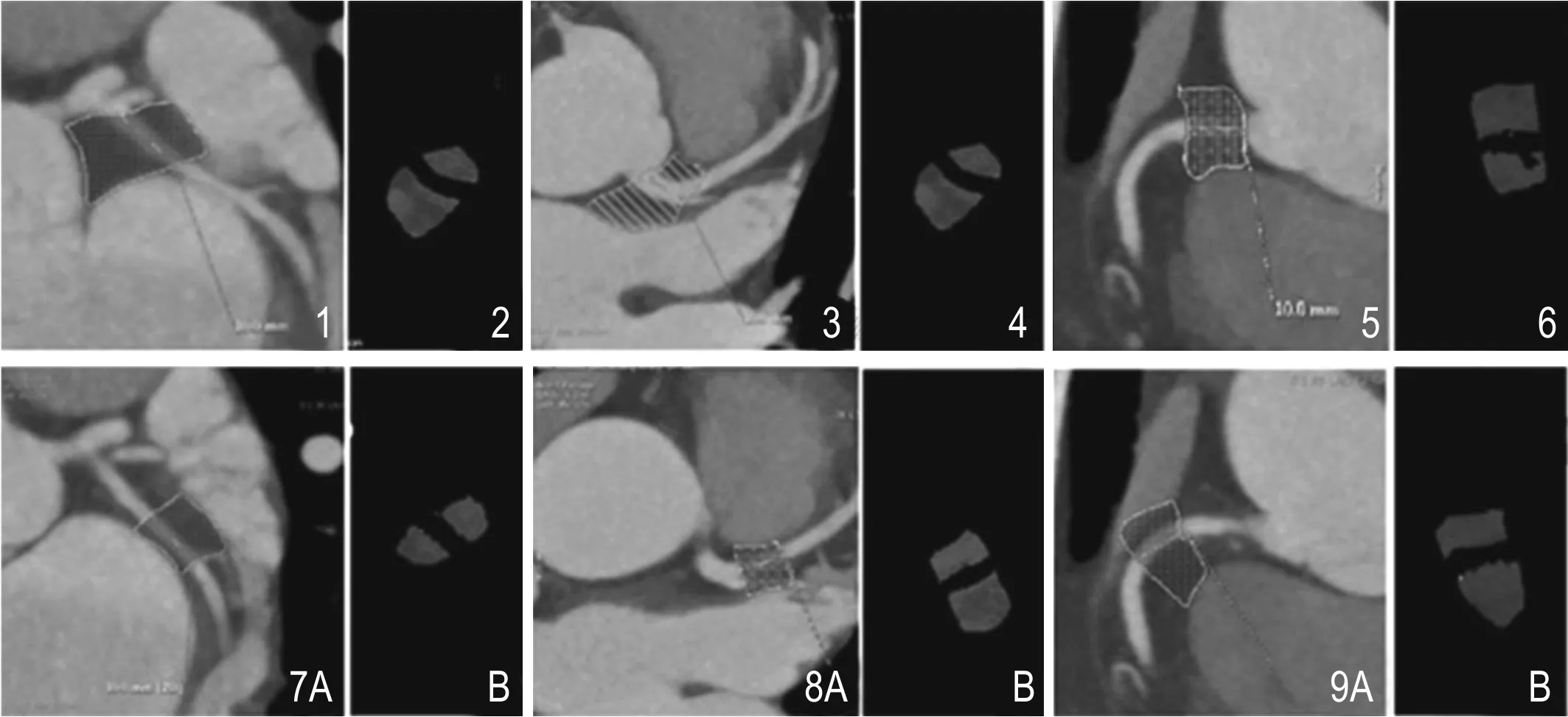
图1 LCX曲面重建图像,利用后处理软件自开口处测量1cm距离,手动画出感兴趣区范围(网状区),自动剪除感兴趣区范围以外结构,利用脂肪阈值测定除去脂肪以外的结构(包括管壁、管腔、心肌、心腔结构)。图2 剩余感兴趣区范围内脂肪组织,为该段血管(LCX第一段)的脂肪体积。图3 LM-LAD曲面重建图像,手动勾勒测量LM-LAD第一段感兴趣区血管及周围脂肪。图4 自动阈值去除脂肪以外的结构,剩余冠周脂肪组织。图5 RCA曲面重建图像,手动勾勒第一段。图6 自动阈值方法保留冠周脂肪成分。图7 脂肪阈值测量LCX第二段(1cm)冠周脂肪体积。图8 阈值方法测量LM-LAD第二段冠周脂肪体积。图9 测量RCA第二段冠周脂肪体积。

表2 冠心病组与非冠心病组PCAT及EAT的比较
3. 临床参数及冠状动脉病变与PCAT体积的相关分析
PCAT与所有研究对象(n=138)Gensini积分、钙化积分、年龄、BMI、TG呈正相关,相关程度依次递减(表3)。PCAT与Gensini积分、钙化积分相关性最为显著,P<0.01。与HDL-C呈负相关(P<0.05)。而与性别、LDL-C未见相关性(P>0.05)。
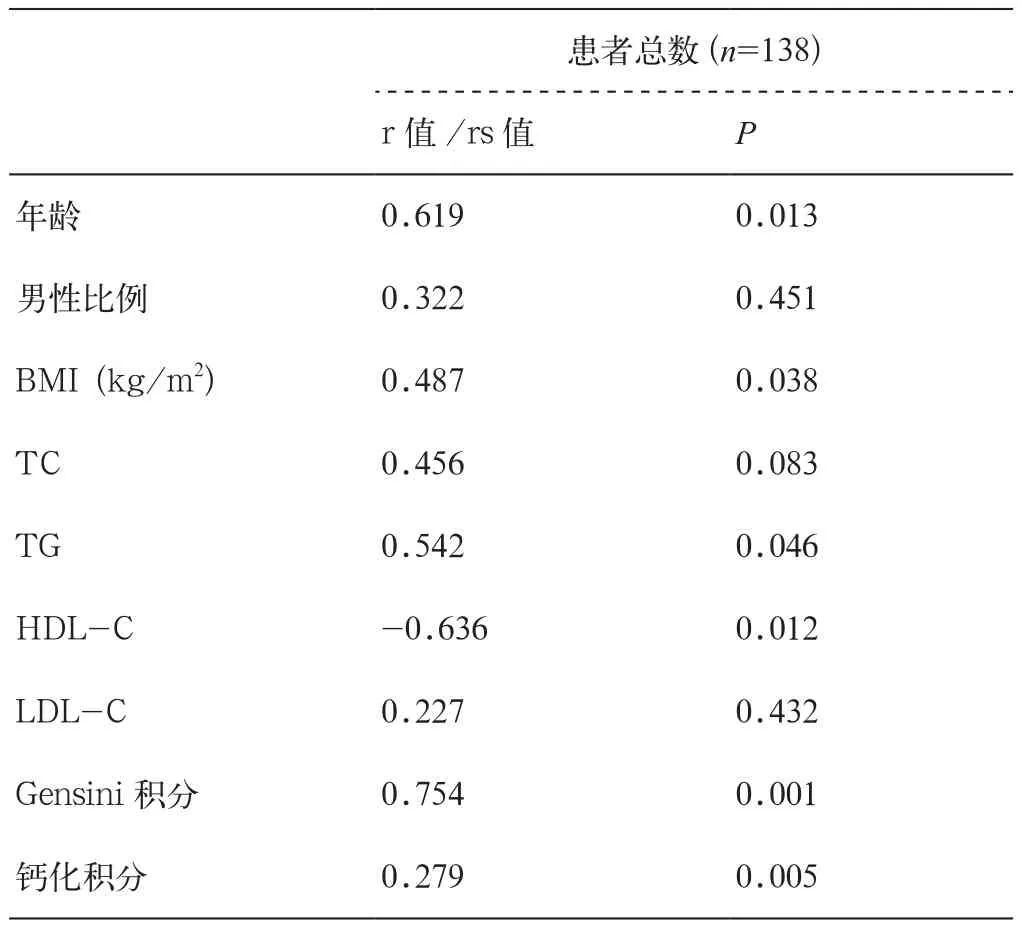
表3 临床参数与PCAT体积的Pearson/Spearman相关分析结果
讨 论
近年多项研究发现心外膜脂肪与动脉粥样硬化的发生及发展密切相关,可用以预测冠心病的危险:Yerramasu等[5]研究发现,CT测量心外膜脂肪组织体积是冠状动脉钙化存在即严重程度的独立标记,同时也预示着个体冠状动脉钙化进展的更高风险。Jeong等[6]认为,与腰围及腹围相比,心外膜脂肪是冠心病最好的预测指标。研究显示[7-9],心外膜脂肪可产生加速动脉硬化进程的因子,如肿瘤坏死因子-α、白介素-6、游离脂肪酸等,通过影响胰岛素敏感性、血压水平、内皮功能、纤溶活性等促进斑块不稳定及血栓形成。心外膜脂肪组织又可分为心肌表面脂肪和冠状动脉周围脂肪,后者对冠状动脉粥样硬化的影响是否更加显著,相关研究还很少。
本研究中,PCAT与Gensini积分、钙化积分、年龄、BMI、TG呈正相关,相关程度依次递减。PCAT与Gensini积分及钙化积分呈显著正相关(P<0.01),反映其与冠状动脉粥样硬化斑块的进程相关,这与国外研究[9]认为心外膜脂肪是预测冠状动脉钙化进展及发生心血管事件的较早期指标相符,但其容积对不同成分斑块的影响仍有待于进一步研究。另外,冠心病组与非冠心病组LM-LAD及RCA冠周脂肪体积有差异,而两组间LCX冠周脂肪差异无统计学意义,这与三支血管斑块出现的频率及狭窄程度严重性分布一致,也可能因回旋支周围组织容量较少,产生损伤血管内膜的细胞因子相对较少有关。
本研究中,PCAT与年龄、BMI呈正相关(P<0.05),可能因为脂肪组织随着年龄、体重的增加而增加,Tansey等[10]通过尸检发现心外膜总量与年龄呈正相关关系,但Iacobellis等[11]利用超声心动图检测心外膜脂肪厚度与年龄无关,笔者分析后者可能与只针对心肌表面脂肪厚度评估及超声探测脂肪厚度相对于CT的局限性有关,可能随着年龄增加,冠周脂肪增加的量较心肌表面脂肪更加显著,需要进一步大样本分层研究。本研究中PCAT与BMI呈正相关(r=0.487),而冠心病组与非冠心病组BMI差异具有统计学意义(P<-0.05),可解释肥胖(尤其向心型肥胖)作为冠心病的危险之一,参与了冠状动脉粥样硬化炎症反应过程,其病理生理原因为BMI较高(过度肥胖)可引起脂肪细胞肥大并表现为促炎状态,进而释放大量的炎症细胞因子,导致各种代谢相关性疾病[12],而PCAT与冠状动脉之间无筋膜分隔,共享一个微循环,通过旁分泌或滋养血管将这些炎症细胞因子输送至血管内皮,引起局灶性的慢性炎症反应及胰岛素抵抗,从而作用于冠状动脉粥样硬化斑块的始动环节[13]。
本研究中,冠心病组与非冠心病组PCAT体积差异较EAT体积显著,而EAT厚度两组间差异无统计学差异。析其原因,一方面可能与未对研究对象体质指数及年龄分层有关,Gorter等[14]研究认为,如果不对BMI分层,冠状动脉周围脂肪体积与冠心病严重性并不相关。另外,也可能因为冠心病组心外膜脂肪体积的增加以冠状动脉周围脂肪为主,而并非心外膜脂肪,这与本研究中两组PCAT体积差异较EAT显著相吻合,需要进一步扩大样本量并对BMI、年龄进行分层研究。
既往MRI测量心外膜体积被认为是金标准,但其扫描时间长、费用高,且与MDCT的各向同性分辨率相比,MRI的Z轴分辨率偏低,不利于体积测量。而超声则局限于测量心肌表面脂肪厚度,简便可行,但范围局限,属于二维测量,可重复性低。而多层螺旋CT可有效克服心脏搏动的影像,基本达到各项同性,测量结构具有较好的重复性,已经替代MDCT成为测量PCAT的金标准[15]。
本研究之不足之处在于,一方面为研究对象已经过临床筛选,故样本会出现选择偏倚;另外作为为横断面研究,只对不同个体PCAT体积与冠心病关系进行了研究,如对同一研究对象数年跟踪,可进一步分析PCAT随冠状动脉斑块的变化情况。
