GCMS测定4类食品接触材料中多环芳烃类化合物的溶出暴露水平
2018-08-04黎绍学秦俊莲陈嘉琪罗尔伦彭密军
黎绍学,秦俊莲,曾 莹,陈嘉琪,罗尔伦,彭密军,*
(1.广东省测试分析研究所,广东省化学危害应急检测技术重点实验室,广东广州 510070;2.深圳市计量质量检测研究院,广东深圳 518131)
多环芳烃(Polycyclic Aromatic Hydrocarbons,PAHs)是指两个以上苯环以稠环形式相连的化合物[1]。PAHs具有高度亲脂性,易溶于有机溶剂,水中溶解度低,随着环的数目增加,水中的溶解度降低。PAHs的含量在自然界中一直处于动态的平衡,但自从人类工业活动的增加,近年PAHs在环境土壤[2]和空气中[3]的含量逐渐上升。作为一类对人体有害的环境污染物,PAHs的危害主要为化学致癌性作用。流行性病学研究表明,PAHs通过皮肤,呼吸道,消化道等均可被人体吸收,有诱发皮肤癌、肺癌、直肠癌、膀胱癌等作用[4]。美国环境保护署(EPA)将毒性最大的苯并芘等16种PAHs列为优先污染物。欧盟REACH指令附件17全面限制在消费品中使用PAHs,对于食品接触材料,要求不得检出PAHs。
对于食品接触材料而言,近年亦多见PAHs迁移污染的报道。王成云等[5]对纸质食品接触材料中18种禁用多环芳烃进行了同时测定,发现一个米色再生包装纸袋中检出高含量的菲。冯坤等[6]运用GC-MS-MS来检测街边小吃接触材料中的PAHs,发现几种小吃食品的塑料和泡沫包装材料中检测到一定量的多环芳烃。Li等[7]在聚苯乙烯食品接触材料中检出稠环较少的PAHs种类,并确认PS食品接触材料为环境中PAHs的污染来源之一。PAHs的来源可能有两个方面,一个是使用回收材料生产食品接触材料,一个是使用劣质食品接触材料添加剂所致。因此,加强对食品接触材料中PAHs溶出暴露水平的研究,对PAHs污染的卫生安全研究有重要的意义。
PAHs的检测方法包括高效液相色谱法(HPLC)、气相色谱质谱联用法(GC-MS)[8-11]、气相色谱质谱质谱法(GC-MS-MS)[12],微萃取-拉曼光谱法[13]。其中,GC-MS因灵敏度高、检出限低、操作简便等优点而被广泛应用于PAHs的检测之中。本文利用GC-MS法的SIM模式对食品接触材料模拟浸泡液中的PAHs溶出水平进行检测,将所测结果进行统计分析,试图筛选出溶出风险最高的PAHs及相应的食品相关产品。
1 材料与方法
1.1 材料与仪器

7890A-5975C型气相色谱质谱联用仪、DB 35-MS UI色谱柱(30 m×0.25 mm×0.25 μm) 德国安捷伦公司;UF55型精密鼓风烘箱 德国Memmert公司。
1.2 实验方法
1.2.1 标准工作液配制 准确吸取多环芳烃混合标液1 mL于100 mL容量瓶中,配制成10 mg/L标准储备液。逐级稀释得到需要的标准工作液,浓度范围从1~200 μg/L。
1.2.2 样品处理 本次检验选择70批次塑料制品进行多环芳烃迁移量调研,按可能接触油脂性食品选择异辛烷作为模拟物,根据GB/T 23296.1-2009[14]的要求及相关迁移规律的研究[15-16],按样品的常见使用条件选择模拟接触的温度和时间。复合膜、袋按室温长期接触油脂性食品为使用条件,按标准要求选择20 ℃及2 d作为模拟条件。一次性餐具按不超过70 ℃短时间接触油脂性食品为使用条件,按标准要求选择70 ℃及2 h作为模拟条件。所调研尼龙餐具为尼龙铲,按标准要求回流4 h作为模拟条件。食品用容器为日常条件使用的塑料盒和塑料杯,按标准要求选择70 ℃及2 h作为模拟条件。将样品准确裁取5 cm×10 cm,置于50 mL具塞玻璃管中,分别准确加入异辛烷各50 mL作为模拟物介质完全浸没样品,按相应的迁移实验温度及时间进行模拟实验,实验结束后静置冷却至室温。取出样品,上清液不过滤直接供GC-MS测定。空白实验同上述步骤处理,进行GC-MS分析。
1.2.3 仪器参数 结合以上检测方法与标准,本方案拟建立采用气相色谱-质谱联用法测定食品接触材料中多环芳烃,并以其迁移量对市售的食品接触材料中多环芳烃评估存在的暴露风险水平。
色谱柱:30 m×0.25 mm(内径)×0.25 μm(膜厚),DB-35 MS UI石英毛细管柱;进样口温度:290 ℃;色谱柱温度程序:初始柱温70 ℃,保持0.5 min,以25 ℃/min升温到155 ℃,保持1 min,再以2 ℃/min升温至160 ℃,然后以5 ℃/min升温至200 ℃,再以8 ℃/min升温至250 ℃,保持2 min,然后以8 ℃/min升温到280 ℃,保持7 min;载气氮气(纯度≥99.999%),流速1 mL/min;进样方式:不分流进样;进样量:1 μL。
质谱参数:色谱与质谱接口温度:280 ℃;电离方式:电子轰击源(EI);电离能量:70 eV;溶剂延迟:3 min;监测方式:选择离子扫描模式(SIM),定性与定量离子见表1。

表1 16种多环芳烃的定性与定量离子Table 1 Qualitative and quantitative ion of 16 kinds of PAHs
2 结果与分析
2.1 方法线性范围与检出限
以3倍的信噪比计算检出限,方法的线性方程、线性范围及检出限见表2。16种多环芳烃在1~100 μg/L的范围内具有良好的线性,相关系数均大于0.995,检出限在50~100 ng/kg,满足本次实际样品的检测。

表2 线性方程、浓度范围及检出限Table 2 Linear equation,concentration range and detection limit
2.2 回收率和精密度
以复合膜袋为例,对空白样品分别添加水平进行浸泡,每个添加水平测定6次,实验结果见表3。16种PAHs模拟液的平均回收率在76.5%~100.7%之间,相对标准偏差为1.0%~3.5%之间,具有较好的回收率和精密度。

表3 方法回收率和精密度(n=6)Table 3 Recoveries and relative standard deviations of the method(n=6)
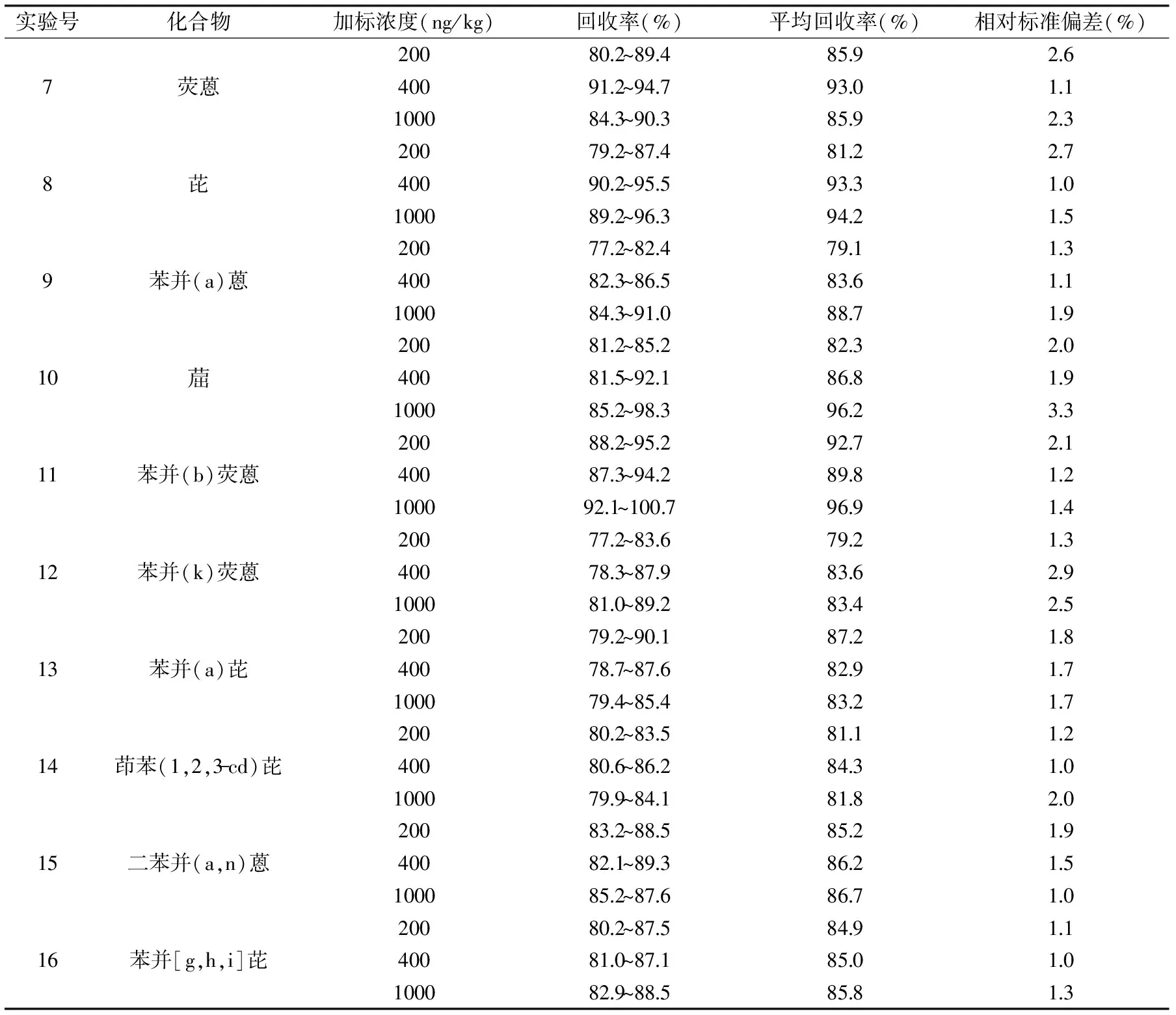
续表
2.3 检出情况统计
对70批次样品的多环芳烃迁移量的检验结果进行检出率及溶出量分布统计显示,主要检出萘、菲、荧蒽、芘4种化合物,其他12种多环芳烃均未有检出,检出率最高的是菲。在各类食品接触材料中,食品用容器、尼龙餐具、一次性餐具等检出率及检出含量最高,均存在一定的风险(见表4)。

表4 各类产品的PAHs迁移Table 4 PAHs migration of 4 kinds of products
2.4 原因分析
由图1~图4,表5中,对检出情况进行分析,样品中PAHs可能有以下几方面的来源:第一是加入了回收利用的劣质材料[17],第二是添加的矿物油为劣质添加剂,第三是印刷油墨[18-19]。而最有可能带入的来源是食品接触材料中所添加的矿物油[20]。
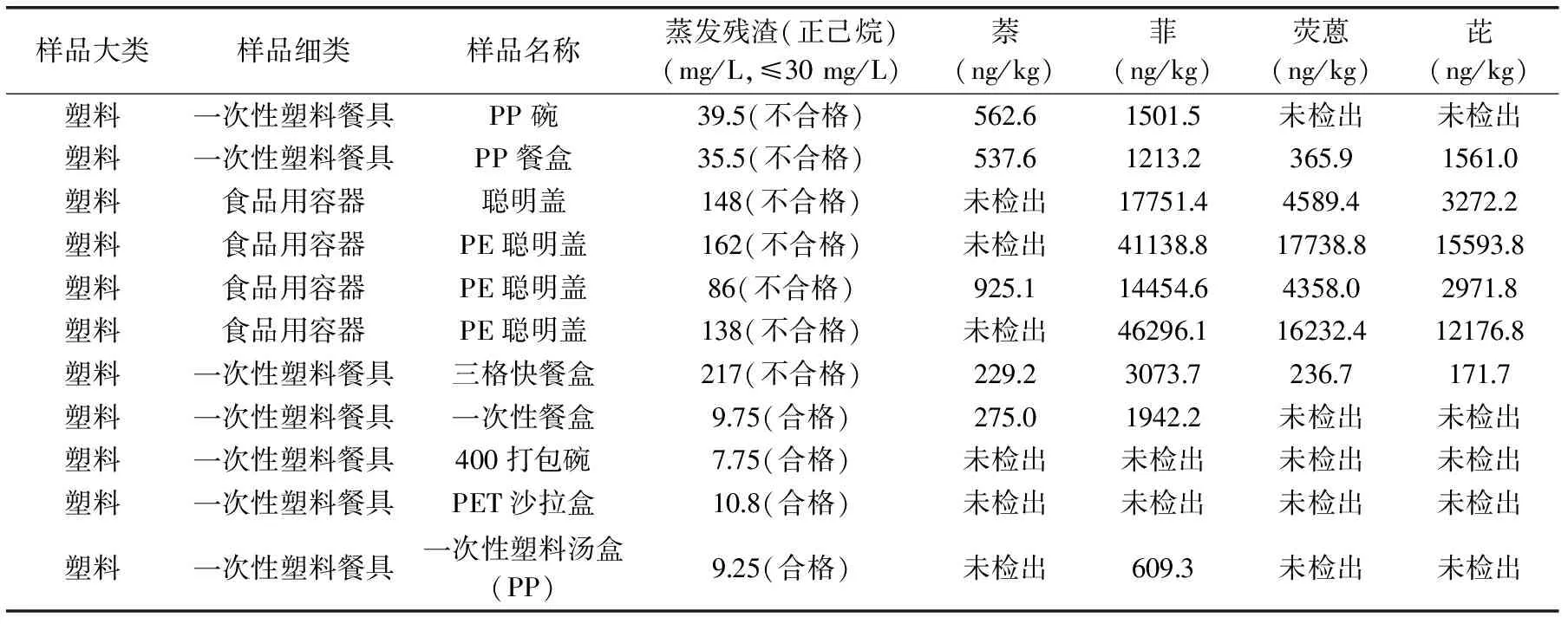
表5 不合格样品蒸发残渣与多环芳烃迁移量对比Table 5 Contrast of evaporative residue and PAHs migration
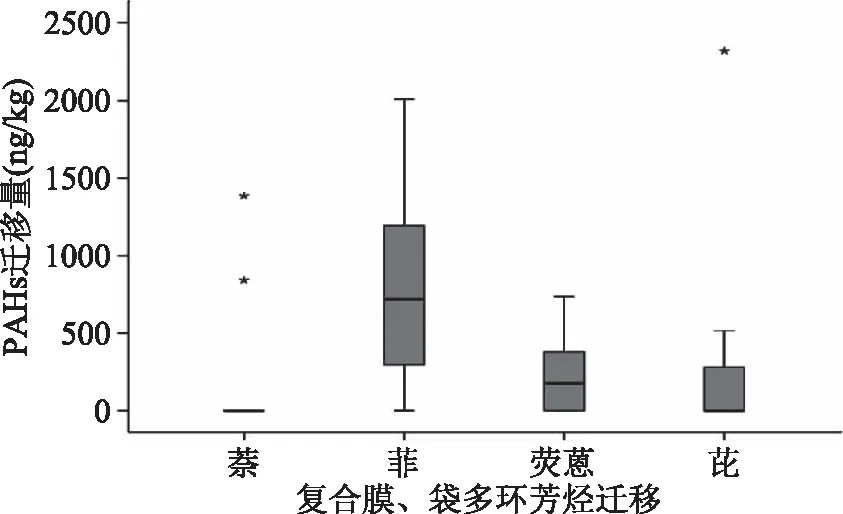
图1 复合膜、袋PAHs迁移Fig.1 PAHs migration of complex films注:*表示数据严重离群;图2~图4同。

图2 尼龙餐具PAHs迁移Fig.2 PAHs migration of nylon tableware注:°表示数据一般离群;图3~图4同。

图3 食品用容器PAHs迁移Fig.3 PAHs migration of food container

图4 一次性餐具PAHs迁移Fig.4 PAHs migration of disposable tableware
在本次PAHs迁移量调研过程中发现蒸发残渣(正己烷)不合格的样品,其多环芳烃的迁移溶出量要远大于蒸发残渣(正己烷)合格的样品。蒸发残渣值越大,多环芳烃溶出量越大,说明食品接触材料中蒸发残渣(正己烷)不合格与多环芳烃的溶出量存在一定的正相关性。蒸发残渣(正己烷)反映的是食品接触材料中矿物油添加剂的用量大小,推测食品接触材料中多环芳烃可能是矿物油带入的。
3 结论
本文建立了食品接触材料中16种多环芳烃类物质迁移量的GC-MS检测方法,方法的准确性和精密度较好,适合公共领域食品接触材料安全卫生的监督执法及风险评估工作。在方法研究的基础上,本文发现了食品接触材料中多环芳烃的高检出率及高溶出量与食品接触材料的蒸发残渣(正己烷)存在一定的相关性,并推测污染源有可能来自于劣质的生产原料。
