儿童隐源性多灶性溃疡性狭窄性小肠炎1例并文献复习
2018-08-03王玉环姜支农
张 萍 孙 桦 张 烨 吴 婕 王玉环 姜支农 黄 瑛
1 病例资料
男,9岁6个月,因“反复贫血伴黑便6年”就诊复旦大学附属儿科医院(我院)。
患儿3岁多家长发现口唇苍白,黄便中少许黑便,外院诊断为“贫血”,未予治疗。5岁时因“间断腹痛1年”于我院门诊行胃镜检查示浅表性胃炎。5岁6个月时因口唇苍白,我院血液科门诊查Hb 85 g·L-1,MCV 69 fl,MCHC 26.7%,诊断为“缺铁性贫血(小细胞低色素性)”,给予口服铁剂治疗1年,期间门诊随访Hb 85~102 g·L-1。6岁2个月时因每天1~2次柏油便,大便成形,持续4个月,至我院消化科住院,之后又4次入住我院。发病以来患儿无发热、黄疸,无恶心、呕吐、腹泻、腹胀,无皮疹、口腔溃疡和关节肿痛,无体重明显减轻。起病前及病程中未应用非甾体类抗炎药(NSAIDs)。
既往史:患儿6岁6个月曾于我院外科行“左腹股沟斜疝修补术”。
家族史:患儿父母体健,否认近亲结婚,否认遗传病史。母孕期有贫血史,母孕产史2-0-0-2。妹妹1岁半,体健。
入院查体:身高和体重分别在P10~25和P25~50百分位。神志清,精神可,皮肤、黏膜无皮疹,无出血点,全身浅表淋巴结未及肿大,呼吸平稳,口唇苍白。口腔黏膜光整无破溃,咽无充血。双肺呼吸音粗,未及干湿啰音。心音有力,律齐,未闻及杂音。腹软,无压痛,肝脾肋下未及,肠鸣音正常。四肢肌力和肌张力正常。病理反射(-)。
辅助检查:表1显示,患儿于我院5次住院的WBC、Hb、CRP、T-SPOT、铁蛋白、自身抗体、粪隐血和胶囊内镜下小肠运作时间。肝肾功能、电解质和白蛋白水平均在正常值范围。血清寄生虫抗体阴性,粪便未找到寄生原虫、未找到寄生虫卵。多次腹部增强CT和小肠MR未见异常。异位胃黏膜显像未见异常。
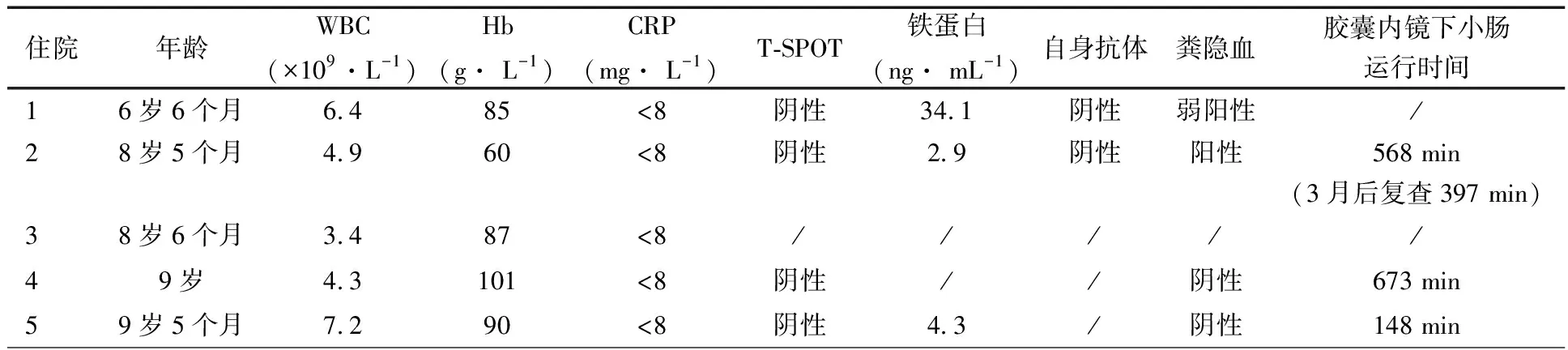
表1 本文患儿检查情况
诊治经过:图1为诊断、治疗和随访等重要临床信息时间轴。患儿第1次住我院(6岁6个月)查胃镜和结肠镜均未明确黑便原因。第2次入我院(8岁5个月)查胶囊内镜示空肠中下段至回肠多发环形狭窄伴溃疡(图2A、B)。外科建议行手术探查活检术明确黑便原因。患儿母亲考虑到手术的风险决定保守治疗,给予口服美沙拉嗪和铁剂。门诊复查胶囊内镜仍示小肠环形狭窄(图2C)。患儿9岁时再次出现解黑便1次伴下腹部隐痛,结肠镜示末端回肠淋巴滤泡增生,病理检查示小肠黏膜局灶淋巴组织增生,隐窝结构保存。未见肉芽肿,未见炎症性肠病病理诊断依据,未见肿瘤,未见结核(图3)。胶囊内镜示小肠多发环形狭窄伴小肠炎(图2D),较前无明显好转。根据Zhang等[1]提出的诊断标准,诊断为隐源性多灶性溃疡性狭窄性小肠炎(Cryptogenic multifocal ulcerating stenosing enteritis,CMUSE)。
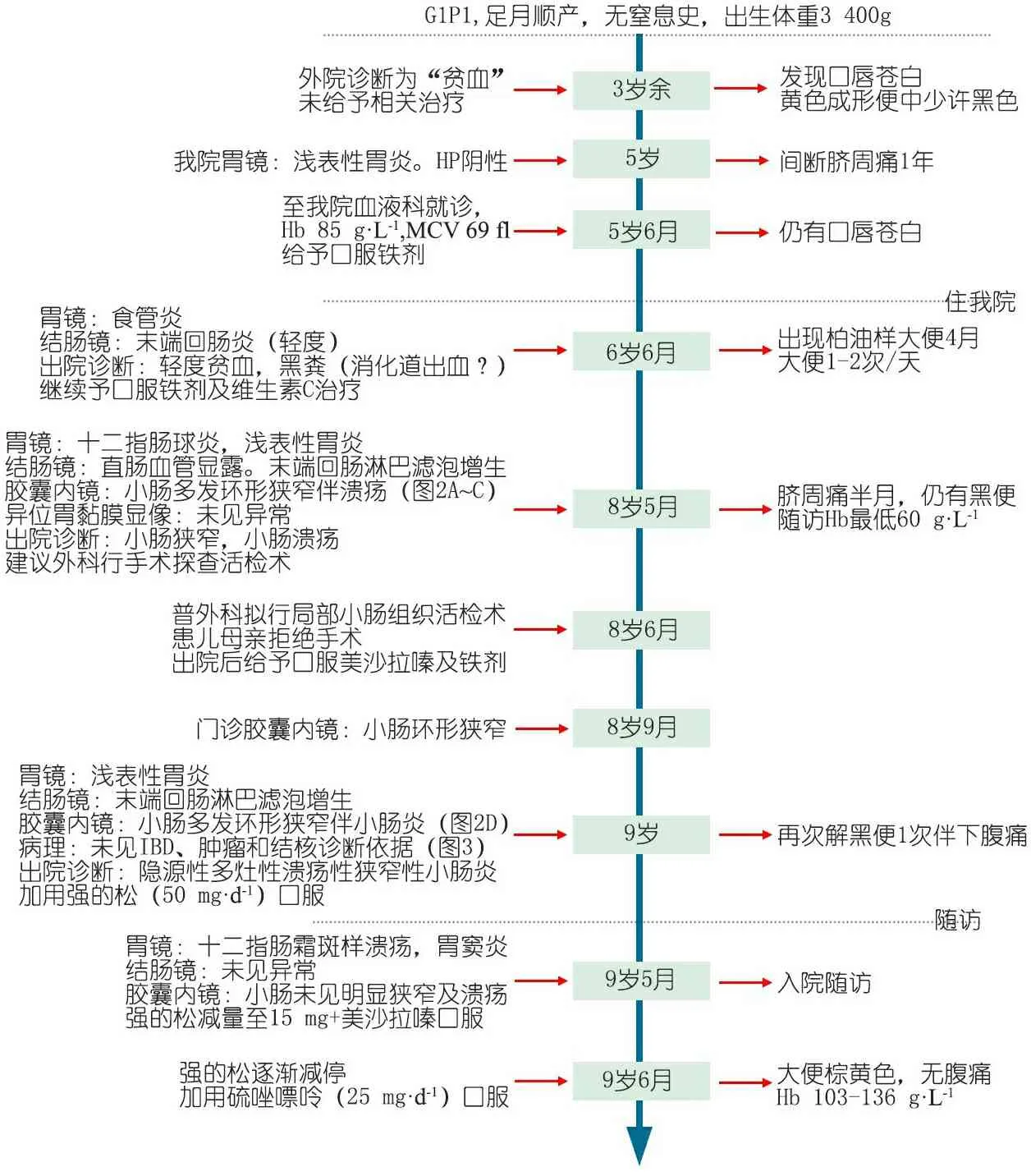
图1 临床信息时间轴
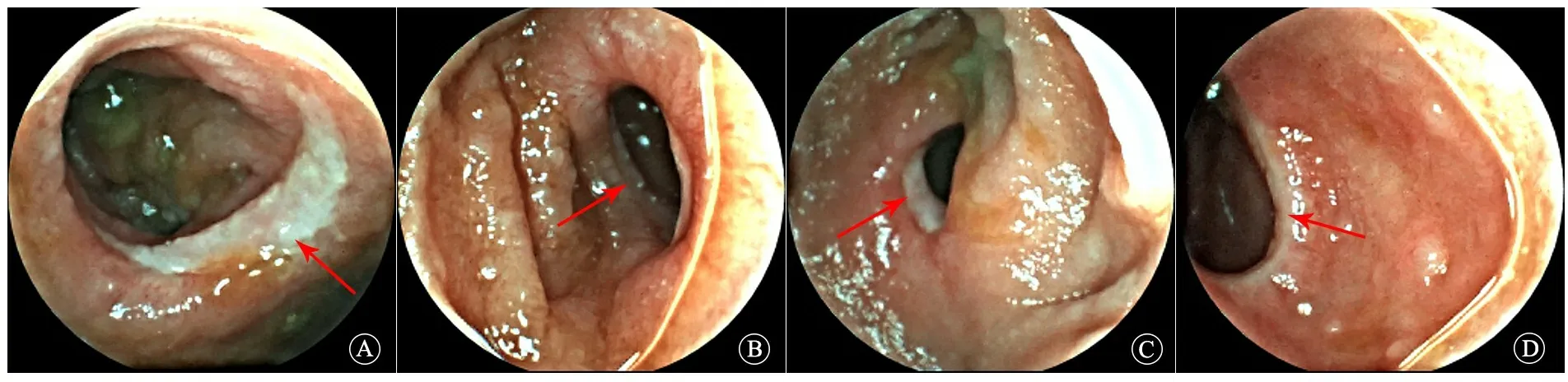
图2 本文病例胶囊内镜表现
注 A:小肠多发浅表溃疡;B:小肠多发狭窄;C:小肠多发溃疡伴狭窄;D:小肠环形狭窄
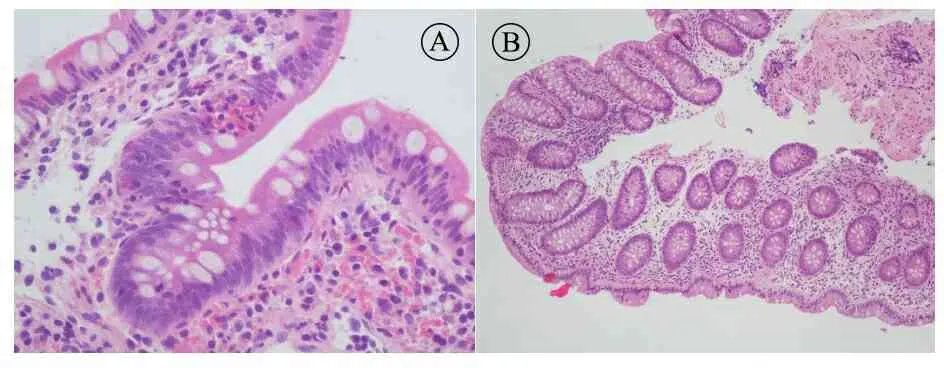
图3 本文病例肠黏膜组织病理学表现
注 A:小肠黏膜局灶淋巴组织增生,隐窝结构保存;B:横结肠黏膜未见诊断性异常。未见肉芽肿。未见炎症性肠病病理诊断依据。未见肿瘤,未见结核
随访:诊断CMUSE后,在口服铁剂治疗基础上,加用强的松龙(50 mg·d-1)口服,1个月后患儿出现视物模糊,眼压21 mmHg,激素减量至20 mg·d-1后视物模糊好转,眼压正常(15~17 mmHg)。口服激素3个月后,患儿出现肛周疼痛、红肿伴白色分泌物,暂停口服激素1周。强的松龙口服5个月时住院随访,胶囊内镜示小肠未见明显管腔狭窄及溃疡性病变。强的松龙口服6个月逐渐减停,加用硫唑嘌呤(25 mg·d-1)口服。随访8个月,患儿大便棕黄色,无腹痛,Hb 136 g·L-1,停用铁剂。
2 讨论
CMUSE是一种罕见的小肠慢性疾病,由Lindholmer于1964年首次报道[2],临床症状多表现为反复发作的贫血、腹痛和柏油样便,以浅表性溃疡、小肠黏膜下层增厚为特征,通常不累及结肠,无全身炎症反应[3,4]。CMUSE的病因目前尚不明确,可能与补体C2缺乏相关[5],亦有报道在同胞中存在遗传基础,与胞浆磷脂酶A2(PLA2G4A)基因突变有关[6]。Fraile等[7]报道CMUSE与X-连锁隐性网状色素障碍有关。Kohoutová等[8]推测,多灶性小肠胶原降解紊乱可能在CMUSE的发病中起着至关重要的作用。
以("cryptogenic multifocal ulcerating stenosing enteritis" OR CMUSE OR "cryptogenic, multifocal, ulcerous, and stenosing enteritis")和("隐源性多灶性溃疡性狭窄性小肠炎" OR CMUSE)检索式分别检索PubMed、EMBASE及中国生物医学文献数据库和万方数据库,建库到目前共报道CMUSE患者88例,英文76例[1,3,6~20],中文12例[21~23]。表2为文献报道的CMUSE患者的临床信息汇总。
CMUSE好发于中青年,18~50岁占68.6%(35/51),<18岁患儿5例,最小发病年龄23月龄,本文病例为国内儿童病例首报。男女性发病比例相当。因检查技术受限,小肠溃疡的诊断并不容易,很多研究报道从起病至考虑CMUSE诊断通常需要数年至数十年[10,14],就诊前平均病程9.9年(1月龄至48年)。CMUSE发病早期以腹痛(55/81,67.9%)、贫血(26/81,32.1%)和消化道出血(15/81,18.5%)为主要表现,大便通常是成形的。CMUSE患者很少有肠外表现,仅报道口腔溃疡、肛管脓肿、脱发伴光过敏和水肿伴多浆膜腔积液各1例[22]。
CMUSE以小肠多发性溃疡和狭窄为特点,Chung等[14]报道CMUSE患者小肠狭窄和溃疡的病变位置不同,小肠狭窄中空肠占25%(5/20),回肠占35%(7/20),两者均有占30%(6/20);而溃疡主要位于空肠(11/20, 55 %)。文献报道最多者小肠狭窄24处[3]。双气囊小肠镜和胶囊内镜是检出小肠病灶重要的诊断工具,但对于CMUSE患者而言,双气囊小肠镜优于胶囊内镜,因为小肠镜下可获取黏膜组织,甚至可在镜下行球囊扩张术治疗。但实际上两者用于CMUSE患者均存在风险,文献报道胶囊内镜滞留率37.9%(11/29)[1,8,9,11,13,16,19,22],12.1%(4/33)因肠腔狭窄造成小肠镜进镜困难[13,22]。根据文献报道,CMUSE早期以溃疡为主,晚期以狭窄为主,故本文病例虽进行4次胶囊内镜检查均在1周内自行排出,但在今后的长期随访中仍应谨慎进行胶囊内镜检查。双气囊小肠镜在儿童病例中的应用目前并不广泛,技术亦欠成熟,考虑狭窄的风险,本文病例并未进行双气囊小肠镜检查。但回顾病例并结合文献,本文病例多次腹部增强CT和小肠MR均未发现肠腔狭窄,处于以溃疡病变为主的CMUSE理论上早期进行双气囊小肠镜的风险较小,随访中可考虑进行该检查。

表2 文献报道CMUSE患者的临床信息
CMUSE是一个排他性诊断,诊断主要依靠病史、临床表现、影像学、内镜及组织病理学表现等。Perlemuter等[3]于2001年提出CMUSE的诊断要点:①不明原因的小肠狭窄;②局限于黏膜及黏膜下层的浅表性溃疡;③慢性或复发性溃疡性狭窄和腹痛;④无全身炎症征象;⑤胃肠道持续性隐匿性出血。Zhang等[1]于2017年将CMUSE的诊断标准更细化:(1)临床病史:①病程长,几年至数十年,②胃肠道持续性隐血伴严重贫血,③部分有家族史;(2)临床特征:①慢性复发性肠梗阻发作,②慢性缺铁性贫血伴疲劳、头晕、水肿或生长迟缓,很少有腹泻,③炎症指标或其他全身炎症生物指标正常,④结肠和胃部组织正常,⑤无肠外表现;(3)影像学表现:灌肠检查可见小肠多发性连续性狭窄;(4)内镜表现:①多发性、多形性浅表性溃疡,与周围正常黏膜分界清晰,②胶囊内镜检查应慎重,因其可能滞留在狭窄处;(5)组织学发现:①坏死性炎性溃疡不会侵犯固有肌层,②非特异性炎症、黏膜下层侵蚀伴纤维化。根据以上诊断标准,本文病例以贫血和黑便起病,无发热,病程6年余,起病前和病程中否认服用NSAIDs,炎症指标正常,胶囊内镜见小肠多发浅表溃疡伴狭窄,未累及其他消化道,组织学病理无特异性表现,故排除克罗恩病(CD)、NSAIDs相关性肠病、结核、肿瘤和美克尔憩室等,诊断为CMUSE。
CMUSE易与克罗恩病、NSAIDs相关性肠炎[16,19,24]、其他小肠慢性感染[19]、药物性小肠损害[25]和肿瘤[8]混淆。CMUSE无肠穿孔、裂隙、瘘管或脓肿形成[3,8,14],除小肠外不累及其他消化道,肠外表现少[13,26],无全身炎症反应,这可能与CMUSE患者中纤维组织形成使全身炎症反应降低有关[3],这些是与CD最大的差别。但仍有很多CMUSE病例被误诊为CD[1,16]。汇总文献,既往误诊为CD 14例(70.0%)[1,15~17,20~23],结核[11,17]和药物相关性肠病[22]各2例(10.0%),炎症性肠病、急性阑尾炎和美克尔憩室[22]各1例(5.0%)。
慢性非特异性多发性小肠溃疡(CNSU)亦是罕见的可致消化道隐匿性出血的慢性小肠病变,目前见诸文献的CNSU大多由日本学者报道[2,27~31]。日本学者Matsumoto等[25]和Yao等[32]将CNSU的临床病理特征归纳为:①与疾病起病和发展相关的致病因素不明确,②因持续性消化道隐匿性出血导致持续贫血,③病变主要在回肠,溃疡局限于黏膜下层,无特异性组织学表现。从慢性复发性和非特异性狭窄性小肠溃疡两个特点看,CNSU和CMUSE在临床和病理特征方面几乎相同,但两者的区别在于:①CNSU患者常有低蛋白血症,而CMUSE鲜少有以低蛋白血症起病者;②糖皮质激素对CNSU治疗无效,而对CMUSE治疗有效。Perlemuter等[3,5]推测CMUSE与血管炎密切相关,因为狭窄和动脉瘤被发现存在于肠系膜上动脉中,故类固醇在CMUSE患者中是有效的。文献报道CNSU存在家族遗传[27],与SLCO2A1基因突变相关[29,33],故有学者建议将其命名为SLCO2A1基因相关性慢性肠炎(CEAS)更合适[33]。CNSU和CMUSE是否为同一个疾病或同一疾病谱系,目前尚无定论,有待更多病例积累。
亦有将其他疾病误诊为CMUSE的报道,Shen等[34]曾报道1例以反复发作的腹痛、呕吐和黑便为主要表现的50岁男性患者,结合患者存在贫血、ESR正常、钡剂灌肠示空肠及近端多发溃疡和狭窄、腹部CT示空肠多发狭窄及肠壁增厚、PET-CT示肠道炎症、胃镜和结肠镜检查均未见异常,给予强的松治疗症状明显好转,故诊断为CMUSE。但患者在出院2个月后因肠穿孔急诊手术,术中见从Triz韧带起至近端回肠可见20多处狭窄,术后病理提示黏膜相关淋巴组织淋巴瘤(MALT)。由于CMUSE的溃疡是局限于黏膜和黏膜下层而非透壁,因此当患者出现肠穿孔时,CMUSE的诊断应受到质疑。
CMUSE主要的治疗包括营养支持、系统性类固醇、肠切除术或球囊扩张术。既往研究显示类固醇在CMUSE中有效[3,14],但亦有研究报道接受类固醇治疗的CMUSE患者疾病复发而需要手术9]、类固醇难治性病例[17]或类固醇依赖[3,8]。在CMUSE患者中类固醇使用的矛盾反应可能与不同疾病阶段密切相关,即早期表现为多个浅表溃疡,晚期表现为严重狭窄,故类固醇可能在疾病早期有效,疾病后期仍需要手术干预。Kijmassuwan等[10]报道1例10岁女孩诊断CMUSE后口服泼尼松龙,逐渐减量过程中加用硫唑嘌呤口服,目前随访10个月无贫血和黑便,但亦有加用硫唑嘌呤无效报道[17]。考虑到糖皮质激素耐药问题,且本文病例在使用过程中出现了视物模糊,故在强的松龙减量过程中,加用硫唑嘌呤,目前随访8个月,患儿处于缓解中。肠内外营养支持联合补铁治疗在短时间内是有效的[4,8],长期缓解还需要手术或其他药物。Singh等[11]报道1例17岁起病的52岁男性患者,长期服用糖皮质激素、美沙拉嗪和硫唑嘌呤,仍存在黑粪,故改用雌激素和孕激素治疗,使用7年间腹痛和黑粪症状均消失,后因出现男性乳房发育和性欲减退不良反应,停用炔雌醇和炔诺酮后再次出现黑粪,故继续使用。最近,亦有使用英夫利西单抗治疗CMUSE得以缓解的报道[15]。
CMUSE的预后目前尚不清楚。部分报道显示CMUSE预后不佳,常反复发作[3,14]。文献报道,CMUSE患者再手术率达29.7% (22/74)(表2),最严重者再手术6次[6],提示CMUSE患者的预后堪忧。在已有的文献报道中,2例CMUSE死亡,1例35岁CMUSE女性患者随访1.5年后因肺炎合并脓毒症死亡[8],1例50岁男性患者诊断后放弃治疗死亡[3],尚无CMUSE直接导致死亡的报道。CMUSE相关性肿瘤尚未见报道。结合文献报道,考虑本文病例尚处于CMUSE疾病早期,后续复发时及时治疗避免再手术是对本病例最大的价值和意义。
