阿米卡星和卷曲霉素在耐多药结核病治疗不良反应的观察及对比分析
2018-08-03任斐许优党丽云武延琴马进宝郑思思
任斐 许优 党丽云 武延琴 马进宝 郑思思
耐多药结核病(MDR-TB)是指结核分枝杆菌至少同时对异烟肼(INH)和利福平(RFP)2种以上药物耐药的结核病。2017年WHO全球结核病报告显示, 2016年全球新发MDR-TB 患者约49万例,其中47%的MDR-TB患者在印度、中国和俄罗斯,MDR-TB已成为全球公共卫生危机[1]。MDR-TB通常需要多种抗结核药物联合使用,且疗程长达24个月,其治疗过程中不良反应发生率高,不良反应的发生是影响患者治疗依从性及治疗成功率的重要原因[2]。二线注射类抗结核药物是治疗MDR-TB患者的核心药物,且使用时间至少6个月以上[3-4];阿米卡星及卷曲霉素是我国主要使用的二线注射类抗结核药物,长时间使用可能具有明显的耳毒性及肾毒性,这在不同的报道中差别较大;但是,阿米卡星与卷曲霉素所致不良反应的差别及其对治疗的影响少见报道[5-6]。为此,笔者回顾性调查了西安市胸科医院使用个体化治疗方案且治疗满1年的MDR-TB患者,分析二线注射类抗结核药物不良反应的发生情况及对治疗的影响,为指导临床合理选择药物提供参考依据。
对象和方法
一、研究对象及分组
回顾性选取2015年1月至2016年12月西安市胸科医院确诊并使用个体化治疗方案治疗满1年的MDR-TB患者185例,排除未使用二线注射类抗结核药物患者45例,临床资料记录不全者22例,二线注射类抗结核药物耐药者6例,共计纳入112例MDR-TB患者。研究对象包括男73例(65.2%),女39例(34.8%),平均年龄(35.52±14.88)岁。根据二线注射类抗结核药物的使用分为阿米卡星及卷曲霉素两组,阿米卡星组43例,卷曲霉素组69例。两组MDR-TB患者的一般资料比较差异均无统计学意义,具有可比性,见表1。

表1 MDR-TB患者一般情况在阿米卡星组和卷曲霉素组中的比较
二、患者的纳入和排除标准
1.纳入标准:(1)年龄18~70岁;(2)痰培养分枝杆菌阳性,经菌种鉴定为结核分枝杆菌复合群,药物敏感性试验(简称“药敏试验”)提示同时对异烟肼和利福平耐药;(3)经西安市胸科医院MDR-TB防治专家组分析讨论后,使用含有阿米卡星或卷曲霉素的耐多药化疗方案进行抗结核治疗。
2排除标准:(1)HIV感染者;(2)妊娠期或哺乳期女性患者;(3)临床资料记录不全者;(4)抗结核药物治疗不满1年者;(5)并发严重心、肝、肾、脑、胃肠道及全身系统疾病者。
三、研究方法
1.治疗方案:经西安市胸科医院MDR-TB防治专家组集体分析讨论后对患者进行抗结核药物治疗。依据《耐药结核病化学治疗指南(2015年)》[3],按照一线及二线抗结核药物药敏试验结果及患者既往用药史对患者制定个体化抗结核药物治疗方案,方案为6Cm(Am)-Lfx(Mfx)-Pto(PAS,E)-Cs(PAS,E)-Z/18Lfx(Mfx)-Pto(PAS,E)-Cs(PAS,E)-Z(Cm:卷曲霉素;Am:阿米卡星;Lfx:左氧氟沙星;Mfx:莫西沙星;Pto:丙硫异烟胺;PAS:对氨基水杨酸钠;E:乙胺丁醇;Cs:环丝氨酸;Z:吡嗪酰胺)。其中,阿米卡星注射液为四川美大康华康药业有限公司产品,0.2 g/支,深部肌内注射或静脉滴注;注射用硫酸卷曲霉素为浙江海正药业股份有限公司产品,0.75 g/支,深部肌内注射或静脉滴注。具体用药剂量见表2。

表2 各类抗结核药物的剂量及用法
2.治疗效果的评价:按照文献[3]及中华医学会《临床诊疗指南:结核病分册》[7]制定的标准评定:(1)痰细菌学阴转为连续2次痰培养结果显示为阴性(至少间隔30 d),阴转时间为第1次痰培养阴性的标本收集时间。(2)影像学检查判断病变累及肺野的范围,以所有病灶相加后占所有的肺野数计算;病灶“显著吸收”为病灶吸收≥1/2原病灶,“吸收”为病灶吸收<1/2原病灶,“不变”为原病灶无明显改变,“恶化”为原病灶扩大或播散。病灶“显著吸收+吸收”可视为好转。
3.药物不良反应的定义及记录:药物不良反应是指合格药物在正常用法用量下出现的与用药目的无关的或意外的有害反应[8]。与二线注射类抗结核药物相关的常见不良反应为耳毒性(包括听力下降和耳鸣)、肾损伤、低钾血症[3,9]。相关定义参考文献[10-11]:(1)听力下降:以500 Hz、1000 Hz和2000 Hz的平均听阈为准,听力损失25 db以下为正常,26 db以上为听力下降,其中26~40 db、41~55 db、56~70 db、71~90 db和>91db依次为轻度聋、中度聋、中重度聋、重度聋和极重度聋。(2)耳鸣:指患者主观上感觉耳内或头部有声音,但外界并无相应声源产生。(3)肾损伤:抗结核药物损伤肾小管引起蛋白尿、管型和血尿,严重的出现氮质血症甚至肾衰竭。(4)低钾血症:血清钾低于3.5 mmol/L。
4.不良反应的处置及分类[8]:临床医生根据患者的主诉、随访检查结果及用药情况等判断不良反应的发生情况。不良反应分为轻度、中度、重度。(1)轻度:症状轻微,一般不需要特殊治疗,也不需要停药;(2)中度:有较明显症状,对器官和功能有一定损伤,需要处理和(或)停药;(3)重度:病症重,可引起对器官功能的明显伤残,甚至危及生命,需要住院治疗,有的需要及时抢救。对症状较轻者予以对症处理,严重不良反应事件报告西安市胸科医院诊疗专家组并指导处理,做好相关记录。
5.数据收集:由经过培训的医务人员查阅MDR-TB患者的住院及随访病历,并对所有患者进行电话随访确认相关信息,记录患者的基本信息(性别、年龄等)、不良反应的起止时间、对治疗的影响等。
四、统计学处理
结 果
一、阿米卡星组与卷曲霉素组MDR-TB患者的疗效对比
阿米卡星组和卷曲霉素组MDR-TB患者治疗后6个月末的痰培养阴转率组间比较,差异有统计学意义(χ2=4.43,P<0.05);两组患者12个月末痰培养阴转率及6个月末、12个月末病变吸收好转率组间比较,差异均无统计学意义(χ2值分别为2.52、0.59、0.43,P值均>0.05)。具体见表3。
二、阿米卡星组与卷曲霉素组MDR-TB患者不良反应发生情况
阿米卡星组共计26例(28例次)患者出现不良反应,其中耳毒性24例次(5例同时出现听力下降和耳鸣,4例仅出现听力下降,15例仅出现耳鸣)。卷曲霉素组37例(50例次)患者出现不良反应,其中耳毒性22例次(3例同时出现听力下降和耳鸣,1例仅出现听力下降,18例仅出现耳鸣)。两组患者不良反应发生率分别为60.5%(26/43)和53.6%(37/69),组间比较差异无统计学意义(χ2=0.50,P>0.05)。两组均无重度不良反应,患者中发生轻度不良反应者分别占65.4%(17/26)和81.1%(30/37),差异无统计学意义(χ2=1.99,P>0.05)。
两组患者听力下降和低钾血症的发生率比较,差异均有统计学意义(χ2值分别为4.53、10.79,P值均<0.05);耳鸣及肾损伤的发生率组间比较,差异无统计学意义(χ2值分别为2.95、1.08,P值均>0.05)。具体见表4。
三、两组患者发生不良反应后对治疗过程的影响
阿米卡星组共计9例(9/43,20.9%)因不良反应而停药,用药时间7~102 d,中位数95 d;卷曲霉素组共计7例(7/69,10.1%)患者因不良反应而停药,用药时间10~150 d,中位数110 d。阿米卡星组和卷曲霉素组4个月内因不良反应导致药物停用的发生率分别为20.9%(9/43)和5.8%(4/69),组间差异有统计学意义(χ2=4.53,P<0.05)。两组患者中仅有1例更换药物。
讨 论
二线注射类抗结核药物中阿米卡星和卷曲霉素为治疗MDR-TB的核心药物,对结核分枝杆菌都具有杀菌作用。本研究中选用含有卷曲霉素或阿米卡星的耐多药肺结核化疗方案对耐多药肺结核患者进行化疗,发现卷曲霉素组和阿米卡星组患者在治疗后的12个月末痰培养阴转率及6个月末、12个月末病变吸收好转率差异均无统计学意义,提示两者在治疗MDR-TB的近期疗效上差别不大。在治疗效果相仿的条件下,药物不良反应发生情况是重要的选择药物的考虑因素。国内报道,MDR-TB治疗过程中的不良反应多以肝功能异常、单纯尿酸升高、骨关节功能异常及胃肠道反应为主,与注射类抗结核药物密切相关的不良反应如耳毒性、肾损伤的发生率分别为7.8%和3.4%,发生率相对较低[2,12]。而本研究中阿米卡星及卷曲霉素的总的不良反应发生率分别为60.5%和53.6%,高于上述报道;可见,二线注射类抗结核药物的不良反应可能被低估[6]。
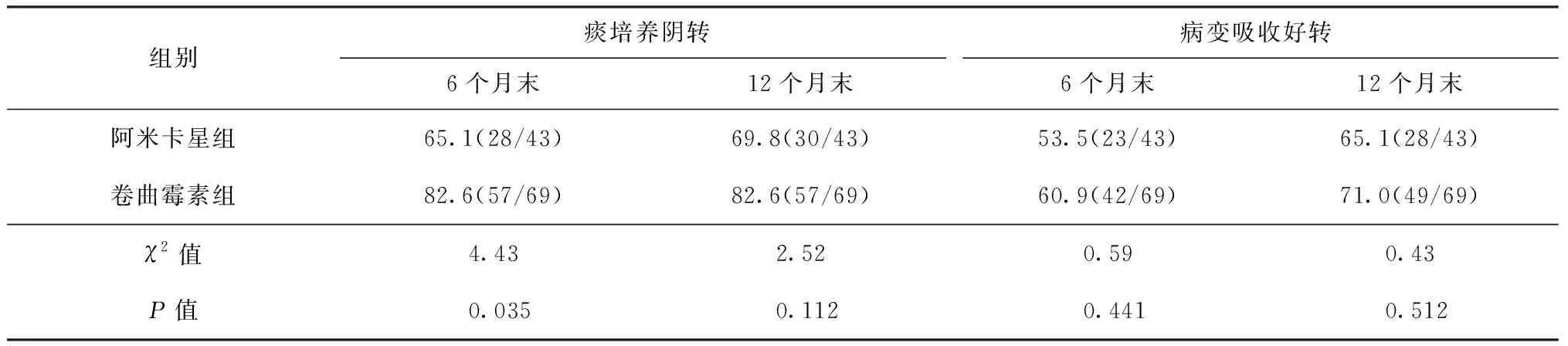
表3 阿米卡星组与卷曲霉素组MDR-TB患者近期疗效的比较
注 表中括号外数值为“比率(%)”;括号内数值分子为“痰培养阴转例数”或“病变吸收好转例数”,分母为“各组总例数”

表4 各类不良反应在两组患者中的发生情况对比
本研究中阿米卡星和卷曲霉素的耳毒性发生率分别为55.8%及31.9%,远远高于国内的报道[13],接近国外应用二线注射类抗结核药物所致耳毒性发生率60%左右的报道[14-15]。本研究中,二线注射类抗结核药物的耳毒性较高的原因除了本研究为回顾性研究、且纳入患者例数较少以外,可能还有如下原因:(1)本研究重点关注注射类抗结核药物的不良反应,课题工作人员除查阅住院及随访病历外,还做了详细的电话访问,大约1/3的患者用药后出现耳塞及间断耳鸣症状但未告知主管医师。(2)本研究中部分患者的高频听力丧失是通过定期的听力检测发现的,而患者尚未出现明显的临床症状。以上情况提示,医务人员应重视注射类抗结核药物的耳毒性,一方面对患者做好相关的健康教育,告知耳塞和间断耳鸣是前庭功能障碍的早期症状,且前庭功能损伤不可逆转,不会随停药而改善[3];另一方面按照文献[3]建议在强化期定期行听力检测,以便尽早发现并及时处理。
本研究中阿米卡星组听力下降的发生率明显高于卷曲霉素组,这与Arnold等[15]的研究结果一致。氨基糖苷类药物是浓度依赖性杀菌剂,其治疗剂量和毒性剂量较接近,可进入内耳外淋巴液,内耳外淋巴液中药物的高浓度与蓄积性是引起耳毒性的主要原因。各种氨基糖苷类药物均可发生耳毒性、耳鸣、听力减退及耳聋等不良反应,发生率依次为卡那霉素>阿米卡星>链霉素,卷曲霉素的耳毒性小于氨基糖苷类药物[5]。但应当注意的是,国外相关研究中阿米卡星的使用剂量为15 mg/kg,而本研究阿米卡星的使用剂量为0.4 g/d,低于WHO推荐的15 mg/kg,其听力下降的发生率却达到了20.9%,虽然低于Ribeiro等[14]报道的60%和Arnold等[15]报道的55%,却也接近Vasconcelos等[16]报道的27%,明显高于国内张红伟等[12]报道的7.9%,其中的原因需要进一步探讨,但足以引起结核科医生的警惕。本研究中虽然两组患者耳鸣的发生率差异无统计学意义,但是应该注意到听力下降的患者多伴有耳鸣,耳鸣是听力损伤较常出现的症状,且多在听力下降之前出现[16-17];考虑到听力损伤的不可逆性,使用二线注射类抗结核药物的MDR-TB患者需要定期行听力测定,尤其对于男性及出现耳鸣的患者需要提高听力测定的频率,以便早期发现听力损伤并及时处理。
卷曲霉素的不良反应中低钾血症也较为多见,在不同的报道中发生率也不尽相同[15,18]。本研究中卷曲霉素导致低钾血症的发生率为30.4%,明显高于阿米卡星的4.7%; Meressa 等[19]的临床观察也发现卷曲霉素导致低钾血症的发生率高于其他注射类抗结核药物,卷曲霉素引起低钾血症的机制目前尚不明确。Varma 等[20]报道了使用阿米卡星6个月以上的2例患者均出现了低钾、低镁情况,考虑可能与产生继发性醛固酮增多症有关。低钾血症的发生率虽然较高,但在密切的电解质监测下和对症补钾治疗后,本组患者中仅有1例更换药物,对治疗的影响并不大。
本研究发现,两组患者不良反应的严重程度虽然并无差别,但4个月内因不良反应导致药物停用的发生率阿米卡星组明显高于卷曲霉素组,这与Arnold等[15]报道的卷曲霉素使用时间明显长于阿米卡星是一致的。Modongo等[21]的研究表明, MDR-TB良好的治疗效果与二线注射类抗结核药物较长的使用时间及累计药物剂量有关,本研究中阿米卡星组6个月末痰培养阴转率明显低于卷曲霉素组可能也与此有关。本研究中阿米卡星的使用剂量为0.4 g/d,如果提高到指南中推荐的阿米卡星的0.5~0.75 g/d的剂量,其耳毒性及肾损伤的发生率理论上应该会更高,也会缩短其使用时间并对治疗效果产生不利影响。虽然有研究认为,针对阿米卡星血清药物浓度的检测,可能会在保证治疗效果的前提下最大程度地减少耳毒性及肾毒性的发生[22];但很多基层单位尚无法开展药物浓度监测,且血药浓度监测本身还有很多需要解决的问题[23]。因此,使用药物浓度监测个体化给药方法短时间内可能尚无法实现。
综上所述,在MDR-TB的治疗中,二线注射类抗结核药物的不良反应尤其是耳毒性的发生率较高,并且可能被低估。使用阿米卡星所致的听力下降及4个月内因不良反应的发生,导致药物停用的发生率高于卷曲霉素。临床医生应当重视二线注射类抗结核药物的不良反应,从不良反应及治疗效果方面考量,MDR-TB治疗中二线注射类抗结核药物应首先选择卷曲霉素。
本研究为回顾性研究,资料来源于患者在专业诊疗机构的病历,且部分数据来自于患者的回忆,存在一定的信息偏倚;其次,本研究纳入观察的样本量较少;最后,其他药物及相关因素也会导致相关的不良反应,比如吸烟、噪音等会引起听力损伤,乙胺丁醇、氟喹诺酮类药物也有潜在的肾脏损伤,本研究未剔除这些混杂因素,可能也会对最终结果产生影响。
