超高效液相色谱-高分辨质谱法筛查婴幼儿配方奶粉中17种头孢菌素类药物残留
2018-08-02程建桥许秀丽洪云鹤吴寒秋王传胜
程建桥, 张 峰, 许秀丽, 洪云鹤, 吴寒秋, 王传胜
(1. 中国检验检疫科学研究院食品安全研究所, 北京 100176; 2. 沈阳化工大学应用化学学院, 辽宁 沈阳 110142)
头孢菌素(cephalosporin)类药物是一大类具有β-内酰胺结构的广谱半合成抗生素(结构通式如图1),对革兰氏阳性菌、阴性菌及螺旋体均显示广谱抗菌活性。主要用于治疗人体因革兰氏菌感染引发的各种炎症,在畜牧养殖领域也常被用于防治奶牛乳房炎症、胃肠道和呼吸系统感染。然而,头孢菌素类药物在畜牧养殖过程中的不规范使用会残留在动物源性食品中,从而引发一系列食品安全问题,同时也有可能导致“超级细菌”的产生[1,2]。
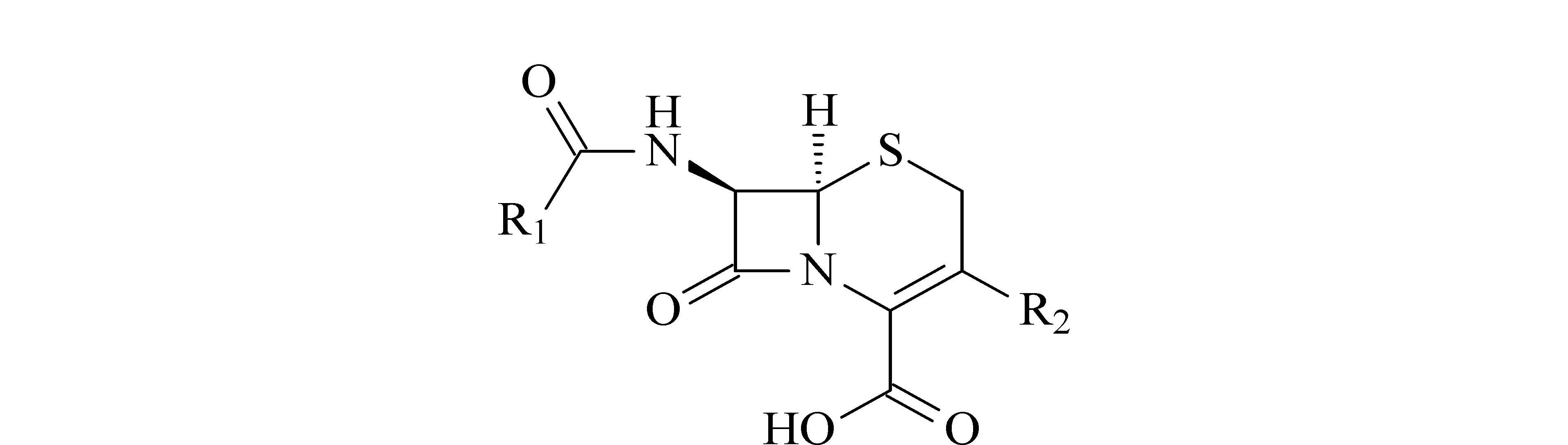
图 1 头孢菌素类药物的结构通式Fig. 1 Structural formula of cephalosporins
从国内外调查情况来看,乳制品中抗生素残留情况较为严重[3]。长期摄入含抗生素残留的动物源性食品,除药物自身的毒副作用外,还可能导致过敏反应和肾脏损伤[4]。美国食品法规21号文件[5]中规定牛奶中头孢噻呋最大残留限量为100 μg/kg,头孢匹林最大残留限量为20 μg/kg;欧盟在食品中兽药残留的No. 37/2010文件[6]中对头孢氨苄、头孢乙腈、头孢唑啉等8种头孢菌素类药物及头孢匹林、头孢噻呋两种物质的代谢物的最大残留限量做了相关规定(含量在20 μg/kg与125 μg/kg之间);我国农业部235号文件[7]规定了牛奶和奶粉中头孢氨苄的最大残留限量为100 μg/kg,头孢噻呋的最大残留限量为100 μg/kg,头孢喹肟的最大残留限量为20 μg/kg。
近年来高分辨质谱(Q-TOF和Q-Orbitrap)在农药残留、兽药残留检测领域普及[8-11],但对于动物源性食品中头孢菌素类药物残留分析的超高效液相色谱-四极杆/静电场轨道阱高分辨质谱(UHPLC-Q-Orbitrap HRMS)筛查方法相关研究报道较少,仅检索到一篇肉类中头孢菌素类药物筛查方法的报道[12],婴幼儿奶粉中头孢菌素类药物残留的筛查方法更未见报道,导致婴幼儿奶粉及牛奶在质量控制方面存在一定的安全隐患。婴幼儿配方奶粉基质复杂,蛋白质、脂质、维生素及配方成分等有机杂质较多,为高通量筛查方法的建立造成了一定的困难。近年来用于奶类样品分析的前处理技术主要有固相萃取(SPE)[13,14]、QuEChERS[15-17]、液-液萃取(LLE)[18]及磁性固相萃取(M-SPE)[19,20]等,常见头孢菌素类药物的结构和化学性质差异较大,传统前处理方法大都只涵盖化学性质相似的几种该类药物[21-25],且不同前处理方法分多次处理同一批样品会消耗大量的检材和时间,很难达到日常筛查的目的。因此,有必要开发出一套适用于婴幼儿奶粉中头孢菌素类药物的前处理技术及高通量筛查方法。
本研究针对复杂的奶粉基质,采用简化的前处理同时结合超高效液相色谱-四极杆/静电场轨道阱高分辨质谱(UHPLC-Q-Orbitrap HRMS)技术,建立了一种快速筛查婴幼儿奶粉中17种常见头孢菌素类药物残留的分析方法。该法操作简单,重现性好,分辨率高,可实现对婴幼儿配方奶粉中17种头孢菌素类药物的筛查,已成功应用于实际样品的检测中。
1 实验部分
1.1 仪器与试剂
Q Exactive四极杆/静电场轨道阱高分辨质谱仪,Dionex UltiMate 3000快速超高效液相色谱系统(美国赛默飞世尔科技公司); Allegra X-22R高速冷冻离心机(美国贝克曼库尔特有限公司); Milli-R04纯水仪(德国Millipore公司); ML104/02分析天平(梅特勒-托利多上海有限公司); HSC-12B针式氮吹仪(天津恒奥科技有限公司)。
头孢菌素类药物标准品:头孢米诺(cefminox)、头孢噻肟(cefotaxime)、头孢他美酯(cefetamet pivoxil)、头孢他啶(ceftazidime)、头孢洛宁(cephalonium)、头孢地尼(cefdinir)、去乙酰头孢匹林(desacetylcephapirin)(纯度>96% ,加拿大Toronto Research Chemicals Inc(TRC)公司);头孢羟氨苄(cefadroxil)、头孢唑啉(cefazolin)、头孢拉定(cefradine)、头孢匹林(cefapirin)、头孢克洛(cefaclor)(纯度>96% ,法国European Pharmacopoeia(EP)公司);头孢匹胺(cefpiramide)、头孢孟多(cefamandole)、头孢吡肟(cefepime)、头孢克肟(cefixmine)(纯度>96% ,美国U. S. Pharma-copoeia(U. S. P)公司);头孢哌酮(cefoperazone)(纯度>96% ,德国Dr. Ehrenstorfer公司)。乙腈、甲醇、正己烷(色谱纯,美国赛默飞世尔科技公司);甲酸(99% ,北京百灵威公司)。奶粉样品为市售。

图 2 17种头孢菌素类药物的色谱图Fig. 2 Chromatograms of the 17 cephalosporins
1.2 标准溶液配制
准确称取头孢菌素类药物标准品0.01 g(精确至0.000 1 g),头孢克洛以甲醇-水(1∶1, v/v)溶液定容至100 mL,其余头孢菌素类药物标准品均以乙腈-水(4∶1, v/v)溶液定容至100 mL,配制成100 mg/L的标准储备溶液,-40 ℃贮存。
混合标准溶液:移取各标准品溶液100 μL于容量瓶中,定容至10 mL,配制成1 mg/L的混合标准品储备溶液,-40 ℃贮存。每周配制一次。用乙腈将混合标准储备溶液逐级稀释,配制成系列工作液。
1.3 仪器条件
色谱条件:SUPELCO Ascentis®C8色谱柱(100 mm×4.6 mm, 3 μm);流动相A为水相,含0.1%(v/v)甲酸;B为乙腈。梯度洗脱程序:0~1 min, 5%B; 1~9 min, 5% ~95%B; 9~10 min, 95%B; 10~10.5 min, 95% ~5%B; 10.5~15 min, 5%B。流速:0.5 mL/min;进样体积:5 μL;柱温30 ℃;样品盘温度:8 ℃。
质谱参数:加热电喷雾离子(HESI)源;鞘气206.85 kPa;辅助气1 000 kPa;喷雾电压3.5 kV; S-lens电压60 V;毛细管温度300 ℃;辅助气加热温度350 ℃;正离子采集模式;Full MS/dd-MS2(data-dependent MS2)扫描模式。
1.4 样品前处理
准确称取1 g(精确至0.001 g)奶粉样品于50 mL聚丙烯离心管中,加入4 mL水涡旋至完全溶解后,再加入6 mL乙腈涡旋提取3 min,于4 ℃ 10 000 r/min离心10 min。取上清液,过0.22 μm滤膜,待分析。
2 结果与讨论
2.1 色谱分离
实验考察了3种色谱柱(Waters BEH Shield RP18 (100 mm×2.1 mm, 1.7 μm), Waters BEH HILIC (100 mm×2.1 mm, 1.7 μm)和SUPELCO Ascentis®C8 (100 mm×4.6 mm, 3 μm))对目标物的分离效果,结果表明:使用Shield RP18色谱柱对目标物进行分离时,部分物质出现两个目标峰,这可能是由于目标物在色谱柱中发生了分解;使用BEH HILIC色谱柱分离目标物时,色谱峰展宽较严重,影响定量的准确性;Ascentis®C8色谱柱适合用于头孢菌素类药物的分离,头孢菌素类药物色谱峰形改善,峰宽减小。
流动相的选择对待测物的分离及质谱检测结果的影响很大。研究中,由于使用的超高效液相色谱系统是二元泵工作模式,头孢菌素类药物在乙腈-水溶液中的溶解性较好,因此流动相的有机相部分均选择为纯乙腈。选择水相时对比了加酸与不加酸(0% ~1%(v/v)甲酸)对色谱峰形的影响,结果显示,在使用0.1%(v/v)甲酸水-乙腈作为流动相时,色谱峰形较好,这是由于流动相中的甲酸与头孢菌素类药物中的氨基与羧基产生了积极的相互作用,促进了电离。
图2为优化的仪器条件下,17种头孢菌素类药物的色谱图。
2.2 质谱条件的考察
对比Full MS、Full MS/dd-MS2和Target-SIM/dd-MS23种扫描模式:Full MS扫描模式下虽然可以达到对目标物的定量检测,但其仅以母离子精确质量数和保留时间对目标物进行定性,易造成假阳性检测结果;Target-SIM/dd-MS2扫描模式是先通过四极杆筛选出目标母离子,母离子进入高能碰撞池发生裂解,从而得到子离子碎片信息,提高了目标物的定性检测准确性,但该扫描模式在对目标物的定量上稍显不足。最终选择Full MS/dd-MS2扫描模式进行目标物的筛查监测,以母离子和碎片离子精确质量数定性,精确母离子定量,可达到对目标物的筛查及定量目的。
在Full MS/dd-MS2扫描模式下,质谱方法设置一级分辨率70 000,二级分辨率35 000, 归一化碰撞能量(normalized collision energies,NCE)在25%时可得到最佳监测结果,分辨率均小于1×10-6,见表1。
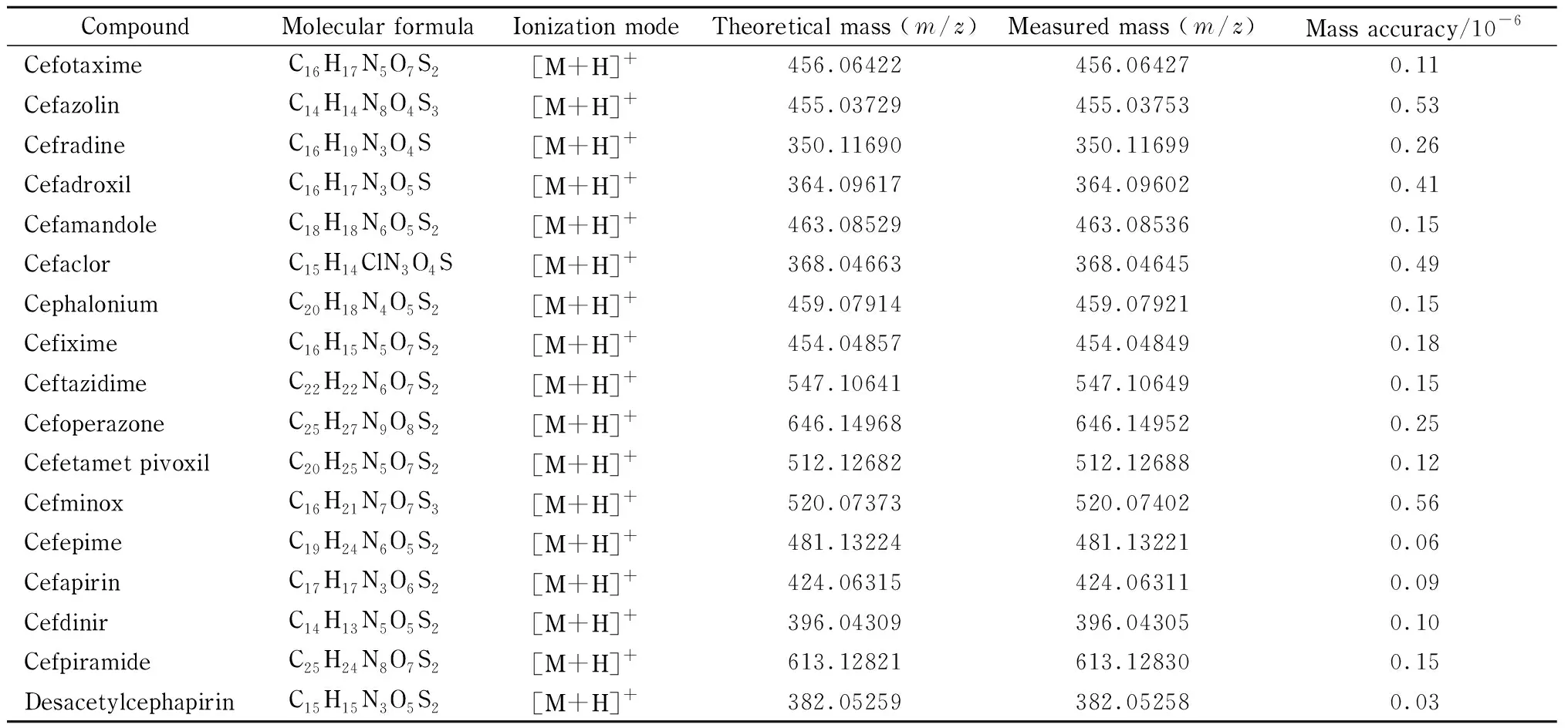
表 1 17种头孢菌素类药物的分子式、离子化方式、理论质量数、精确质量数和分辨率Table 1 Formula, ionization mode, theoretical mass, measured mass and mass accuracy for the 17 cephalosporins
2.3 前处理方法的选择
17种头孢菌素类药物的极性、溶解性、稳定性等存在很大的差异,为婴幼儿奶粉中头孢菌素类药物筛查的前处理净化带来一定困难。因此,在前处理方式的选择上,本研究对比了LLE、SPE、QuEChERS和直接提取-高速低温离心处理的效果。
首先准确称取空白奶粉样品1 g(精确至0.001 g)于50 mL聚丙烯离心管中,添加混合标准溶液至含量为50 μg/kg,加入5 mL水涡旋至完全溶解,再加入5 mL乙腈涡旋提取3 min,于10 000 r/min离心10 min。取上清液,分别采用LLE、SPE、QuEChERS和直接提取-高速低温离心处理方法进行前处理,比较萃取效果。
2.3.1液-液萃取
取上清液(约5 mL),加入乙腈饱和正己烷溶液振摇约3 min,取下层清液过0.22 μm滤膜,上机检测。由于提取过程中选用乙腈-水溶液作为提取溶剂,而水与正己烷互不相溶,乙腈微溶于正己烷,因此选用乙腈饱和正己烷溶液作为萃取液,除去提取液中的脂类杂质。结果表明:仅有10种目标化合物满足回收率要求(60% ~120%),原因可能为乙腈饱和正己烷溶液虽然可除去奶粉中脂类及非极性杂质干扰,但同时造成了部分低极性的头孢菌素类物质在净化过程中的损失,导致回收率偏低。
2.3.2固相萃取
取2 mL上清液,过PRiME HLB固相萃取柱(6 mL, 200 mg, 美国Waters公司)。待样品溶液全部流出后,加入2 mL 0.1%(v/v)甲酸-乙腈溶液淋洗,收集、合并全部流出液,氮吹至液体少于1 mL,用乙腈定容到2 mL,过0.22 μm滤膜,上机检测。PRiME HLB固相萃取柱为杂质吸附型固相萃取柱,不需要活化,上样后收集流出液即可,最大限度地缩短了前处理时间。结果表明有12种化合物满足回收率要求。研究中还对比了不洗脱、乙腈洗脱、0.1%(v/v)甲酸-乙腈溶液洗脱的效果,结果显示0.1%(v/v)甲酸-乙腈溶液更适用于作洗脱液,这可能是由于甲酸改变了洗脱液的酸碱度,能使磷脂等杂质吸附在PRiME HLB固相萃取柱上,而头孢菌素类药物则没有保留。
2.3.3QuEChERS净化
取上清液(约5 mL),加入0.9 g无水硫酸镁,150 mg C18填料和150 mg乙二胺-N-丙基硅烷(PSA),振摇3 min后,静置,取上清液,过0.22 μm滤膜,上机检测。结果表明满足回收率要求的仅9种化合物。此外,实验考察了C18填料、PSA以及QuEChERS方法组合净化剂(MgSO4+PSA+C18)的净化效果。结果显示:在奶粉基质中,组合净化材料为(0.9 g MgSO4+150 mg C18+150 mg PSA)时基质影响弱,回收率较高。
2.3.4直接提取-高速低温离心
取上清液(约5 mL), 于4 ℃以10 000 r/min离心10 min,取2 mL上清液,过0.22 μm滤膜,上机检测。使用直接提取-高速低温离心的方式可使13种化合物的回收率在60% ~120%内,这可能是因为直接提取-高速低温离心法最大限度地降低了头孢菌素类药物在净化过程中的损失。乙腈提取去除了奶粉溶液中蛋白质等杂质干扰,高速低温离心去除了部分动物脂肪,因此,在婴幼儿配方奶粉中头孢菌素类药物残留筛查中,本研究选用操作简单、节约资源的直接提取-高速低温离心的前处理方法。
2.4 提取溶剂体积的选择
配制50 μg/kg的奶粉加标样品,离心净化,考察水和乙腈的体积(水体积+乙腈体积)分别为2 mL+8 mL、3 mL+7 mL、4 mL+6 mL、5 mL+5 mL、6 mL+4 mL、7 mL+3 mL和8 mL+2 mL时对17种头孢菌素类药物回收率的影响,结果见图3。可以看出,水、乙腈的体积为4 mL+6 mL时效果最好。
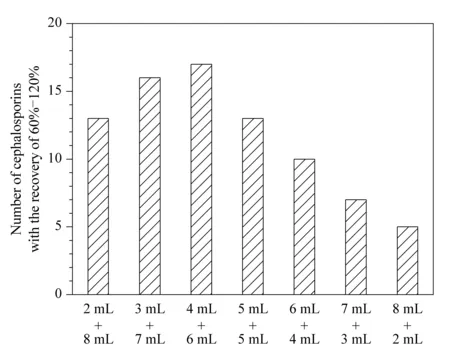
图 3 提取溶剂中水和乙腈的体积对头孢菌素类药物 回收率的影响(n=3)Fig. 3 Effect of volumes of water and acetonitrile in extraction solvent on the recoveries of cephalosporins (n=3)
2.5 基质效应
准确称取1 g(精确至0.001 g)奶粉样品于50 mL聚丙烯离心管中,加入4 mL水涡旋至完全溶解后,加入6 mL乙腈涡旋提取3 min,于4 ℃ 10 000 r/min离心10 min。上清液即为奶粉样品的空白基质溶液。基质效应根据相同浓度的分析物在纯有机溶液中与在空白基质溶液中的响应比值来评估,基质效应值根据方程(1)来计算[26,27]:
ME=B/A×100%
(1)
其中,A是指纯溶剂标准溶液获得的峰面积,而B指的是标准品在空白基质溶液中获得的峰面积。结果如表2所示,经提取-高速低温离心处理后奶粉样品的净化效果良好,头孢菌素类药物基质效应为85.6% ~118.6%(n=5),在80% ~120%之间,不存在明显的基质效应。因此,该法可满足婴幼儿配方奶粉中头孢菌素类药物残留的日常检测需求。
2.6 方法验证
方法验证参照欧盟2002/657/EC和美国食品药品监督管理局生物分析程序指导手册[28,29]进行。验证中每组数据至少取5次平行测定的平均结果。
2.6.1线性关系、检出限和定量限
配制17种头孢菌素类药物系列混合标准溶液(5~200 μg/L),以峰面积(Y)为纵坐标,质量浓度(X, μg/L)为横坐标,绘制标准曲线,17种化合物在5~200 μg/L内呈良好的线性关系,其线性相关系数(r2)均大于0.99。
注入一系列浓度的头孢菌素类药物混合标准溶液到仪器中,以3倍信噪比确定仪器的检出限(LOD);在空白样品中分别添加一系列浓度的头孢菌素类药物混合标准溶液,进行前处理和测定,以10倍信噪比确定方法的定量限(LOQ)。如表2所示,各化合物的检出限和定量限分别在0.006 0~0.040 μg/L和0.71~4.6 μg/kg范围内,表明该方法具有较好的灵敏度,可以对含量较低的分析物进行定量。
2.6.2回收率和精密度
在空白奶粉样品中添加5、50、200 μg/kg 3个水平的混合标准溶液,经1.4节处理后,每个水平重复测定5次,得到方法的回收率和精密度(见表3)。3个添加水平下17种头孢菌素类药物的回收率为69.6% ~101.4% ,精密度(RSD)小于10% 。
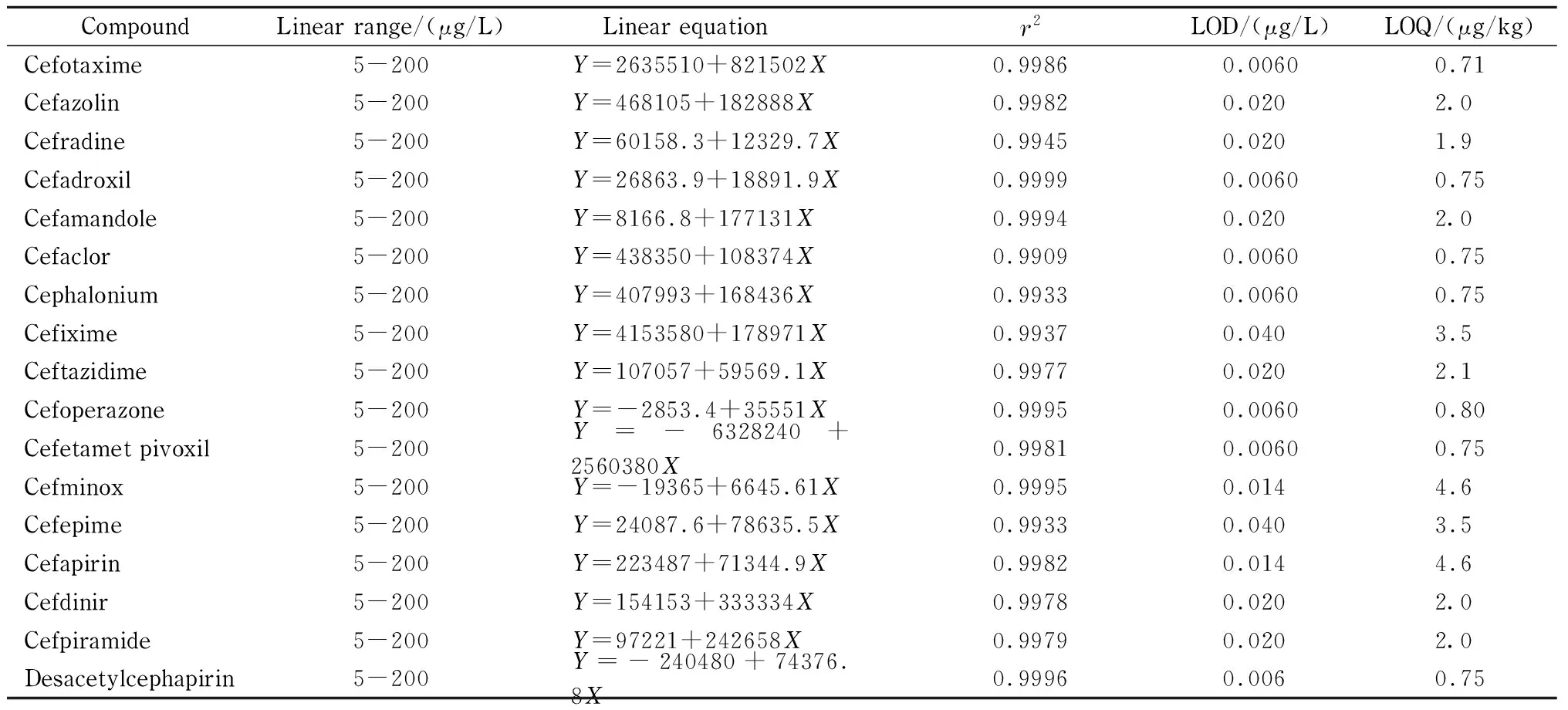
表 2 17种头孢菌素类药物的线性范围、线性方程、相关系数、检出限和定量限Table 2 Linear ranges, linear equations, correlation coefficients (r2), LODs and LOQs of the 17 cephalosporins
Y: peak area;X: mass concentration, μg/L.

表 3 17种头孢菌素类药物的基质效应以及在奶粉中3个添加水平下的回收率、日内精密度、日间精密度Table 3 Matrix effects and the spiked recoveries, intra-day precisions and inter-day precisions of the 17 cephalosporins at three levels in milk powder
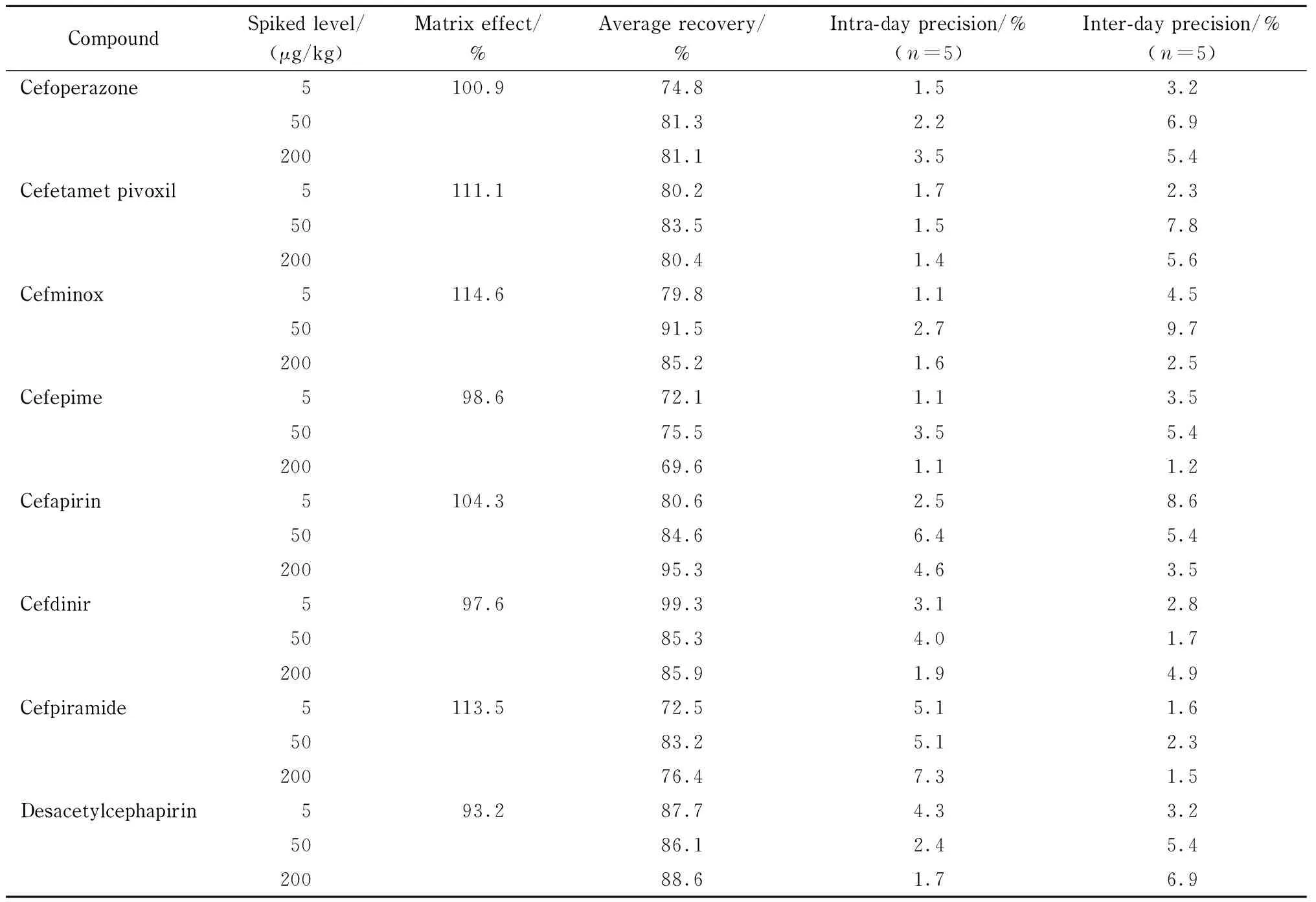
表 3 (续)Table 3 (Continued)
2.7 实际样品筛查
该法已经成功地应用于30例北京市售进口婴幼儿奶粉样品中头孢菌素类药物筛查,结果显示本次抽样筛查结果良好,未见可疑头孢菌素类药物残留。
3 结论
本研究建立了婴幼儿配方奶粉中17种头孢菌素类药物残留的超高效液相色谱-四极杆/静电场轨道阱高分辨质谱(UHPLC-Q-Orbitrap HRMS)快速筛查方法。目标物经乙腈提取后,通过简单的低温高速离心达到净化目的。使用C8色谱柱,Full MS/dd-MS2质谱扫描模式,对17种头孢菌素类药物进行了定性定量分析。该法操作简单,重现性好,分辨率高,能同时对婴幼儿配方奶粉中17头孢菌素类药物残留进行筛查定量。
猜你喜欢
杂志排行
色谱的其它文章
- 全二维气相色谱-质谱分析煤油基吸热型碳氢燃料烃族组成
- QuEChERS-超高效液相色谱-串联质谱法测定不同植被类型土壤中11种甲氧基丙烯酸酯类杀菌剂
- 离子液体分散液液微萃取-超高效液相色谱-串联质谱法测定食品接触材料中全氟辛酸和全氟辛烷磺酸的迁移量
- 超高效液相色谱-串联质谱法快速测定鸡蛋中氟虫腈及其代谢物残留
- 固相萃取-高效液相色谱-串联质谱法同时测定牛奶和羊奶中莫奈太尔及其代谢产物残留
- Determination of 11 synthetic musks in imported seafood by solid phase extraction and gas chromatography-mass spectrometry
